17 липня, 2015
Случай вторичного гиповентиляционного синдрома вследствие приема психотропных препаратов

Гиповентиляционный синдром – симптомокомплекс, возникающий вследствие недостаточной вентиляции легких и обусловливающий развитие гипоксемии и гиперкапнии.
Различают первичный и вторичный гиповентиляционный синдром. Первичный, или врожденный центральный гиповентиляционный синдром (congenital central hypoventilation syndrome – CCHS) является редким аутосомно-доминантным заболеванием, характеризующимся отсутствием автоматического контроля над процессом дыхания, снижением чувствительности к гипоксии и гиперкапнии при отсутствии нейромышечных, легочных, кардиологических заболеваний или поражения ствола мозга. В мире описано около 300 случаев данного заболевания. Во время сна у пациентов наблюдается гиповентиляция. У наиболее тяжелых больных гиповентиляция отмечается как во время сна, так и в период бодрствования. У таких пациентов заболевание проявляется уже в первые часы жизни и характеризуется цианозом и увеличением уровня углекислого газа, но зарегистрированы также случаи более поздней манифестации гиповентиляционного синдрома. Поскольку CCHS-синдром обычно проявляется в периоде новорожденности и мимикрирует под множество заболеваний, дифференциальная диагностика требует исключения различных состояний, сопровождающихся альвеолярной гиповентиляцией [3, 11].
Вторичный гиповентиляционный синдром развивается вследствие различных причин, основными из которых являются:
• медикаментозно-опосредованное угнетение активности дыхательного центра (прием транквилизаторов, антидепрессантов, наркотических анальгетиков и др.);
• поражения продолговатого мозга (энцефалит, кровоизлияние, новообразование и др.);
• поражения спинного мозга (травма, опухоль, сосудистая патология);
• поражение клеток передних рогов спинного мозга (полиомиелит, боковой амиотрофический склероз);
• нарушение иннервации дыхательной мускулатуры (синдром Гийена-Барре, дифтерия и др.);
• нарушение нервно-мышечной передачи (миастения, столбняк, ботулизм);
• поражения дыхательной мускулатуры (например, прогрессирующая мышечная дистрофия, дерматомиозит);
• поражения опорных структур грудной клетки (травма и др.) [8].
В последнее десятилетие показания к назначению психотропных препаратов значительно расширились, и их стали применять для лечения неврозов и нарушений сна, при панических расстройствах, навязчивых состояниях, фобиях, у пациентов с хроническим болевым синдромом, при невралгиях, при лечении язвенной болезни желудка и двенадцатиперстной кишки и ряда других заболеваний. Высокая фармакологическая активность препаратов данной группы, их влияние на весь нейромедиаторный обмен, а также широкое применение – все это обусловливает актуальность проблемы осложнений фармакотерапии.
Большинство антидепрессантов воздействуют не только на молекулярные структуры, непосредственно определяющие их терапевтический эффект (транспортеры моноаминов, моноаминоксидазы, пресинаптические ауто- и гетерорецепторы), но и на постсинаптические рецепторы, что является нейробиологической основой многих побочных реакций [6].
Под влиянием длительного приема антидепрессантов происходит сложная адаптационная перестройка функционирования центральных синапсов: в коре больших полушарий и лимбической системе возрастает чувствительность постсинаптических α1-адренорецепторов и рецепторов серотонина 5-НТ2, наблюдается десенситизация и уменьшается плотность β-адренорецепторов и рецепторов дофамина, снижается количество ГАМКβ-рецепторов [2].
Особенностью психофармакотерапии на современном этапе является широкое применение различных комбинаций психотропных средств. Одновременное использование препаратов различных групп и классов позволяет эффективно воздействовать на разные виды психических нарушений у больных со сложной полиморфной симптоматикой и достигать клинического улучшения в случаях резистентности к монотерапии. Однако при этом вероятность развития побочных эффектов возрастает прямо пропорционально количеству назначенных препаратов. Вследствие снижения уровня метаболизма психотропных средств, которые в основном метаболизируются системой цитохрома P450 в печени, период их полувыведения может увеличиваться в 4 и более раз, что приводит к возникновению токсических эффектов [7]. Кроме того, следует учитывать лекарственные взаимодействия препаратов, под которыми подразумеваются такие явления, когда при одновременном назначении двух или более лекарственных средств развивается эффект, отличающийся от наблюдаемого на фоне применения каждого из них в монотерапии. Результатом взаимодействия чаще всего является изменение интенсивности эффекта препаратов, реже отмечаются качественные изменения в их действии [5]. Например, при сочетанном назначении нейролептиков, антидепрессантов, транквилизаторов, антигистаминных средств наблюдается суммация их седативного действия и повышается угнетающее влияние на ЦНС, в том числе и на дыхательный центр [1, 4, 5, 10-12].
Фармакологическое поражение дыхательного центра проявляется угнетением центральной инспираторной активности, в результате чего развивается гиповентиляция. Последняя характеризуется уменьшением количества воздуха, поступающего из внешней среды в альвеолы за единицу времени. Если потребление кислорода в покое не снижается в той же степени, развивается гипоксемия. Следует отметить важнейшее физиологическое свойство гиповентиляции: она всегда вызывает повышение парциального давления углекислого газа в артериальной крови – РаСО2, и этот показатель имеет большое значение для ее диагностики. При уменьшении альвеолярной вентиляции наполовину уровень РаСО2 повышается в два раза. В норме существует связь между активностью дыхательного центра и стимуляцией центральных и периферических хеморецепторов – при снижении уровня РаО2 и/или повышении РаСО2 увеличивается эфферентная импульсация из дыхательного центра к дыхательной мускулатуре, что ведет к повышению вентиляции и нормализации газового состава крови. При угнетении дыхательного центра происходит нарушение центральной регуляции дыхания, передачи стимулов к дыхательной мускулатуре, что проявляется снижением альвеолярной вентиляции, минутной вентиляции, дыхательного объема и частоты дыхания [9].
Ниже приводим описание клинического случая вторичного гиповентиляционного синдрома на фоне приема комбинации психотропных препаратов.
Пациент Б., 60 лет, поступил в клинику с жалобами на сухой кашель, резко выраженную общую слабость, быструю утомляемость, боли в коленных суставах. Три месяца назад при плановом медицинском осмотре на обзорной рентгенографии органов грудной полости были обнаружены изменения в паренхиме легких в сочетании с двухсторонней прикорневой лимфаденопатией. Вскоре появился сухой кашель. Пациент был госпитализирован в терапевтическое отделение по месту жительства с диагнозом негоспитальной пневмонии. После проведения безуспешной антибактериальной терапии больной был направлен в Национальный институт фтизиатрии и пульмонологии им. Ф.Г. Яновского НАМН Украины для уточнения диагноза.
Пациент на протяжении года наблюдается психиатром по поводу депрессивного расстройства. Получает комбинированную психофармакотерапию – миансерин (30 мг/сут), эсциталопрам (20 мг/сут), гидазепам (100 мг/сут).
На момент госпитализации общее состояние было удовлетворительным. В состоянии покоя наблюдался умеренный цианоз кожи и видимых слизистых оболочек. Над легкими дыхание везикулярное, хрипы отсутствуют. Частота дыхания – 14 в минуту. Артериальное давление – 140/80 мм рт. ст. Частота сердечных сокращений – 84 уд/мин, тоны сердца обычной звучности. Другие органы и системы при физикальном обследовании – без особенностей. Анализы крови и мочи без изменений.
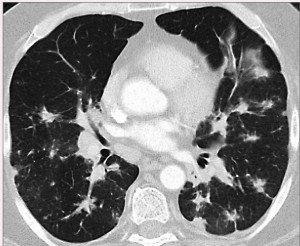
Мультисрезовая компьютерная томография легких – МСКТ (рис. 1): билатерально в легких, преимущественно в средненижних легочных полях, определяются участки усиления и сетчатая деформация легочного рисунка за счет уплотнения междольковых перегородок с участками консолидации паренхимы, группами мелких узелков. Увеличены размеры внутригрудных лимфатических узлов паратрахеальной, парааортальной, бронхопульмональной и бифуркационной групп. Трахея, бронхи проходимы. Заключение: саркоидоз легких и внутригрудных лимфатических узлов.
Показатели функции внешнего дыхания: общая емкость легких (TLC) и жизненная емкость легких (VC) в норме, отмечалось умеренное снижение объема форсированного выдоха за первую секунду (FEV1) – 65,9% от должного и уменьшение FEV1/FVC – 56,2%. Нарушений диффузионной способности легких не выявлено: DLCO – 88,4% от должного.
На основании типичных КТ-признаков, совместимых клинических (сухой кашель) и функциональных (бронхообструкция) данных больному установлен диагноз: саркоидоз органов дыхания II стадии, впервые выявленный.
Назначена терапия метилпреднизолоном в дозе 24 мг/сут в течение 8 недель с последующим снижением дозы до 12 мг/сут к концу третьего месяца (время второго визита).
Вместе с тем требовал объяснения факт отсутствия одышки при наличии выраженного цианоза. Кроме того, с учетом минимального характера расстройств легочной вентиляции причина развития цианоза оставалась неясной.
Больному был выполнен анализ газового состава капиллярной крови, результаты которого указывали на наличие резко выраженной гипоксемии (РаО2 – 50 мм рт. ст.) и умеренной гиперкапнии (РаСО2 – 49 мм рт. ст.). Степень гипоксемии соответствовала показаниям для назначения долговременной оксигенотерапии. При этом минутный объем дыхания (MV), измеренный при проведении спирометрии, практически соответствовал уровню здорового человека (9,7 л/мин), то есть тяжелая гипоксемия и умеренная гиперкапния не вызывали компенсаторной гипервентиляции.
Учитывая тяжелые нарушения газового состава крови, причиной которых не могли быть органические и функциональные изменения в легких, обусловленные саркоидозом, у больного было заподозрено наличие гиповентиляционного синдрома, в связи с чем была проведена диагностическая проба с гипервентиляцией.
Суть этой пробы состоит в переключении пациента с автоматического режима дыхания на произвольный. Больной выполнял дыхательные движения в течение 5 мин по команде инструктора: «Глубокий вдох, глубокий выдох». В результате проведения пробы достигнута полная нормализация содержания кислорода в крови с развитием гипокапнии: РаО2 – 80 мм рт. ст., РаСО2 – 29 мм рт. ст. У пациентов с хроническими заболеваниями легких и нарушениями легочной вентиляции и диффузии проведение пробы с гипервентиляцией, как правило, приводит к ухудшению газового состава крови. Таким образом, результаты пробы позволили заключить, что гиповентиляция у больного обусловлена внелегочными механизмами.
С целью исключения возможных органических изменений в структурах продолговатого мозга, ответственного за центральную регуляцию дыхания, пациенту была проведена магнитно-резонансная томография головного мозга. Заключение: признаки немногочисленных сосудистых очагов в лобных долях, нерезкие явления энцефалопатии. Супратенториальные и субтенториальные структуры головного мозга, в том числе гипофиз, хиазма, подкорковые ядра, краниовертебральная область, – без особенностей.
С помощью метода окклюзионной спирометрии было исследовано функциональное состояние дыхательных мышц – сила дыхательных мышц как вдоха (Pmax In), так и выдоха (Pmax Еx) находилась в пределах нормы.
В ходе исследования функционального состояния дыхательного центра выявлено резкое снижение центральной инспираторной активности (нейрореспираторный импульс составил 18,1% от должного), то есть уменьшение эфферентного потока стимулов к дыхательным мышцам.
Результаты проведенных исследований позволили заключить, что у больного наряду с саркоидозом органов дыхания имеет место вторичный гиповентиляционный синдром с развитием тяжелой гипоксемии и умеренной гиперкапнии. Основной причиной возникновения синдрома является угнетение дыхательного центра, с наибольшей вероятностью обусловленное приемом психотропных препаратов.
Лечащий врач-психиатр ознакомился с результатами обследования и принял решение отменить прием гидазепама и уменьшить дозу миансерина и эсциталопрама.
Через три месяца больной поступил в клинику для контрольного обследования. Состояние пациента значительно улучшилось – исчез кашель, уменьшился цианоз, существенно повысилась физическая активность.
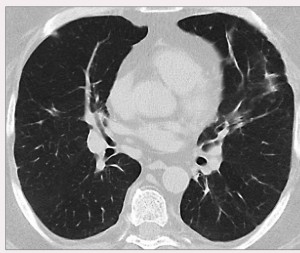
При МСКТ отмечалось почти полное разрешение участков консолидации паренхимы, значительное уменьшение внутригрудных лимфатических узлов (рис. 2).
 Статические объемы легких (TLC, VC) сохранялись на прежнем уровне, отмечалось увеличение минутного объема дыхания (MV – 14,7 л/мин), улучшение бронхиальной проходимости, о чем свидетельствовало увеличение FEV1 (78,2% от должного) и FEV1/FVC (64,1%). Диффузионная способность легких существенно не изменилась (DLCO – 91,6% от должного).
Статические объемы легких (TLC, VC) сохранялись на прежнем уровне, отмечалось увеличение минутного объема дыхания (MV – 14,7 л/мин), улучшение бронхиальной проходимости, о чем свидетельствовало увеличение FEV1 (78,2% от должного) и FEV1/FVC (64,1%). Диффузионная способность легких существенно не изменилась (DLCO – 91,6% от должного).
Степень тяжести гиповентиляционного синдрома значительно уменьшилась – отмечено снижение степени гипоксемии (РаО2 – 61 мм рт. ст.) и гиперкапнии (РаСО2 – 46 мм рт. ст.).
Улучшилось функциональное состояние дыхательного центра – центральная инспираторная активность возросла вдвое (нейрореспираторный импульс составил 37,4% от должного), сохраняясь при этом на достаточно низком уровне.
Больной был выписан из клиники с рекомендациями продолжать терапию кортикостероидами с постепенным снижением дозы препарата до уровня поддерживающей.
Литература
1. Бакумов П.А. Применение транквилизаторов в терапевтической практике / П.А. Бакумов, А.В. Евсеев // Лекарственный вестник. – 2004. – № 2. – С. 9-18.
2. Венгеровский А.И. Лекции по фармакологии для врачей и провизоров: учеб. пособие для мед. вузов / А.И. Венгеровский. – М.: Физико-математическая литература, 2007. – 704 с.
3. Врожденный центральный гиповентиляционный синдром (клинический случай синдрома Ундины) / И.Ф. Острейков [и др.] // Земский врач. – 2012. – № 2 (13). – С. 39-42.
4. Косарев В.В. Поражения легких, обусловленные воздействием лекарственных средств / В.В. Косарев, С.А. Бабанов // Врач. – 2012. – № 11. – С. 9-12.
5. Малин Д.И. Лекарственные взаимодействия психотропных средств (часть І) / Д.И. Малин // Concilium medicum. – 2000. – Т. 2, № 6. – С. 12-22.
6. Марценковский И.А. Клиническая фармакология антидепрессантов: механизмы эффективности и побочных эффектов / И.А. Марценковский // НейроNews: психоневрология и нейропсихиатрия. – 2006. – № 1 (1). – С. 18-24.
7. Мосолов С.Н. Биологические основы современной антипсихотической терапии / С.Н. Мосолов // Российский психиатрический журнал. – 1998. – № 6. – С. 7-12.
8. Пульмонология: национальное руководство / Под ред. А.Г. Чучалина. – М.: ГЭОТАР-Медиа, 2009. – 960 с.
9. Уэст Дж. Патофизиология органов дыхания: пер. с англ. / Дж. Уэст // М.: БИНОМ, 2008. – 232 с.
10. Griffin C.E. Benzodiazepine Pharmacology and Central Nervous System-Mediated Effects / C.E. Griffin [et al.] // The Ochsner Journal. – 2013. – № 13. – P. 214-223.
11. Muzumdar H. Central Alveolar Hypoventilation Syndromes / H. Muzumdar, R. Arens // Sleep Med Clin. – 2008. – № 3 (4). – P.601-615.
12. Therapeutic Update on Drug-Induced Pulmonary Disorders / N. L. Fagan [et al.] // US Pharm. – 1999. – № 7. – P. 3-6.