22 січня, 2017
Влияние дефицита магния на формирование «болезней цивилизации» у детей
 «Болезни цивилизации» и детский возраст. Возможно ли это? К сожалению, да. У детей разного возраста повышаются риски развития таких необычных для педиатрии проблем, как хронический стресс, депрессия, детское и подростковое ожирение, сахарный диабет (СД), метаболический синдром, артериальная гипертензия, эндотелиальная дисфункция, бронхиальная астма, дислипидемия. Этим патологическим состояниям часто сопутствуют гиподинамия и неполноценное питание, в котором зачастую избыточная калорийность сочетается с дефицитом целого ряда эссенциальных нутриентов, в частности магния.
«Болезни цивилизации» и детский возраст. Возможно ли это? К сожалению, да. У детей разного возраста повышаются риски развития таких необычных для педиатрии проблем, как хронический стресс, депрессия, детское и подростковое ожирение, сахарный диабет (СД), метаболический синдром, артериальная гипертензия, эндотелиальная дисфункция, бронхиальная астма, дислипидемия. Этим патологическим состояниям часто сопутствуют гиподинамия и неполноценное питание, в котором зачастую избыточная калорийность сочетается с дефицитом целого ряда эссенциальных нутриентов, в частности магния.
Магний является типичным внутриклеточным катионом (по содержанию в клетке магний занимает второе место после калия), тем не менее 60% общего количества магния содержится в костной ткани, причем 20-30% от этого количества может быть достаточно быстро мобилизовано, и только 39% от общего количества магния содержится в клетках сердца, головного мозга, почек и других органов (Н.Ю. Семиголовский, 2008).
В экстрацеллюлярном пространстве содержится около 1% магниевого депо, в сыворотке крови – лишь часть этого количества. Около 60% сывороточного магния ионизировано, остальная часть связана с протеинами, фосфатами, цитратами. Концентрация магния в цереброспинальной жидкости выше, чем в сыворотке крови.
Магний, вступая в обратимые хелатоподобные связи со многими органическими веществами, обеспечивает возможность метаболизма около 300 ферментов: креатинкиназы, аденилатциклазы, фосфофруктокиназы, NAD+-киназы, K+/Na+-АТФазы, Са-АТФазы и др. Магний участвует в реакциях окислительного фосфорилирования, синтезе белка, циклах мочевины, глюкозы и лимонной кислоты, обмене нуклеиновых кислот и липидов, а также в образовании богатых энергией фосфатов.
Ионы кальция действуют как физиологический антагонист магния, причем магний конкурирует с кальцием на одном и том же канале клеточной мембраны сократительного аппарата.
Под термином «магниевый дефицит» понимают снижение общего содержания магния в организме, тогда как понятие «гипомагниемия» означает снижение концентрации магния в сыворотке (в норме 0,8-1,2 ммоль/л).
Нормальные показатели магния в сыворотке крови не исключают общего дефицита магния и, следовательно, недостаток магния в тканях организма, так как при дефиците магний может высвобождаться из костей, предотвращая снижение его сывороточной концентрации. Поэтому клиническая ценность определения концентрации магния в сыворотке крови и даже в ее форменных элементах ограничена и имеет значимость лишь при наличии гипомагниемии. Умеренной недостаточности магния в организме соответствует его уровень в сыворотке крови 0,5-0,7 ммоль/л, выраженной (угрожающей жизни) – ниже 0,5 ммоль/л.
В клинике дефицит магния проявляется следующими симптомокомплексами:
• психоневрологическим (страх, тревога, депрессия, дисфория, снижение концентрации внимания, повышенная раздражительность, гиперрефлексия, мнестические расстройства, головокружение, нарушение сна, синдром хронической усталости);
• сердечно-сосудистым (ангиоспазм, отклонения артериального давления, электрическая нестабильность миокарда – нарушения сердечного ритма, синдром удлиненного интервала QT на электрокардиограмме);
• висцеральным (бронхо- и ларингоспазм, расстройства стула, боли в животе, тошнота, рвота, пилороспазм);
• мышечно-тетаническим (парестезии, судороги скелетных мышц, увеличение тонуса матки, выкидыши, преждевременные роды).
По современным представлениям, в основе этих нарушений лежат:
• дефицит функционально активных ферментов;
• развитие генерализованного воспаления с последующей системной дисплазией соединительной ткани;
• изменение соотношения Ca/Mg и, как следствие, нарушение электролитного обмена, основных биохимических и физиологических процессов.
Таким образом, дефицит магния – достаточно распространенное состояние, ассоциируемое с широким спектром заболеваний.
Так, магний чрезвычайно важен для нормального функционирования нервной системы. Одним из важнейших эффектов магния является торможение процессов возбуждения в коре головного мозга и связанная с этим реализация наркотического, снотворного, седативного, аналгетического и противосудорожного эффектов. Большинство эффектов характеризует влияние фармакологических средств на состав, распределение магния и активность Mg2+/Ca2+-ATФaз в различных структурах головного и спинного мозга.
Анализаторные функции мозга интегративно связаны с трансмиттерной функцией возбуждающих аминокислот. Учитывая тот факт, что дикарбоновые аминокислоты могут выступать в качестве переносчиков двухвалентных катионов Меn+, можно предположить, что их сдвиги лежат в основе сложных нейрохимических изменений при ряде психических и нервных заболеваний. Экспериментальными исследованиями была доказана роль магния в качестве модулятора эффектов возбуждающих аминокислот в центральной нервной системе (ЦНС). Металл выступает в качестве модулятора аспарагиновой, глутаминовой кислот и глицина. При дефиците магния снижается способность к концентрации внимания и функции памяти. Нейрональная память, реализующаяся через потенциал-зависимый тип N-метил-D-аспартат-чувствительных рецепторов, регулируется магнием. Bruno (1995) выявил у вальпроата магния четкие антидегенеративные эффекты при воздействии на культуру церебральных нейронов. Классикой нейрохимии стало воззрение на магний как на ион с четкими нейроседативными свойствами. Магний – это своего рода природный изоляционный материал на пути проведения нервного импульса. Исследование De Bloc (1999) показало, что синтез ацетилхолина в головном мозге возможен только в условиях наличия ионов магния. Кора головного мозга обладает выраженной реактивностью, поэтому расстройства высшей нервной деятельности сопровождаются не только нарушениями энергетического обмена (интенсивность дыхания, гликолиза окислительного фосфорилирования), но и изменениями трансмембранного транспорта ионов, в первую очередь магния (Чекман, 1992; De Block, 1999). Armand (1998) на большом экспериментальном и клиническом материале показал зависимость выраженности эпилептиформной готовности в коре головного мозга от уровня ионов магния. В исследованиях Chien и соавт. (1999) показано, что дефицит цитозольного магния в нейронах является наиболее ранним и точным маркером апоптоза нервных клеток.
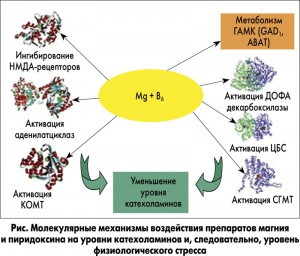
Дефицит магния в организме – обычное явление для людей, подвергающихся хроническим стрессам, страдающих депрессией и аутизмом. Препараты магния и высокие дозы витамина В6 уже более 20 лет составляют основу фармакологического протокола лечения детского аутизма (Rimland, 1998), вегетативной дистонии (Вейн, 2002). Стрессы различной природы (физические, психические) увеличивают потребность в магнии и служат причиной внутриклеточной магниевой недостаточности. Стресс и магниевая недостаточность являются взаимообусловливаемыми процессами, обоюдно усугубляющими друг друга. Состояние острого и хронического стресса ведет к истощению внутриклеточного пула Mg2+ и его потере с мочой, так как в стрессовой ситуации выделяется повышенное количество адреналина и норадреналина, способствующих выведению магния из клеток. Катехоламины воздействуют, в частности, на лизосомы: образующиеся при деградации триацилглицеридов свободные жирные кислоты способствуют связыванию магния и, как следствие, дефициту свободного ионизированного магния. При нормальном снабжении клеток магнием эти катехоламиновые воздействия удается снизить. В результате повышается резистентность к стрессу (рис.).
Отмечено снижение внутриклеточной концентрации магния в нейронах при психических и неврологических состояниях – шизофрении (Раюшкин, 1998), эпилепсии, тике (Quilichini, 2003), гипоталамическом синдроме, головной боли, связанной с патологией регуляции тонуса сосудов мозга (Mazotta, 1999), гипоакузии (Gaspar, 1995), нарушении тонкой моторики, в том числе дисграфии (Lech, 1990).
Низкий уровень ионизированного магния индуцирует эпилептиформную активность мозга (Armand, 1999). По данным О.А. Громовой и соавт., дефицит магния встречается у 70% детей с синдромом дефицита внимания и гиперактивностью и у больных с ранними формами цереброваскулярных заболеваний.
У подростков с девиантными формами поведения дефицит магния, как правило, усугубляется. Этому способствуют такие стрессовые факторы взросления, как переезд из маленьких городов в большие к месту учебы, перенаселение, дискотеки (воздействие мигающего света, очень громкая музыка), начало потребления пива, алкоголя, наркотиков, курение (Спасов, 2000). Применение Магне-В6® у больных с эпилепсией повышает восприимчивость к противосудорожным препаратам (депакин, финлепсин), снижает тяжесть эпилептических приступов. Lech и соавт. (2000) сообщают, что введение препаратов Магне-В6® в комплексную терапию эпилепсии у детей приводит к достоверному снижению частоты и более легкому течению приступов.
Дефицит магния осложняет состояние вследствие черепно-мозговой травмы – ЧМТ (Заваденко, Гузилова, 2006). Включение магния и пиридоксина (раствор для перорального применения Магне-В6® по 10 мл 2-3 раза в сутки) в комплексное лечение ЧМТ у больных с наличием в клинической картине эмоционально-волевых нарушений позволяло добиться стабильных положительных поведенческих реакций уже на 1-2 сутки (Мочалов, 1999). Delva и Lechi (2003) выявили связь между низким уровнем магния в лимфоцитах и повышенным уровнем альдостерона.
Исследования Suter и соавт. (1999) показали, что длительно существующий дефицит магния, особенно на фоне эссенциальной гипертонии, является достоверным фактором риска возникновения острых нарушений мозгового кровообращения. Кровеносные сосуды, снабжающие ткани мозга, чрезвычайно чувствительны к магниевому балансу. При снижении уровня магния возрастает тонус мозговых сосудов, что ведет к ишемическому повреждению, так как, принимая участие в высвобождении энергии, требующейся для функционирования мышечной клетки, и играя одну из главных ролей в сопряжении «сокращение – расслабление» миоцита, магний контролирует работу мышц, в частности миокарда. Акт сокращения миоцита инициируется ионами кальция через активацию взаимодействия между четырьмя белками сократительного аппарата кардиомиоцита с образованием актино-миозиновых комплексов, которые, обладая АТФазной активностью, при наличии кальция и магния гидролизуют АТФ и обеспечивают энергией для сокращения мышцы, то есть систолы сердца. Высвобождаясь из комплекса с АТФ по мере потребления последней, магний способствует выходу кальция из связи с тропонином С, в результате чего прекращается взаимодействие актина и миозина (начало диастолы). Избыточное количество цитоплазматического кальция реабсорбируется против градиента концентрации в полость продольных канальцев саркоплазматического ретикулума (СПР) с помощью Са-насоса под влиянием Са++/Mg++-зависимой АТФазы СПР, а оттуда по градиенту концентрации – в цистерны СПР. Таким образом осуществляется регуляция ионами Mg++ цикла «систола – диастола» как за счет участия в энергетическом обмене, так и вследствие его прямого антагонизма с Са++.
Описанные механизмы играют важную роль в вазодилатирующей активности магния. Вазодилатирующая роль магния опосредуется через синтез циклического аденозинмонофосфата (АМФ), являющегося мощным фактором вазодилатации, ингибирующее влияние на ренин-ангиотензиновую систему и симпатическую иннервацию, а также через усиление натрийуреза вследствие повышения почечного кровотока и активации простациклина.
В эксперименте было показано ингибирующее влияние магния на выброс эндотелина, повышение которого, сопровождая тромбоз коронарной артерии при инфаркте миокарда, приводит к выраженной локальной вазоконстрикции в зоне ишемического риска. В этих исследованиях отмечается гипокоагуляционный эффект магния через инактивацию протромбина, тромбина, фактора Кристмаса, проконвертина и плазменного компонента тромбопластина, а также его антиагрегантное действие на форменные элементы крови (эритроциты, тромбоциты, лейкоциты). Работы Chouinard (1990) показали, что дефицит ионов магния увеличивает активность тромбоксана, что сопровождается повреждением сосудистой стенки.
Среди метаболических функций, проявляющихся на уровне целостного организма, необходимо подчеркнуть его роль в поддержании нормального липидного спектра крови, участие в обеспечении ответа тканей на инсулин и торможение гормона паращитовидной железы. Так, доказано, что длительно существующий дефицит магния снижает чувствительность костной ткани к паратгормону и ухудшает усвоение кальция. Q. Tu и соавт. (2003) отметили увеличение абсорбции Са2+, уровня остеокальцина в крови в ответ на магниевую диету.
Длительный дефицит магния служит фактором для манифестации и развертывания генетически детерминированной программы атеросклероза. В условиях атерогенной диеты недостаток в пище магния способствует прогрессированию склеротического поражения сосудов и наоборот, назначение магния приводит к регрессу гиперхолестеринемии. При дефиците магния в крови повышено содержание триацилглицеридов, хиломикронов, липопротеидов очень низкой и низкой плотности и снижен уровень липопротеидов высокой плотности. Недостаток магния влияет на жирнокислотный состав липидов, снижает активность ферментов системы элонгации и десатурации жирных кислот, блокируя синтез арахидоновой кислоты. Недостаток магния снижает антиоксидантную защиту организма.
A.D. Liese и соавт. (2003) показали, что это свойство магния приобретает особое значение у больных СД и углеводным типом питания в сочетании с высоким уровнем триглицеридов. Снижение чувствительности к инсулину и СД 2-го типа быстрее развиваются на фоне дефицита магния.
Дефицит магния повышает чувствительность организма к инфекции, в том числе к нейроинфекции (Baneijee, 1999; Roberts, 1999). При дефиците магния в организме бактериальный токсический шок происходит более выраженно и микроорганизмы более активно продуцируют β-лактамазу, определяющую устойчивость к воздействию антибиотиков пенициллинового ряда. При дефиците магния золотистый стафилококк усиленно вырабатывает токсин‑1, отвечающий за развитие синдрома токсического шока.
Дефицит магния со стороны ЦНС ведет к повышению активности глубоких сухожильных рефлексов, атаксии, тремору, дезориентации, судорожным состояниям, нистагму, парестезии. При дефиците магния снижается и острота слуха. Потеря слуха, вызванная шумом (свыше 85 децибел), усугубляется дефицитом магния. В исследованиях Gaspar (1995) установлено, что при назначении препаратов магния в дозе 167 мг в течение 2 мес потеря слуха, вызванная шумом, предотвращается. Armez и соавт. (1999) в своих исследованиях доказали, что нормальный уровень магния в организме обеспечивает активность нейромедиаторной аминокислоты глицина, участвующей в таких важных неврологических функциях, как тонкая моторика, точность движений, поддержание позы и ходьба.
Клинически у ребенка при дефиците магния можно выявить специфические нервно-мышечные знаки, связанные с повышенной возбудимостью нервных и мышечных клеток:
• покалывания в области стоп и ладоней (парестезии) – связаны с перевозбуждением чувствительных окончаний;
• гиперактивность: человек не может долго находиться на одном месте, постоянно двигается, даже во сне (синдром «беспокойных ног» связан с повышенной возбудимостью скелетной мускулатуры);
• мышечные контрактуры, судороги (затрудненная реполяризация клеток);
• сердечно-сосудистые нарушения: сердцебиение, тахикардия, аритмия, чувство жара;
• пищеварительные нарушения: поносы, иногда запоры (синдром раздраженной толстой кишки), боли в животе, ощущение комка в горле (спазм в области глотки);
• дыхательные расстройства: учащение дыхательного ритма, чувство удушья (в основном при стрессах);
• расстройства мочеиспускания: частые позывы (поллакиурия), боли в области мочевого пузыря (цисталгии);
• боли в спине и пояснице.
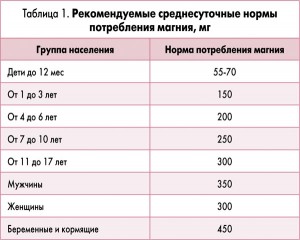
При проведении исследования касаемо потребления магния с продуктами питания в суточном рационе здоровых детей школьного возраста, проживающих в городе и селе, нами было установлено, что в среднем ребенок получает 136,15±8,05 мг (min=52 мг, max=211,9 мг), что составляет 54,4% от нормы (табл. 1) и может быть связано как со снижением потребления (качество продуктов, избыток углеводов и жиров в рационе), так и с повышенными потребностями в период роста и развития.
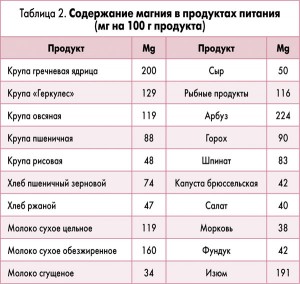
Полноценный рацион способен обеспечить организм ребенка достаточным количеством магния. В таблице 2 представлены продукты с наибольшим содержанием магния, но в небольших количествах магний есть практически во всех продуктах, поэтому составить рациональное меню для ребенка из них несложно. Но это только в том случае, если для рациона используются качественные продукты. В современном рационе крайне мало продуктов с максимальным содержанием магния – нерафинированных злаковых, а также свежих фруктов и овощей. Ситуацию усугубляет система fast food, в основе которой лежит использование рафинированной пищи, избыток сахара и соли, а также продукты, которые выводят магний из организма (например, ортофосфорная кислота, содержащаяся в кока-коле и других лимонадах, различные консерванты). Нельзя исключить негативную роль термической и промышленной обработки продуктов. Поэтому при выраженном алиментарном дефиците, который наблюдается в настоящее время, к сожалению, рационального питания уже недостаточно и требуется медикаментозная коррекция. С этой целью могут успешно применяться препараты, содержащие биоорганические соли магния пидолата, цитрата и лактата в сочетании с пиридоксином, который будет помогать лучше усваиваться магнию в желудочно-кишечном тракте и проникать в клетки организма ребенка.
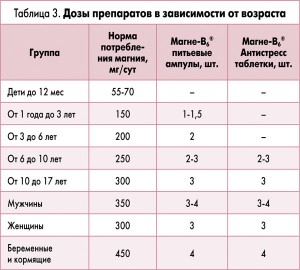
В таблице 3 приводятся дозы препаратов Магне-В6® и Магне-В6® Антистресс с учетом возраста ребенка и в соответствии с рекомендуемой суточной потребностью в магнии (адаптировано по В.А. Тутельян, 2002).
Учитывая постоянный алиментарный дефицит ряда эссенциальных микроэлементов в жизни ребенка, обязательно должны соблюдаться принципы адекватного, рационального, сбалансированного питания, подразумевающего удовлетворение потребности детей в пищевых веществах и энергии, в том числе в макронутриентах (белки, жиры, углеводы) и микронутриентах (минеральные вещества: йод, кальций, магний, железо и др., витамины), в соответствии с возрастными физиологическими потребностями.
Приведенные литературные и собственные данные свидетельствуют о неоспоримой значимости такой проблемы, как дефицит магния в формировании здоровья ребенка и различных патологических состояний в его организме.
Выявленный дефицит магния актуализирует решение вопроса о необходимости проведения курсов фармакоподдержки детей разных возрастных групп препаратами магния.
Список литературы находится в редакции.