8 липня, 2016
Особенности фармакодинамики лекарственных средств у детей: значение фармакогеномики и фармакогенетики

Тенденцией нынешнего времени является гораздо более сложное, чем за всю историю медицины положение врачей. Это обусловлено наличием огромного выбора фармакологических средств для лечения большинства заболеваний, чего не было когда-либо прежде, при этом классы лекарственных препаратов и их механизм действия становятся все более сложными. Определенные трудности возникают в лечении взрослых пациентов, но проблема еще более усугубляется в силу целого ряда обстоятельств в педиатрической популяции, особенно в неонатологии. Так, для многих лекарственных средств фармакокинетический профиль существенно отличается у детей и взрослых. Приверженность к лечению у детей сильно зависит от лекарственной формы препарата, его вкусовых характеристик, внешнего вида и простоты применения, а также особых факторов, связанных с родителями или опекунами (в частности, их убеждений в отношении медикаментозной терапии и представлений о соотношении пользы и риска препаратов). Важно также то обстоятельство, что в педиатрии широко применяется практика назначения лекарственных средств по незарегистрированным показаниям (оff-label) и нелицензированных (unlicensed) фармакологических препаратов.
Данные о безопасности и эффективности большинства применяемых в клинике фармакологических средств изучены у взрослых, и лишь сравнительно небольшое число лекарств, представленных на фармацевтическом рынке, разрешены к применению у детей. Так, в проспективном обсервационном исследовании [1], включавшем педиатрических пациентов в возрасте до 12 лет, госпитализированных в стационар 3-го уровня медицинской помощи, оценивали назначение лекарственных средств off-label. Установлено, что из 1645 прописанных препаратов 1152 (70%) были назначены в режиме off-label по 14 категориям, среди которых наиболее частыми были несоответствие дозировок препаратов и возрастных ограничений пациентов, указанных в инструкции по применению лекарственных средств. Чаще всего не по строгим показаниям назначались препараты для лечения бронхолегочных заболеваний (82%), антибактериальные средства (73%), а также препараты для медикаментозной терапии патологии центральной нервной системы (53%). Показано, что важными предикторами назначения off-label у педиатрических пациентов были возраст до 2 лет (относительный риск (ОР) 1,68 при 95% доверительном интервале (ДИ); р<0,001) и длительность нахождения пациента в стационаре от 6 до 10 дней (ОР 1,91 при 95% ДИ; р<0,001).
Важно отметить, что лекарственные средства для детей являются значительно менее прибыльным сегментом фармацевтического рынка. Большинство выпускаемых лекарственных средств (65-80%) не были протестированы на детях. Производители сталкиваются с экономическими, этическими, техническими и правовыми проблемами при проведении клинических исследований в данной возрастной группе [2]. Однако потребность в безопасных лекарственных средствах для применения в педиатрической практике остается крайне высокой. Показатели фармакокинетики и фармакодинамики лекарственных средств различаются при применении у разных возрастных групп, что может значительно снизить их эффективность и привести к развитию нежелательных реакций при применении у детей. Именно поэтому мы сочли своевременной публикацию тематического раздела, посвященного педиатрическим назначениям. В представленном обзоре рассматриваются вопросы, касающиеся применения лекарственных средств в детской популяции.
Чтобы определить способ применения лекарственных средств у детей, необходимо знать онтогенез всех систем, связанных с воздействием препаратов, и ответную реакцию организма. Основным направлением при разработке препаратов для педиатрических пациентов является установление безопасных и эффективных дозировок лекарственных средств с применением научных методов и рациональных подходов к их использованию (в основном посредством оценки безопасности, эффективности и фармакокинетических исследований в детской популяции). Причем у детей необходимо обеспечить безопасность и эффективность лекарственного средства уже при первом его приеме.
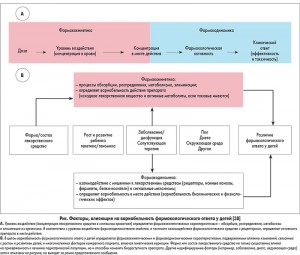
Расчет терапевтической дозы лекарства у детей обычно проводится в соответствии с массой тела или площадью поверхности тела пациента без учета изменения функции органов и систем быстрорастущего организма [3]. Долговременная медикаментозная терапия должна быть индивидуализированной и учитывать особенности фармакокинетических и/или фармакодинамических параметров препарата (рис.). На фармакокинетические параметры препаратов оказывает влияние ряд физиологических (масса и объемы различных тканей и органов организма, скорость кровотока, экскреция почками или с желчью), физико-химических (коэффициент разделения между органом/тканью и кровью) и биохимических факторов (скорость метаболизма лекарственных средств) [4]. Возраст-зависимые изменения абсорбции, распределения, метаболизма и экскреции могут привести к значительным различиям фармакокинетических параметров и реакции на лекарства у новорожденных, детей более старшего возраста и взрослых.
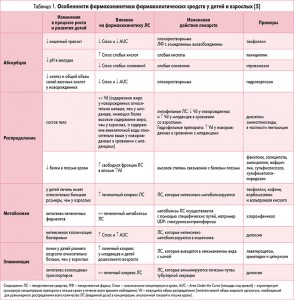
В последние десятилетия при исследовании фармакологических свойств лекарственных средств приоритет отдавался изучению фармакокинетики, а фармакодинамике уделялось меньшее внимание, в частности, в педиатрической популяции, включая ее возрастные особенности. Фармакокинетика лекарственных средств у детей более подробно освещена нами ранее [3]. Суммарно различия фармакокинетических свойств лекарственных средств у детей и взрослых представлены в таблице 1.
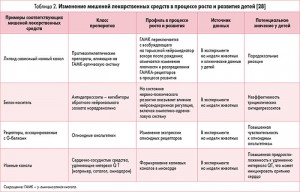
Ряд важных мишеней лекарственных средств не описаны у детей, в некоторых случаях информация о фармакодинамике препарата основывается на экспериментальных данных, реже – на исследованиях у взрослых [6]. В то же время данные фармакодинамики имеют большое значение в понимании возрастных особенностей действия и в разработке эффективных лекарственных средств для детей, особенно новорожденных [7]. Так, в эксперименте на животных установлено, что максимальная экспрессия ряда рецепторов отмечается сразу после рождения [8].
Фармакодинамика
Фармакодинамика – это раздел фармакологии, изучающий биохимические и физиологические эффекты препарата и механизмы его действия на организм человека [9]. При этом свойства и способ введения лекарственного средства определяют возможность воздействия лишь в определенной части тела (ткани-мишени). Терапевтический эффект достигается в результате взаимодействия лекарственного средства с органом-мишенью. Однако влияние на другие клетки, ткани или органы способно приводить к появлению нежелательных побочных реакций [10]. Возраст ребенка, а также генетические вариации, наличие патологии и нутрициональный статус могут оказывать влияние на фармакодинамику (и фармакокинетику) и общий клинический ответ на препарат.
Фармакодинамика изучает такие показатели, как мишени к лекарственным средствам (рецепторы, ионные каналы, ферменты, транспортные системы, гены), сигнальные механизмы, эффекторы и химическое взаимодействие [7]. У детей в зависимости от возраста отличается количество рецепторов, их локализация в различных тканях и, соответственно, возможность связывания с препаратом, что оказывает влияние на выраженность основного фармакологического эффекта. Следует подчеркнуть то обстоятельство, что доказанная эффективность у взрослых не гарантирует столь же благоприятный эффект и профиль безопасности у детей, подтверждая необходимость проведения клинических исследований в педиатрической популяции для оценки эффективности и токсичности лекарственного средства. Например, предполагается, что больший кислотосупрессивный эффект лансопразола у детей раннего возраста обусловлен снижением элиминации препарата [11]. Продемонстрировано, что у детей младшего возраста отмечается более высокая гепатотоксичность вальпроевой кислоты, связанная с повышенным образованием гепатотоксических метаболитов [12].
Наряду с фармакокинетическими данными фармакодинамика позволяет объяснить связь между введенной дозой препарата и наблюдаемым ответом и занимает центральное место при определении оптимальных режимов дозирования [13]. Так, результаты клинических исследований [14] позволили установить, что у детей препубертатного возраста отмечается усиленный фармакологический ответ на стандартную дозу варфарина (антикоагулянт непрямого действия, в течение многих лет применяемый в педиатрии) по сравнению с более старшими детьми (12-18 лет) и взрослыми пациентами (37-76 лет). Окончательный механизм большей чувствительности к варфарину остается неизвестным. В ряде проспективных исследований [15] установлено, что при использовании варфарина у детей существуют определенные трудности, в частности, пациентам в возрасте до 12 мес требуются относительно большие дозы для достижения и поддержания международного нормализованного отношения (МНО) в необходимом терапевтическом интервале, более быстрая коррекция терапии при изменении МНО для предупреждения передозировки препарата, более частый лабораторный контроль при подборе дозы, а затем более редкий – при ее поддержании. Нестабильность фармакодинамики препарата, множественные лекарственные взаимодействия, зависимость от диеты пациента требуют более тщательного контроля терапии и нередко коррекции дозы. Кроме того, в связи с отсутствием детских дозировок при низкой массе тела пациента, а также повышенной чувствительности ребенка к данным препаратам, возможно, возникнет необходимость в дроблении дозы препарата и даже его аптечной навеске.
Другим примером является изменение иммуносупрессивного действия циклоспорина в зависимости от возраста детей. Так, в группе детей до 1 года отмечен более выраженный иммуносупрессивный эффект циклоспорина в сравнении со старшими детьми и взрослыми, что, как предполагается, связано с определенной незрелостью иммунной системы у детей и оказывает влияние на терапевтическую эффективность различных дозировок препарата [16]. Кроме того, метаболизм циклоспорина зависит от возраста. Показано, что клиренс циклоспорина у детей в 1,5-2 раза выше, а период полувыведения меньше в сравнении со взрослыми лицами, что обусловливает применение более высоких дозировок циклоспорина в педиатрической практике, чем у взрослых пациентов [17, 18]. Данных об изменении фармакодинамики лекарственных средств в растущем и развивающемся организме ребенка в настоящее время недостаточно. Имеющиеся данные касаются экспрессии рецепторов органов-мишеней к лекарственным препаратам, тесно связанной с возрастом. Вместе с тем в этом направлении необходимы дальнейшие исследования, включая проведение клинических испытаний.
Рецепторы лекарственных средств
С молекулярно-биологической точки зрения термин «рецептор» обозначает белковую структуру, которой присуща способность специфически распознавать природный агонист, активироваться под его воздействием и вызывать передачу сигнала в клетку или между внутриклеточными компартментами [19].
Рецепторы фармакологических средств представляют собой биологические компоненты, локализованные на клеточной мембране (мембранные рецепторы) или в цитоплазме (внутриклеточные рецепторы), селективно связывающиеся с сигнальными молекулами лекарств и инициирующие фармакологический ответ [20]. Установлено 4 основных типа рецепторов.
1. Рецепторы, сопряженные с ионными каналами, обеспечивающие проницаемость мембран для ионов. Так, никотиновые холинорецепторы (Н-холинорецепторы) усиливают проницаемость мембран для ионов Na+, K+, Ca2+, вызывая деполяризацию и возбуждение функции клеток [21]. Другим примером являются рецепторы ГАМКА, при активации которых отмечается изменение проницаемости плазматических мембран для ионов Cl–, следствием чего является деполяризация (пресинаптическое торможение) или гиперполяризация (постсинаптическое торможение) [22].
2. Рецепторы, ассоциированные с G-белками (М-холинорецепторы, адренорецепторы, гистаминовые рецепторы). С их помощью осуществляется опосредованное через G-белки влияние на ионные каналы и на активность ферментов, регулирующих образование вторичных мессенджеров (циклические мононуклеотиды: циклический аденозинмонофосфат, циклический гуанозинмонофосфат, инозитолтрифосфат, диацилглицерин и др.) [23]. G-белки регулируют активность протеинкиназ, обеспечивающих внутриклеточное фосфорилирование важных регуляторных белков и формирование разнообразных эффектов.
3. Рецепторы, сопряженные с ферментами. Они связаны с плазматической мембраной клеток, фосфорилируют белки клеток и изменяют их активность. К ним относятся рецепторы к инсулину, лимфокинам, эпидермальному и тромбоцитарному факторам роста.
4. Рецепторы – регуляторы транскрипции ДНК. Они являются внутриклеточными и представляют собой растворимые цитозольные или ядерные белки. Функция рецепторов – активация или ингибирование транскрипции генов. К таким рецепторам относятся: суперсемейство рецепторов с внутренней тирозинкиназной активностью, рецепторы для трансформирующего фактора роста β, рецепторы, сопряженные с JAK-киназами и другими типами тирозинкиназ, рецепторы с гуанилат-циклазной активностью [24].
Первые три типа относятся к мембранным рецепторам и локализованы на цитоплазматической мембране, а четвертый – к цитозольным рецепторам.
Рецепторы, обеспечивающие проявление действия определенных веществ, называют специфическими. Так, рецепторы с тирозинкиназной активностью взаимодействуют с гормонами (инсулин, инсулиноподобный фактор роста) и паракринными/аутокринными регуляторами (тромбоцитарный фактор роста, эпидермальный фактор роста) [25]. В возрасте 1-3 лет полностью завершается формирование и созревание рецепторного клеточного аппарата, в связи с чем на фоне разбалансированности различных звеньев (например, завершение формирования α- и β-адренорецепторов происходит с большим разрывом во времени) высок риск развития извращенных эффектов и характерен неадекватный ответ в виде гиперреакции на введение адреномиметиков.
Результаты экспериментальных исследований на моделях животных позволили установить преобразование экспрессии опиоидных рецепторов в перинатальном периоде. В частности, определенные типы рецепторов более распространены сразу после рождения, а другие появляются у детей постарше [26]. Модификация чувствительности рецепторного звена наблюдается в период полового созревания. Так, чувствительность μ-рецепторов к опиатам возрастает, и для достижения адекватного анальгетического эффекта требуются меньшие дозы наркотических анальгетиков наряду с более быстрым формированием наркотической зависимости. Кроме того, снижается чувствительность М-холинорецепторов, гистаминовых рецепторов; выявлена высокая связывающая способность альбуминов крови к большинству ксенобиотиков [27] (табл. 2).
Фармакогеномика и фармакогенетика
Большая часть данных по фармакогеномике и фармакогенетике получена в исследованиях у взрослых, что создает определенные трудности при их интерпретации в соответствующих клинических рекомендациях для детей. В то же время разрабатываются подходы к накоплению такой информации в детской популяции. Так, для уточнения взаимосвязи хорошо известных неблагоприятных побочных реакций на лекарственные средства с генетическими мутациями данные по фармакогеномике, как правило, сопоставляются с информацией, полученной как от Службы фармаконадзора, так и по результатам исследования геномных ассоциаций (Genome Wide Association Stadies, GWAS). Кроме того, такую информацию также можно получить при проведении специально спланированных исследований с применением панелей, предназначенных для изучения наиболее вероятных генов [29].
Основной задачей исследования геномных ассоциаций является выявление новых терапевтических мишеней и, в зависимости от генетических вариантов, – прогнозирование ответа на медикаментозное лечение [30]. Среди примеров исследований геномных ассоциаций в педиатрической популяции следует отметить болезнь Кавасаки, острый лимфобластный лейкоз, раннее начало бронхиальной астмы и хронические воспалительные заболевания кишечника у детей [30]. Вместе с тем существуют определенные трудности при интерпретации исследований геномных ассоциаций. Так, анализ статистической значимости в исследованиях с определением десятков тысяч генов требует достаточного опыта в области генетико-статистического анализа, позволяющего извлечь наиболее значимый паратипический информационный «шум», превышающий генотипический «сигнал» [31]. Еще одна проблема – необходимость повторения результатов и функциональное подтверждение, позволяющие интерпретировать основные механизмы рассматриваемых эффектов [32]. Это особенно важно при разработке подходов к проведению интервенционных или терапевтических вмешательств. В этой связи специально спланированные исследования, по-видимому, позволят подтвердить известные механизмы, и, возможно, выявить ранее неизвестные ассоциации. В качестве примера можно привести определение генетических вариантов, связанных с цисплатин-индуцированной потерей слуха у детей с раком [33]. В этом направлении в педиатрической популяции необходимы дальнейшие исследования, включающие данные изучений геномных ассоциаций, которые позволят создать столь необходимую доказательную базу.
Исследования по оценке нежелательных лекарственных реакций при конкретных генетических полиморфизмах могли бы быть особенно ценными с позиций их прогнозирования. Так, у лиц с повышенной скоростью метаболизма фермента CYP2D6 низкие дозы кодеина могут оказаться токсичными. Известен случай, когда в Канаде младенец умер после получения высокой дозы морфина через грудное молоко, при этом мать принимала кодеин в качестве обезболивающего [34]. Опубликованы данные об интоксикации и/или смерти после применения кодеина у детей с повышенной скоростью метаболизма фермента CYP2D6 [34а].
Несмотря на многообещающие перспективы изучения вариабельности ответа на медикаментозную терапию, фармакогеномика и фармакогенетические исследования также создают целый ряд проблем. Среди них – важные и сложные этические вопросы, связанные с исследованиями по сбору генетических данных у детей. Исследователи должны заручиться согласием родителей или опекунов на участие детей в любом генетическом исследовании, в том числе на получение биологических образцов, даже при проведении долгосрочных исследований по изучению риска неблагоприятных событий, когда ребенок достигнет зрелого возраста. Также существует целый ряд технических проблем, например с получением биологических образцов при проведении педиатрического исследования. Кроме того, некоторые системы наблюдения побочных эффектов лекарственных средств основаны на спонтанных сообщениях и содержат недостаточно данных для проведения соответствующего исследования. Зачастую количество включенных в исследования участников контрольной группы недостаточно для определения генетических различий, а за основу контроля берутся данные взрослой популяции или других исследований, которые не могут быть непосредственно сопоставимы с детьми [34].
Исследования последних лет были сфокусированы на оценке экспрессии генов или фенотипа без изменений в последовательности ДНК. Многие из этих изменений, как предполагается, обусловлены метилированием ДНК или модификацией гистонов, которые могут влиять на экспрессию генов без изменений в его кодирующей последовательности (эпигенетические изменения) [35]. Например, появляются работы, в которых предполагается, что различия в характере метилирования ДНК в клетках имеют большое значение для роста и развития плода [36]. В то же время эпигенетика является относительно новой областью, и клинические последствия медикаментозной терапии у детей в основном остаются неизученными. Так, в настоящее время большая часть генетических исследований проводятся на моделях животных. Существуют определенные трудности в широкомасштабном изучении согласованности генотипов и фенотипов; имеющиеся исследования были проведены у взрослых, и поэтому не отражают генотипических (фенотипических) различий в педиатрической популяции. Продолжение этой работы для детей позволит продемонстрировать, как такие изменения влияют на клинически значимые результаты, в том числе ответ на лекарственную терапию. Несмотря на то что в ряде исследований отмечена связь между полиморфизмом генов и эффектом лекарственных средств или фенотипическим ответом у детей, в рекомендациях такая информация не указывается. Чтобы устранить этот пробел, Консорциум по имплементации клинической фармакогенетики работает над созданием руководящих принципов, позволяющих учитывать результаты генетических исследований при назначении конкретных препаратов. Для интеграции фармакогеномики в клиническую практику потребуется связать определенные генотипы с соответствующими фенотипами и, наконец, – учесть эти данные в клинических рекомендациях [37].
Заключение
Применение лекарственных средств в педиатрической практике должно проводиться с осторожностью, необходимо учитывать физиологические особенности различных возрастных групп. Для проведения эффективной и безопасной фармакотерапии у детей обязательным условием является фундаментальное понимание возрастных особенностей фармакокинетики и фармакодинамики лекарственных средств. Фармакотерапия заболеваний детского возраста должна проводиться с обязательным участием клинического фармаколога, владеющего знаниями в области фармакокинетики, фармакодинамики, а также об эффективности и безопасности лекарственных средств.
Литература
1 Saiyed М.М., Lalwani Т., Rana D. Off-Label Medicine Use in Pediatric Inpatients: A Prospective Observational Study at a Tertiary Care Hospital in India // Int J of Ped. – V. 2014 (2014), Article ID415815, 6 p. http://dx.doi.org/10.1155/2014/415815
2 Маличенко В.С., Маличенко С.Б., Явися А.М. Роль международно-правовых механизмов регулирования обращения лекарственных средств в обеспечении эффективной онкологической помощи // Российский онкологический журнал. –2014. – № 1.
3. Беловол А.Н., Князькова И.И. Клиническая фармакология лекар-ственных средств у детей: особенности фармакокинетики // Здоров’я України. Тематичний номер «Педіатрія». – 2015. – № 3.
4. Василевский И.В. Клиническая фармакология и педиатрическая практика // Международные обзоры: клиническая практика и здо-ровье. – 2014. – № 6. – С. 5-23.
5. Batchelor H.K., Marriott J.F. Paediatric pharmacokinetics: key considerations // Br J Clin Pharmacol. – 2015. – Mar. – 79 (3): 395-404.
6. Use of medicines in children – St. James’s Hospital // Материалы сайта www.stjames.ie
7. Tayman C., Rayyan M., Allegaert K. Neonatal Pharmacology: Extensive Interindividual Variability Despite Limited Size // J Pediatr Pharmacol Ther. – 2011. – Jul.-Sep. – 16 (3): – 170-184.
8. Funk R.S., Brown J.T., Abdel-Rahman S.M. Pediatric pharmacokinetics: Human development and drug disposition. Pediatric Clinics of North America. – 2012. – 59 (5). – 1001-1016.
9. Клиническая фармакология: национальное руководство / под ред. Ю.Б. Белоусова, В.Г. Кукеса, В.К. Лепахина, В.И. Петрова. – М.: ГЭОТАР-Медиа, 2009. – 976 с.
10. Беловол А.Н., Князькова И.И., Фролова Т.В. К вопросу о коррекции факторов риска сердечно-сосудистых заболеваний у детей и подростков // Здоров’я України. Тематичний номер «Педіатрія». – 2012. – № 3. – С. 17, 19.
11. Kearns G.L., Winter H.S. Proton pump inhibitors in pediatrics: relevant pharmacokinetics and pharmacodynamics // J Pediatr Gastroenterol Nutr. – 2003. – Nov.-Dec. – 37. – Suppl. 1: S52-9.
12. Anderson G.D. Children versus adults: pharmacokinetic and adverse-effect differences // Epilepsia. – 2002. – 43. – Suppl. 3: 53-9.
13. Allegaert К., van de Velde M., van den Anker J. Neonatal clinical pharmacology // Paediatr Anaesth. – 2014. – Jan. – 24 (1): 30-8.
14. Takahashi H., Ishikawa S., Nomoto S. еt al. Developmental changes in pharmacokinetics and pharmacodynamics of warfarin enantiomers in Japanese children // Clin Pharmacol Ther. – 2000. – Nov. – 68 (5): 541-55.
15. Bonduel M.M. Oral anticoagulation therapy in children // Thromb. Res. – 2006. – 118. – 85-94.
16. Marshall J.D., Kearns G.L. Developmental pharmacodynamics of cyclosporine // Clin Pharmacol Ther. – 1999. – Jul. – 66 (1): 66-75.
17. Drosos A.A., Voulgari P.V., Katsaraki A. et al. Influence of cyclosporin A on radiological progression in early rheumatoid arthritis patients: a 42-month prospective study // Rheumatol. Int. – 2000. – V. 19, № 3. – Р. 113-118.
18. Алексеева Е.И., Шахбазян И.Е., Валиева С.И. и др. Опыт пятнадцатилетнего применения циклоспорина в детской ревматологии // Вопросы современной педиатрии. – 2008. – № 6. – С. 104-117.
19. Humphrey P.P.A., Barnard E.A. International Union of Pharmacology. XIX. The IUPHAR receptor code: a proposal for an alphanumeric classification system. Pharmacol Rev. – 1998. – 50. – 271-277.
20. Danhof M., de Jongh J., de Lange E.C. еt al. Mechanism-based pharmacokinetic-pharmacodynamic modeling: biophase distribution, receptor theory, and dynamical systems analysis // Annu Rev Pharmacol Toxicol. – 2007. – 47. – 357-400.
21. Changeux J. -P., Edelstein S.J. Allosteric mechanisms in normal and pathological nicotinic acetylcholine receptors. Curr. Opin. Neurobiol. – 2001. – 11. – 369-377.
22. Тюренков И.Н., Перфилова В.Н. ГАМКА-рецепторы: структура и функции // Экспериментальная и клиническая фармакология. – 2010. – Т. 73, № 10.
23. Крутецкая З.И., Лебедев О.Е., Курилова Л.С. Механизмы внутри-клеточной сигнализации. – С. -Пб.: Изд-во С.‑Петербург. ун-та. – 2003. – 208 с.
24. Черников М.В. Клеточные рецепторы: современный взгляд на клас-сификацию и архитектуру // Бюл. Волгоградского научного центра РАМН. – 2009. – № 1. – С. 13-16.
25. Weinman E.J., Hall R.A., Friedman P.A. et al. The association of nherf adaptor proteins with g protein–coupled receptors and receptor tyrosine kinases // Annual Review of Physiology. – 2006. – Vol. 68: 491-505.
26. Neville K.A., Becker M.L., Goldman J.L., Kearns G.L. Developmental pharmacogenomics. Paediatric Anaesthesia. – 2011. – 21 (3). – 255-265.
27. Лозинский Е.Ю., Елисеева Е.В., Шмыкова И.И., Галанова Ю.Д. Особенности клинической фармакологии детского возраста // Pacific Medical Journal. – 2005. – № 3. – Р. 14-18.
28. Mulla H. Understanding developmental pharmacodynamics: Importance for drug development and clinical practice // Paediatric Drugs. – 2010. – 12 (4). – 223-233.
29. Carleton B. Demonstrating utility of pharmacogenetics in pediatric populations: Methodological considerations // Clin Pharmacol & Ther. – 2010. – 88 (6). – 757-759.
30. Neville K.A., Becker M.L., Goldman J.L., Kearns G.L. Developmental pharmacogenomics // Paediatric Anaesthesia. – 2011. – 21 (3). – 255-265.
31. Martin L.J., Gao G., Kang G. et al. Improving the signal-to-noise ratio in genome-wide association studies // Genetic Epidemiology. – 2009. – 33. – Suppl. 1. – S29-32.
32. Stranger B.E., Stahl E.A., Raj T. Progress and promise of genome-wide association studies for human complex trait genetics // Genetics. – 2011. – 187 (2). – 367-383.
33. Pussegoda K., Ross C.J., Visscher H. et al. Replication of TPMT and ABCC3 genetic variants highly associated with cisplatin-induced hearing loss in child-ren // Clin Pharmacol & Therap. – 2013. – 94 (2). – 243-251.
34. Carleton B. Demonstrating utility of pharmacogenetics in pediatric populations: Methodological considerations // Clin Pharmacol & Therap. – 2010. – 88 (6). – 757-759.
34а. Codeine in normal doses to breastfeeding mothers can in rare cases cause serious adverse reactions in the infant. Internet Document. Swedish Med.l Products Agency. – Dec. 2006 (www.lakemedelsverket.se).
35. Лебедев И.Н. Эпимутации импринтированных генов в геноме человека: классификация, причины возникновения, связь с наследственной патологией / И.Н. Лебедев, Е.А. Саженова // Генетика. – 2008. – Т. 44, № 10. – С. 1356-1373.
36. Banister C.E., Koestler D.C., Maccani M.A. et al. Infant growth restriction is associated with distinct patterns of DNA methylation in human placentas // Epigenetics. – 2011. – 6 (7). – 920-927.
37. Caudle K.E., Klein T.E., Hoffman J.M. et al. Incorporation of pharmacogenomics into routine clinical practice: The Clinical Pharmacogenetics Implementation Consortium (CPIC) Guideline Development Process // Current Drug Metabolism. – 2014. – 15 (2). – 209-217.
38. Improving medicines for children in Canada / The Expert Panel on Therapeutic Products for Infants, Children, and Youth. – 2014. – 268 p.