8 липня, 2016
Спонтанный пневмоторакс у детей: диагностика и тактика ведения
Пневмотораксом называют наличие воздуха или газа в плевральной полости (пространстве между висцеральной и париетальной плеврой). Пневмоторакс может приводить к нарушению вентиляции легких и оксигенации крови. Клинические последствия пневмоторакса зависят от степени коллапса легкого на пораженной стороне. Если пневмоторакс существенный, это может приводить к смещению органов средостения и нарушать системную гемодинамику. Воздух может проникать в плевральную полость из окружающей среды через дефект грудной стенки (например, вследствие травмы) или из легочной паренхимы (при повреждении висцеральной плевры).
Различают следующие виды пневмоторакса:
• спонтанный пневмоторакс – развивающийся внезапно, без очевидной причины (первичный, то есть возникающий без предшествующей истории легочных заболеваний, и вторичный, который может возникать на фоне целого ряда заболеваний с поражением легочной паренхимы);
• ятрогенный (вследствие диагностических или лечебных манипуляций, приводящих к повреждению плевры и умышленному или ненамеренному попаданию воздуха в плевральную полость);
• травматический (вследствие проникающего ранения грудной клетки или тупой травмы грудной клетки с разрывом легкого);
• напряженный (жизнеугрожающее состояние, характеризующееся нарастающим давлением воздуха в плевральной полости из-за наличия клапанного механизма проникновения воздуха, что приводит к существенному смещению органов средостения и нарушению не только вентиляции легких, но и гемодинамики);
• пневмомедиастинум (наличие воздуха или газа в средостении, возникающее спонтанно или вследствие травмы/манипуляций).
Первичный спонтанный пневмоторакс (ПСП) – относительно редкое состояние в педиатрической
практике. Тем не менее среди всех случаев нетравматического пневмоторакса он составляет 80-85%.
По данным литературы, ежегодная заболеваемость ПСП в общей популяции составляет 5-10 случаев на 100 тыс. населения. В США среди детей и подростков частота ПСП составляет 4 случая на 100 тыс. населения среди лиц мужского пола и 1,1 случая на 100 тыс. среди лиц женского пола. Высокая частота распространения отмечается у молодых людей в возрасте от 10 до 30 лет и редко старше 40. Пик заболеваемости приходится на возраст от 16 до 24 лет [12, 13]. Курение достоверно повышает риск возникновения пневмоторакса примерно в 20 раз [1, 2, 5].
Основным отличием ПСП от вторичного является то, что последний возникает на фоне хронического обструктивного заболевания легких и связанной с ним эмфиземы легких. Кроме того, вторичный пневмоторакс может развиться у больных с интерстициальными заболеваниями легких (гистиоцитоз Х и лейомиоматоз), острыми инфекционными деструкциями легких, бронхиолитом, первичными и метастатическими опухолями, тромбоэмболией, легочным эндометриозом, туберкулезом и муковисцидозом. По данным литературы, вторичный спонтанный пневмоторакс встречается не более чем в 15% случаев [2, 5].
Патофизиология. Обычно у пациентов с ПСП не выявлялась явная клинически значимая легочная патология, что и отображает название этого состояния – «спонтанный». Хотя у 76-100% таких пациентов при проведении инструментальных методов обследования (видеоторакоскопия, открытая торакотомия) обнаруживаются субплевральные буллы [1, 2]. Буллами легкого принято считать наполненный воздухом тонкостенный пузырь более 1 см в диаметре, не имеющий эпителиальной выстилки. Буллы могут быть множественными и одиночными, иметь разную форму и размер. Считается, что причиной развития булл являются локальные нарушения проходимости бронхиол и мелких бронхов с образованием в них клапанного механизма в результате рубцовых изменений. При этом рубцовые изменения приводят к формированию бронхиального клапана в направлении альвеол. Со временем происходит постепенное растягивание альвеол, атрофия перегородок между ними и формирование напряженных тонкостенных полостей [2]. Буллы могут быть стабильными или достигать больших размеров. Чаще всего буллы являются проявлениями системных заболеваний: дисплазии соединительной ткани, недостаточности α1-антитрипсина. В связи с этим спонтанный пневмоторакс часто наблюдается при таких наследственных заболеваниях, как синдром Элерса-Данлоса, синдром Марфана. Таким образом, разрыв субплеврально расположенных булл в легком является основной причиной возникновения данного заболевания. Механизм формирования булл остается до конца неясным. При спонтанном пневмотораксе происходит повышение внутриплеврального давления, которое способствует полному или частичному сдавлению легкого (снимок). Значительный первичный спонтанный пневмоторакс приводит к резкому уменьшению жизненной емкости легких и увеличению альвеолярно-артериального градиента по кислороду, в результате чего развивается гипоксемия различной степени тяжести. Кроме того, гипоксемия является результатом нарушения вентиляционно-перфузионных отношений и появления шунта справа налево, а тяжесть этих расстройств зависит от величины пневмоторакса.
Следует заметить, что кроме анатомических предпосылок для возникновения пневмоторакса необходимо еще и воздействие так называемых триггерных факторов. К ним относятся все случаи резкого повышения внутригрудного давления: сильный кашель, подъем тяжестей, игра на духовых инструментах, резкие движения, при которых происходит резкое повышение внутригрудного давления, что приводит к разрыву булл.
Классификации спонтанного пневмоторакса в значительной степени условны и имеют больше педагогическую значимость. В публикациях встречаются классификации различной степени подробности, однако принципиальных различий между ними мы не отметили [1, 2]. Для клинической практики большее значение имеет разделение пневмоторакса на напряженный и ненапряженный, а также распространенность пневмоторакса. Таким образом, клиницисту следует ориентироваться на степень коллапса легкого (по данным лучевых методов исследования), проявления дыхательной недостаточности (клинически) и определение газового состояния крови.
Классификация первичного спонтанного пневмоторакса
1. По распространенности:
– полный коллапс легкого;
– неполный коллапс легкого;
– ограниченный пневмоторакс.
2. По кратности:
– первичный;
– повторный (рецидивирующий).
Осложнениями спонтанного пневмоторакса являются пневмомедиастиум и подкожная эмфизема, которые встречаются редко.
Клиническая картина. Подавляющее большинство случаев ПСП возникают в покое. Воздействие триггерных факторов (физическая нагрузка, пение, крик и др.) обычно отмечают за 1-2 суток до возникновения заболевания. Основной жалобой у пациентов со спонтанным пневмотораксом является боль в грудной клетке со стороны расположения пневмоторакса. Интенсивность боли может варьировать от минимальной до выраженной, первоначально пациенты ее описывают как острую, а позднее – как ноющую или тупую. Обычно боль в грудной клетке исчезает в первые двое суток, даже если пневмоторакс остается нелеченным. Боль зачастую локализуется в передней части грудной клетки, при значительных объемах пневмоторакса может иррадиировать в шею или спину. Редко отмечается иррадиация боли в эпигастральную область.
Вторым по значимости симптомом является одышка, которая напрямую коррелирует со степенью коллапса легкого. Только при значительном объеме пневмоторакса пациенты жалуются на одышку в покое, в остальных случаях одышка появляется при выполнении физической нагрузки или подъеме по лестнице. Во всех случаях у пациентов наблюдается тахипное, таким образом, нормальная частота дыхания исключает наличие спонтанного пневмоторакса у пациента.
В 62% случаев наблюдается редкий сухой кашель, усиливающийся при глубоком вдохе или физической нагрузке. Появление продуктивного кашля и мокроты с прожилками крови, как правило, указывает на значительный объем пневмоторакса и коллапс легкого.
Большинство пациентов со спонтанным пневмотораксом имеют характерный фенотип (признаки дисплазии соединительной ткани): высокий рост, астеническое телосложение, слабо выраженное развитие подкожно-жировой клетчатки. По результатам собственных наблюдений, мальчики составляют 96% пациентов со спонтанным пневмотораксом.
Симметричность грудной клетки и участие ее сторон в акте дыхания также являются важными диагностическими критериями. При наличии пневмоторакса более чем в 15% случаев отмечается уменьшение объема грудной клетки на стороне поражения и возникновение функционального (компенсаторного) сколиоза. Пальпация грудной клетки безболезненна.
При наличии объема поражения более 1/2 гемиторакса наблюдается уменьшение экскурсии грудной клетки на пораженной стороне, а также отмечается коробочный оттенок перкуторного звука, ослабление голосового дрожания и дыхания. Важное диагностическое значение имеет тахикардия, которая наблюдается у подавляющего количества пациентов со спонтанным пневмотораксом.
Цианоз у пациентов со спонтанным пневмотораксом отмечается крайне редко и указывает на полный коллапс легкого у детей раннего возраста или же на напряженный пневмоторакс. Увеличение объема грудной клетки на стороне поражения, расширение межреберных промежутков и уменьшение дыхательной экскурсии легкого, а также тимпанит и смещение границ средостения в противоположную сторону являются симптомами напряженного пневмоторакса. Смещение средостения приводит к сдавлению нижней полой вены и к значительному уменьшению венозного возврата. Без соответствующей коррекции напряженный пневмоторакс быстро приводит к кардиореспираторному коллапсу. Для диагностики данного состояния рентгенологическое исследование грудной клетки, как правило, не требуется. Необходима экстренная торакотомия, промедление с проведением которой может привести к остановке сердца.
Следует отметить, что у пациентов с небольшим пневмотораксом, занимающим менее 15% от объема гемиторакса, физикальная симптоматика обычно отсутствует.
Таким образом, к ведущим диагностическим критериям спонтанного пневмоторакса относятся:
– боль в грудной клетке (специфичность – 57%, чувствительность – 79%);
– одышка (специфичность – 43%, чувствительность – 98%);
– аускультативные изменения при их наличии (специфичность – 98%, чувствительность – 90%).
Наличие одновременно всех трех симптомов с высокой вероятностью предполагает пневмоторакс в 99% случаев, а при наличии только одышки и аускультативных изменений вероятность пневмоторакса также велика – 98%. Сочетание боли в груди и одышки характерно для пневмоторакса, но менее специфично и отмечается в 40% случаев. Изолированный симптом одышки встречается при пневмотораксе только в 12% случаев, а изолированная боль в грудной клетке описана только в 2% наблюдений [2, 11]. Спонтанный пневмоторакс без вышеописанных симптомов наблюдался менее чем у 1% детей.
Сильный кашель и физическая нагрузка у пациентов со спонтанным пневмотораксом могут приводить к резкому изменению внутригрудного давления и расслоению медиастинальных тканей, что провоцирует возникновение подкожной эмфиземы с распространением ее в область шеи и на переднюю грудную стенку. У пациентов с подкожной эмфиземой признаки спонтанного пневмоторакса могут быть стерты.
Наиболее частыми осложнениями спонтанного пневмоторакса являются:
– внутриплевральные кровотечения вследствие надрыва легочной паренхимы;
– напряженный спонтанный пневмоторакс. Развиваются прогрессирующая дыхательная недостаточность, медиастинальная подкожная эмфизема;
– серозно-фибринозный пневмоплеврит.
Диагностика. Диагноз ПСП устанавливается на основании данных анамнеза и определения свободного края легкого (становится видимой тонкая линия висцеральной плевры) на обзорной рентгенограмме органов грудной клетки, выполненной в положении стоя. При этом рекомендовано проведение рентгенографии в двух проекциях: прямой и боковой. Для выявления пневмоторакса небольшого объема, особенно верхушечного, следует выполнять рентгенографию на выдохе, так как постоянный объем воздуха в плевральной полости при пневмотораксе более четко прослеживается тогда, когда общий размер данной половины грудной клетки уменьшается при выдохе. При необходимости целесообразно получение боковых снимков в положении больного лежа (пораженная сторона легких должна находиться внизу).
Рентгенологически для пневмоторакса небольшого объема характерны сверхпрозрачность и исчезновение легочного рисунка на периферии, а также появление тонкой линии, представляющей рефракцию висцеральной плевры от париетальной. Значительно реже может отмечаться присутствие небольшого количества плевральной жидкости на стороне поражения, о чем можно судить по сглаживанию реберно-диафрагмального угла.
Пневмоторакс следует дифференцировать с кожными складками, артефактами на грудной стенке (например, из-за одежды больного), а также с большими субплеврально расположенными буллами в паренхиме легкого или тонкостенными воздушными кистами. При проведении дифференциальной диагностики необходимо учитывать, что буллы и кисты имеют вогнутые внутренние края и закругленные контуры.
Компьютерная томография (КТ) грудной клетки на настоящий момент является «золотым» стандартом для диагностики и дифференциальной диагностики спонтанного пневмоторакса. По результатам КТ у 89% пациентов с ПСП обнаруживают буллы.
В отдельных публикациях у пациентов со спонтанным пневмотораксом рекомендуют определять функцию легких методом стандартной спирометрии, пытаясь провести корреляцию между функцией внешнего дыхания и тяжестью пневмоторакса. Однако на практике получить достоверные данные результатов спирометрии у пациентов со спонтанным пневмотораксом не удается, кроме того, проведение самого исследования чревато увеличением объема спонтанного пневмоторакса и ухудшением общего состояния.
Ультразвуковое исследование может быть использовано в комплексном обследовании таких пациентов с целью определения наличия воздуха в плевральных полостях, но оценить объем пневмоторакса по данным эхографии затруднительно [5]. Положительная прогностическая ценность ультразвукового исследования в диагностике пневмоторакса, по данным Goodman [6], составляет 100%, а отрицательная – 82%.
Средняя частота рецидивов, по данным литературы [1, 2, 11], при ПСП составляет 30% случаев. Как правило, это обусловлено наличием у пациентов буллезной эмфиземы или дисплазии соединительной ткани. В большинстве случаев рецидив ПСП развивается в течение 6 мес после его первого эпизода. У пациентов с рецидивом спонтанного пневмоторакса рентгенологически часто определяется фиброз легочной ткани. Курение является независимым фактором риска рецидивов пневмоторакса [1, 2, 11].
Тактика терапии спонтанного пневмоторакса
На данный момент медицинская наука и практика еще далеки от того, чтобы утверждать, что оптимальная тактика в отношении пневмоторакса однозначно определена и стандартизирована, особенно у детей. Лечение детей с пневмотораксом, главным образом, базируется на опыте ведения взрослых пациентов, который экстраполирован на педиатрическую практику. На сегодняшний день основными рекомендациями по данной проблеме являются рекомендации Американской коллегии врачей по заболеваниям грудной клетки [14] и Британского торакального общества [15].
В целом тактика ведения данной категории пациентов зависит, в первую очередь, от объема пневмоторакса, наличия и выраженности дыхательной недостаточности, а также тех или иных сопутствующих заболеваний. Основной целью лечения является удаление воздуха из плевральной полости и профилактика рецидивов пневмоторакса.
Лечение может быть консервативным, ограничивающимся выжидательным наблюдением и кислородной поддержкой, или инвазивным. Хотя показания к консервативной терапии достаточно хорошо определены, критерии для проведения дренажных процедур являются довольно противоречивыми. Спектр возможных вмешательств включает в себя плевральную пункцию с аспирацией содержимого, дренирование плевральной полости с или без проведения плевродеза, а также более инвазивные хирургические вмешательства.
Пациенты со спонтанным пневмотораксом нуждаются в госпитализации в торакальное или пульмонологическое отделение. Вопрос о тактике их лечения иногда еще является предметом дискуссий между пульмонологами и торакальными хирургами, на что указывает анализ зарубежных публикаций. В результате опроса американских пульмонологов и торакальных хирургов об их тактике лечения пациентов с пневмотораксом выяснилось, что более 50% опрошенных придерживаются тактики простого наблюдения при ПСП с неполным коллапсом легкого. При рецидиве же пневмоторакса выполняется дренирование плевральной полости, а противорецидивное лечение проводят не более 40% опрошенных врачей [8]. Решение вопроса о проведении плеврального дренирования следует рассматривать только при наличии спонтанного пневмоторакса объемом более 20% гемиторакса. Если же объем пневмоторакса составляет менее 20% гемиторакса, то решение относительно дренирования зависит от конкретной клинической ситуации. У представленных нами на рис. 1, 2, 3 пациентов консервативная тактика была успешна, а выздоровление наблюдалось на 9-11-е сутки от момента его диагностики.
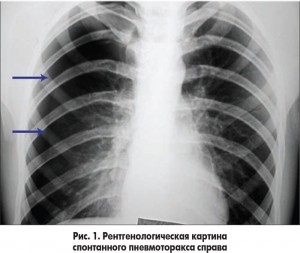
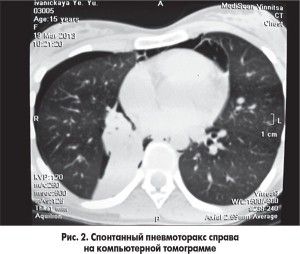
Таким образом, вычисление объема пневмоторакса является важным параметром выбора дальнейшей тактики терапии у детей со спонтанным пневмотораксом. В практической медицине наиболее приемлема формула R. Light [3], основанная на том, что диаметр одного легкого (DL) и диаметр гемиторакса (DH) пропорциональны величине их диаметров в третьей степени. Измерения проводятся на рентгенограмме в прямой проекции и выражаются в сантиметрах (рис. 3).
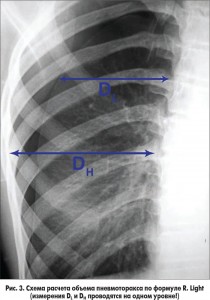
Объем (V) пневмоторакса в % = (1-DL/DH)×100
У взрослых и подростков по рекомендациям экспертов Британского торакального общества предлагается еще более простой метод определения объема пневмоторакса. Необходимо отметить, что существуют различия в месте измерения дистанции от грудной клетки до края легкого в английской («b» на рис. 4) и американской медицинских школах («а» на рис. 4).
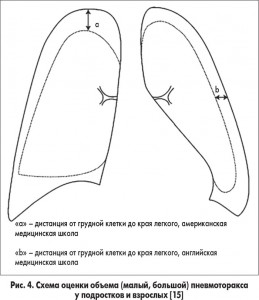
При этом пневмоторакс у подростков и взрослых в зависимости от расстояния между легким и грудной стенкой подразделяется на:
– малый (<2 см);
– большой (>2 см) [1, 2].
Пневмотораксы объемом <15% гемиторакса по формуле R. Light или <2 см от грудной клетки до края легкого по рекомендациям руководства Британского торакального общества и при стабильном клиническом состоянии пациента рекомендовано вести консервативно.
Консервативная терапия спонтанного пневмоторакса у детей основана на положении пациента лежа с приподнятой головой и туловищем до 30-35° (положение Фовлера). При наличии признаков дыхательной недостаточности обязательным является проведение оксигенотерапии методом носовых канюлей или через маску. При наличии даже минимального кашля целесообразно профилактическое назначение противокашлевых средств коротким курсом (3-5 дней). Рекомендовано применение препаратов центрального механизма действия (например, рапитус, синекод, пакселадин). Это направление терапии обусловлено тем, что кашель может привести к увеличению объема пневмоторакса. С целью купирования болевого синдрома необходимо применение нестероидных противовоспалительных препаратов, которые обычно требуют одно- или двукратного приема. В редких случаях при более выраженном болевом синдроме для аналгезии можно использовать методы регионального обезболивания (эпидуральная, межреберная и паравертебральная блокады). Антибиотикотерапия при ПСП не показана. Скорость разрешения спонтанного пневмоторакса составляет 1,25% объема гемиторакса в течение 24 ч, что позволяет прогнозировать время разрешения пневмоторакса у пациента.
По результатам исследования A. Bobbio и соавт. (2015), консервативная терапия спонтанного пневмоторакса имеет высокую эффективность [16]. При общем количестве наблюдений 4259 хирургические процедуры выполнялись только у 24% пациентов.
Общепризнано недопустимым является проведение плевральных пункций у пациентов с ПСП, которые во многих случаях могут привести к ухудшению течения заболевания. При необходимости возможно проведение простой аспирации воздуха при помощи катетера. По данным литературы, простая аспирация при ПСП у детей приводит к расправлению легкого в 59-80% случаев. Необходимо также учитывать, что простая аспирация воздуха имеет определенные преимущества перед дренированием плевральной полости (менее болезненна, значительно лучше переносится детьми).
Показаниями к дренированию плевральной полости являются:
– напряженный пневмоторакс;
– значительный объем пневмоторакса или коллапса легкого (рис. 5);
– рецидив спонтанного пневмоторакса;
– отсутствие эффекта от консервативной терапии.
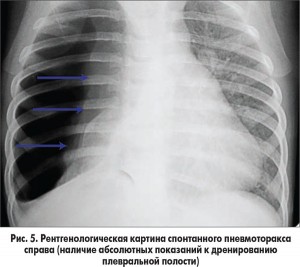
Плевральное дренирование при спонтанном пневмотораксе у детей следует проводить в пятом межреберье по передней аксиллярной линии или во втором межреберье по среднеключичной линии. Эффективность плеврального дренажа составляет 84-97%. Использование источника отрицательного давления при дренировании плевральной полости может затягивать разрешение пневмоторакса, поэтому наиболее приемлемо использование методики «водяного замка». Показанием для удаления дренажа является отсутствие сброса воздуха через дренаж в течение суток. Невозможность путем дренирования расправить легкое в течение 3-4 суток, стойкое нестабильное состояние пациента диктуют рассмотрение вопроса о проведении оперативного вмешательства путем торакотомии.
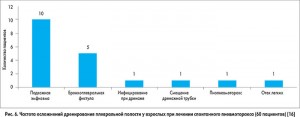
В исследовании Aparup Dhua и соавт. (2015) приводятся данные о частоте возникновения осложнений у взрослых при лечении спонтанного пневмоторакса методом дренирования плевральной полости [16]. Частота осложнений, возникающих при дренировании плевральной полости, по данным указанных авторов (рис. 6), является достаточно высокой (31,6% случаев), к наиболее частым из которых относятся подкожная эмфизема (16,6%) и бронхоплевральная фистула (8,3%).
Химический плевродез обычно проводят путем введения через дренажную трубку доксициклина или взвеси талька в физиологическом растворе. В педиатрической практике необходимо учитывать, что тетрациклины противопоказаны для применения у детей до 9 лет. После введения склерозирующего препарата необходимо перекрывать дренажную трубку на час. Данный вид лечения показан пациентам с повторным эпизодом (рецидивом) пневмоторакса с одной стороны, но может предлагаться и при первом эпизоде заболевания в случае эмфизематозных изменений в легочной паренхиме, а также при имевших место эпизодах пневмоторакса как с одной, так и с другой стороны. Учитывая развитие значительного болевого синдрома при проведении данной процедуры, ей должна предшествовать адекватная анестезия [2, 7].
Таким образом, своевременная постановка диагноза и взвешенный поход к терапии с четким разграничением показаний для инвазивной и консервативной терапии является залогом успешного и рационального лечения спонтанного пневмоторакса у детей.
Литература
1. Справочник по пульмонологии / Под ред. А.Г. Чучалина, М.М. Ильковича. – Москва: ГЭОТАР-медиа, 2009. – 927 с.
2. Henry M., Arnold T., Harvey J. et al. BTS guidelines for the management of spontaneous pneumothorax // Thorax. – 2003. – Vol. 58 (Suppl II). – P. 39-52.
3. Light R.W. Pneumothorax. In: Pleural diseases. – 3rd ed. Baltimore: Williams and Wilkins, 1995. – P. 242-277.
4. Gupta D., Hansell A., Nichols T. et al. Epidemiology of pneumothorax in England // Thorax. – 2000. – Vol. 55. – P. 666-671.
5. Sistrom C.L., Reiheld C.T., Gay S.B., Wallace K.K. Detection and estimation of the volume of pneumothorax using real-time sonography: efficacy determined by receiver operating characteristic analysis // Am J Roentgenol. – 1996 Feb. – Vol. 166 (2). – P. 317-321.
6. Goodman T.R. et al. Ultrasound detection of pneumothorax // Clinical Radiology. – 1999. – Vol. 54. – P. 736-739.
7. Noppen M., Alexander P., Driesen P. et al. Manual aspiration versus chest tube drainage in first episodes of primary spontaneous pneumothorax // Am J Respir Crit Care Med. – 2002. – Vol. 165. – P. 1240-1244.
8. Hansen A.K., Nielsen P.H., Moller N.G. et al. Operative pleurodesis in spontaneous pneumothorax // Scand J Thorac Cardiovasc Surg. – 1989. – Vol. 23. – P. 279-28.
9. Hamed H., Fentiman I.S., Chaudary M.A. et al. Comparison of bleomycin and talc for the control of pleural effusions secondary to carcinoma of the breast // Br J Surg. – 1989. – Vol. 76. – P. 1266-1267.
10. Light R.W. Tension pneumothorax // Intensive Care Med. – 1994. – Vol. 20. – P. 468-469.
11. Baumann M.H., Strange C., Heffner J.E. et al. Management of spontaneous pneumothorax: an American College of Chest Physicians Delphi consensus statement // Chest. – 2001. – Vol. 119. – P. 590-602.
12. Davis A.M., Wensley D.F., Phelan P.D. Spontaneous pneumothorax in paediatric patients // Respir Med. – 1993. – Vol. 87 (7). – P. 531.
13. Robinson P.D., Cooper P., Ranganathan S.C. Evidence-based management of paediatric primary spontaneous pneumothorax // Paediatr Respir Rev. – 2009. – Vol. 10 (3). – P. 110.
14. Baumann M.H., Strange C., Heffner J.E. et al. AACP Pneumothorax Consensus Group. Management of spontaneous pneumothorax: an American College of Chest Physicians Delphi consensus statement // Chest. – 2001. – Vol. 119 (2). – 590 p.
15. MacDuff A., Arnold A., Harvey J., BTS Pleural Disease Guideline Group. Management of spontaneous pneumothorax: British Thoracic Society Pleural Disease Guideline 2010. – Thorax. – 2010. – Vol. 65.
16. Aparup Dhua et al. Assessment of spontaneous pneumothorax in adults in a tertiary care hospital // Lung India. – March-April 2015. – Vol. 32. – P. 132-136.
17. Bobbio A. et al. Epidemiology of spontaneous pneumothorax: gender-related differences // Thorax. – 2015. – Vol. 70. – P. 653-658.




