4 липня, 2016
Ацетонемический синдром у детей: современные возможности терапии и профилактики
В повседневной клинической практике врач-педиатр постоянно сталкивается с ацетонемическим синдромом у детей. Данное состояние представляет собой совокупность симптомов, которые обусловлены повышением содержания в крови продуктов распада жирных кислот и кетогенных аминов – кетоновых тел: ацетона, ацетоуксусной кислоты и β-оксимасляной кислоты. Различают первичный (идиопатический) и вторичный (на фоне соматических, инфекционных, эндокринных заболеваний, опухолей и поражений центральной нервной системы) ацетонемический синдром. Основными проявлениями ацетонемического синдрома являются стереотипные повторные приступы рвоты, чередующиеся с периодами полного благополучия. Примерно 50% пациентов с этой патологией нуждаются в госпитализации и внутривенном введении жидкости.
Основополагающим фактором в развитии ацетонемического синдрома считается аномалия конституции – так называемый нервно-артритический диатез, однако любые стрессогенные, токсические, алиментарные, эндокринные влияния на энергетический обмен, даже у детей без данной аномалии, могут вызывать развитие ацетонемической рвоты. Немаловажное значение в возникновении кетоза у детей имеют инфекционные заболевания различной этиологии. Пусковым фактором развития кетоза является стресс с относительным преимуществом контринсулярных гормонов и алиментарные нарушения в виде голодания или чрезмерного потребления жирной и белковой пищи (кетогенных аминокислот) при недостатке углеводов. Кроме того, синдром интоксикации, сопровождающий инфекционные заболевания у детей, особенно раннего возраста, очень часто проявляется рвотой и отказом ребенка от еды, независимо от нозологической формы заболевания. Возникает алиментарное голодание, в том числе и углеводное, которое дает старт развитию кетоза.
Увеличение количества кетоновых тел в крови запускает целый каскад патологических изменений, которые ухудшают течение заболевания и состояние ребенка. Во-первых, при кетозе возникает метаболический ацидоз с увеличенным анионным интервалом – кетоацидоз. Его компенсация осуществляется за счет гипервентиляции, которая приводит к гипокапнии, вызывающей вазоконстрикцию, в том числе и церебральных сосудов. Во-вторых, излишек кетоновых тел оказывает наркотическое влияние на центральную нервную систему, вплоть до развития комы. В-третьих, ацетон является жирорастворителем и повреждает липидный бислой клеточных мембран.
Помимо этого, повышенная концентрация кетоновых тел приводит к раздражению слизистой оболочки желудочно-кишечного тракта, что клинически манифестирует рвотой и абдоминальным болевым синдромом. Перечисленные неблагоприятные эффекты кетоза в сочетании с другими расстройствами водно-электролитного и кислотно-основного равновесия (гипо-, изо- и гипертоническое обезвоживание, метаболический ацидоз вследствие потерь бикарбоната и/или накопления лактата) увеличивают продолжительность пребывания ребенка в отделении интенсивной терапии.
Клиническая симптоматика ацетонемического синдрома включает в себя проявления непосредственно кетоза и синдромы, характерные для того или иного патологического процесса-триггера (гастроэнтерит, пневмония, респираторная инфекция, нейроинфекция и др.). Непосредственно кетоз характеризуется многократной или неукротимой рвотой (при попытке напоить или покормить ребенка), бледностью кожи с характерным румянцем, гиподинамией, мышечной гипотонией. Беспокойство и возбуждение в начале криза сменяются вялостью, слабостью, сонливостью, в редких случаях возможны симптомы менингизма и судороги. Возникают гемодинамические нарушения (гиповолемия, ослабление сердечных тонов, тахикардия, аритмия), спастический абдоминальный синдром (схваткообразная или упорная боль в животе, тошнота, задержка стула). Температура тела повышается до 37,5-38,5°C; в моче, рвотных массах, выдыхаемом воздухе появляется ацетон, в крови возрастает концентрация кетоновых тел. Интенсивность этих симптомов нарастает на протяжении нескольких суток. При объективном обследовании, как правило, определяются симптомы обезвоживания: сухость слизистых оболочек и кожи, снижение тургора, отсутствие слезовыделения, запавшие глаза. Диурез снижается в зависимости от степени обезвоживания.
Диагностика ацетонемического синдрома базируется на изучении анамнеза, анализе жалоб, клинической симптоматики и результатов определенных инструментальных и лабораторных методов обследования. Необходимо обязательно установить природу ацетонемического синдрома: является ли он первичным или вторичным.
Диагностические критерии синдрома циклической ацетонемической рвоты (первичного АС) определены международным консенсусом (1994).
Обязательные критерии:
– повторные, тяжелые, отдельные приступы рвоты;
– различной продолжительности периоды совершенно нормального самочувствия между приступами;
– продолжительность приступов рвоты от нескольких часов до суток;
– отрицательные лабораторные, рентгенологические и эндоскопические результаты обследования, которые могли бы объяснить этиологию рвоты как проявление патологии органов ЖКТ.
Дополнительные критерии:
– рвота характеризуется стереотипией, и каждый приступ аналогичен предыдущему по времени, интенсивности и продолжительности;
– приступы рвоты могут заканчиваться спонтанно и без лечения;
– сопутствующие симптомы включают тошноту, боль в животе, головную боль, слабость, фотофобию, заторможенность;
– сопутствующие признаки включают лихорадку, бледность, диарею, дегидратацию, чрезмерную саливацию и социальную дезадаптацию;
– рвотные массы часто содержат желчь, слизь и кровь. Гематемезис преимущественно является следствием ретроградного пролабирования кардиальной части желудка через гастроэзофагеальный сфинктер (то есть пропульсивной гастропатии).
Лечение ацетонемического синдрома можно разделить на два этапа: купирование ацетонемического криза и проведение в период между приступами мероприятий, направленных на профилактику рецидивов.
Всем пациентам с ацетонемическим синдромом назначается диета, подразумевающая употребление легкоусвояемых углеводов и большого количества жидкости с ограничением в рационе жиров. Раннему восстановлению нормального пищеварительного процесса способствует назначение прокинетиков (домперидон, метоклопрамид, ондансетрон), ферментов и кофакторов углеводного метаболизма (тиамин, кокарбоксилаза, пиридоксин).
При обезвоживании 1-й степени показана диетотерапия с включением легкодоступных углеводов и пероральная регидратация (компот из сухофруктов, чай с сахаром или препараты, содержащие регидратационные соли).
Если ацетонемический синдром сопровождается дегидратацией 2-й степени (6-9% потери массы тела), то необходимо проведение инфузионной терапии.
При этом объем жидкости для внутривенного введения должен составлять 40-50% от суммы дефицита жидкости и физиологической потребности для данного возраста. Для ее расчета используется простое эмпирическое правило: 100 мл/кг на первые 10 кг массы тела, 50 мл/кг на следующие 10 кг массы тела, 20 мл/кг на каждый килограмм массы тела свыше 20 кг.
Задача инфузионной терапии – быстро устранить гиповолемию и дефицит внеклеточной жидкости с целью улучшения перфузии и микроциркуляции. Она должна включать ощелачивающие препараты, повышающие уровень бикарбонатов плазмы и нормализующие кислотно-основное состояние, а также достаточное количество легкоусвояемых углеводов, которые метаболизируются разными путями, в том числе и независимо от инсулина.
Показаниями для назначения инфузионной терапии являются:
• стойкая и многократная рвота, которая не прекращается после назначения прокинетиков;
• умеренная (до 10% массы тела) и/или тяжелая (до 15% массы тела) дегидратация;
• декомпенсированный метаболический ацидоз с увеличенным анионным интервалом;
• гемодинамические и микроциркуляторные расстройства, признаки расстройств сознания (сопор, кетоацидотическая кома);
• анатомические и функциональные нарушения, препятствующие оральной регидратации (пороки развития лицевого скелета и полости рта);
• неврологические расстройства (бульбарные и псевдобульбарные нарушения).
В качестве инфузионных растворов используются 5-10%-ный раствор глюкозы с инсулином и кристаллоидные натрийсодержащие растворы (0,9%-ный раствор натрия хлорида, раствор Рингера) в соотношении 1:1 или 2:1 с учетом показателей водно-электролитного обмена. Относительно новым препаратом, обладающим более выраженными антикетогенными свойствами по сравнению с другими углеводами (глюкозой, сахароспиртами), является Ксилат®, два основных компонента которого – ксилитол и натрия ацетат. Ксилитол представляет собой пятиатомный спирт, который при внутривенном введении быстро включается в общий метаболизм и способствует утилизации кетоновых тел. В отличие от фруктозы и сорбита, ксилитол не вызывает снижения уровня нуклеотидов в печени и безопасен для пациентов с непереносимостью фруктозы. Натрия ацетат, также входящий в состав препарата Ксилат®, обладает ощелачивающим действием. Этот компонент постепенно корригирует метаболический ацидоз, благодаря чему у пациентов не возникает резких колебаний рН. Оба компонента обеспечивают гиперосмолярность раствора Ксилат®, а также реологическое, дезинтоксикационное и антикетогенное действие. За счет действия препарата Ксилат® уменьшаются проявления периферического вазоспазма и тканевой гипоксии, а также обеспечивается мягкий диуретический эффект. В результате усиливается выведение кетоновых продуктов с мочой и снижается интоксикация. Благодаря мягкому действию на кислотно-основное состояние Ксилат® способствует снятию приступов тошноты и рвоты и устраняет основные клинические симптомы ацетонемического синдрома.
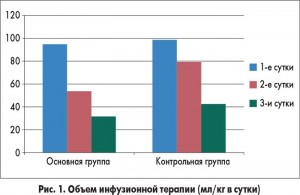
В нашей стране было проведено клиническое исследование по изучению эффективности и безопасности препарата Ксилат® в лечении недиабетического кетоацидоза у детей в возрасте от 1 до 5 лет с различной инфекционной патологией (М.А. Георгеянц, 2006). В нем участвовало 18 детей, у 6 из которых был диагностирован гастроэнтероколит, у 4 – гнойный менингит, у 5 – пневмония, у 3 – острая респираторная инфекция с судорожным синдромом. Дети были госпитализированы на 2-4-е сутки от начала заболевания. Нарушение сознания отмечалось у 6 (33,3%) детей, обезвоживание I степени – у 4 (22,2%), II степени – у 14 (77,8%). Основную группу представляли 10 больных, которым помимо традиционной терапии была назначена внутривенная инфузия препарата Ксилат® в дозировке 20 мл/кг. Контрольная группа пациентов (n=8) получала стандартное лечение. В ходе исследования было обнаружено, что у 80% пациентов из основной группы рвота прекращалась уже на 1-е сутки, а у пациентов из контрольной группы рвотные позывы отмечались у 12,5% даже на 4-е сутки от начала терапии. Уменьшение диспептических явлений у ребенка позволяет существенно снизить объем инфузионной терапии и значительно раньше отказаться от внутривенного введения препаратов, что улучшает качество жизни пациента и нивелирует негативное отношение к лечению (рис. 1).
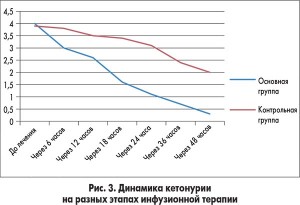
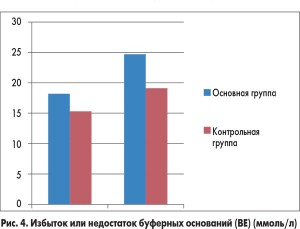
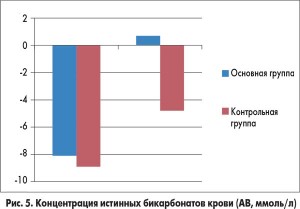
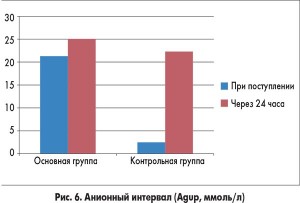
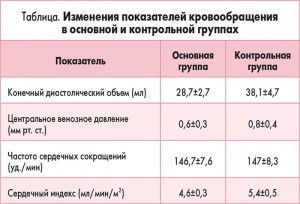
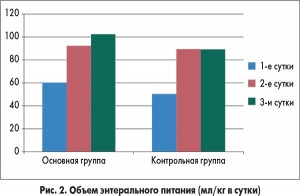 У пациентов из основной группы толерантность к энтеральному питанию восстановилась гораздо быстрее по сравнению с детьми, которые получали стандартную терапию (рис. 2). Включение в программу инфузионной терапии у детей с ацетонемическим синдромом комплексного препарата Ксилат® способствовало достоверному уменьшению кетонурии уже через 12 ч от начала лечения (рис. 3). Использование препарата Ксилат® приводит к нормализации таких показателей кислотно-основного состояния, как BE (base excess – отклонение концентрации буферных оснований от нормальных значений), который характеризует сдвиг ионов всех буферных систем и указывает на природу нарушений кислотно-основного гомеостаза (рис. 4), АВ (aktual bikarbonate – истинные бикарбонаты) (рис. 5), а также Agup – анионного интервала (рис. 6) до начала 2-х суток терапии. Также в ходе исследования были изучены изменения основных показателей кровообращения, таких как конечный диастолический объем, сердечный индекс, центральное венозное давление и частота сердечных сокращений в обеих группах (табл.).
У пациентов из основной группы толерантность к энтеральному питанию восстановилась гораздо быстрее по сравнению с детьми, которые получали стандартную терапию (рис. 2). Включение в программу инфузионной терапии у детей с ацетонемическим синдромом комплексного препарата Ксилат® способствовало достоверному уменьшению кетонурии уже через 12 ч от начала лечения (рис. 3). Использование препарата Ксилат® приводит к нормализации таких показателей кислотно-основного состояния, как BE (base excess – отклонение концентрации буферных оснований от нормальных значений), который характеризует сдвиг ионов всех буферных систем и указывает на природу нарушений кислотно-основного гомеостаза (рис. 4), АВ (aktual bikarbonate – истинные бикарбонаты) (рис. 5), а также Agup – анионного интервала (рис. 6) до начала 2-х суток терапии. Также в ходе исследования были изучены изменения основных показателей кровообращения, таких как конечный диастолический объем, сердечный индекс, центральное венозное давление и частота сердечных сокращений в обеих группах (табл.).
При выраженном абдоминальном спастическом синдроме парентерально вводятся спазмолитики (папаверин, платифиллин, дротаверин в возрастной дозировке). Если ребенок возбужден, беспокоен, выражена гиперестезия, применяют транквилизаторы – препараты диазепама в средневозрастных дозировках.
В период между приступами проводятся мероприятия по профилактике рецидивов ацетонемических кризов, включающие ряд направлений, главным из которых является лечебное питание с ограничением употребления продуктов, богатых пуринами, а также пищевых аллергенов и аллергизирующих веществ. Необходимо ограничить употребление мяса молодых животных, птицы и субпродуктов (почки, сердце, печенка, легкие, мозг, кровяная и ливерная колбаса), поскольку они содержат большое количество пуринов, бобовых культур (горох, соя, бобы, фасоль), некоторых видов рыбы (шпроты, сардины, килька, треска, судак, щука), грибов (белый гриб), соли, поскольку она задерживает жидкость в тканях и препятствует выведению через почки мочекислых соединений. Следует исключить из рациона холодец, соусы, мясные и рыбные бульоны, так как 50% пуринов при отваривании переходят в бульон. Не следует злоупотреблять продуктами, стимулирующими центральную нервную систему (кофе, какао, крепкий чай, острые закуски, пряности). Слабоминерализованные минеральные воды действуют диуретически, активизируют процессы гломерулярной фильтрации, нормализуют водно-солевой обмен. Минеральные воды назначают из расчета 3-5 мл/кг на прием трижды в сутки на протяжении месяца 3-4 курсами в год. Ощелачивание мочи повышает растворимость мочевой кислоты и препятствует формированию уратных конкрементов.
Подготовила Анастасия Лазаренко