10 квітня, 2016
Респираторная аллергия у детей: как достичь эффективного и безопасного контроля?
Бронхиальная астма (БА) – самая распространенная хроническая болезнь в детском возрасте. В настоящее время имеется достаточно широкий выбор эффективных препаратов с хорошим профилем безопасности, но несмотря на это, немалая доля больных БА получает неадекватное лечение. Еще большую проблему составляет сочетание БА с другими аллергическими заболеваниями, в частности с аллергическим ринитом (АР).
О том, как наиболее эффективно достичь контроля респираторной аллергии у детей при наименьшем риске нежелательных явлений, практикующим врачам напомнила заведующая кафедрой педиатрии № 1 Национальной медицинской академии последипломного образования им. П.Л. Шупика, доктор медицинских наук, профессор Елена Николаевна Охотникова. Ее доклад прозвучал на научно практической конференции «Современные диагностические возможности и алгоритмы лечения различных аллергических состояний», проходившей в конце прошлого года в г. Киеве.
Хронические респираторные заболевания являются одной из наиболее актуальных медико-социальных проблем современного общества и входят в четверку неинфекционных болезней, поражающих сотни миллионов людей и ежегодно уносящих миллионы жизней. Среди хронических обструктивных заболеваний легких, частота которых в Украине в 4 раза выше, чем в Европе, в детском возрасте особое место занимает БА. К сожалению, на ранних стадиях БА у нас выявляют менее чем у 1% больных. Несвоевременная диагностика и отсутствие адекватного лечения приводят к неудовлетворительному контролю болезни, что существенно снижает качество жизни больных и повышает риск смерти.
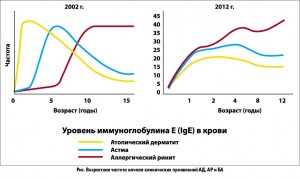
Важным аспектом проблемы является частое сочетание у детей нескольких аллергических заболеваний, например БА с АР или атопическим дерматитом (АД). Развитие аллергических заболеваний в течение жизни у предрасположенных к возникновению атопии лиц получило название «аллергического» или «атопического марша». У детей первыми проявлениями аллергии чаще всего являются пищевая аллергия и АД, которые развиваются преимущественно в грудном возрасте после прекращения грудного вскармливания и введения прикорма. В дальнейшем возникает аллергия к бытовым и пыльцевым аллергенам и формируются респираторные симптомы аллергии – БА и АР.
При этом в последние годы временной интервал от развития АД до манифестации БА и АР существенно сократился. Если раньше БА и АР чаще развивались в первые 5-6 лет жизни, то сейчас это преимущественно происходит уже в возрасте 1-2 лет (рис.).
В шведском исследовании BAMSE, целью которого было проследить развитие АД, БА и АР от рождения до 12 лет, было показано, что большинство эпизодов аллергических заболеваний развиваются в раннем детстве, начиная уже с первых месяцев жизни. Коморбидность БА и АР прогрессивно увеличивалась с возрастом. Так, у детей до года БА сочеталась с АР в 38% случаев, а к 12 годам коморбидность возросла до 67%. В целом к 12 годам 58% участвовавших в исследовании детей перенесли хотя бы один эпизод аллергического заболевания. В исследовании E.P. de Groot (2012) ставилась задача определить, как влияет течение АР на контроль БА. В исследуемую группу были включены дети с БА 5-18 лет, которые находились на поддерживающей терапии ингаляционными кортикостероидами в течение трех предыдущих месяцев. Исследование показало, что 76% детей с БА имеют АР, причем у 91,7% из них отмечались симптомы АР в течение последних 12 мес, что свидетельствует о параллельной персистенции АР и астмы. Полученные данные указывают на необходимость активного выявления АР и АД при наличии БА и наоборот, а также адекватного лечения всех имеющихся у ребенка аллергических заболеваний.
Кроме того, при БА чаще встречается и другая респираторная патология. Согласно данным, полученным в двух отечественных исследованиях, 52,3% детей <3 лет с БА имели аденоидит и аденоидные вегетации ІІ-ІІІ степени и 15,6% пациентов – АР. В возрасте <6 лет 75,8% детей с БА имели аденоидные вегетации и аденоидит, 65,4% – АР (Е.Н. Охотникова и соавт., 2006, 2009).
В соответствии с обновленными рекомендациями GINA-2014/2015 ключевыми направлениями ведения детей с БА являются:
- элиминационные мероприятия (устранение контакта с аллергенами),
- письменный план действий,
- контролирующая фармакотерапия,
- лечение обострений,
- аллерген-специфическая иммунотерапия,
- реабилитация,
- обучение.
Начальная терапия обострений БА у детей ≤5 лет включает оксигенотерапию, ингаляционные β2-агонисты короткого действия и системные кортикостероиды. Применяют 24% кислород через лицевую маску обычно со скоростью 1 л/мин для достижения сатурации крови кислородом 94-98%. Сальбутамол используют с помощью дозированного ингалятора и спейсера (2-6 вдохов) или небулайзера (2,5 мг) через каждые 20 мин в течение первого часа. Если симптомы сохраняются или возникают снова, следует назначить дополнительно две ингаляции в час. Если за 3-4 ч потребовалось выполнить более десяти ингаляций β2-агониста короткого действия, пациента следует госпитализировать. Детям с умеренными и тяжелыми обострениями назначают системные пероральные кортикостероиды (1-2 мг/кг в эквивалентной дозе преднизолона до максимальной дозы 20 мг для детей младше 2 лет и 30 мг для детей 2-5 лет). Достаточным для большинства детей является 3-5-дневный курс приема. Дополнительно при умеренных и тяжелых обострениях можно назначить 2 ингаляции ипратропия бромида по 80 мкг с помощью ингалятора или 250 мкг через небулайзер каждые 20 мин в течение первого часа. У детей с тяжелыми обострениями в возрасте ≥2 лет рекомендуется рассмотреть возможность введения 3 доз изотонического раствора магния сульфата (150 мг) через небулайзер в первый час лечения.
Но если обострения БА повторяются, ее лечение, согласно современным рекомендациям, не может ограничиваться только купированием приступов. В настоящее время ключевой задачей терапии астмы является достижение стабильного контроля заболевания.
Согласно рекомендациям GINA-2014/2015, оценка состояния ребенка с БА должна включать определение степени контроля заболевания и адекватности терапии. Контроль заболевания подразумевает не только оценку выраженности симптомов (за последние 4 недели), но и проверку наличия факторов риска плохого ответа и обострений, включая низкий уровень функции легких и сопутствующую патологию (риносинусит, гастроэзофагеальную рефлюксную болезнь, ожирение, обструктивное апноэ сна, депрессию, тревожные расстройства). Очень важно при каждом визите контролировать проведение терапии: проверить технику ингаляции и ее соблюдение, спросить о побочных эффектах, уточнить у пациента, есть ли у него индивидуальный письменный план, выяснить отношение пациента и его родителей к астме и ее лечению, совместно сформулировать цели терапии.
Общепринятый подход ступенчатой терапии БА в детской практике реализуется при обязательном исключении альтернативного диагноза, оценке степени приверженности рекомендациям врача и соблюдения требований элиминации триггеров. Возможность перехода на следующую (step up) или предыдущую ступень терапии (step down) должна оцениваться через регулярные интервалы времени (обычно – 3 мес).
У детей в возрасте <5 лет на первой ступени терапии БА препаратом выбора является ингаляционный β2-агонист короткого действия по потребности. Эта ступень применима к детям с вирус-индуцированными эпизодами свистящего дыхания (wheezing) с отсутствием или редкими симптомами в промежутках между ОРВИ. Оральные бронходилататоры не рекомендованы в связи с их медленным началом действия и высокой частотой побочных эффектов. При недостаточной эффективности β2-агониста короткого действия рекомендуется рассмотреть интермиттирующий курс ингаляционных кортикостероидов (ИКС). Учитывая риск побочных эффектов, препараты данной группы можно назначить только в том случае, если врач уверен в том, что лечение будет применяться должным образом.
Показаниями к переходу на вторую ступень являются неудовлетворительный контроль симптомов БА или 3 и более обострений заболевания в год. Она также может применяться в качестве пробной терапии при частых эпизодах wheezing (каждые 6-8 недель и чаще). Вторая ступень лечения подразумевает постоянную контролирующую терапию в комбинации с β2-агонистом короткого действия по необходимости. В качестве базисной терапии назначают ИКС в низких дозах или антилейкотриеновые препараты.
Третья ступень терапии предусматривает назначение средних доз ИКС (удвоение дозы) или комбинацию антагонистов лейкотриенових рецепторов с низкой дозой ИКС в сочетании с применением ингаляционного β2-агониста короткого действия по потребности.
При переходе на четвертую ступень рекомендуется обратиться за консультацией к профильному специалисту, после чего могут быть назначены следующие варианты терапии:
- прием высоких доз ИКС и/или их более частое дозирование;
- добавление антагониста лейкотриеновых рецепторов, теофиллина или низкой дозы оральных кортикостероидов к средним дозам ИКС.
Комбинированные препараты ИКС и β2-агонисты длительного действия для детей этого возраста не рекомендованы.
Базисная терапия у детей 6-11 лет и подростков проводится по такому же алгоритму, как у взрослых, с несколькими уточнениями. На первой ступени назначают β2-агонисты короткого действия по необходимости, но может быть рассмотрена и терапия низкими дозами ИКС. Показанием к их назначению являются симптомы астмы чаще 2 раз в месяц, пробуждения из-за БА чаще 1 раза в месяц, наличие любых симптомов БА, если присутствуют какие-либо факторы обострения астмы. Рассмотреть более высокую ступень терапии следует в том случае, если тревожные симптомы БА присутствуют в течение многих дней, имеют место пробуждения от астмы один и более раз в неделю, особенно при наличии какого-либо фактора риска обострения БА. На второй ступени назначают низкие дозы ИКС или антагонисты лейкотриеновых рецепторов, на третьей – низкие дозы ИКС в сочетании с β2-агонистом длительного действия или антилейкотриеновым препаратом либо средние/высокие дозы ИКС, на четвертом – средние/высокие дозы ИКС в сочетании с β2-агонистом длительного действия или антилейкотриеновым препаратом. На пятой ступени к лечению добавляют анти-IgE препараты или низкие дозы оральных кортикостероидов. Детям 6-11 лет теофиллины, в отличие от взрослых, не рекомендуются. На любой ступени заболевания применяются β2-агонисты короткого действия по требованию.
Снижение контролирующей терапии (step down) разрешается, когда симптомы БА хорошо контролируются и функция легких стабильна в течение 3 мес и более, нет ОРВИ, а также не планируются путешествия. Уменьшение дозы ИКС на 25-50% в течение 3 мес обосновано и безопасно у большинства пациентов. Целью стратегии step down является найти минимально эффективные дозы ИКС, обеспечивающие контроль симптомов при минимальном риске побочных эффектов.
Следует отметить, что ИКС оказывают воздействие на многие звенья патогенеза БА, но не влияют на бронхоспазм и гиперплазию гладкой мускулатуры бронхов, в частности потому, что вне их влияния остаются цистеинил-лейкотриены (Cys-лейкотриены, табл.).
Известно, что Cys-лейкотриены (LTC4, LTD4 и LTE4) обладают выраженным бронхоконстрикторным эффектом (в 1000 раз мощнее, чем у гистамина, и в 100 раз – чем у простагландинов) и способствуют формированию гиперреактивности бронхов в ответ на действие триггеров. Кроме того, они поддерживают воспаление в дыхательных путях и бронхоспазм за счет увеличения проницаемости сосудов, отека слизистой, усиления бронхиальной секреции, стимуляции хемотаксиса и адгезии нейтрофилов и эозинофилов. Наконец, Cys-лейкотриены способствуют пролиферации эпителиальных и гладкомышечных клеток, что приводит к развитию структурной перестройки бронхов вплоть до необратимого характера заболевания и инвалидности пациента.
Антагонисты лейкотриеновых рецепторов блокируют эффекты Cys-лейкотриенов и, что очень важно, предотвращают ремоделирование бронхов. Высокую эффективность терапии БА обеспечивает сочетанное применение препаратов данного класса (например, монтелукаста) с ИКС, поскольку именно такая комбинация позволяет влиять на все основные звенья патогенеза. В ряде ситуаций оправдана монотерапия монтелукастом. Так, по данным клинических исследований, эффективность базисной терапии оригинальным препаратом монтелукаст (Сингуляр) сопоставима с низкими дозами ИКС. Согласно приказу МЗ Украины от 08.10.2013 г. № 868 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при бронхіальній астмі», у детей младше 5 лет, которые не могут получать лечение ИКС, антагонисты рецепторов лейкотриенов являются эффективным выбором для первой линии терапии.
Особого внимания Сингуляр заслуживает у детей с сочетанной аллергической патологией, о высокой распространенности которой говорилось выше, так как этот препарат не только помогает контролировать БА, но и снижает выраженность симптомов АР и АД посредством универсального влияния на аллергическое воспаление. Так, по данным S. Pijaskic и соавт. (2007), у детей школьного возраста с сочетанием БА и АР и сохраняющимися симптомами, несмотря на лечение фиксированной комбинацией ИКС и β2-агониста длительного действия, добавление препарата Сингуляр улучшает контроль БА и уменьшает симптомы АР. В исследовании E. Matkovskaya et al. (2012) добавление лекарственного средства Сингуляр у детей с БА в сочетании с АР и АД приводит к стабилизации атопического синдрома. Важно подчеркнуть, что стабильный контроль БА, АР и АД дает возможность безопасно проводить аллерген-специфическую иммунотерапию.
Сингуляр принимается в таблетированной форме 1 раз в сутки, что удобно для пациентов и обеспечивает лучший комплайенс по сравнению с ИКС.
Подготовил Вячеслав Килимчук
Цей матеріал призначений тільки для медичних фахівців, розповсюдження
під час спеціалізованих медичних заходів і друку в спеціалізованих медичних журналах (виданнях). Ця інформація надана компанією як професійна підтримка фахівців охорони здоров,я. Інформація щодо будь-якого продукту може не збігатися з інструкцією для медичного застосування препарату.
Будь ласка, ознайомтеся з повним текстом інструкції для отримання детальної інформації або даних щодо продуктів, які розглядаються
в цій публікації, до їх призначення.
© 2016 ТОВ «Універсальне агентство «ПРО-ФАРМА».
Усі права захищені. Матеріал створений у березні 2016 р.
Матеріал придатний до березня 2018 р.
MUSC-1170723-0004.
Адреса: 03038, м. Київ, вул. М. Амосова, 12, 3-й поверх,
бізнес-центр «Горизонт Парк». Тел.: (044) 393-74-80.
У разі виникнення питань щодо препаратів МСД
звертайтеся за електронною адресою:
medinfo@merck.com, http://medical.msd.com.