10 грудня, 2016
Cучасні можливості патогенетичної фармакотерапії діабетичної кардіоваскулярної автономної нейропатії
Кардіоваскулярна автономна нейропатія (КАН) – одна з найбільш прогностично несприятливих і клінічно значущих форм автономної діабетичної нейропатії, яка діагностується незадовільно, може бути причиною ішемії коронарних судин, «німого» інфаркту міокарда; значно збільшує ймовірність синдрому «раптової смерті», може бути передвісником розвитку гострих порушень мозкового кровотоку, причому навіть доклінічна стадія КАН збільшує ризик «раптової смерті». Рівень смертності при КАН досягає 50%, а наявність вегетативної дисфункції в клінічній картині цукрового діабету (ЦД) є ознакою незадовільного прогнозу (С.Т. Зубкова, Н.Д. Тронько, 2006; Р. Valensi, 2015). Отже, пошук шляхів і способів ефективного лікування КАН є одним із пріоритетних завдань сучасної діабетології.
Згідно з сучасними уявленнями лікування автономної нейропатії, зокрема діабетичної КАН, повиннo бути патогенетичним, безпечним і покращувати функцію автономної нервової системи. Очевидно, що на першому плані повинні бути заходи, скеровані на зменшення інсулінової резистентності (ІР), корекцію гіперглікемії, дисліпопротеїнемій (ДЛП), порушень метаболізму міокарда, кардіоміопатії, попередження та лікування тромбоутворення, симптоматичну терапію супутніх захворювань і синдромів (артеріальної гіпертензії, ішемічної хвороби серця, серцевої недостатності та аритмій). Патогенетичне лікування КАН при ЦД включає використання інгібіторів альдозоредуктази (ІАР); замісну терапію міоінозитолом (МІ); використання блокаторів рецепторів кінцевих продуктів неферментативного глікування (РКПНГ); корекцію порушень транспорту і вмісту чинників росту в нервах; корекцію антинейрального аутоімунітету; корекцію процесів пригнічення ендоневральної перфузії з розвитком гіпоксії; використання інгібіторів протеїнкінази С (PKC); антиоксидантів і в першу чергу αліпоєвої кислоти (αЛК); жиророзчинного попередника вітаміну В1 бенфотіаміну; γліноленової кислоти (γЛЛК), ацетил-Lкарнітину; препаратів ω-3 поліненасичених жирних кислот (ω-3 ПНЖК); лікування ортостатичної гіпотонії тощо (D. Ziegler, 2010; V. Serhiyenko та співавт., 2016). В таблиці наведено основні характеристики препаратів, які використовуються в патогенетичній терапії діабетичної КАН.
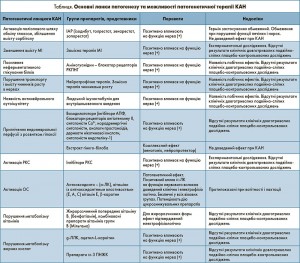
Інгібітори ІАР пригнічують поліоловий шлях обміну глюкози, попереджують зменшення редокс-потенціалів. Ізодибут – інгібітор сорбітолового шляху обміну глюкози успішно застосовується в якості патогенетичного засобу в лікуванні діабетичної нейропатії. Повідомляється, що толрестат у хворих на ЦД із симетричною полінейропатією сприяє покращенню показників кардіоваскулярних тестів (КВТ) автономних рефлексів і вібраційної чутливості. Призначення зенарестату протягом 12 міс супроводжувалось дозозалежними змінами щільності нервових волокон, збільшенням швидкості нервової провідності (ШНП), покращенням систолічної функції міокарда. Зопорестат – п репарат із групи ІАР нової генерації – виявив достатню ефективність в експериментальних дослідженнях, однак досвід клінічного застосування цих препаратів не підтвердив їх ефективності в лікуванні діабетичної КАН (K.E. Schemmel et al., 2010).
Замісна терапія МІ. Проведено поодинокі клінічні дослідження з вивчення ефективності МІ в лікуванні діабетичної нейропатії. Отримані результати є досить позитивними, однак потребують проведення подвійно-сліпих плацебо-контрольованих досліджень (D. Ziegler, 2010).
Аміногуанідин. Аміногуанідин покращує ШНП, посилює кровотік, пригнічує утворення КПНГ, затримує появу і розвиток альбумінурії. Аналіз результатів контрольованих клінічних досліджень виявив достатньо високу ефективність аміногуанідину у хворих із діабетичною нейропатією, однак розвиток низки побічних ефектів став причиною відміни його застосування. Проте в клінічних дослідженнях аміногуанідин виявив значну токсичність і здатність провокувати розвиток аутоімунних захворювань (R. Singh et al., 2001). Використання похідних аміногуанідину супроводжується клінічною ефект ивн істю і відсутністю небажаних побічних проявів. Отримані результати є багатообіцяючими, однак потребують проведення подальших клінічніх плацебо-контрольованих досліджень.
Нейротрофічна терапія. Пригнічення експресії чинника росту нерву (nerve growth factor, NGF) і його рецепторів гальмує ретроградний аксональний транспорт NGF і зменшує активність дрібних демієлізованих нейронів, а також їх нейропептидів, в тому числі субстанції Р і гензв’язаного пептиду кальцитоніна – потужніх вазодилататорів. Використання рекомбінантного людського NGF нормалізує концентрацію нейропептиду і запобігає розвитку сенсорної нейропатії в експерименті. Однак результати мультицентричних, плацебоконтрольованих досліджень заперечують позитивний вплив рекомбінантного людського NGF у хворих із діабетичною нейропатією (В.О. Сергієнко, 2012).
Антинейральний аутоімунітет. Внутрішньовенне призначення людського імуноглобуліну рекомендується
хворим із формами діабетичної периферичної нейропатії (ДПН), які пов’язані із ознаками антинейрального аутоімунітету. Однак це стосується переважно хворих із дефіцитом імуноглобуліну А. До побічних проявів слід віднести головний біль, розвиток анафілактичної реакції.
Пригнічення ендоневральної перфузії з розвитком гіпоксії. І. Експериментальні та поодинокі клінічні дослідження свідчать на користь ефективності вазодилататорів у покращенні ШНП, проте недостатньо інформації про їх вплив на перебіг ДПН при проведенні клінічних контрольованих подвійно-сліпих досліджень. Результати досліджень особливостей впливу інгібіторів АПФ на показники варібельності ритму серця (ВРС) у хворих на ЦД з КАН є діаметрально протилежними. Зокрема, призначення квінаприлу протягом 3 міс супроводжується статистично значущим посиленням парасимпатичної активності, а використання трандолаприлу протягом 12 міс не впливає на показники автономної функції міокарда. Однак більшість з цих фармакологічних агентів не володіють доведеними клінічними і електрофізіологічними позитивними ефектами, мають певні обмеження до застосування (G. Deli et al., 2013).
Пригнічення ендоневральної перфузії з розвитком гіпоксії. ІІ. Екстракт гінкго-білоба. Комплексний ефект (венотонік, нейропротектор). Не доведено ефект при діабетичній КАН.
Інгібітори протеїнкінази С. Результати доклінічних досліджень показали, що використання інгібіторів PKC сприяє попередженню патофізіологічних змін у судинах нирок і сітківки (N.B. Bishara, 2002). Однак на сьогодні відсутні фармакологічні агенти, що здатні блокувати «токсичні» ізоформи PKC.
Альфа-ліпоєва кислота. Приймаючи до уваги, що одним з провідних патогенетичних механізмів нейропатії є оксидантний стрес (ОС), необхідність призначення антиоксидантів очевидна. Використання фізіологічних антиоксидантів, включаючи α-ЛК – п отужну ліпофільну «пастку» вільних радикалів, сприяє попередженню нейроваскулярних порушень, забезпечує основу для патогенетично-обгрунтованого застосування αЛК в клініці, зокрема, лікуванні діабетичної КАН (Б.Н. Маньковский, 2012; Т.В. Мохорт, 2015). Існують принаймі дві гіпотези щодо особливостей дії α-ЛК. Перша – с прияння зміни плинності мембрани, опосередковані сульгідрильними групами α-ЛК. Друга, найбільш ймовірна гіпотеза, – здатність α-ЛК функціонувати в якості «очисника» радикалів. Зокрема, відомо, що антиоксидантна («очисна») активність у хворих на ЦД 2 типу пригнічена; глутатіон, пробукол, α-токоферол і α-ЛК запобігають пригніченню моторної і сенсорної нервової провідності, порушенням мікроциркуляції в нервовій тканині. Альфа-ліпоєва кислота сприяє дозозалежній нормалізації ШНП, а також швидкості кровотоку в капілярах нервової тканини, збільшенню вмісту. Отже, одним з найбільш ймовірних механізмів покращення нейроваскулярних показників є посилення вільнорадикально-зв’язувальної активності. Повідомляється, що щоденне вживання 800 мг α-ЛК протягом 4 міс супроводжується покращанням показників ВРС, інтервалу QT. Результати мультицентричного рандомізованого подвійного сліпого дослідження серед 460 хворих на ЦД з легкою та/або помірною ДПН, які перорально отримували 600 мг αЛК на добу (n=233) або плацебо (n=227) протягом 4 років, показали, що α-ЛК не впливає на первинну комбіновану кінцеву точку, однак сприяє клінічно значущому поліпшенню і профілактиці прогресування ДПН, добре переноситься хворими (D. Ziegler et al., 2011). Нами обстежено 33 хворих на ЦД 2 типу із верифікованою функціональною стадією КАН у віці 50-59 років, тривалістю захворювання 16 років, показниками глікованого Hb (HbA1c) 7,03±0,13%; систолічний артеріальний тиск (САТ) 143,5±1,83 мм рт. ст., діастолічний АТ (ДАТ) 90,5±1,37 мм рт. ст. Хворих на ЦД 2 типу та КАН було розподілено на дві групи, які протягом 3 міс крім дієтотерапії (стіл № 9) отримували пероральні цукрознижувальні препарати – ПЦП (n=15, контроль, перша група). Пацієнтам другої групи (n=18) призначено дієтотерапію (стіл № 9), ПЦП і 600 мг препарату α-ЛК (Тіогама®, Woerwag Pharma® GmbH & Co). Роботу проведено відповідно до етичних принципів Гельсінської декларації (2004). В результаті проведених досліджень виявлено наступні ефекти α-ЛК: cприяння позитивним статистично значущим змінам щодо зменшення препрандіальної глікемії, ІР – імунореактивного інсуліну (ІРІ), індексу ІР (HOMAІР); антиатерогенний вплив, а саме статистично значуще зменшення вмісту загального холестерину (ЗХС), холестерину ліпопротеїнів низької щільності (ХС-ЛПНЩ), показників коефіцієнту атерогенності (КА), підвищення вмісту холестерину ліпопротеїнів високої щільності (ХС-ЛПВЩ); зменшення концентрації чинників системного запалення і прозапальних цитокінів; лептину та показників співвідношення фактор некрозу пухлини-α/інтерлейкін-10 (ФНП-α/ ІЛ-10); вмісту неактивного N-термінального фрагменту мозкового натрійуретичного пептиду (NT-proBNP); стану системи простациклін І2-тромбоксан А2 в крові. Крім того, встановлено, що α-ЛК сприяє зменшенню «нейропатичного» подовження коригованого інтервалу QT (QTc), дисперсії інтервалу QT (QTd) і показників просторового кута QRST; збільшенню деяких часових і спектральних параметрів ВРС в активний і пасивний періоди доби; параметрів добового моніторування АТ (ДМАТ): зменшенню варіабельності САТ (SD САТ) в активний період доби, САТ, індексу площі артеріальної гіпертензії САТ (ІП АГ САТ), індексу часу артеріальної гіпертензії САТ (ІЧ АГ САТ) і SD САТ в пасивний період доби; параметрів добового моніторування жорсткості артерій: індексу аугментації в аорті (ІА ао) і швидкості поширення пульсової хвилі (ШППХ) в активний і пасивний період доби, позитивній динаміці стану вегетативної нервової системи (ВНС). Отже, виявлені нами позитивні ефекти αЛК частково підтверджують її нейротропні, кардіо-, ангіо- і цитопротекторні властивості (В.О. Сергієнко, 2014). Таким чином, у α-ЛК, яка впливає на енергетичний метаболізм і редукцію ОС, відмічений значний потенціал, що зумовлює патогенетичну обґрунтованість для використання цього фармакологічного агента в лікуванні діабетичної КАН.
Бенфотіамін – жиророзчинний попередник вітаміну В1. Існує достатньо результатів експериментальних та клінічних досліджень, які дозволяють припустити, що гіперінсулінемія (ГІ), ІР, хронічна гіперглікемія при ЦД 2 типу негативно впливають на метаболізм тіаміну, зокрема, внаслідок пригнічення функціонального стану транспортерів тіаміну-1 (THTR-1) і THTR-2, активності транскетолази (ТК), що може призвести до накопичення інтермедіатів початкових стадій гліколізу – гліцеральдегід-3-фосфату (ГА-3-Ф), фруктозо-6-фосфату (Ф-6-Ф) і дигідроксиацетон-фосфату (ДГА-Ф). Накопичення інтермедіатів в умовах хронічної гіперглікемії посилює продукцію вільних радикалів в мітохондріях, може ініціювати індуковані гіперглікемією метаболічні шляхи, які сприяють приєднанню судинних ушкоджень, в тому числі активації РКС, акумуляції КПНГ, активації шляхів біосинтезу гексозаміну, дикарбонільних сполук. Посилення активності РКС збільшує проникність судин, активує чинник росту ендотелію судин і провокує процеси тромбоутворення в судинах внаслідок гіперекспресії інгібітора активатора плазміногена-1. Активація РКПНГ, верифікована на кардіоміоцитах (КМЦ), перицитів і подоцитів, стимулює передачу пострецепторних сигналів, формування внутрішньоклітинних активних форм О2 і гальмує експресію гена, що призводить до пошкодження функціонально-структурного стану судин. Стимуляція шляху дикарбонільних сполук сприяє подальшому збільшенню утворення КПНГ і порушенням функціонально-структурного стану КМЦ (K. Sriram et al., 2012; W.A. Nix et al., 2015). Отже, важливе значення у розвитку судинних захворювань, а також КАН при ЦД, ймовірно, належить патофізіологічним наслідкам пригнічення активності ТК і накопичення ГА-3-Ф, Ф-6-Ф і ДГА-Ф. Гальмування тіаміном утворення КПНГ може бути пов’язане з так званим ефектом КПНГ-вимикача, тобто його здатністю розщеплювати b-дикарбонільні зв’язки, утворені в результаті процесів неферментативного глікування. Клінічний потенціал тіаміну (бенфотіаміну) в комплексі лікування хворих на ЦД і/або діабетичних мікро-, макросудинних порушень узгоджується з думкою, що при ЦД спостерігається дефіцит вітаміну В1, індукований ОС і/або аутоокисненням глюкози, що сприяє окисненню тіаміну і утворенню біологічно-неактивних продуктів – тіохрому і оксодигідротіохрому. Зокрема, внутрішньоочеревинне введення мишам із стрептозотоциновим діабетом (СТД) бенфотіаміну супроводжується збільшенням показників співвідношення відновлений/окиснений глутатіон; не впливає на вміст глюкози і КПНГ і/або концентрацію карбонільних груп окисно-модифікованих білків; сприяє нівелюванню пролонгації часу піку скорочення, а також зменшенню вмісту Ca2+ в саркоплазматичному ретикулумі; не впливає на показники концентрації неактивного внутрішньоклітинного Ca2+. Отже, використання бенфотіаміну в «лікуванні» щурів із СТД супроводжується нівелюванням дисфункції міокарда на рівні клітини, що можна пояснити пригніченням процесів ОС, але не формуванням КПНГ і/або утворенням карбонільних груп окисно-модифікованих білків. Ця явна розбіжність в бенфотіамін-опосередкованому впливі щодо формування КПНГ і активації ОС вказує, що, ймовірно, інший (інші) механізм(и) можуть провокувати активацію ОС і дисфункцію процесів скорочення при ЦД. Можливими причинами є патофізіологічні зміни метаболізму глюкози в цілому і активація РКС. Крім того, бенфотіамін може безпосередньо брати участь у регуляції метаболізму глюкози. Тіамін і бенфотіамін активують ТК – ключовий фермент пентозофосфатного шляху, тим самим полегшуючи перетворення ГА-3-Ф і Ф-6-Ф в пентозо-5-фосфати. Таким чином, бенфотіамін пригнічує процеси ОС в КМЦ, не впливає на стан формування КПНГ, або утворення карбонільних груп окисно-модифікованих білків, що в цілому свідчить про здатність бенфотіаміну «рятувати» кардіоміоцити в умовах хронічної гіперглікемії, однак навряд чи впливати на формування КПНГ і/або утворення карбонільних груп окисно-модифікованих білків (L. Pacal et al., 2011; A. Adaikal akoteswari et al., 2012). Враховуючи здатність бенфотіаміну сприяти «виживанню» клітин та покращенню функціонування серцево-судинної системи при ЦД, необхідний подальший поглиблений аналіз механізмів дії і клінічного значення застосування бенфотіаміну в лікуванні КАН при ЦД. Нами обстежено 32 хворих на ЦД 2 типу із верифікованою функціональною стадією КАН у віці 50-59 років, тривалістю захворювання 16 років, показниками HbA1c 7,0±0,13%; САТ 144,9±1,67 мм рт. ст., ДАТ 90,7±1,24 мм рт. ст. Пацієнтів з ЦД 2 типу та КАН було розподілено на дві групи, які протягом 3 міс крім дієтотерапії (стіл № 9) отримували ПЦП (n=15, контроль, перша група); друга група (n=17) – дієтотерапію (стіл № 9), ПЦП і препарат Бенфогама® 300, Woerwag Pharma® GmbH & Co (300 мг/добу). Роботу проведено відповідно до етичних принципів Гельсінської декларації (2004). В результаті проведених досліджень виявлено наявність/відсутність наступних ефектів бенфотіаміну: cприяння позитивним статистично значущим змінам щодо зменшення вмісту циркулюючого інсуліну, концентрації С-реактивного протеїну (вчСРП), ФНП-α, інтерлейкіну-6 (ІЛ-6), тромбоксану В2 (TXB2), співвідношення TXB2/6-keto-простагландин F1α, (TXB2/6ketoPGF1α); позитивний статистично значущий вплив щодо зменшення показників QTc, QTd і просторового кута QRS-T, збільшення високочастотного компоненту кардіоритму (HF) в активний і пасивний період доби, зменшення ШППХ в пасивний період доби, позитивній динаміці стану ВНС у хворих на ЦД 2 типу з функціональною стадією КАН; відсутність статистично значущих змін вмісту HbA1c, препрандіальної глікемії, показників ліпідного обміну, лептину, ІЛ-8, ІЛ-10, співвідношення ФНП-α/ІЛ-10, концентрації NT-proBNP і 6ketoPG1α, показників ДМАТ в активний і пасивний період доби, показників ригідності артерій в активний період доби, Іа ао, індексу аугментації у плечовій артерії (ІА бр) в пасивний період доби. Таким чином, виявлені позитивні ефекти бенфотіаміну частково підтверджують його нейротропні, кардіо-, ангіо- і цитопротекторні властивості (В.О. Сергієнко, 2015). Широкий терапевтичний потенціал бенфотіаміну дозволяє ефективно використовувати препарати, що містять жиророзчинні похідні тіаміну, з метою регуляції активності вільнорадикальних процесів; корекції дисфункції ендотелію при серцево-судинних захворюваннях (ССЗ); стабілізації клінічного та антиоксидантного ефектів. Бенфотіамін, сприяючи підвищенню активності ТК, перешкоджає активації патофізіологічних механізмів шляхом переорієнтації напрямку метаболізму Ф-6-Ф і ГА-3-Ф; здатний сприяти корекції нейронального і судинного дефіциту за допомогою процесів, які відбуваються за участі оксиду азота (NO), що має значний терапевтичний потенціал для лікування ССЗ.
Гамма-ліноленова кислота. Вазоактивні простаноїди, метаболіти арахідоновї кислоти і дигомо-α-ЛЛК, зокрема простагландини, та інші ейкозаноїди необхідні для забезпечення фізіологічного перебігу процесів ШНП і кровотоку. В результаті подвійно-сліпого плацебо-контрольованого дослідження встановлено, що призначення хворим із ДПН γЛЛК супроводжується позитивною динамікою клінічного перебігу захворювання, а також посиленням ШНП, однак відсутні результати клінічніх довготривалих подвійно-сліпих плацебо-контрольованих досліджень.
Ацетил-L-карнітин. L-карнітин – есенціальний ко-фактор метаболізму жирних кислот, човник в переміщенні кінцевих продуктів пероксимального окиснення жирних кислот в мітохондріях; модулятор внутрішньомітохондріального відношення ацилкоензим А/коензим А. Провідна роль L-карнітину полягає в посиленні метаболізму вільних жирних кислот (ВЖК), однак існують експериментальні дані про активацію L-карнітином метаболізму глюкози. Вважається, що ЦД 2 типу характеризується порушеннями обміну L-карнітину в мітохондріях. В результаті декількох досліджень виявлено, що призначення L-карнітину сприяє деякому покращенню енергозабезпечення і функціонування лівого шлуночка (ЛШ). Пропіоніл-L-карнітин сприяє покращенню функціонального стану, використання в якості енергії окиснення глюкози в ураженому міокарді щурів (не дивлячись на збільшений рівень ВЖК). Включення L-карнітину в режим харчування діабетичних мишей з ожирінням сприяє збільшенню рівня ацил-карнітину в плазмі крові, посмугованих м’язах, печінці та жировій тканині; активності піруватдегідрогенази в посмугованих м’язах; призначення комплексу цинк-карнітин зменшує гіперглікемію та покращує толерантність до глюкози (R.M. Witteles, M.B. Fowler, 2008). Інфузія L-карнітину за допомогою гіперінсулінемічної-еуглікемічної помпи покращує контроль глікемічного профіля, знижує концентрацію циркулюючих ліпідів. Призначення L-карнітину протягом 3 або 6 міс вперше діагностованим хворим на ЦД 2 типу з порушеннями ліпідного обміну супроводжується статистично значущим зменшенням рівня ліпопротеїну (ЛП) (а) в плазмі крові. Результати подвійно-сліпого плацебо- контрольованого дослідження у пацієнтів з верифікованою гіперЛП (а) виявили, що призначення L-карнітину (2 г/добу) сприяє значному зменшенню концентрації ЛП (а) в плазмі крові; включення L-карнітину в режим харчування пацієнтів з вперше виявленим ЦД 2 типу супроводжується аналогічними змінами; комбінування L-карнітину із симвастатином (20 мг/добу) сприяє більш значному зменшенню концентрації ліпідів, зокрема тригліцеридів (ТГ) і ЛП (а), ніж монотерапія статинами. Отже, L-карнітин може використовуватись в якості одного з компонентів ліпід-модифікуючої терапії у хворих на ЦД 2 типу з КАН (R.A. Power et al., 2007; V. Serhiyenko та співавт., 2016).
Довголанцюгові ω-3 ПНЖК (ДЛ ω-3 ПНЖК). Позитивний зв’язок між споживанням ДЛ ω-3 ПНЖК, які знаходяться у риб’ячому жирі, та низькою поширеністю ішемічної хвороби серця був уперше виявлений у 1980 р. H.O. Bang, J. Dyerberg у гренландських ескімосів, що, на думку авторів, є результатом постійного споживання риби і/або морепродуктів. Відомо, що ці традиційні продукти харчування ескімосів містять велику кількість ω3 ПНЖК з риб’ячого жиру (C20C22(ω-3)). Загальне добове споживання ω-3 ПНЖК з їжею в США становить приблизно 1,6 г, причому на α-ЛЛК припадає близько 1,4 г/добу, ейкозапентаєнової (ЕПК) і докозагексаєнової кислоти (ДГК) – 0,10,2 г/добу. Оскільки коефіцієнт конверсії α-ЛЛК в ЕПК і ДГК коливається в межах 0,215%, загальна кількість доступних для організму ЕПК і ДГК в раціоні харчування в цілому значно нижча рекомендованої (P.C. Calder, 2013). Одна з гіпотез механізму впливу ω-3 ПНЖК на ритм серця базується на тому, що ω-3 ПНЖК знижують рівень ДАТ, що сприяє більш повільному ритму серця. Омега-3 ПНЖК можуть стимулювати продукцію NO, що збільшує вазодилатацію великих артерій і судин та, відповідно, знижує ДАТ; сприяти збільшенню фракції викиду ЛШ за рахунок підвищення наповнення шлуночків під час діастоли і тим самим забезпечувати енергозберігаюче діастолічне розслаблення. Омега-3 ПНЖК позитивно впливають на рівень електричного порогу, за якого викликається фібриляція шлуночків, сприяють зниженню вмісту ТХВ2, покращенню кровотоку і зниженню «жорсткості» стінки судин. Крім того, ω-3 ПНЖК змінюють провідність іонних каналів у мембранах КМЦ і тим самим запобігають розвитку аритмії. Призначення ω-3 ПНЖК сприяє підвищенню ВРС, а нормалізація параметрів ВРС поєднується з низьким ризиком «раптової» смерті. Аналіз результатів перехресного дослідження у хворих на ішемічну хворобу серця виявив, що щоденне вживання 3 і/або 6 г ЕПК і ДГК сприяє підвищенню варіабельності RR-інтервалів; при цьому зменшення співвідношення LF/HF свідчить про пригнічення активності симпатичної нервової системи (J.H. Christensen, 2011). Нами обстежено 36 хворих на ЦД 2 типу із верифікованою функціональною стадією КАН у віці 50-59 років, тривалістю захворювання 16 років, показниками HbA1c 7,04±0,12%; САТ 144,8±1,79 мм рт. ст., ДАТ 91,7±1,29 мм рт. ст. Хворих на ЦД 2 типу та КАН було розподілено на дві групи, які протягом 3 міс крім дієтотерапії (стіл № 9) отримували ПЦП (n=15, контроль, перша група); друга група (n=21) – дієтотерапію (стіл № 9), ПЦП і препарат ω-3 ПНЖК, який вміщує в одній капсулі близько 90% етилових ефірів ДЛ ω-3 ПНЖК (1000 мг), зокрема етилових ефірів ЕПК – 460 мг, ДГК – 380 мг і 4 мг α-токоферола ацетата. Роботу проведено відповідно до етичних принципів Гельсінської декларації (2004).
В результаті проведених досліджень встановлено, що використання препарату ω-3 ПНЖК протягом 3 міс не супроводжується статистично значущими змінами концентрації HbA1c, препрандіальної глікемії, ІРІ, параметрів НОМАІР у хворих на ЦД 2 типу і КАН, а також в контрольній групі. Омега-3 ПНЖК, на відміну від отриманих показників у хворих контрольної групи, сприяють статистично значущому зменшенню концентрації ТГ, параметрів КА, збільшенню вмісту ХС-ЛПВЩ, однак суттєво не впливають на динаміку концентрації ЗХС, а також ХС-ЛПНЩ в крові пацієнтів з ЦД 2 типу і функціональною стадією КАН. Призначення ω-3 ПНЖК хворим на ЦД 2 типу з функціональною стадією КАН сприяє статистично значущому зменшенню вмісту вчСРП, лептину, ФНП-α, показників ФНП-α/ІЛ-10, концентрації NT-proBNP, TXB2, співвідношення TXB2/6ketoPG1-α, збільшенню вмісту 6ketoPG1-α і в той же час не супроводжується суттєвою динамікою вмісту ІЛ-10. Використання ω-3 ПНЖК сприяє статистично значущому зменшенню QTс, QTd і просторового кута QRST і не супроводжується суттєвими змінами показників QTd, а в контрольній групі не виявлено їх позитивної динаміки. Омега-3 ПНЖК, на відміну від результатів, отриманих в контрольній групі, сприяють статистично значущому збільшенню часових параметрів ВРС: середніх NN за 5-хвилинний проміжок часу (SDANNi), стандартного відхилення всіх NN-інтервалів (SDNN) і кореня квадратного середнього від квадратів різниці послідовних RR-інтервалів (RMSSD); спектральних параметрів ВРС: низькочастотного компоненту кардіоритму (LF), HF і співвідношення LF/HF, в той же час не впливають на дуже низькочастотний компонент кардіоритму (VLF) в активний і пасивний періоди доби. Омега-3 ПНЖК сприяють статистично значущому зменшенню показників ІА ао і ШППХ в активний і пасивний періоди доби; параметрів ДАТ, а також ІП АГ ДАТ, ІЧ АГ ДАТ та SD ДАТ, в той же час не впливають на параметри САТ, ІП АГ САТ, ІЧ АГ САТ і SD САТ в активний і пасивний періоди доби. Призначення препарату ω-3 ПНЖК сприяє покращенню стану ВНС, зокрема статистично значущому зменшенню кількості балів (згідно з опитувальником А.М. Вейна).
Бенфотіамін, α-ЛК і ω-3 ПНЖК в лікуванні діабетичної КАН. Нами обстежено 43 хворих на ЦД 2 типу із функціональною стадією КАН у віці 50-59 років, тривалістю ЦД 16 років; HbA1c 6,96±0,1%; САТ 144,9±1,0 мм рт. ст. і ДАТ 90,9±0,83 мм рт. ст. Хворих розподілили на дві групи, які протягом 3 міс крім дієтотерапії (стіл № 9) отримували ПЦП (n=15, контрольна); друга група (n=28) – дієтотерапію (стіл № 9), ПЦП і 300 мг/добу бенфотіаміна, 600 мг α-ЛК/добу і одну капсулу/добу препарату ω-3 ПНЖК. Роботу проведено відповідно до етичних принципів Гельсінської декларації (2004). В результаті проведених досліджень виявлено, що комбінування бенфотіаміну, α-ЛК і α-3 ПНЖК в лікуванні хворих на ЦД 2 типу з функціональною стадією КАН сприяє статистично значущому зменшенню препрандіальної глікемії, циркулюючого інсуліну і НОМА-ІР; концентрації ЗХС, ТГ, ХСЛПНЩ, показників КА; концентрації вчСРП, лептину, ФНП-α, співвідношення ФНП-α/ІЛ-10; концентрації NT-proBNP; показників QTc, QTd і QRST; циркадного індексу (ЦІ) HF і ЦІ LF/HF; статистично значущому збільшенню ХС-ЛПВЩ; показників SDNN, SDANNi і RMSSD; спектральних параметрів ВРС в активний період доби: VLF, LF і HF-компоненти кардіоритму; LF-компоненти кардіоритму в пасивний період доби; параметрів HF-компоненти; ІА ао в активний період доби; параметрів ІА бр; показників ШППХ в активний період доби; ІА ао в пасивний період доби; показників ІА бр, а також ШППХ в пасивний період доби, в той же час не впливає на вміст ІЛ-10, співвідношення LF/ HF, показники VLF-компоненти кардіоритму, ЦІ VLF і ЦІ LF. Комбінування бенфотіаміну, α-ЛК і препарату ω-3 ПНЖК у хворих на ЦД 2 типу з КАН супроводжується найбільш вираженими позитивними статистично значущими змінами стану ВНС. Отже, комбіноване використання бенфотіаміну, α-ЛК і ω-3 ПНЖК у хворих на ЦД 2 типу з функціональною стадією КАН сприяє найбільш виразним позитивним статистично значущим змінам метаболічних і функціональних порушень. Отримані результати дозволяють вважати, що ефективність комбінованої терапії бенфотіаміном, α-ЛК і ω-3 ПНЖК не пов’язана із станом компенсації захворювання, а є результатом безпосереднього впливу цих фармакологічних агентів на досліджувані показники, що обґрунтовує доцільність її використання в лікуванні функціональної стадії КАН у хворих на ЦД 2 типу. Отже, призначення протягом 3 міс бенфотіаміну 300 мг/добу, що характеризується нейротропними, ангіо- і цитопротекторними, антиоксидантними властивостями; α-ЛК 600 мг/добу, що має потужні антиоксидантні властивості, і однієї капсули/добу препарату α-3 ПНЖК, який крім гіполіпідемічного ефекту має антиоксидантні, антиаритмічні, протизапальні, імунокорегуючі, антикоагулянтні та інші властивості, дозволяє одночасно впливати на різні ланки патогенезу КАН при ЦД 2 типу та ефективно усувати дисфункцію ВНС. Запропонована схема лікування дозволяє підвищити ефективність лікування хворих на ЦД 2 типу з КАН за відсутності побічних явищ, отримати більш виражений позитивний і стійкий ефект.
Перспективні напрямки лікування діабетичної КАН. Відродження зацікавленості до судинної гіпотези розвитку КАН, значення ОС, нейротрофічної гіпотези і значення аутоімунних порушень відкриває нові напрямки лікування. До перспективних належить пошук і використання засобів, які посилюють кровоплин через vasa vasorum, зокрема, бутапросту (аналога простацикліна), блокаторів ТХА2 і препаратів, що сприяють посиленню і/або нормалізації активності Na+, K+-АТФази (цилостазолу – п отенційного інгібітора фосфодиестерази); α-ЛК, бенфотіаміну, γЛЛК, ω-3 ПНЖК, а також одночасного призначення α-ЛК, ω-3 ПНЖК і γЛЛК. Крім того, комбіноване використання α-ЛК, бенфотіаміну, ω-3 ПНЖК, γЛЛК і ІАР є найбільш раціональним і патогенетично обґрунтованим.




