3 червня, 2016
Однократная доза нового инсулина гларгин 300 Ед/мл обеспечивает длительный стабильный гликемический контроль у японских и европейских пациентов с сахарным диабетом 1 типа
Одобрение и использование в Европе с 2000 года и в Японии с 2003 года инсулина гларгин 100 Ед/мл (Gla‑100) позволило установить, что базальная инсулинотерапия является надежным вариантом лечения для пациентов, страдающих сахарным диабетом (СД) и нуждающихся в инсулине. Gla‑100 обеспечивает эффективный гликемический контроль у лиц с диабетом, снижая частоту тяжелой и ночной гипогликемии по сравнению с НПХ-инсулином в японской и европейской популяциях [1, 2]. Тем не менее существует потенциал для дальнейшего совершенствования лечения диабета с помощью разработки новых аналогов инсулина, которые обеспечивают достижение гликемических целей с большим снижением риска гипогликемии и большей гибкостью в выборе времени инъекций базального инсулина. Недавно был разработан новый инсулин гларгин 300 Ед/мл (Gla‑300), который обеспечивает стабильную активность и большую продолжительность действия и может способствовать оптимизации лечения СД.
Введение
Как и в Gla‑100, в Gla‑300 используется принцип подкожной преципитации для замедления высвобождения. Было сделано предположение, что скорость повторного растворения подкожного депо Gla‑300 меньше, что может обеспечить более стабильный и продолжительный фармакокинетический и фармакодинамический профили с улучшением контроля уровня глюкозы в крови по сравнению с Gla‑100.
Для того чтобы подтвердить потенциальные преимущества Gla‑300 по сравнению с Gla‑100, были выполнены исследования с использованием эугликемического клэмп-метода (ЭК), в которых оценивали фармакокинетические и фармакодинамические профили одно- и многократных инъекций Gla‑300 в сравнении с Gla‑100 в разных дозах у лиц с СД 1 типа [3, 4]. В настоящей работе рассматриваются два исследования с ЭК-тестом, посвященные сравнительной оценке фармакокинетических и фармакодинамических профилей однократных инъекций Gla‑300 и Gla‑100 и проведенные на японской (NCT01493115) и европейской когортах (NCT01195454).
Материалы и методы
Участники
Первое исследование включало японских мужчин и женщин в возрасте 20-65 лет с СД 1 типа длительностью ≥1 года, диагностированным в соответствии с рекомендациями Японского диабетического общества [5].
Во втором исследовании принимали участие европейские мужчины и женщины в возрасте 18-65 лет с СД 1 типа длительностью ≥1 года, диагностированным в соответствии с рекомендациями Американской диабетической ассоциации [6].
В обоих исследованиях критериями включения были: стабильный режим инсулинотерапии в течение ≥2 месяцев, общая доза инсулина <1,2 Ед/кг/сут, индекс массы тела (ИМТ) 18-30 кг/м2, концентрация C-пептида в сыворотке натощак <0,3 нмоль/л, уровень гликозилированного гемоглобина (HbA1c) ≤8,6% в японском исследовании и ≤9% – в европейском [7].
Основным критерием исключения было отсутствие к моменту проведения исследования и в анамнезе другого клинически значимого заболевания.
Дизайн исследования и лечение
Японское исследование было одноцентровым рандомизированным двойным слепым перекрестным с тремя группами, тремя периодами лечения и тремя разными последовательностями назначения вариантов терапии. Участники были рандомизированы в одну из трех групп с разной последовательностью назначения однократных подкожных инъекций Gla‑300 0,4 и 0,6 Ед/кг и Gla‑100 0,4 Ед/кг с периодом вымывания 6-20 дней между вариантами лечения (рис. 1А).
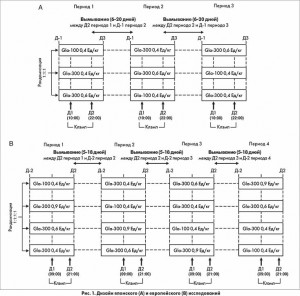
Европейское исследование было одноцентровым рандомизированным двойным слепым перекрестным с четырьмя группами, четырьмя периодами и четырьмя разными последовательностями назначения вариантов лечения. Участники были рандомизированы в одну из четырех групп с разной последовательностью назначения однократных подкожных инъекций Gla‑300 0,4, 0,6 и 0,9 Ед/кг и Gla‑100 0,4 Ед/кг с периодом вымывания 5-18 дней между вариантами лечения (рис. 1B).
В обоих исследованиях инсулин вводили подкожно в околопупочной области живота натощак.
Оценка
В течение каждого периода лечения выполнялась процедура ЭК. Участников обоих исследований постепенно переводили с их текущего режима инсулинотерапии. В японском исследовании пациентов подключали к устройству для ЭК после ночного голодания (≥10 ч) и примерно за 2 ч до применения препарата. В европейском исследовании участники подключались к устройству приблизительно за 5 ч до введения дозы инсулина. Уровень глюкозы крови поддерживали в эугликемическом диапазоне 4,4-6,6 ммоль/л с помощью внутривенной инфузии инсулина глюлизин и глюкозы. Когда уровень глюкозы в крови оставался стабильным (5,5 ммоль/л ± 20%) в течение не менее 1 ч без инфузии глюкозы введение инсулина глюлизин прекращали и выполняли инъекцию Gla‑300 или Gla‑100. Целевой уровень глюкозы в крови (5,5 ммоль/л) поддерживали в течение всего периода ЭК-теста (36 ч). Дополнительные дозы инсулина короткого действия (например, инсулина глюлизин) вводили, если уровень глюкозы в крови превышал 13,9 ммоль/л или 11,1 ммоль/л в течение 30 мин в японском и европейском исследованиях соответственно. Образцы крови для оценки концентрации инсулина гларгин (INS) собирали перед введением дозы препарата и через 1, 2, 4, 6, 8, 12, 16, 20, 24, 28, 32 и 36 ч после. Из-за перекрестной реактивности с другими инсулинами INS определяли только до применения инсулина короткого действия, а после этого устанавливалось значение, равное нулю. В обоих исследованиях оценивали общий уровень самого инсулина гларгин вместе с его активными метаболитами (21A-Gly-инсулин и 21A-Gly-des‑30B-Thr-инсулин) с помощью радиоиммунологического анализа, а в японском исследовании дополнительно – отдельные концентрации инсулина гларгин и метаболитов с помощью жидкостной хроматографии и тандемной масс-спектрометрии с нижним пределом количественного определения 30 пмоль/л (5,02 мкЕд/мл).
Фармакокинетическими конечными точками в обоих исследованиях были площадь под кривой «концентрация инсулина – время» в диапазоне от 0 до 24 и 36 ч после введения дозы (INS-AUC0-24/36), время до достижения 50% от INS-AUC0-36 (T50%-INS-AUC0-36), максимальная концентрация инсулина гларгин (INS-C max) и время до достижения INS-C max (INS-T max).
Фармакодинамическими конечными точками в обоих исследованиях были активность инсулина, оцениваемая по площади под кривой «стандартизированная по массе тела скорость инфузии глюкозы (GIR) – время» в диапазоне от 0 до 36 ч (GIR-AUC0-36), время до достижения 50% от GIR-AUC0-36 (T50%-GIR-AUC0-36) и длительность контроля уровня глюкозы в заранее установленном диапазоне (время от введения дозы препарата до последнего значения сглаженной кривой концентрации глюкозы крови ≤6,1; 7,2 и 8,3 ммоль/л). Вспомогательными критериями оценки были максимальные значения GIR, определенные с помощью метода локально взвешенной регрессии (GIR max) и время до достижения GIR max (GIR-T max). В европейском исследовании также оценивали GIR-AUC0-24.
Оценка безопасности выполнена у всех участников, которым была введена по меньшей мере одна доза исследуемого препарата, и включала регистрацию нежелательных явлений, электрокардиографию (ЭКГ), определение показателей жизненно важных функций, лабораторные тесты, определение уровня антител к инсулину, оценку местной переносимости препарата. Нежелательные явления оценивали по степени тяжести и возможной связи с исследуемым препаратом.
Результаты
Участники
В японском исследовании приняли участие в общей сложности 18 пациентов с СД 1 типа (16 мужчин и 2 женщины). Средний возраст составил 34,8±11,5 года, ИМТ – 22,42±2,10 кг/м2. Все рандомизированные участники завершили исследование.
В европейское исследование включили 24 пациента с СД 1 типа (5 женщин и 19 мужчин) со средним возрастом 42,6±10,0 лет и ИМТ 25,6±2,0 кг/м2. Два человека досрочно прекратили участие в исследовании по причинам личного характера, в результате чего исследуемую когорту составили 22 пациента.
Фармакокинетика
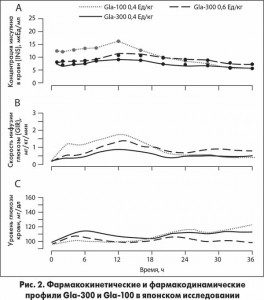
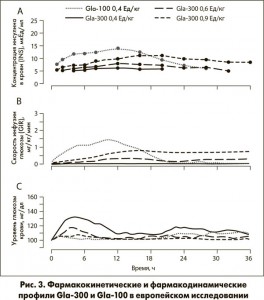
Фармакокинетические профили Gla‑300 и Gla‑100 после однократной инъекции показаны на рисунке 2А для японского исследования и на рисунке 3А для европейского. Было установлено, что Gla‑300 и Gla‑100 имеют различные фармакокинетические профили независимо от дозы препарата и этнической принадлежности участников.
Кривые INS обеих доз Gla‑300 не имели ярко выраженных пиков, хотя высота кривой увеличивалась с повышением дозы. GLA‑100 показал более отчетливое повышение концентрации, достигая максимума через 12 ч с последующим снижением.
INS-C max и INS-AUC0-24 были больше для Gla‑100 по сравнению со всеми дозами Gla‑300. Только для дозы Gla‑300 0,9 Ед/кг, которую применяли в европейском исследовании, INS-AUC0-36 была больше, чем для Gla‑100.
INS-T max и T50%-INS-AUC0-36 были больше для всех доз Gla‑300 по сравнению с Gla‑100 в обоих исследованиях. Медиана INS была достигнута через 32 и 36 ч после введения дозы Gla‑300 0,6 Ед/кг (в европейском и японском исследовании соответственно) и через 36 ч после введения дозы Gla‑300 0,9 Ед/кг (только европейские участники).
Фармакодинамика
Фармакодинамические профили Gla‑300 и Gla‑100 после однократной инъекции показаны на рисунках 2В и 2С для японского исследования и на рисунках 3B и 3C для европейского.
В обоих исследованиях Gla‑300 и Gla‑100 имели различные фармакодинамические профили, что соответствует отличиям в их фармакокинетике.
В японском исследовании уровень глюкозы в крови для обеих доз Gla‑300 постепенно повышался примерно к 6 часу, а затем стабилизировался на целевом уровне до 36 ч. В отличие от него Gla‑100 поддерживал уровень глюкозы в крови на целевом уровне примерно до 24 часов, а затем ее концентрация постепенно возрастала. В европейском исследовании глюкодинамический эффект также наблюдался в течение 36 часов.
В обоих исследованиях активность инсулина для всех доз GLA‑300 нарастала плавнее, а GIR max были меньше, чем у Gla‑100 (рис. 2B и 3B). Общее потребление экзогенной глюкозы (GIR-AUC0-36) возрастало с увеличением дозы GLA‑300, но только для дозы 0,9 Ед/кг этот показатель был больше, чем у Gla‑100 0,4 Ед/кг.
В соответствии с профилями GIR показатель T50%-GIR-AUC0-36 сдвинулся примерно на 5-7 ч для GLA‑300 (до 18 ч после введения дозы). Из-за заранее установленного времени завершения ЭК-теста через 36 ч полная длительность активности Gla‑300 не могла быть оценена.
Концентрация метаболитов
В отдельном анализе японской когорты, в котором оценивали концентрацию метаболитов инсулина гларгин, было показано, что концентрация основного метаболита (21A-Gly-инсулин) для всех видов лечения примерно в три раза превышала нижний предел количественного определения (30 пмоль/л или 0,2 нг/мл). Самая высокая концентрация наблюдалась при применении Gla‑100 (104 пмоль/л или 0,628 нг/мл), а затем – Gla‑300 0,6 Ед/кг (75 пмоль/л или 0,452 нг/мл) и 0,4 Ед/кг (66 пмоль/л или 0,402 нг/мл). Напротив, в большинстве индивидуальных образцов крови концентрация самого инсулина гларгин и второго метаболита была ниже нижнего предела количественного определения.
Безопасность
В обоих исследованиях Gla‑300 и Gla‑100 хорошо переносились без отличий по профилю безопасности. Титры антител против инсулина и кросс-реактивность не претерпели значительных изменений в течение всего исследования. Никаких серьезных нежелательных явлений или случаев досрочного выбывания из исследования в связи с неблагоприятными событиями не было зафиксировано ни в одном из исследований.
Обсуждение
В этих двух исследованиях с использованием ЭК-теста, с одинаковым дизайном и участием японских и европейских пациентов с СД 1 типа были показаны различия фармакокинетических и фармакодинамических профилей Gla‑100 и Gla‑300. Концентрация инсулина и его активность при применении Gla‑300 нарастали более плавно, были более стабильными и длительными по сравнению с Gla‑100. Это сопровождалось более равномерным метаболическим эффектом Gla‑300, наблюдаемым в частности при введении Gla‑300 0,6 и 0,9 Ед/кг и проявляющимся в увеличении T50%-GIR-AUC0-36 (примерно 18 ч) по сравнению с Gla‑100 (примерно 12 ч). В результате контроль уровня глюкозы в крови был более устойчивым и сохранялся в течение 36 часов для всех доз Gla‑300. Потенциально Gla‑300 может быть активным и спустя 36 часов. Следует отметить, что самая высокая доза Gla‑300 (0,9 Ед/кг) не оценивалась в японском исследовании, поскольку это не актуально для рутинной клинической практики в этой стране, где обычно используются более низкие дозы Gla‑100 по сравнению с западными странами.
Результаты этих исследований позволяют предположить, что рН-зависимая преципитация и повторное растворение инсулина гларгин зависит от концентрации введенного раствора [9]. Это контрастирует с инсулинами, которые остаются растворимыми после инъекции. Этот специфичный для гларгина феномен может основываться на поверхность-зависимом высвобождении, которое пропорционально объему связанного аморфного осадка.
Фармакокинетические и фармакодинамические показатели в японском и европейском исследовании в целом согласовывались друг с другом, что позволяет предположить подобные результаты при стабильных состояниях и в других популяциях [3]. На основании этого сходства можно ожидать, что потенциальные преимущества в управлении диабетом при применении Gla‑300 один раз в день в связи с более стабильными фармакокинетическим и фармакодинамическим профилями по сравнению с Gla‑100 будут наблюдаться в разных этнических группах. Эти преимущества включают достижение гликемических целей с меньшим риском гипогликемии и большей гибкостью в интервалах между дозированиями.
Продолжающаяся программа клинических испытаний EDITION, посвященная сравнению гликемического контроля и частоты гипогликемии на фоне терапии Gla‑300 и Gla‑100 в различных популяциях больных СД 1 и 2 типа, поможет определить, проявятся ли более стабильные и длительные фармакокинетические и фармакодинамические профили Gla‑300 в виде клинических преимуществ. Полученные к настоящему времени результаты этой программы показывают, что Gla‑300 является столь же эффективным, как Gla‑100, в достижении гликемического контроля, но с меньшим риском гипогликемии и увеличения массы тела [10-15].
Литература
1. Yamamoto-Honda R., Takahashi Y., Yoshida Y. et al. Use of insulin glargine in Japanese patients with type 1 diabetes. Intern Med 2007; 46: 937-943.
2. Pieber T.R., Eugene-Jolchine I., Derobert E. Efficacy and safety of HOE901 versus NPH insulin in patients with type 1 diabetes. The European Study Group of HOE901 in type 1 diabetes. Diabetes Care 2000; 23: 157-162.
3. Jax T., Heise H., Dahmen R. et al. New insulin glargine formulation has a flat and prolonged steady state profile in subjects with type 1 diabetes. Diabetologia 2013; 56(Suppl. 1): S414.
4. Tillner J., Bergmann K., Teichert L., Dahmen R., Heise T., Becker R.H.A. Euglycaemic single dose clamp profile of new insulin glargine formulation in subjects with type 1 diabetes is flat and prolonged. Diabetologia 2013; 56(Suppl. 1): S415.
5. Seino Y., Nanjo K., Tajima N. et al. Report of the Committee on the classification and diagnostic criteria of diabetes mellitus. Diabetol Int 2010; 1: 2-20.
6. The Expert Committee On The Diagnosis And Classification Of Diabetes Mellitus. Report of the expert committee on the diagnosis and classification of diabetes mellitus. Diabetes Care 1998; 21: S5-S19.
7. Kashiwagi A., Kasuga M., Araki E. et al. International clinical harmonization of glycated hemoglobin in Japan: from Japan Diabetes Society to National Glycohemoglobin Standardization Program values. J Diabetes Investig 2012; 3: 39-40.
8. Steinstraesser A., Schmidt R., Bergmann K., Dahmen R., Becker R.H. Investigational new insulin glargine 300 U/ml has the same metabolism as insulin glargine 100 U/ml. Diabetes Obes Metab 2014; 16: 873-876.
9. Cochran E., Musso C., Gorden P. The use of U‑500 in patients with extreme insulin resistance. Diabetes Care 2005; 28: 1240-1244.
10. Riddle M.C., Bolli G.B., Zieman M., Meuhlen-Bartmer I., Bizet F., Home P.D. New insulin glargine 300 units/mL versus glargine 100 units/mL in people with type 2 diabetes using basal and mealtime insulin: glucose control and hypoglycemia in a 6-month randomized controlled trial (EDITION1). Diabetes Care 2014; 37: 2755-2762.
11. Yki-Jarvinen H., Bergenstal R.M., Ziemen M. et al. New insulin glargine 300 units/mL versus glargine 100 units/mL in people with type 2 diabetes using oral agents and basal insulin: glucose control and hypoglycemia in a 6-month randomized controlled trial (EDITION2). Diabetes Care 2014; 37: 3235-3243.
12. Bolli G.B., Riddle M.C., Bergenstal B. et al. New insulin glargine 300 U/mL: glycemic control and hypoglycemia in insulin naive people with T2DM (EDITION3) (Abstract). Diabetes 2014; 63(Suppl. 1): A19.
13. Home P.D., Bergenstal B., Riddle M.C. et al. Glycemic control and hypoglycemia with new insulin glargine 300 U/mL in people with T1DM (EDITION4) (Abstract). Diabetes 2014; 63(Suppl. 1A): LB19.
14. Matsuhisa M., Koyama M., Cheng X.N., Shimizu S., Hirose T. New insulin glargine 300 U/mL: glycemic control and hypoglycemia in Japanese people with T1DM (EDITION JP 1) (Abstract). Diabetes 2014; 63(Suppl. 1A): LB22.
15. Terauchi Y., Koyama M., Cheng X.N., Shimizu S., Hirose T. Glycemic control and hypoglycemia in Japanese people with T2DM receiving new insulin glargine 300 U/mLin combination with OADs (EDITION JP 2) (Abstract). Diabetes 2014; 63(Suppl. 1A): LB24.
Diabetes, Obesity and Metabolism 17: 254-260, 2015.
Статья представлена в сокращении.
Перевод с англ. Натальи Мищенко


