31 серпня, 2015
Декомпенсований діабет та інсульт: деякі секрети ведення хворих із поєднаною патологією
Відомо, що важливим фактором ризику виникнення цереброваскулярних захворювань є цукровий діабет (ЦД). У хворих на ЦД ризик ішемічного інсульту вищий у 1,8-6 разів (C.M. Burchfiel et al., 1994), при цьому наявність і вираженість діабетичної ангіопатії значною мірою визначає прогноз захворювання. У літературі переважно висвітлюються фактори ризику та патогенез інсульту у хворих на ЦД, але представлено недостатньо даних про особливості перебігу й інтенсивну терапію пацієнтів з інсультом та декомпенсованим ЦД. Про особливості ведення таких хворих розповів доцент кафедри анестезіології та інтенсивної терапії Національної медичної академії післядипломної освіти ім. П.Л. Шупика, кандидат медичних наук Олександр Анатолійович Галушко. Його доповідь була представлена на VII британсько-українському симпозіумі з питань анестезіології, інтенсивної терапії та медицини болю, що проходив 22-25 квітня 2015 року у м. Києві.
Глибокі та різнобічні порушення метаболічних процесів, властиві ЦД, можуть за певних умов призводити до надтяжких ускладнень, що становлять безпосередню загрозу життю хворого та вимагають невідкладної допомоги. До таких критичних (невідкладних) станів при ЦД належать кетоацидоз і різні види коматозних станів (кетоацидотична, гіперосмолярна, гіпоглікемічна, молочнокисла коми). Найбільші складнощі у лікарів викликає диференційна діагностика та поєднання інсульту з кетоацидозом (переважно у хворих на ЦД 1 типу) та гіперосмолярним синдромом – ГОС (переважно у хворих на ЦД 2 типу), тому увагу приділено саме цим станам.
Діабетичний кетоацидоз
Діабетичний кетоацидоз (ДКА) – стан вираженої декомпенсації захворювання, зумовлений абсолютним дефіцитом інсуліну, підвищенням рівня контрінсулярних гормонів, різким зниженням утилізації глюкози тканинами, активацією ліполізу та кетогенезу.
Зазвичай кетоацидоз ускладнює перебіг ЦД 1 типу. Причиною його розвитку можуть бути неадекватна цукрознижувальна терапія, інфекції, гострі неінфекційні захворювання, вживання деяких ліків тощо.
Клінічні прояви ДКА вперше описав Дрешфельд у 1886 році. З того часу і аж до початку застосування інсуліну в 1922 році смертність від цього ускладнення наближалася до 100%. Широке впровадження в практику інсулінотерапії знизило смертність до 30%, а з удосконаленням методів інтенсивної терапії відбулося подальше її зниження до 2-5%.
Проблема ДКА та інсульту має кілька граней. По-перше, численні літературні дані свідчать про те, що дія гормонів стресу на фоні цереброваскулярного захворювання може викликати та поглиблювати ДКА. По-друге, ДКА є фактором ризику розвитку інсульту та погіршення його перебігу. Пов’язане це з тим, що при кетоацидозі, як правило, присутні системне запалення, оксидативний стрес, ендотеліальна дисфункція, судинні розлади, коагулопатія, через які підвищується ризик ішемічних і геморагічних ускладнень (J.A. Edge et al., 2001; N.S. Glaser et al., 2004; J.J. Lin et al., 2008). А на початку лікування ДКА, коли відновлюється перфузія головного мозку, можуть виникати реперфузійні ушкодження (J. Alvarez-Sabin et al., 2004). По-третє, ці патологічні стани можуть виникати й поодинці та через подібність клінічної картини дезорієнтувати лікаря та сприяти вибору неоптимальної тактики лікування. Зокрема, досить складним завданням виявляється диференційна діагностика інсульту та енцефалопатичної форми ДКА, яка є «завершальним акордом» діабетичної коми й характеризується глибокими порушеннями функції головного мозку. Інтерпретація симптоматики особливо ускладнюється у літніх і менш комунікативних пацієнтів. Таким чином, ДКА та інсульт можуть спостерігатись окремо або провокувати розвиток одне одного, але в будь-якому випадку необхідна ретельна диференційна діагностика, адже ці стани потребують різних терапевтичних втручань.
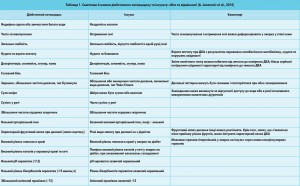
В таблиці 1 наведено основні симптоми й ознаки ДКА та інсульту, а також відмічено збіги та відмінності, на які має звернути увагу лікар. З таблиці видно, що досить важко диференціювати ДКА та інсульт за клінічними симптомами. Найважливіші відмінності полягають у результатах аналізу кислотно-лужного стану крові. Отже, у всіх пацієнтів із ЦД та підозрою на інсульт для своєчасної діагностики ДКА необхідно визначити рН та рівень бікарбонату в крові. Про виражений кетоацидоз свідчать показники pH <7,25 та бікарбонату <15 ммоль/л, про м’який/компенсований – рН 7,25-7,35 та бікарбонат 15-22 ммоль/л. Порушення дихання може ще більше ускладнити диференційну діагностику, оскільки ацидоз може бути наслідком не тільки метаболічних, але й респіраторних порушень. У таких випадках може бути корисним вимірювання аніонного проміжку.
Слід також зазначити, що внаслідок інсульт-індукованого стресу рівень глюкози підвищений у більшості хворих на ЦД з кетоацидозом чи без нього. У диференціюванні симптоматичної стресової гіперглікемії може допомогти визначення рівня глікозильованого гемоглобіну.
Терапія ДКА, у тому числі на фоні інсульту, має бути спрямована на корекцію широкого спектра метаболічних порушень. Важливо розуміти, що ДКА є наслідком взаємопоєднаного розвитку гіперглікемії, гіперкетонемії, метаболічного ацидозу, дегідратації та дисбалансу електролітів (І.П. Шлапак і співавт., 2010). Виходячи з цього, основні напрями лікувальної тактики включають: регідратацію; інсулінотерапію; парціальну корекцію метаболічного ацидозу тяжкого ступеня; призначення препаратів антикетогенної дії (глюкоза з інсуліном, Ксилат); компенсацію втрат електролітів, насамперед калію. Необхідно забезпечити постійне спостереження за станом хворого (важливого значення набуває достатня компетентність персоналу). Хворі з ознаками ДКА тяжкого ступеня потребують госпіталізації у відділення інтенсивної терапії.
Інфузійну терапію при ДКА слід розпочинати енергійно і в перші години проводити в високому темпі. Рекомендовані об’єми стартової інфузійної терапії при гіперглікемічних кризах наведено у таблиці 2.
 При інсульті на фоні ЦД інфузійна терапія має певні особливості. Інфузійна підтримка має проводитись обережно і невеликими порціями, з постійним контролем артеріального тиску, гематокриту і рівня натрію. Оскільки рідинна ресусцитація має бути обмеженою, слід очікувати, що ДКА може мати тривалий клінічний перебіг, що несе значний ризик розвитку нових інсультів та ускладнень (A. Jovanovic et al., 2014).
При інсульті на фоні ЦД інфузійна терапія має певні особливості. Інфузійна підтримка має проводитись обережно і невеликими порціями, з постійним контролем артеріального тиску, гематокриту і рівня натрію. Оскільки рідинна ресусцитація має бути обмеженою, слід очікувати, що ДКА може мати тривалий клінічний перебіг, що несе значний ризик розвитку нових інсультів та ускладнень (A. Jovanovic et al., 2014).
При вирішенні питання про спосіб доступу до судинного русла слід пам’ятати, що мінімально інвазивні процедури (катетеризація периферичної вени) мають переваги перед встановленням центрального венозного катетера, оскільки він може бути фактором ризику тромбоемболії судин головного мозку (R.E. Kusminsky, 2007).
Інсулінотерапія відіграє ключову роль у лікуванні ДКА. Її розпочинають одразу після встановлення факту наявності у хворого гіперглікемії та ознак декомпенсації ЦД. Використовується інсулін короткої дії. Доведено, що інсулінотерапія в режимі малих доз більш ефективна і безпечна. Великі дози інсуліну (>20 ОД за одне введення) можуть надто різко знизити рівень глюкози крові, що може призвести до гіпоглікемії, набряку мозку та низки інших ускладнень. Крім того, різке зниження концентрації глюкози супроводжується не менш різким падінням концентрації калію в сироватці, тому в разі використання великих доз інсуліну небезпека гіпокаліємії різко збільшується. Стартовий болюс інсуліну становить 0,15 ОД/кг (близько 10 ОД) внутрішньовенно. Потім потрібно налагодити постійну інфузію. Рекомендується застосовувати пристрої для постійного дозованого введення (інфузомати). Початкова швидкість має становити 4-5 ОД/год (орієнтовний розрахунок 0,05-0,1 ОД/кг/год). Контроль глікемії слід проводити щогодини. Швидкість зниження гіперглікемії не повинна перевищувати 2-3 ммоль/л за годину. Якщо рівень глікемії за перші 3 години не знизився на 30% від початкового рівня (по 10% за годину), то швидкість збільшують удвічі. При зменшенні глікемії до 16,7 ммоль/л – швидкість введення зменшують до 2-4 ОД/год. Після досягнення 14 ммоль/л у програму інфузійної терапії додають розчини 5% глюкози з адекватною кількістю інсуліну.
Щодо корекції метаболічного ацидозу слід пам’ятати, що діабетичний ацидоз розвивається через посилене надходження кетонових тіл унаслідок інсулінової недостатності. Тому етіологічним лікуванням цього виду ацидозу є замісна інсулінотерапія, яка в більшості випадків допомагає його усунути. Гідрокарбонат натрію посилює властиву ДКА гіпокаліємію, викликає гіпернатріємію, гіперосмолярність, посилює внутрішньоклітинний ацидоз та ацидоз спинномозкової рідини, особливо в нейронах головного мозку за рахунок швидкого надходження СО2 в спинномозкову рідину та всередину клітини, що може призводити до набряку мозку. Нині рекомендації щодо використання бікарбонату натрію при ДКА обмежені необхідністю парціальної корекції метаболічного ацидозу тяжкого ступеня (рН крові <7,1). Якщо немає можливості визначити показники кислотно-лужного стану, за наявності гіперпное можливе використання бікарбонату натрію в дозі 1 ммоль/кг маси тіла одноразово.
Важливу роль у лікуванні пацієнтів з ДКА відіграють препарати антикетогенної дії, зокрема ксилітол – п’ятиатомний спирт, який при парентеральному введенні швидко включається в загальний метаболізм. Вважається, що ксилітолу властива найбільша антикетогенна дія серед усіх відомих речовин. Вона реалізується через кілька механізмів:
– включення в пентозофосфатний цикл як джерело гліцерофосфату, що зменшує кількість вільних жирних кислот, здатних окиснюватися до ацетил-коА;
– підвищення інтенсивності гліколізу з посиленням утворення піровиноградної кислоти, яка сприяє окисленню ацетил-коА в циклі Кребса;
– посилення глікогеноутворення в печінці, що зменшує мобілізацію жиру на периферії;
– стимуляцію секреції інсуліну (Е.П. Коновалов и соавт., 2005).
На українському ринку представлено препарат Ксилат, основним компонентом якого є ксилітол.
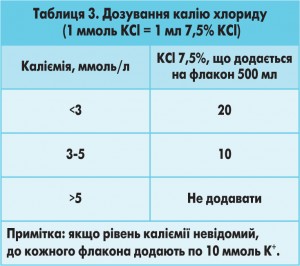
Компенсація втрат калію є ще одним важливим компонентом ведення хворих з ДКА. Вихідний рівень калію в сироватці хворих з ДКА частіше перевищує норму, але через 3-5 годин швидко виникає гіпокаліємія внаслідок інтенсивного повернення калію у внутрішньоклітинний сектор. У цей час гіпокаліємія й пов’язані з нею аритмії стають реальною загрозою. Орієнтоване дозування калію хлориду залежить від рівня каліємії (табл. 3). Дозу калію титрують для підтримання каліємії на рівні 4-5 ммоль/л (під контролем рівня калію, який проводять спочатку кожні 2 години, потім – через 4 години).
 Слід обов’язково проводити моніторинг ЕКГ, однак це не може заміняти визначення рівня каліємії.
Слід обов’язково проводити моніторинг ЕКГ, однак це не може заміняти визначення рівня каліємії.
Важливо пам’ятати, що терапію препаратами калію не розпочинають при олігурії (діурез <30 мл/год) і при концентрації калію в сироватці понад 5 ммоль/л.
Ефективне лікування ДКА передбачає також виявлення та лікування захворювання, яке спричинило декомпенсацію діабету. Часто такою причиною є інфекція сечових або дихальних шляхів, зазвичай прихована. З метою діагностики проводять посіви крові та середньої порції сечі, рентгенологічне дослідження грудної клітки тощо. Застосовувати антибіотики всім пацієнтам з підозрою на інфекцію в рутинній практиці не рекомендують, але іноді їх застосування виправдане в період очікування результатів бактеріологічних посівів, особливо у осіб похилого віку та пацієнтів з гіпотензією.
Дискусійним питанням є використання діуретиків у пацієнтів з ДКА. Паралельне й інтенсивне використання осмотичних розчинів (наприклад, манітолу) та петльових діуретиків (фуросеміду, торасеміду і буметаніду) може посилити наявний рівень зневоднення і поглибити тяжкість ДКА. Одночасне застосування регідратації та осмотичних діуретиків застосовується на практиці, але чіткі терапевтичні принципи та алгоритми такого лікування відсутні. Невідомі також оптимальна швидкість регідратації, відповідні дози осмотичних та інших діуретиків, залишаються дискусійними й способи моніторингу обсягу навантаження, включаючи вимірювання центрального венозного тиску.
Оцінка ефективності терапії хворих з ДКА має включати регулярний контроль неврологічного статусу. Вважається, що корекція гіперглікемії та кетозу зумовлює його покращення. Якщо виявляється погіршення неврологічного стану в процесі терапії, слід виключити можливі його причини: набряк мозку (до 10% випадків), інсульт, інфекцію ЦНС, черепно-мозкову травму. У зв’язку з клінічним припущенням наявності цих станів слід виконати відповідні діагностичні процедури і корекцію терапії.
Гіперосмолярний синдром
ГОС – ще одна загрозлива для життя хворих на ЦД патологія, що потребує невідкладної допомоги. Для неї характерні висока гіперглікемія та гіперосмолярність за незначного кетозу або його відсутності.
ДКА зазвичай розвивається при декомпенсаціі ЦД 1 типу, а ГОС – при ЦД 2 типу. Пов’язане це з тим, що при ЦД 2 типу збережена певною мірою секреція інсуліну, який спрямовує глюкозу на поєднання з ацетил-КоА, що не переходить на кетогенез, а утилізується у циклі Кребса. Також при ЦД 2 типу знижена секреція гормонів-антагоністів інсуліну, зокрема глюкагону. Доведено, що підвищення секреції глюкагону сприяє ліполізу і, відповідно, кетогенезу. Нарешті, гіперосмолярність пригнічує ліполіз і поєднані з ним кетогенез із кетоацидозом. Так виникає гіперглікемія без кетоацидозу.
Смертність від гіперосмолярної коми коливається від 10 до 60%. Це значно вищий показник, ніж при ДКА, за якого летальність становить від 1,2 до 9%.
В клінічній картині ГОС переважають ознаки вираженої дегідратації: зниження тургору шкіри (що буває важко встановити у похилих людей), сухість слизової оболонки, холодні кінцівки, слабкий пульс. Часто спостерігається артеріальна гіпотензія різного ступеня тяжкості, у тому числі шоковий синдром.
Клінічну картину ГОС підтверджує комплекс клініко-лабораторних ознак, зокрема:
– гіперглікемія (від 30 до 55,5 ммоль/л і більше);
– гіперосмолярність плазми крові (від 320 мОсм/л і більше);
– підвищений гематокрит (часто перевищує 55%);
– лейкоцитоз;
– азотемія (досить часто);
– кетонемія та кетонурія зазвичай відсутні.
Отже, для діагностики цього патологічного стану обов’язково необхідно визначити осмоляльність сироватки або її осмотичний тиск методом реєстрації пониження точки її замерзання. У нормі цей показник становить 285-293 мОсм/кг води. Осмоляльність або осмолярність сироватки можна визначити і розрахунковим способом. До формули обчислення осмолярності, рекомендованої Американською діабетичною асоціацією, входять лише натрій та глюкоза:
Осмолярність = (2 × натрій [ммоль/л]) + глюкоза (ммоль/л).
Інсульт може провокувати розвиток ГОС у хворого на ЦД, а ГОС, в свою чергу, може значно погіршувати перебіг цереброваскулярного захворювання. Встановлено, що вже при підвищенні осмолярності крові >300 мОсм/л виникають ознаки неврологічних порушень, зумовлені дегідратацією головного мозку (А.П. Зільбер, 1995). Було показано, що гостра та тяжка гіперглікемія сприяють апоптозу нейронів і редукції росту нейритів (H. Honma, 2003). Неврологічні порушення можуть виникати навіть у відтермінований період ГОС. Так, повідомлялося про розвиток тетраплегії на 5-й день після госпіталізації пацієнтки до стаціонару (A. Allione, 2004).
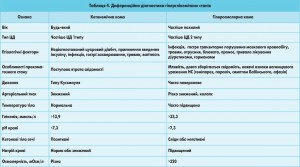
ДКА та ГОС потребують дещо різних підходів до інтенсивної терапії, тому важливо вміти розрізняти ці стани. Диференційну діагностику цих гіперглікемічних невідкладних станів наведено у таблиці 4.
 Ураховуючи тяжкість клінічного стану пацієнтів, їх преморбідний статус і належність до старшої вікової групи, рекомендується госпіталізація до відділення інтенсивної терапії, де необхідно:
Ураховуючи тяжкість клінічного стану пацієнтів, їх преморбідний статус і належність до старшої вікової групи, рекомендується госпіталізація до відділення інтенсивної терапії, де необхідно:
– катетеризувати центральну вену, виміряти центральний венозний тиск, налагодити інфузійну терапію;
– катетеризувати сечовий міхур для погодинного оцінювання водного балансу;
– поставити зонд у шлунок;
– за необхідності провести інтубацію трахеї.
Регідратація – найважливіший компонент лікування ГОС. До зниження осмолярності плазми <330 мОсм/л можна вводити гіпотонічний 0,45% розчин NaCl, надалі – тільки ізотонічні розчини. Вважається, що використання гіпотонічних розчинів має більший ризик виникнення набряку мозку, а також розвитку дифузної демієлінізації. Однак при гіперосмолярності плазми з гіпернатріємією >150 ммоль/л рекомендовано використовувати 0,45% розчин натрію хлориду. Осмолярність сироватки слід знижувати поступово – у межах 3 мОсм/л за годину. Для попередження розвитку ускладнень інфузійну терапію сольовими розчинами слід доповнювати введенням колоїдних розчинів, які здатні утримуватися в судинному руслі та підтримувати онкотичний тиск і рН крові. Слід уникати переливання гіперосмолярних розчинів.
Проведення інсулінотерапії при ГОС також має певні особливості. Найважливіше, що треба пам’ятати: інсулінотерапію необхідно розпочинати тільки після адекватної регідратації – приблизно через 2 години. Якщо інсулін вводити до початку регідратації, вода надходитиме всередину клітин, що потенційно може спричинити наростання гіпотензії, колапсу та призвести до смерті. Слід пам’ятати, що при ГОС рівень глюкози в крові знижується паралельно з регідратацією, тобто інфузійна терапія сприяє поступовому зниженню глікемії. Тому при ГОС потрібна невелика доза інсуліну. Зазвичай вводять болюс 10 ОД внутрішньовенно з подальшою інфузією 4 ОД/год. Глікемію в жодному разі не слід знижувати швидше, ніж на 3 ммоль/год. Більш швидке зниження рівня гіперглікемії може призвести до створення зворотного осмотичного градієнта між внутрішньо- та позаклітинним простором, масивного накопичення рідини в тканинах із прогресуючим набряком легень та набряком і набуханням головного мозку.
Як і при ДКА, важливою є корекція електролітного дисбалансу. Дефіцит калію часто залишається нерозпізнаним при ГОС через те, що нестача інсуліну викликає переміщення калію в позаклітинний простір, тому початковий рівень цього мікроелемента може бути нормальним чи перевищувати норму. З початком введення рідини та інсуліну рівень калію може різко знижуватися, бо інсулін «заганяє» його у клітини. Після відновлення достатнього діурезу (>30 мл/год) треба розпочати ліквідацію дефіциту калію. Гіпокаліємія при ГОС розвивається ще швидше, ніж при ДКА, а значна гіперкаліємія, навпаки, зустрічається вкрай рідко. Тому введення хлориду калію зі швидкістю 1,5 г/год має починатися ще до того, як стане відомим результат визначення концентрації калію в крові. Після виведення з гострої декомпенсації препарати калію слід призначити на 5-7 днів перорально. Необхідно регулярно контролювати рівень електролітів (на початку кожні
1-2 години), а також серцевий ритм.
Усіх пацієнтів із ГОС незалежно від стартової концентрації натрію (від низького рівня до високого) госпіталізують у стані гіпертонічної дегідратації. Вірогідно, це пов’язано з переміщенням води з клітин, через що концентрація натрію в сироватці знижується приблизно на 1,6 ммоль/л на кожні 5,5 ммоль/л понад 5,5 ммоль/л глюкози крові (R. Venkatraman, 2006). Отже,
«виправлений» Na = Na + 1,6 × (глікемія – 5,5)/5,5.
Гіперхлоремічний ацидоз часто виникає при переливанні великої кількості рідини, що містить еквівалентні дози натрію та хлору (великі дози ізотонічного розчину NaCl). Для попередження цього стану варто застосовувати фізіологічні мультиелектролітні розчини.
Гіпомагніємія може проявлятися аритміями, м’язовою слабкістю, судомами, ступором чи психомоторним збудженням. Гіпомагніємія зустрічається приблизно у 90% хворих з некомпенсованим ЦД. За винятком пацієнтів із нирковою недостатністю терапія препаратами магнію безпечна і фізіологічно виправдана.
Слід приділити належну увагу діагностиці та терапії захворювань, що спровокували розвиток ГОС. Це можуть бути гострі супутні захворювання, інфекції, неадекватна цукрознижувальна терапія, синдром діабетичної стопи тощо. За необхідності призначають антибіотики. Хворим старечого віку в разі глибокої коми, вираженої гіперосмолярності доцільно проводити профілактику тромбозу малими дозами гепарину.
Підготувала Наталя Міщенко


