20 грудня, 2016
Антимикробная резистентность и инфекционный контроль: текущее состояние проблемы

21 сентября состоялось совещание Генеральной aссамблеи Организации Объединенных Наций, посвященное проблеме устойчивости патогенов к антибактериальным препаратам (АБП), по итогам которого было принято решение о наращивании усилий мирового сообщества и активизации многосекторальной деятельности на национальных уровнях. Информационный бюллетень Всемирной организации здравоохранения (ВОЗ), опубликованный в сентябре 2016 г., отражает негативную динамику уровней антибиотикорезистентности (АБР) ключевых возбудителей во всех регионах мира.
Так, повсеместно фиксируется неуклонный рост устойчивости K. pneumoniae к АБП «последней надежды» – карбапенемам, достигающей в некоторых странах 50%. Широкое распространение получила резистентность E. coli к фторхинолонам – наиболее часто применяемым средствам при лечении инфекций мочевых путей. Как минимум в 10 странах (Австралия, Австрия, Канада, Франция, Япония, Норвегия, Словения, ЮАР, Швеция, Великобритания) зафиксированы случаи неэффективного лечения гонореи цефалоспоринами III поколения. Вызывает обеспокоенность резистентность к АБП первой линии S. aureus – по последним оценкам, вероятность гибели пациента, инфицированного метициллинрезистентным золотистым стафилококком (MRSA), на 64% выше, чем больного, у которого обнаружен чувствительный штамм возбудителя. В настоящее время препаратом выбора для лечения опасных для жизни инфекций, вызываемых Enterobacteriaceae, является колистин, однако в ряде стран зафиксированы случаи устойчивости к этому АБП. Ситуация с лечением туберкулеза и вовсе пугающая – в 2014 г. зарегистрировано около 480 тыс. случаев заболевания туберкулезом со множественной лекарственной устойчивостью (МЛУ-ТБ). Опасность данной ситуации заключается в том, что успех терапии МЛУ-ТБ достигается только в половине случаев. В завершающей части бюллетеня эксперты ВОЗ отмечают, что устойчивость к АБП – многогранная проблема, которая касается мирового сообщества и определяется множеством взаимосвязанных факторов. Для профилактики возникновения и распространения АБР необходимы согласованные действия во всех странах и на всех континентах, поскольку изолированные усилия в решении глобальной проблемы абсолютно неэффективны. Именно поэтому ВОЗ рекомендует государствам подготовить национальные планы действий по борьбе с АБР, привлекая дополнительные инвестиции и инновационные подходы к исследованиям и разработке новых АБП, вакцин и средств диагностики.
Украина является многолетним активным участником борьбы с АБР. В частности, 17-18 ноября в рамках Европейского дня рационального использования АБП в Киеве на базе Национальной медицинской академии последипломного образования (НМАПО) им. П. Л. Шупика состоялась Международная научно-практическая конференция «Инфекционный контроль и антимикробная резистентность». Мероприятие было посвящено обсуждению возможных путей решения оптимизации инфекционного контроля и ситуации касательно АБР, а также реализации Соглашения об ассоциации между Украиной и Европейским союзом (ЕС), подготовки Стратегического плана действий Украины по АБР в медицине, ветеринарии, сельском хозяйстве и пищевой промышленности. Организаторами конференции выступили НМАПО им. П. Л. Шупика, Всеукраинская ассоциация инфекционного контроля и антимикробной резистентности, Национальный комитет инфекционного контроля и антимикробной резистентности и Международный научно-медицинский центр им. академика Зарифы Алиевой. В работе форума приняли участие представители ВОЗ, Верховной Рады Украины, Министерства здравоохранения Украины, Национальной академии медицинских наук (НАМН) Украины, Национального Центра общественного здоровья Украины, Государственной службы Украины по вопросу безопасности продуктов питания и защиты потребителей, ведущие украинские ученые, а также их коллеги из стран СНГ, ЕС и США.
Глава Национального комитета Украины по антимикробной резистентности и инфекционному контролю, заведующий кафедрой микробиологии, эпидемиологии и инфекционного контроля НМАПО им. П. Л. Шупика, доктор медицинских наук, профессор Айдын Гурбанович Салманов посвятил выступление актуальной проблеме современной хирургии – послеоперационным гнойно-воспалительным инфекционным осложнениям, частота которых, к сожалению, не имеет тенденции к снижению.
– Фактическая заболеваемость послеоперационными инфекциями в Украине в 2014-2015 гг. составила 0,159 и 0,137% (на 100 операций) соответственно при аналогичных показателях порядка 0,05-0,07 в начале 2000-х годов. При этом в 2015 г. доля послеоперационных инфекций в общей структуре внутрибольничных оценивалась в 62%. Одной из причин снижения эффективности профилактики и лечения пациентов с инфекциями – резистентность возбудителей к АБП, которые используются в клинической практике. В этиологической структуре послеоперационных гнойно-воспалительных инфекций (ГВИ) в Украине сегодня преобладают грамположительные микроорганизмы (57,5%). Частота выделения возбудителей: S. аureus – 49%, E. сoli – 15,1%, P. aeruginosa – 10,2%, Enterobacter spp. – 9,5%, E. faecalis – 8,2%, S. epidermidis – 3%, Acinetobacter baumannii – 1,4%, Klebsiella – 1,3%. Интересно, что последние 5 лет отмечается перераспределение основных патогенов послеоперационных ГВИ – доля S. аureus несколько снижается при одновременном росте частоты встречаемости S. epidermidis и бактерий рода Acinetobacter. Уровень АБР основных возбудителей послеоперационных ГВИ в Украине представляет серьезную проблему. Так, количество штаммов, резистентных к одному АБП, на сегодня, по средним оценочным меркам, составляет 70,7%, к АБП 2-3 классов – 37,5% (S. aureus – 31,4%, E. faecalis – 37,5%, E. coli – 34,9%, Enterobacter spp. – 47,3%, P. aeruginosa – 67,8%), к АБП 4 и более классов – 34,4% (S. aureus – 25,9%, E. faecalis – 31,0%, E. coli – 26,3%, Enterobacter spp. – 30,3%, P. aeruginosa – 50,2%), ко всем АБП – 29,6%.
Говоря о ведущем патогене послеоперационных инфекций – S. aureus, важно отметить, что основную проблему, конечно же, представляют штаммы MRSA, устойчивые ко многим АБП. Их распространенность в хирургических стационарах Украины в 2015 г. составила в среднем 40,4% со значительной вариабельностью по регионам страны (Киевская и Николаевская области – более 70%; Одесская, Кировоградская, Луганская – менее 30%). Важно отметить, что в Европе распространенность штаммов MRSA в стационарах хирургического профиля, как правило, не превышает 30%, следовательно, украинские показатели, к сожалению, далеки от желаемых.
На сегодняшний день сложилась крайне сложная ситуация, когда элиминировать инфекцию, вызванную «супермикроорганизмами», резистентными к АБП, несмотря на все достижения современной медицины, становится все сложнее и сложнее. Эта проблема усугубляется фактическим отсутствием новых классов АБП и неуклонным ростом уровня устойчивости патогенов к старым. Например, согласно данным всемирно известного исследования SMART (Study for Monitoring Antimicrobial Resistance Trends), включившего более 200 центров по всему миру, в 2009-2010 гг. было выделено 1643 изолята E. coli из образцов мочи пациентов, госпитализированных по поводу инфекций мочевых путей. При этом в результатах испытания отмечается, что чувствительность E. сoli к цефалоспоринам и фторхинолонам из года в год снижается (р<0,05). Важно также отметить, что чувствительность этого микроорганизма к эртапенему сохраняется на уровне >99% на протяжении более 8 лет. Важно отметить, что он не обладает клинически значимой активностью в отношении P. аeruginosa и других неферментирующих грамотрицательных бактерий, что позволяет избежать селекционного давления на развитие резистентности у данных возбудителей. Эртапенем используют в лечении внутрибольничных инфекций, вызванных полирезистентными возбудителями, при отсутствии риска наличия Р. aeruginosa.
Оценить риск присутствия Р. аeruginosa помогают следующие клинические критерии:
• пребывание пациента в отделении интенсивной терапии;
• предыдущее лечение АБП нескольких классов;
• наличие кистозного фиброза;
• прогрессирующая ВИЧ-инфекция, СПИД;
• злокачественное новообразование, выраженная нейтропения;
• септический шок;
• искусственная вентиляция легких или наличие центрального катетера в сочетании с катетером-баллоном Фолея.
По данным E. Goldstein и соавт. (2006), эртапенем обладает таким уникальным свойством, как увеличение чувствительности грамотрицательных бактерий к имипенему и некоторым другим АБП (левофлоксацин, цефепим и др.).
На сегодня мы имеем Стратегический план действий Украины по профилактике инфекций, связанных с оказанием медицинской помощи, и АБР, посвященный механизму реализации соглашения об ассоциации между Украиной и ЕС в области медицины и внедрения международных стандартов качества медицинской помощи, в том числе инфекционного контроля и АБР в рамках реформирования отечественной системы здравоохранения. В контексте данной Стратегии основными рекомендациями касательно предупреждения селекции устойчивых к АБП штаммов являются:
• контроль за использованием АБП в хирургических стационарах;
• эпидемиологический надзор за послеоперационными инфекциями и микробиологический мониторинг АБР их возбудителей;
• профилактика нозокомиальной передачи резистентных штаммов микроорганизмов в хирургических стационарах.
Рациональное использование АБП в хирургии предполагает:
• исключение понятия «профилактическое лечение»;
• избегание лечения колонизации;
• сокращение длительности курсов антибактериальной терапии (АБТ);
• интраоперационную профилактику. Важными мерами борьбы с распространением АБР также являются фармакодинамическое обоснование режимов дозирования АБП, использование больничного формуляра, основанного на локальных данных по АБР микроорганизмов. При этом большое значение имеет взаимодействие клиницистов, микробиологов, клинических эпидемиологов, фармакологов и специалистов по инфекционному контролю.
Результаты мониторинга АБР патогенов у пациентов, перенесших кардиологическое оперативное вмешательство, были представлены в докладе заведующего отделением хирургии инфекционного эндокардита Национального института сердечно-сосудистой хирургии им. Н. М. Амосова НАМН Украины, доктора медицинских наук Алексея Антоновича Крикунова.
– Особую проблему для терапии сегодня представляют внутрибольничные инфекции – патогены т. н. группы ESКAPE (E – E. faecium, S – S. аureus, K – K. рneumoniae, A – А. baumannii, P – P. аeruginosa, E – Enterobacter spp.) – ввиду наличия у них сформированных механизмов устойчивости к АБП широкого спектра действия. На базе нашего учреждения на протяжении многих лет проводится идентификация патогенов, вызывающих инфекционный эндокардит, сепсис, бактериемию. Важно заметить, что средняя частота идентификации возбудителя составляет 50%, при этом грамположительные микроорганизмы обнаруживаются в 67% случаев, грамотрицательные – в 24%, грибы – в 9%. Регулярные исследования на базе нашего института позволяют сегодня говорить не только о конкретных возбудителях, но и об уровнях их резистентности к основным АБП по состоянию на 2015 г.:
• E. faecium (частота выделения – 5,5-22,4%); количество штаммов, резистентных к ванкомицину и линезолиду, составило 48,0 и 34,2% соответственно;
• S. aureus (частота выделения – 1,5-10%); устойчивость к ванкомицину и линезолиду отмечалась в 64,3 и 14% случаев соответственно;
• частота выделения K. рneumoniae возросла с 0% в 2004 г. до 36,7% в 2015 г.; к коломицину и фосфомицину продемонстрировали устойчивость 42,9 и 10,0% штаммов соответственно;
• A. baumannii (частота выделения – 5,9-44,2%); чувствительность к коломицину и фосфомицину отсутствовала у 15,4 и 10,1% штаммов соответственно;
• P. aeruginosa (частота выделения – 11,8-36,6%); уровни устойчивости к коломицину и фосфомицину – 65,3 и 44,0% соответственно;
• Enterobacter spp. (частота выделения – 5,9-61,9%); к коломицину и фосфомицину оказались нечувствительны 44,1 и 4,2% штаммов соответственно.
Грибковая микрофлора обнаруживалась в 2,3-20,4% случаев. В 2014-2015 гг. зарегистрированы случаи септических заболеваний, вызванных сочетанием возбудителей группы ESKAPE и грибковой микрофлоры, которые сопровождались тяжелыми органными поражениями.
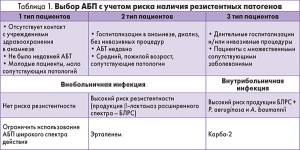
Эмпирический выбор АБП в хирургии, в том числе кардиохирургии, должен основываться на наличии данных о риске присутствия резистентных возбудителей. Его алгоритм отражен в таблице 1.
К альтернативным методам терапии инфекционных заболеваний относят использование антител, фаголизинов, бактериофагов (в том числе синтезированных), иммуностимуляторов, вакцин, антибактериальных пептидов, препаратов, разрушающих биопленки. Беспокойство вызывает тот факт, что все указанные средства малоактивны в отношении патогенов из группы ESKAPE. Таким образом, маловероятно, что в ближайшее десятилетие появится альтернатива АБП для ликвидации этих и других угрожающих жизни возбудителей.
На основании собственного опыта мы предприняли ряд мер для повышения эффективности терапии и предупреждения селекции резистентных штаммов. Среди них:
• интраоперационное использование общей управляемой гипертермической перфузии у больных инфекционным эндокардитом;
• пассивная иммунизация + комбинированная АБТ;
• использование препаратов с т. н. антикворумным действием.
На тенденции к возрастанию уровней АБР в лечении хирургической патологии остановился и профессор кафедры здравоохранения и инфекционных болезней университета Sapienza (г. Рим, Италия) Марко Фальконе.
– Наиболее устрашающим фактом в вопросе АБР является скорость, с которой формируется устойчивость патогенов к новым АБП. Если отрезок времени от момента начала использования до регистрации первого случая резистентности для старых АБП (ампициллин, хлорамфеникол, ванкомицин, эритромицин и др.) составлял десятилетия, то для новых АБП он сократился до нескольких лет.
В настоящее время описано 4 основных механизма развития АБР:
• инактивация АБП (выработка патогеном ферментов, разрушающих АБП);
• модификация рецепторного аппарата (в результате мутации изменяется структура рецептора микробной клетки, что предотвращает контакт с АБП и его проникновение в клетку);
• активация клеточных каналов (специальные мембранные белки формируют клеточные каналы, посредством которых элиминируются АБП);
• использование альтернативного метаболического пути.
Важной проблемой хирургических стационаров на протяжении многих лет остаются MRSA-штаммы. Факторами, повышающими вероятность инфицирования указанными штаммами, являются мужской пол, возраст >75 лет, использование в течение последних 6 мес таких групп АБП, как цефалоспорины и карбапенемы, случаи госпитализации в предшествующие 12 мес, перемещение между отделениями лечебного учреждения, а также использование мочевого катетера.
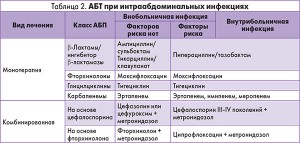
Алгоритм АБТ у пациентов хирургического профиля с интраабдоминальной инфекцией представлен в таблице 2.
В исследовании Catena и соавт. (2013) проводилось сравнение эффективности 3-дневной терапии ампициллином/сульбактамом (n=71; 3 г/сут) и эртапенемом (n=71; 1 г/сут) при различных формах интраабдоминальной инфекции у пациентов хирургического стационара. Результаты показали, что соотношение эффективность/неэффективность оказалось не в пользу ампициллина/сульбактама – 51/10 vs 69/2 в группе эртапенема. Это позволяет говорить о высокой эффективности монотерапии эртапенемом в лечении интраабдоминальной инфекции.
Вопросы АБТ билиарных инфекций были подняты в докладе заместителя директора по научной работе ГУ «Национальный институт хирургии и трансплантологии им. А. А. Шалимова» НАМН Украины, руководителя отдела лапароскопической хирургии и холелитиаза, доктора медицинских наук, профессора Михаила Ефимовича Ничитайло.
– При абдоминальных инфекциях определяющим является хирургическое лечение: ликвидация патологического очага, хирургическая деконтаминация и детоксикация, а также профилактика реинфицирования. Все эти принципы абсолютно применимы и для хирургии билиарного тракта. Наш опыт применения различных лечебно-диагностических алгоритмов показывает, что использование преимуществ миниинвазивных технологий позволяет эффективно лечить пациентов с билиарной хирургической патологией, существенно снижая сроки послеоперационной и трудовой реабилитации больных.
Обязательным дополнением к проводимому хирургическому вмешательству является АБТ. Абсолютным показанием к проведению АБТ при билиарных инфекциях являются: гангренозно-перфоративный вариант острого холецистита, холедохолитиаз, холангит с механической желтухой, перитонит.
Эмпирическая АБТ проводится по следующим принципам:
• при выбранном режиме терапии происходит воздействие на всех потенциальных возбудителей инфекции;
• принимается во внимание риск выделения полирезистентных возбудителей;
• режим терапии не должен создавать условия для селекции в отделении устойчивых штаммов микроорганизмов.
При холангите в связи с риском выделения неклостридиальных анаэробов необходимо использование препаратов, активных в отношении данных микроорганизмов, например, цефепим 4-6 г/сут + метронидазол 1,5 г/сут; эртапенем (Инванз) 1 г/сут; моксифлоксацин 400 мг 1 р/сут. В связи с тем, что цефалоспорины и фторхинолоны разрушаются под действием БЛРС, оптимальным решением будет использование именно современных карбапенемов. Клинически удобная классификация карбапенемов представлена в таблице 3.
Кроме того, концентрация эртапенема в желчном пузыре превышает минимальную подавляющую (МПК) основных возбудителей более чем в 10 раз, при этом является оптимальным выбором с точки зрения спектра активности в отношении штаммов, синтезирующих БЛРС, и удобства применения.
Проблема АБР является не только медицинской. Именно поэтому к участию в конференции были привлечены не только специалисты здравоохранения, но и эксперты ветеринарной, сельскохозяйственной и пищевой отраслей. В частности, старший научный сотрудник, заведующая научно-исследовательским бактериологическим отделом Государственного научно-исследовательского института лабораторной диагностики и ветеринарно-санитарной экспертизы, кандидат ветеринарных наук Татьяна Александровна Гаркавенко в докладе «Антибиотикорезистентность возбудителей зоонозов животных в Украине» представила динамический анализ АБР различных микроорганизмов к наиболее часто используемым АБП. Было отмечено, что в ветеринарии, как и в медицине, наблюдается отчетливая тенденция к росту устойчивости патогенов к антибиотикам. Кроме того, в отрасли существует ряд проблем, связанных с использованием различными лабораториями разных видов дисков для определения чувствительности к АБП (отсутствие стандартизованного подхода), с неточностями в анализе существующих данных, а также с отсутствием общегосударственных программ контроля.
Данная конференция позволила взглянуть на единую проблему под разными углами. Ее масштаб и высокий интерес участников к дискуссионным вопросам позволяют надеяться на дальнейшее активное участие Украины во всемирном движении по борьбе с АБР. В завершение профессор А. Г. Салманов анонсировал будущие мероприятия, посвященные вопросу контроля АБР и представляющие практическую ценность для клиницистов различного профиля.
Подготовила Александра Меркулова