1 квітня, 2015
Обзор рекомендаций Европейского общества урологов (EAU) 2014 г. по диагностике и лечению инфекций мочевыводящих путей, ассоциированных с урологическими расстройствами
Осложненные инфекции мочевыводящих путей (ОИМП) – это инфекции, развивающиеся на фоне структурных или функциональных нарушений в урогенитальном тракте или основного заболевания, приводящего к формированию дисфункции защитных механизмов организма, увеличивающей риск инфицирования или неэффективности терапии.
ОИМП могут быть вызваны различными микроорганизмами. При этом широта спектра возбудителей ОИМП превосходит аналогичную при неосложненных ИМП, а сами патогены, вероятно, более устойчивы к антибактериальным препаратам.
В структуре возбудителей ОИМП преобладают бактерии семейства Enterobacteriaceae. В частности, E. coli является наиболее распространенной причиной ОИМП. При этом в зависимости от условий, неферментирующие (например, Pseudomonas aeruginosa) и грамположительные кокки (стафилококки и стрептококки) также могут играть значительную роль в развитии инфекционного процесса.
Выбор тактики лечения ОИМП зависит от тяжести заболевания. Терапия должна включать три основных направления: коррекцию урологических нарушений, адекватную антибактериальную терапию и проведение поддерживающей терапии. Необходимо учитывать, что пациенты с ОИМП часто нуждаются в госпитализации. С целью предупреждения появления устойчивых штаммов возбудителей при назначении терапии руководствуются результатами культурального исследования мочи, которое должно проводиться максимально часто.
В составе эмпирической терапии следует использовать антибиотики, спектр активности которых охватывает основные патогены (класс рекомендаций A). Препаратами выбора в этом случае являются фторхинолоны с преимущественно почечной экскрецией, аминопенициллины в комбинации с ингибиторами β-лактамаз (ИБЛ), цефалоспорины II-III поколения или аминогликозиды – при необходимости проведения парентеральной терапии (уровень доказательств 1b, класс рекомендаций B).
При неэффективности стартовой терапии или при тяжелой инфекции следует выбирать антибиотик с более широким спектром действия, в том числе включающим активность в отношении Pseudomonas (1b, B), например фторхинолон (если он не использовался в стартовой терапии), пиперациллин в комбинации с ИБЛ, цефалоспорин III поколения или карбапенем в качестве монотерапии или в сочетании с аминогликозидом (1b, B).
Обычно длительность терапии составляет 7-14 дней (1b, A), однако в некоторых случаях она может быть продлена до 21 дня (1b, A).
До тех пор пока влияние отягчающих факторов не будет устранено, полного излечения без эпизодов рецидива, как правило, достичь не удается. Поэтому посев мочи следует проводить через 5-9 дней после завершения терапии, а также 4-6 нед спустя (B).
Определение и классификация
ОИМП определяет наличие двух обязательных критериев, которые включают положительный результат культурального исследования порции мочи и один из перечисленных факторов:
• Наличие постоянного катетера, стента (уретры, мочеточника, почки) или временной катетеризации мочевого пузыря.
• Объем остаточной мочи >100 мл.
• Обструктивная уропатия различной этиологии, например вследствие инфравезикальной обструкции на фоне нейрогенного мочевого пузыря, камней и опухолей.
• Везикоуретеральный рефлюкс или другие функциональные нарушения.
• Реконструкция мочевыводящих путей с использованием сегмента подвздошной кишки или созданием кондуита.
• Химические или радиационные повреждения уроэпителия.
• Пери- и послеоперационные ИМП.
• Почечная недостаточность и трансплантация почки, сахарный диабет, иммунодефицит.
ОИМП встречаются в гетерогенной группе больных. Тем не менее возраст и пол пациента как таковые не входят в определение ОИМП. Что касается прогноза и клинических исследований, желательно стратифицировать ОИМП, ассоциирующиеся с урологическими расстройствами, по меньшей мере на две группы:
• развивающиеся у пациентов, у которых осложняющие факторы могут быть устранены в процессе терапии (например, при удалении камня или постоянного катетера);
• формирующиеся у больных, у которых осложняющие факторы не могут быть или не были ликвидированы во время лечения (например, постоянный катетер, резидуальные камни, сохраняющиеся после проведенной терапии, или нейрогенный мочевой пузырь).
Клиническая картина
При ОИМП могут встречаться, но не всегда такие симптомы, как дизурия, боль в боку, болезненность в реберно-позвоночном углу, надлобковая боль и лихорадка. Клиническая картина может варьировать от обструктивных форм острого пиелонефрита с тяжелым течением, осложненных уросепсисом, до катетер-ассоциированных послеоперационных ИМП, которые могут разрешиться спонтанно непосредственно после удаления катетера. Следует также правильно трактовать клинические проявления, особенно симптомов нижних мочевых путей, которые могут быть вызваны не только ИМП, но и другими урологическими заболеваниями и состояниями, в частности доброкачественной гиперплазией предстательной железы или трансуретральной резекцией простаты.
Культуральное исследование мочи
Значительной бактериурией при ОИМП считается содержание в 1 мл средней порции мочи более 105 колониеобразующих единиц (КОЕ) уропатогенов у женщин и более 104 КОЕ у мужчин. При взятии пробы мочи на анализ через катетер, диагностически значимым считается содержание в 1 мл мочи более 104 КОЕ возбудителей. Для постановки диагноза при бессимптомном течении заболевания необходимо выявить возбудителя (более 105 КОЕ/мл) по крайней мере в двух порциях мочи, собранных с интервалом не менее 24 ч. Пиурия констатируется в случае обнаружения при мощном увеличении (×400) более 10 лейкоцитов в ресуспензированном осадке центрифугированной мочи или аналогичного количества лейкоцитов в 1 мм3 нецентрифугированной мочи. Исследование методом щупа может также использоваться для рутинной оценки проб мочи, в том числе для проведения теста на лейкоцитарную эстеразу, гемоглобин и, вероятно, нитриты.
Микробиология
Спектр уропатогенов и устойчивость к антибиотикам
Пациенты с ОИМП как внебольничной, так и нозокомиальной этиологии, как правило, инфицированы микроорганизмами, обладающими устойчивостью к противомикробным препаратам, что существенно увеличивает частоту неэффективности терапии в тех случаях, когда невозможно устранить последствия основного заболевания. Тем не менее само по себе обнаружение устойчивого штамма не является достаточным основанием для верификации диагноза ОИМП. Помимо этого, необходимо подтвердить наличие урологических нарушений (анатомических или функциональных) или основного заболевания, предрасполагающего к ИМП.
ОИМП отличается от ИМП большей широтой спектра потенциальных возбудителей и повышенной частотой встречаемости антибиотикорезистентных штаммов (особенно при ОИМП, связанных с лечением). Типичными возбудителями ОИМП являются E. coli, Proteus, Klebsiella, Pseudomonas, Serratia spp. и энтерококки. В структуре возбудителей ключевая роль принадлежит энтеробактериям (60-75% случаев), и в частности E. coli, как наиболее распространенному уропатогену, особенно при первом эпизоде ИМП. В противном случае, спектр возбудителей может значительно изменяться по прошествии времени и существенно отличаться в различных стационарах.
ОИМП, связанные с мочекаменной болезнью
В подгруппе ОИМП, ассоциированных с уролитиазом, этиологическая значимость таких возбудителей, как E. coli и энтерококки, значительно уменьшается. В то же время существенно возрастает частота выявления Proteus и Pseudomonas spp.
Среди уреазопродуцирующих микроорганизмов преобладают Proteus, Providencia и Morganella spp., Corynebacterium urealyticum, однако Klebsiella, Pseudomonas, Serratia spp. и стафилококки также в некоторой степени являются продуцентами уреазы.
У 88% пациентов с коралловидными камнями на момент постановки этого диагноза обнаруживаются ИМП. При этом 82% пациентов инфицированы уреазопродуцирующими микроорганизмами. Фермент уреаза обеспечивает разложение мочевины до углекислого газа и аммиака. Повышенные концентрации аммиака в моче приводят к повреждению гликозаминогликанового слоя, в результате чего облегчается процесс адгезии бактерий и усиливается образование коралловидных кристаллов. Эти агрегаты участвуют в формировании почечных камней и оседают на поверхности мочевых катетеров.
Патогенный потенциал коагулазонегативных стафилококков и не относящихся к группе D стрептококков является спорным. При определенных обстоятельствах, например при наличии камней или инородных тел, стафилококки могут выступать в роли патогенов. В противном случае они не являются широко распространенными возбудителями ОИМП (0-11%), о чем свидетельствуют данные опубликованных отчетов.
Катетер-ассоциированные ОИМП
При катетер-ассоциированной ИМП распределение микроорганизмов осуществляется аналогичным образом, однако в этих случаях необходимо учитывать наличие биопленок. Антибактериальная терапия оказывается эффективной только на ранних стадиях развития инфекционного процесса.
Лечение
Выбор антибиотиков
Эмпирическое лечение ОИМП требует знания спектра вероятных возбудителей и местных особенностей паттерна антибиотикорезистентности, а также проведения оценки степени тяжести основного урологического заболевания (включая исследование функции почек).
Как правило, бактериемия диагностируется слишком поздно и не влияет на выбор антибиотиков. Тем не менее даже подозрение на наличие бактериемии должно влиять на схему эмпирической терапии. Тяжесть ассоциированного заболевания и основной урологической патологии по-прежнему имеет первостепенное значение для прогноза.
Интенсивное использование любого антибиотика, особенно при эмпирической терапии в группе пациентов с высоким риском рецидива инфекции, приводит к появлению резистентных штаммов. По возможности, эмпирическая терапия должна быть заменена на лечение, направленное против конкретного возбудителя, который был выявлен в культуре мочи. Поэтому образец мочи для культурального исследования должен быть получен до начала терапии, и выбор противомикробного средства должен быть пересмотрен как только будут получены результаты анализа.
У пациентов с почечной недостаточностью, независимо от ее взаимосвязи с урологической патологией, корректировка дозы антибиотика (при помощи мониторинга концентрации препарата) должна быть произведена после начала лечения.
При эмпирической терапии в большинстве случаев рекомендуется использовать фторхинолоны с преимущественно почечной экскрецией, поскольку они имеют широкий спектр антимикробной активности, охватывающей большую часть вероятных возбудителей ОИМП, и позволяют создать высокие уровни концентрации действующего вещества в моче и тканях урогенитального тракта. Фторхинолоны могут быть с успехом использованы как перорально, так и парентерально.
В качестве альтернативы фторхиноловым антибиотикам могут рассматриваться аминопенициллины в сочетании с ИБЛ, цефалоспорины II-III поколений или, в случае парентеральной терапии, аминогликозиды. Новая группа пероральных карбапенемов (эртапенем) в проспективном рандомизированном исследовании продемонстрировала эффективность, сравнимую с цефтриаксоном.
В большинстве стран E. coli показывает высокий уровень устойчивости к триметоприму-сульфаметоксазолу (18-25% по последним оценкам в США) и его назначения следует избегать в качестве средства первой линии терапии. Фосфомицин трометамол может использоваться только в качестве однодозового лечения неосложненного цистита. Аминопенициллины (ампицилл ин или амоксициллин) не эффективны в отношении E. coli.
ин или амоксициллин) не эффективны в отношении E. coli.
В случае неэффективности стартовой терапии, отсутствия результатов микробиологического исследования или необходимости назначения стартовой терапии при тяжелой инфекции в выборе антибиотика предпочтение следует отдавать препаратам с расширенным спектром активности, охватывающим Pseudomonas, таким как фторхинолоны (если они не использовались для стартовой терапии), пиперациллин в сочетании с ИБЛ, цефалоспорины III поколения или карбапенемы в комбинации с аминогликозидами. Кроме того, многие эксперты сходятся во мнении, что эмпирическая терапия у госпитализированных пациентов с серьезной ИМП должна включать внутривенное введение препаратов с антисинегнойной активностью в связи с высоким риском развития уросепсиса.
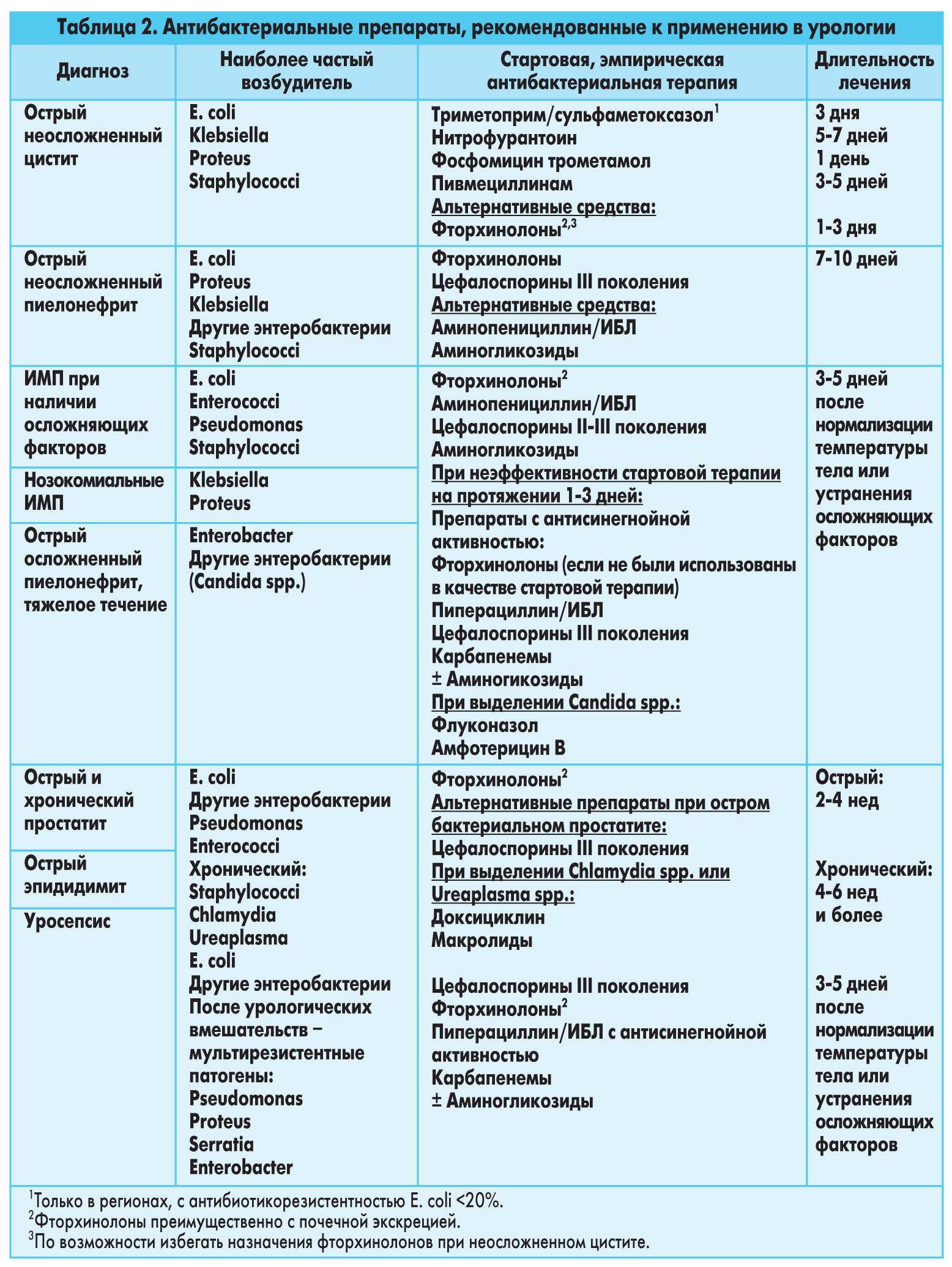
Чаще всего лечение пациентов может осуществляться в амбулаторных условиях. В более серьезных ситуациях (например, у госпитализированных больных) антибиотики должны вводиться парентеральным путем. Наиболее широкое применение в качестве эмпирической терапии находят фторхинолоны или аминогликозиды в сочетании с ИБЛ. Через несколько дней после начала парентерального введения антибиотиков на фоне улучшения состояния больные могут быть переведены на терапию пероральными формами противомикробных средств. Схема лечения должна быть пересмотрена после идентификации возбудителя ИМП и определения спектра его устойчивости к действию антибиотиков. Залогом успеха лечения ОИМП является сочетание эффективной антимикробной терапии, оптимального управления сопутствующими урологическими нарушениями или другими заболеваниями, а также организация мероприятий, направленных на поддержание жизнеобеспечения организма. Рекомендуемые варианты антибактериальной терапии приведены в таблицах 1, 2.
Длительность антибактериальной терапии
Как правило, курс лечения занимает 7-14 дней, при этом его продолжительность тесно связана с лечением сопутствующих нарушений. В зависимости от особенностей клинической ситуации терапия может быть продлена на срок до 21 дня.
ОИМП, обусловленные мочекаменной болезнью
При наличии условий, способствующих камнеобразованию или сохранению очага инфекции, рост камней будет продолжаться. В связи с этим полное удаление камней и назначение адекватной антимикробной терапии является необходимым для выздоровления больного. Кроме того, устранение инфекции, скорее всего, приводит к предупреждению роста коралловидных камней. Назначение длительных курсов антимикробной терапии оправдано в тех случаях, когда не удается провести радикальное удаление камней.
ОИМП, связанные с установкой постоянного катетера
Согласно имеющимся данным, проведение лечения бессимптомной бактериурии на фоне краткосрочной (<30 дней) или длительной катетеризации является неоправданным, поскольку оно способствует появлению резистентных штаммов возбудителей. При краткосрочной катетеризации антибиотики могут отсрочить развитие бактериурии, но не уменьшают ее осложнений.
Манифестные формы ОИМП, ассоциированные с наличием постоянного катетера, требуют применения антибактериального препарата с максимально узким спектром активности, учитывающим вид уропатогена и его чувствительность к антибиотикам, установленные в ходе микробиологического исследования и изучения антибиотикорезистентности конкретного штамма.
Оптимальная продолжительность курса терапии в таких случаях остается неуточненной. Известно, что как слишком короткие, так и чрезмерно длительные курсы терапии могут привести к появлению устойчивых штаммов. Разумным компромиссом в этой ситуации может быть применение 7-дневных курсов лечения.
ОИМП у пациентов с повреждением спинного мозга
В случае персистирующих ИМП и при подозрении на то, что у пациента формируется задержка мочи, следует провести полную оценку функционального состояния мочевого пузыря. Ключевое значение имеет адекватное дренирование мочевого пузыря, необходимое для защиты мочевыводящих путей.
Считается, что бессимптомная бактериурия у пациентов с повреждением спинного мозга, в том числе на фоне временной катетеризации, не требует лечения. Изучение эффективности конкретных антибактериальных препаратов, а также оптимальной длительности терапии у больных с повреждением спинного мозга и манифестными ИМП было проведено лишь в нескольких исследованиях. В настоящее время в этих случаях чаще всего используются курсы антибактериальной терапии длительностью 7-10 дней. При этом преимущества в эффективности у отдельных классов антибиотиков или конкретных препаратов отсутствуют.
Наблюдение после лечения
Особенностью ОИМП является высокая вероятность участия в инфекционном процессе резистентных штаммов уропатогенов. Это скорее связано не с имеющимся урологическим нарушением, а с тем, что пациенты с ОИМП склонны к рецидивам инфекции. В связи с этим до лечения антибиотиками и после его завершения следует проводить культуральное исследование мочи с целью выделения возбудителя и определения его чувствительности к антибиотикам.
Полная версия руководства на английском языке:
http://www.uroweb.org/
Сокращенный перевод с англ.
Антона Пройдака