17 травня, 2016
Инновационные подходы в терапии ревматологических заболеваний: направления и методы
24-25 марта в г. Киеве проходила научно-практическая конференция «Обоснования и направления инновационной терапии в ревматологии». В фокусе внимания выступающих и гостей оказались следующие темы: гармонизация национальных стандартов диагностики и лечения ревматологических заболеваний, успехи, достигнутые отраслью за последние годы во всем мире, клинические вопросы применения современных методов терапии на практике. В рамках мероприятия были проведены круглые столы, секционные заседания, интерактивные мастер-классы, состоялась также междисциплинарная панельная дискуссия.
 О путях обеспечения ремиссии и приверженности пациентов к терапии ревматоидного артрита (РА) рассказал вице-президент НАМН Украины, президент Ассоциации ревматологов Украины, академик НАМН Украины, доктор медицинских наук, профессор Владимир Николаевич Коваленко.
О путях обеспечения ремиссии и приверженности пациентов к терапии ревматоидного артрита (РА) рассказал вице-президент НАМН Украины, президент Ассоциации ревматологов Украины, академик НАМН Украины, доктор медицинских наук, профессор Владимир Николаевич Коваленко.
– Всемирная организация здравоохранения относит плохую приверженность к терапии к основным причинам неоптимального клинического ответа в лечении хронических заболеваний. Согласно данным статистики около 50% пациентов с хронической патологией не придерживаются назначенной им схемы лечения. Результатами безответственного поведения больного становятся усугубление симптоматики и прогрессирование болезни, ухудшение прогноза заболевания, снижение качества жизни, увеличение затрат на систему здравоохранения. Методы оценки уровня комплайенса пациента можно разделить на субъективные (самоотчет пациента, определение врачом), объективные прямые (определение концентрации препаратов или их метаболитов в биологических средах организма) и объективные непрямые (учет аптечных рецептов, подсчет таблеток/флаконов, электронный мониторинг, анкетирование). Основными опросниками, используемыми для оценки приверженности к лечению, сегодня являются: шкала Morisky (Morisky Medication Adherence Scale – MMAS), шкала отчетов MARS (Medication Adherence Report Scale), опросник представлений о медикаментах (Beliefs about Medicines Questionnaire – BMQ). При этом единственным валидизированным специально для ревматологии является опросник CQR (Compliance Questionnaire Rheumatology). К основным предикторам низкого комплайенса пациента относятся: недостатки системы здравоохранения (неадекватный мониторинг, плохой уровень взаимодействия «врач – пациент», недоступность лечебных учреждений и/или медикаментов, высокая стоимость лечения); особенности лечения (сложность терапевтических схем, побочные эффекты, асимптомное течение заболевания); личностные особенности пациента (психологические проблемы, в том числе депрессия, когнитивные нарушения, отсутствие физической возможности получать лечение, неверие в результат, непонимание сути болезни). Согласно результатам исследования D. Chocuette (2011) ≥50% больных РА, которым была назначена биологическая терапия, не покупали либо не принимали препараты. При этом до 72% пациентов называют причиной несоблюдения схемы терапии побочные эффекты на фоне приема назначенных медикаментов.
Стратегия повышения приверженности к лечению должна состоять из таких этапов:
- организация обучающих мероприятий для больного и членов его семьи;
- упрощение режима приема препаратов, использование специальных коробочек для медикаментов, различных способов напоминания;
- оптимизация графика посещений врача;
- совершенствование коммуникации между врачом и пациентом.
Учитывая длительность и характеристики применяемых медикаментов, в повышении комплайенса пациентов с РА существует ряд особенностей. Так, для улучшения приверженности к терапии метотрексатом (МТ) целесообразно использовать:
- дополнительный прием фолатов;
- применение антиэметиков (с целью уменьшения проявлений тошноты и рвоты, индуцированных МТ);
- снижение дозы МТ или перерывы в схемах приема (при наличии клинической возможности);
- переход с пероральной формы МТ на парентеральную;
- переход на другой базисный противоревматический препарат;
- биологическую монотерапию.
Назначая терапию пациенту с РА, важно помнить, что согласно рекомендациям ACR/EULAR (2014) ревматолог должен учитывать мнение больного при определении цели и стратегии лечения для достижения ремиссии. При этом приверженность к терапии зависит от степени информированности пациента о заболевании, а также от уровня взаимодействия между врачом и больным.
 Заведующий ревматологическим отделением Запорожской областной клинической больницы, доктор медицинских наук Дмитрий Геннадьевич Рекалов уделил внимание проблемам, связанным с распространенностью ревматических заболеваний в мире и в Украине.
Заведующий ревматологическим отделением Запорожской областной клинической больницы, доктор медицинских наук Дмитрий Геннадьевич Рекалов уделил внимание проблемам, связанным с распространенностью ревматических заболеваний в мире и в Украине.
– Ревматические заболевания – одна из наиболее сложных медицинских проблем во всем мире и в Украине: их профилактика невозможна, этиология не установлена, а лечение в большинстве случаев помогает только замедлить темпы прогрессирования патологических процессов, которые в течение 7-10 лет приводят к инвалидизации пациентов. Такие заболевания, как РА, псориатический артрит (ПсА), анкилозирующий спондилит (АС), сопряжены не только со значительным дискомфортом, но и сильной болью, существенно снижающей двигательную активность больных, которые вынуждены менять свой образ жизни и приспосабливаться к болезни. При этом распространенность ревматических заболеваний и в целом патологии костно-мышечной системы (КМС) постоянно растет. По данным исследования распространенности патологии КМС (проект «Фармконсалтинг» компании «Морион»), в 2013 г. абсолютное число больных РА составило 113 тыс. человек, АС – 10,5 тыс. человек. Увеличивается также доля трудоспособного населения в структуре распространенности заболеваний КМС: в Украине этот показатель составляет 43%; 72% пациентов испытывают трудности в процессе повседневной деятельности. При этом ранняя диагностика заболеваний не является правилом для многих пациентов: у 67% опрошенных диагноз был установлен в течение года от появления первых симптомов. Только в 2014 г. государственный бюджет Украины потерял около 604 млн грн из-за дополнительных прямых расходов, связанных с лечением РА и АС, выплатами по инвалидности и временной нетрудоспособности, а также потерями от снижения занятости и прочими последствиями этих заболеваний. По данным Госкомстата 2014 г., это составляет около 1,2% от общих расходов на здравоохранение. В этот же период ВВП страны недополучил как минимум 203 млн грн в виде дополнительных косвенных потерь, обусловленных РА и АС. Таким образом, сегодня необходима координация усилий в сфере здравоохранения для снижения уровня заболеваемости, инвалидности и смертности среди пациентов с патологией КМС. Для снижения показателей временной нетрудоспособности, уменьшения количества и продолжительности госпитализаций, предупреждения полной нетрудоспособности и улучшения показателей трудоустройства среди пациентов с заболеваниями КМС следует прежде всего добиться улучшения диагностики этой патологии. Следующим шагом является формирование в Украине коалиции «Fit for Work» и имплементация положений этой инициативы для оптимизации расходов на здравоохранение и увеличения численности трудоспособного населения.
 Об особенностях диагностики и лечения ревматической полимиалгии (РП) рассказала заведующая отделением ревматологии и внутренней патологии КБ «Феофания» ГУД (г. Киев), доктор медицинских наук, профессор Ирина Юрьевна Головач.
Об особенностях диагностики и лечения ревматической полимиалгии (РП) рассказала заведующая отделением ревматологии и внутренней патологии КБ «Феофания» ГУД (г. Киев), доктор медицинских наук, профессор Ирина Юрьевна Головач.
– РП представляет собой воспалительное ревматическое заболевание, которое начинается остро и сопровождается выраженными симметричными болями в области плечевого, тазового пояса и шеи, ограничением движений, значительным изменением лабораторных показателей, свидетельствующих об острой фазе воспаления, и анемией.
РП достаточно широко распространена. К примеру, в США среди лиц старше 50 лет это заболевание диагностируется у 50 человек на 100 тыс. населения, чаще всего у женщин (в соотношении примерно 2:1).
В настоящее время, к сожалению, существует неопределенность в диагностике РП. Этиология заболевания неизвестна, тип наследования – полигенный, в последние годы широко обсуждается роль вирусной инфекции в развитии заболевания, однако неопровержимых доказательств этому пока нет. Существует мнение, что причинами развития РП могут быть стресс и переохлаждение. Описание патогенеза РП принято начинать с воздействия стимулирующих факторов, действующих через Тoll-подобные рецепторы. Активация последних приводит к усилению активности дендритных клеток и моноцитов, в результате чего повышается выработка таких провоспалительных цитокинов, как ИЛ-1, ИЛ-6, ИЛ-8, ФНО и др., обусловливающих развитие системного воспаления и изменения со стороны костно-мышечной и сосудистой систем. Заболевание, как правило, начинается остро и неожиданно. Наиболее характерным проявлением РП является синдром поражения опорно-двигательного аппарата: боль и скованность в проксимальных отделах конечностей. В 100% случаев поражения симметричны. Постоянные боли режущего, тянущего, рвущего характера резко усиливаются при движении. Характерна утренняя скованность.
Лабораторные феномены РП:
- повышение скорости оседания эритроцитов – СОЭ (>50 мм/ч) и уровня С-реактивного белка;
- анемия (нормохромная, нормоцитарная – так называемая анемия хронических заболеванияй);
- уровни так называемых мышечных ферментов (креатинфосфокиназы, альдолазы) и миоглобина в пределах нормы;
- отрицательный результат исследования на наличие ревматоидного фактора, АЦЦП;
- негативный результат на наличие антинуклеарных антител;
- увеличение концентрации ИЛ-6, коррелирующее с выраженностью воспаления;
- незначительное повышение печеночных проб (АлАТ, АсАТ, ГГТП).
Ультрасонография и магнитно-резонансная томография определяют бурситы, синовиты, тендосиновиты, на позитронно-эмиссионной томографии обнаруживается субклиническое поражение крупных сосудов. В практике важно определять упрощенный индекс активности РП (SDAI PMR).
SDAI PMR = показатель визуально-аналоговой шкалы (ВАШ) пациента (0-10 см) + показатель ВАШ исследователя (0-10 см) + утренняя скованность (мин) + элевация верхних конечностей (3-0) + СОЭ (мм/ч × 0,1), где 0,1 – поправочный стандартный коэффициент.
Активность РП считается низкой (ремиссия) при значении индекса <7, средней – от 7 до 17, высокой – >17.
Практическому врачу следует помнить, что перед постановкой диагноза РП необходимо исключить ряд заболеваний со сходной симптоматикой, таких как паранеопластический синдром, миеломная болезнь, РА, дерматомиозит/полимиозит, плечелопаточный периартрит, тендиниты мышц плеча, субакромиальный бурсит, хронические бактериальные и вирусные инфекции, ряд эндокринопатий.
Основные принципы терапии РП (EULAR/ACR, 2015):
- В качестве стартовой терапии у больных РП рекомендуется использовать глюкокортикостероиды (ГКС) вместо нестероидных противовоспалительных преператов (НПВП), за исключением возможного кратковременного применения НПВП и/или аналгетиков в случаях, когда болевой синдром ассоциирован с другой патологией (к примеру, сопутствующим ОА).
- Период лечения пациентов с РП эффективной дозой ГКС должен быть максимально коротким.
- Минимально эффективными дозами ГКС следует считать 12,5-25 мг преднизолона. Более высокие стартовые дозы препарата целесообразно назначать только пациентам с высоким риском рецидива и низким риском нежелательных явлений, в то время как для больных с сопутствующей патологией (сахарный диабет, остеопороз, глаукома и т.д.) предпочтительны более низкие дозы ГКС. В качестве стартовых настоятельно не рекомендуются дозы ГКС ≤7,5 и >30 мг/сут.
- Схемы назначения ГКС должны быть строго индивидуальными, учитывать активность заболевания, данные лабораторных исследований, а также выраженность побочных эффектов. Предложены следующие принципы снижения доз препаратов:
а) стартовое снижение: рекомендуется медленно уменьшать дозу ГКС до 10 мг/сут в пересчете на преднизолон в течение 4-8 нед;
б) терапия рецидивов: рекомендуется увеличить дозу перорального преднизолона до уровня, предшествовавшего рецидиву, и в последующем уменьшать ее постепенно (в течение 4-8 нед) до дозы, во время приема которой случился рецидив;
в) уменьшение доз во время ремиссии: после ее достижения необходимо уменьшать дозу перорального преднизолона на 1 мг каждые 4 нед на протяжении всего периода ремиссии.
- Рекомендовано рассматривать внутримышечные инъекции метилпреднизолона как альтернативу пероральным ГКС.
- Рекомендовано назначать однократный прием всей дозы ГКС. Разделять дозу препарата на несколько приемов следует в случае интенсивного болевого синдрома в ночное время суток.
- Возможно рассмотрение раннего назначения МТ в дополнение к терапии ГКС, особенно у больных с высоким риском рецидива, а также у лиц с сопутствующей патологией. МТ также может применяться у пациентов, находящихся в ремиссии, но которые, тем не менее, не демонстрируют желаемого ответа на терапию ГКС. Рекомендуемая доза МТ составляет 7,5-10 мг/нед для перорального приема.
- Не рекомендуется использование блокаторов ФНО в терапии РП, так как до сих пор нет достаточной доказательной базы в пользу включения их в схему терапии.
- Рекомендуется применять индивидуальную программу физических упражнений для пациентов.
- Не рекомендуется использование в терапии РП растительных препаратов. Особенно категоричны авторы документа в отношении китайских травяных препаратов Yanghe и капсул Biqi у пациентов с РП.
Важно отметить, что указанные рекомендации имеют лишь частичную доказательную базу, поэтому при лечении с РП необходимо ориентироваться в первую очередь на состояние пациента.
 Доктор медицинских наук, профессор Людмила Викторовна Химион (кафедра семейной медицины Национальной медицинской академии последипломного образования им. П.Л. Шупика) представила доклад «Интегрированное ведение пациентов с псориатическим артритом».
Доктор медицинских наук, профессор Людмила Викторовна Химион (кафедра семейной медицины Национальной медицинской академии последипломного образования им. П.Л. Шупика) представила доклад «Интегрированное ведение пациентов с псориатическим артритом».
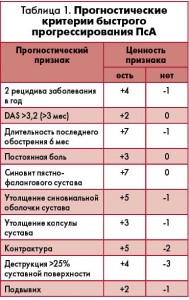
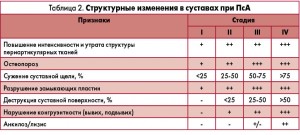
– Псориатический артрит – заболевание, которое характеризуется мультиморбидностью и коморбидностью. ПсА часто сочетается с традиционными факторами сердечно-сосудистого (СС) риска: артериальной гипертензией, сахарным диабетом, метаболическим синдромом, ишемической болезнью сердца, дислипидемиями, подагрой. Ситуация усугубляется наличием иммунозависимого воспаления и побочными эффектами противоревматической терапии – как известно, некоторые препараты оказывают негативное влияние на СС-систему, и не всегда врачи уделяют этой проблеме должное внимание. Не удивительно, что у этих больных отмечается высокий уровень СС-заболеваемости, ранней инвалидизации и низкая продолжительность жизни. Не менее часто у пациентов с ПсА встречаются заболевания органов пищеварения, почек и мочевыводящих путей, патология щитовидной железы. Таким образом, ведение пациентов с ПсА требует междисциплинарного подхода и консультаций дерматолога, офтальмолога, ортопеда, эндокринолога и кардиолога с исследованием метаболических показателей, маркеров воспаления и применением инструментальных методов обследования (электрокардиографии – ЭКГ, эхокардиографии – ЭхоКГ, допплерографического исследования). Помимо контроля коморбидных заболеваний, важной задачей врача, наблюдающего пациента с ПсА, является оценка скорости прогрессирования заболевания (табл. 1), мониторирование структурных изменений суставов (табл. 2), своевременное выявление и лечение остеопороза с целью продления периода до оперативного лечения. Прогностические критерии быстрого прогрессирования ПсА представлены в таблице.
Своевременное дифференцированное применение консервативных и оперативных ортопедических вмешательств позволяет улучшить функциональное состояние и качество жизни пациентов с ПсА. Например, показаниями к оперативным вмешательствам на коленных суставах у пациентов с ПсА являются:
- сохранение признаков синовита на фоне консервативного лечения в течение 6 мес;
- признаки анкилозирования и остеолиза;
- деформации и патологические установки в суставах в результате вывихов и подвывихов.
Противопоказаниями к оперативному лечению являются: тяжелые заболевания внутренних органов, фаза обострения псориаза, пустулезная форма псориаза с поражением кожи на участке оперативного доступа, функционально выгодные установки (особенно в дистальных и межфаланговых суставах).
На конференции прозвучало много докладов и сообщений, посвященных по-настоящему революционным событиям в ревматологии. Это и неудивительно, поскольку сегодня в практике врачей-ревматологов широко применяются последние достижения иммунологии, сделавшей за последнее время огромный рывок вперед. Столь высокий уровень состоявшейся конференции не может не радовать, а повышенный интерес к мероприятию является гарантией внедрения новых знаний в широкую клиническую практику.