20 березня, 2016
Применение биологических препаратов в реальной практике: как повысить эффективность лечения и снизить риски?
По материалам научно-практической конференции «Стандартизированные подходы к диагностике и лечению
ревматических заболеваний» (22-23 октября, г. Киев)
Внедрение в клиническую практику биологических препаратов радикально изменило возможности лечения пациентов с аутоиммунными заболеваниями. Однако по мере расширения спектра биологических препаратов и накопления опыта их применения возникает все больше вопросов в отношении оптимизации данного вида терапии, выбора препаратов с наиболее высокой первичной и вторичной эффективностью и наименьшим количеством побочных эффектов. Эти вопросы актуальны не только для пациентов и врачей, но и для организаторов системы здравоохранения, что связано с высокой стоимостью биологической терапии и необходимостью выбора препаратов с оптимальным соотношением эффективность/безопасность для включения в программы государственных гарантий бесплатного оказания медицинской помощи пациентам с тяжелыми ревматологическими заболеваниями.
Данные мировой клинической практики в области первичной и вторичной эффективности биологических препаратов были проанализированы в ходе выступления главного внештатного ревматолога Министерства здравоохранения Украины, заведующего кафедрой внутренних болезней стоматологического факультета Национального медицинского университета им. А.А. Богомольца, доктора медицинских наук, профессора Олега Борисовича Яременко.
– Наиболее широкое признание среди методов биологической терапии в ревматологии получила антицитокиновая терапия и, прежде всего, нейтрализация фактора некроза опухоли α (ФНО-α), роль которого в патогенезе ревматологических заболеваний не вызывает сомнений.
В настоящее время в мире расходы на приобретение ингибиторов ФНО составляют большую часть в общей структуре расходов на покупку противоревматических препаратов, и вопросы первичной и вторичной эффективности представителей этой группы очень активно изучаются не только в рандомизированных клинических исследованиях (РКИ), но и в обсервационных. Именно обсервационные исследования предоставляют возможность анализировать результаты применения препаратов в реальной клинической практике на протяжении длительного времени в крупных когортах пациентов с различными вариантами течения заболеваний и различными сопутствующими состояниями. Наблюдения в рамках таких исследований позволяют получить информацию о долговременной эффективности лекарственных средств, выявить побочные эффекты, редко встречающиеся при проведении РКИ, их последствия и т.д. Например, по данным голландского регистра DREAM, в который включали пациентов с ревматоидным артритом, частота достижения целей терапии при лечении ингибиторами ФНО оказалась ниже таковой в РКИ. При этом только в 34-79% случаев характеристики пациентов отвечали критериям включения в РКИ. Таким образом, данные регистров сегодня рассматриваются как ценный источник информации наряду с результатами РКИ, более того – высказывается мнение о том, что эти данные целесообразно использовать при составлении унифицированных клинических протоколов по лечению пациентов с ревматическими заболеваниями.
В крупных регистрах существует возможность оценить количество пациентов, получающих одну и ту же терапию на протяжении длительного времени. Этот показатель рассматривается в качестве суррогатного критерия первичной и вторичной эффективности и переносимости лекарственных средств. Так, в одном из крупнейших регистров – датском регистре DANBIO, в котором на протяжении 10 лет оценивали частоту приема и отмены биологических препаратов, – показано, что среди представителей группы ингибиторов ФНО наибольшее количество пациентов, остающихся на терапии длительно (в течение 4 лет), и наименьшая частота отмены характерны для этанерцепта. Эти данные совпадают с результатами системного обзора регистров стран Европейского Союза (A. Arora, 2013), согласно которым показатели длительности приема препаратов и количества больных, получающих лечение, оказались большими для этанерцепта и адалимумаба по сравнению с другими представителями группы ингибиторов ФНО (инфликсимабом). При этом количество пациентов, получавших этанерцепт в течение 1-5 лет, на 4-7% превышало таковое в когорте лечившихся адалимумабом.
Закономерно возникает вопрос о причинах различий в частоте и сроках приема биологических препаратов одной и той же группы. Безусловно, эти показатели зависят от выраженности клинического ответа на терапию и профиля переносимости препарата. Данному вопросу сегодня уделяется большое внимание, и в публикациях последних лет звучит мнение о том, что выраженность ответа на биологическую терапию зависит от многих факторов, в том числе – от иммуногенности, т.е. способности препарата индуцировать образование антител, которые могут снижать его концентрацию в крови, как это показано, в частности, для инфликсимаба и адалимумаба (G.M. Bartels et al., 2011; G.S. Wolbink et al., 2009). В свою очередь, уменьшение концентрации препарата в крови обусловливает снижение клинического ответа и потребность в повышении его дозы с течением времени, что может негативно отражаться на переносимости терапии. Данные систематического обзора, посвященного оценке частоты случаев изменения доз ингибиторов ФНО, свидетельствуют о том, что необходимость в их повышении наиболее часто возникает при лечении инфликсимабом и реже всего – при использовании этанерцепта (R. Moots et al., 2013).
Помимо самого факта выработки антител, большое значение имеет титр образующихся антител и их тип (нейтрализующие или ненейтрализующие). Если суммировать данные, накопленные в отношении ингибиторов ФНО при их применении у пациентов с различными ревматологическими заболеваниями – ревматоидным артритом, псориатическим артритом, анкилозирующим спондилоартритом, то очевидно, что реже всего антитела образуются на фоне терапии этанерцептом, и их наличие не влияет на эффективность терапии (F.B. Vincent et al., 2013). Это связано с особенностями структуры молекулы этанерцепта, который, в отличие от адалимумаба и инфликсимаба, не является моноклональным антителом, а представляет собой гибридную молекулу, включающую ФНО-рецептор с молекулярной массой 75 kD и Fc-фрагмент иммуноглобулина І человека.
Одним из путей предупреждения низкого ответа на терапию биологическими препаратами является применение метотрексата: в ходе исследований показана более высокая частота достижения клинического результата у пациентов, принимающих комбинированное лечение, и данный эффект метотрексата является дозозависимым.
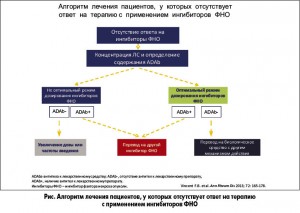
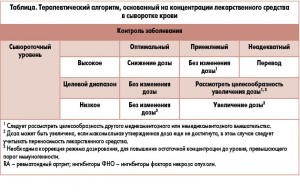
В настоящее время разработаны алгоритмы действий при отсутствии ответа на терапию биологическими агентами, основанные на оценке концентрации действующего вещества в крови и наличия антител к препарату (рис., табл.).
Следует помнить, что длительность приема биологического препарата и удовлетворенность пациентов результатами терапии во многом зависят от его профиля безопасности и переносимости. Согласно данным Кокрановского метаанализа в большинстве случаев биологические препараты демонстрируют сопоставимый профиль безопасности, тем не менее, для этанерцепта характерен меньший риск отмены терапии вследствие возникновения нежелательных явлений (Singh et al., 2009).
Важный вопрос, который всегда беспокоит ревматологов, назначающих своим пациентам биологическую терапию, – повышение риска возникновения инфекционных и опухолевых заболеваний. Следует отметить, что анализ данных относительно всех случаев выявления онкологических заболеваний упациентов, принимавших биологические препараты, не показал достоверного увеличения риска их развития на фоне терапии ингибиторами ФНО (J. Asking et al., 2011). Исключением является рак кожи, риск развития которого повышается при использовании всех биологических агентов.
Что касается риска реактивации туберкулеза, то результаты регистров RATIO и BSRBR свидетельствуют о том, что наиболее низкая частота развития этого осложнения наблюдается при применении этанерцепта по сравнению с использованием других ингибиторов ФНО – адалимумаба и инфликсимаба.
Таким образом, в реальной клинической практике мы можем влиять на различные риски, связанные с применением биологических препаратов, путем правильного выбора препарата (с учетом данных анамнеза пациентов), контроля показателей эффективности терапии и использования комбинированных схем лечения.
Важным моментом при проведении биологической терапии с применением ингибиторов ФНО является тщательный терапевтический мониторинг эффективности лекарственного средства (не реже, чем каждые 3 месяца). Результаты мониторинга позволяют вовремя выявить отсутствие или недостаточную первичную эффективность терапии, нежелательные реакции на препараты, вторичную утрату терапевтического ответа. Методы терапевтического мониторинга эффективности биологических препаратов в клинической практике должны быть усовершенствованы с учетом данных исследований, касающихся взаимосвязи концентрация-ответ.
Подготовила Наталья Очеретяная
Статья напечатана при поддержке Представительства «Файзер Эйч. Си. Пи. Корпорейшн» в Украине.
WUKENB0316030