14 січня, 2016
Диагностика подагры: рекомендации и клиническая практика
Подагра – системное тофусное заболевание, характеризующееся отложением в различных тканях кристаллов моноурата натрия и развитием в связи с этим воспаления, у лиц с гиперурикемией, обусловленной внешнесредовыми и/или генетическими факторами. Это заболевание наиболее часто встречается в популяции взрослых людей, приводит к снижению трудоспособности и ассоциируется с ухудшением качества жизни. Кроме того, подагра может обусловливать развитие сердечно-сосудистых заболеваний, которые являются основной причиной смерти пациентов с этим заболеванием. Так, в исследовании, включавшем 61 527 человек, отмечена связь подагры с высоким риском общей и сердечно-сосудистой смертности.
По данным популяционных исследований, распространенность подагры составляет от 1 до 4%. В США она достигает 3,9% среди взрослого населения (8,3 млн человек). Современные эпидемиологические исследования свидетельствуют об увеличении в последние десятилетия распространенности подагры, что связано с изменениями пищевого рациона, образа жизни, увеличением продолжительности жизни. В исследовании C. Kuo и соавт. отмечено, что распространенность подагры в Великобритании в 2012 г. составила 2,49%, а количество вновь выявленных случаев заболевания – 1,77 на 1 тыс. населения, что на 63,9 и 29,6% превышало показатели 1997 г. Частота этой патологии, некогда известной как «болезнь королей», возрастает не только в странах с высоким уровнем жизни, но и в регионах, где ранее подагра считалась достаточно редким заболеванием.
Традиционно полагают, что подагра преимущественно поражает мужчин старше 45 лет. Однако современная тенденция отображает снижение возраста дебюта заболевания и увеличение частоты случаев подагры среди женщин. В исследовании NHANES продемонстрировано, что распространенность подагры у женщин в США возросла до 2%, составив 2,2 млн. Отмечено, что дебют подагрического артрита у женщин наступает в среднем на 10 лет позже по сравнению с мужчинами. Среди возможных причин полового диморфизма предполагается влияние эстрогенов, оказывающих выраженное урикозурическое действие; после наступления менопаузы этот эффект теряется. В ряде исследований отмечено, что у большинства женщин начало подагры наблюдается в период постменопаузы. В то же время половые различия в частоте встречаемости заболевания практически нивелируются в пожилом и старческом возрасте.
Клинический случай поздней диагностики подагры
Пациент Н., 64 лет, поступил в ревматологическое отделение городской больницы № 28 г. Харькова в ноябре 2014 г. с жалобами на боль и отечность в суставах кистей, стоп, локтевых, коленных и голеностопных суставах, ограничение их подвижности, эпизоды субфебрилитета, общую слабость.
Из анамнеза заболевания известно, что в 56 лет впервые появилась боль в I плюснефаланговых суставах, отечность и ограничение их подвижности, постепенно присоединилась боль в суставах кистей, стоп, коленных, локтевых, деформации и ограничение подвижности, участились приступы обострений артрита, через несколько лет образовались тофусы на конечностях. Обострения участились до 4-5 раз в год. Лечился самостоятельно: диклофенак, мази, растирки, к врачу не обращался. Беспуриновую диету не соблюдал. 3 недели назад вновь усилились боль и отечность в суставах, повысилась температура до 38°С, вызвал на дом участкового врача. Лечился амбулаторно: диклофенак натрия, аллопуринол – без эффекта.
Данные объективного исследования при поступлении: общее состояние средней тяжести обусловлено суставным статусом. Сознание ясное, питание достаточное. Кожные покровы и видимые слизистые оболочки обычной окраски. Щитовидная железа не увеличена. Периферические лимфоузлы не пальпируются. Грудные железы – без уплотнений. Частота дыхательных движений (ЧДД) 20 в минуту. Аускультативно в легких жесткое дыхание, хрипов нет. Границы относительной сердечной тупости расширены влево на 1 см кнаружи от левой среднеключичной линии. Сердце – деятельность ритмичная, ослаблен I тон на верхушке, акцент II тона на аорте. Частота сердечных сокращений (ЧСС) = Пс 76 уд/мин. Уровень артериального давления (АД) 170/110 мм рт. ст. Язык влажный, обложен белым налетом. Живот мягкий, безболезненный. Печень у края реберной дуги по правой среднеключичной линии. Селезенка не увеличена. Симптом поколачивания отрицательный с обеих сторон. Стул и диурез в норме. Деформация и отечность суставов кистей, сглаженность контуров суставов стоп, деформация I плюснефаланговых суставов, тофусы над локтевыми суставами, пальцами кистей, деформация коленных суставов по типу «трилистника», болезненность при пальпации суставов, хруст в них при движениях. Сгибание в коленных суставах <90°, разгибание в них <170°. При ходьбе хромает.
Данные дополнительных методов исследования: в крови при поступлении – эритроциты 4,8×1012/л, гемоглобин 148 г/л, ЦП 0,93, лейкоциты 7,6×109/л, эозинофилы 2%, палочкоядерные 4%, сегментоядерные 68%, лимфоциты 22%, моноциты 4%, скорость оседания эритроцитов (СОЭ) 27 мм/ч, С-реактивный белок 24 мг/мл, глюкоза 4,8 ммоль/л, общий белок 76 г/л, аспартатаминотрансфераза 26, аланинаминотрансфераза 11 ед/л, сиаловые кислоты 2,95 (норма 1,8-2,7 ммоль/л), общий холестерин 5,2 ммоль/л мочевина 4,5 ммоль/л, креатинин 111 мкмоль/л, мочевая кислота 535,0 мкмоль/л.
В моче: цвет светло-желтый, удельный вес 1017, прозрачность умеренная, реакция сл. кислая, белок, глюкоза, ацетон не найдены, лейкоциты 2-4 в п/зр, эритроциты и соли не обнаружены, слизь – умеренное количество.
ЭКГ: ритм синусовый, ЧСС 74 в минуту, гипертрофия левого желудочка, нарушение внутрижелудочковой проводимости. Диффузные нарушения процессов реполяризации.
Ro-грамма стоп в прямой проекции. Заключение. Подагрический артрит III ст.
Ro-грамма кистей в прямой проекции. Заключение. Подагрический артрит мелких суставов кистей и лучезапястного сустава справа III-IV ст.
Ro-грамма коленных суставов в 2 проекциях. Заключение: артрит коленных суставов III ст.
С учетом перечисленных данных был поставлен клинический диагноз: подагра, обострение хронического подагрического полиартрита, с преимущественным поражением суставов кистей, Ro-изменения III-IV ст., стоп, Ro-изменения III-IV ст., коленных суставов, Ro-изменения III ст., голеностопных, локтевых суставов в сочетании с полиостеоартрозом, ФН II ст. Подагрические тофусы в области локтевых суставов и кистей. Подагрическая нефропатия: нефролитиаз, хроническая почечная недостаточность (ХПН) 0 ст. Симптоматическая артериальная гипертензия III ст. Риск 4.
В стационаре назначено: мелоксикам, аллопуринол, толперизон, лосартан, нифедипин пролонгированного действия, витамины группы В, реосорбилакт, ФТЛ, ЛФК.
На фоне проводимой терапии уменьшились боль и отечность в суставах, стабилизировалось АД.
Рекомендовано: диспансерное наблюдение ревматолога, диета с ограничением пуринов, аллопуринол 0,1 г/сут длительно под контролем уровня эозинофилов, мочевой кислоты, при боли мелоксикам 15 мг/сут 7-10 дней, лосартан 50 мг/сут под контролем уровня АД, ФТЛ, ЛФК.
Данный клинический пример демонстрирует несвоевременную диагностику подагры (позднее обращение пациента).
Диагностика подагры в реальной клинической практике
Облигатным фактором риска развития подагры является стойкая гиперурикемия, то есть повышение концентрации мочевой кислоты в сыворотке крови. Мочевая кислота является конечным продуктом пуринового (уратного) обмена, образующимся в результате ферментативного окисления ксантина под действием ксантиноксидазы. В организме человека более 98% мочевой кислоты преобразуется в мононатриевый урат, по содержанию которого определяется концентрация мочевой кислоты. Общий уратный баланс организма может быть нарушен в результате либо повышенного поступления или синтеза пуринов с последующей повышенной почечной экскрецией уратов и вторичной задержкой их при недостаточности этой функции почек, либо первичных поражений тех функций почек, которые обусловливают экскрецию уратов. Гиперурикемией считается содержание мочевой кислоты в сыворотке крови >360 мкмоль/л (6 мг/дл).
Целесообразно рассмотреть при клиническом обследовании и при выявлении оценить следующие коморбидные состояния (уровень доказательств С для всех):
– ожирение, особенности питания;
– избыточное употребление алкоголя;
– метаболический синдром, сахарный диабет 2 типа;
– артериальная гипертензия;
– дислипидемия, модифицируемые факторы риска ишемической болезни сердца или инсульта;
– препараты, увеличивающие уровень уратов в сыворотке крови;
– мочекаменная болезнь в анамнезе;
– патология почек (гломерулонефрит, или интерстициальный нефрит, в частности анальгетическая нефропатия, поликистоз почек);
– в некоторых случаях семейная предрасположенность или приобретенные причины гиперпродукции мочевой кислоты (в частности, врожденный дефект пуринового обмена, или псориаз, миелопролиферативные или лимфопролиферативные заболевания соответственно);
– свинцовая интоксикация.
Особое место среди причин гиперурикемии занимают лекарственные препараты, о чем следует помнить при опросе пациентов.
К лекарственным средствам, повышающим содержание мочевой кислоты в сыворотке крови, относятся диуретики (петлевые и тиазидные), филграстим, β-адреноблокаторы, рибавирин, интерферон, ацетилсалициловая кислота в малых дозах, ритонавир, пиразинамид, этамбутол, дарунавир, никотиновая кислота, ниацин, диданозин, молочная кислота, ритуксимаб, циклоспорин, базиликсимаб, такролимус, терипаратид, фруктоза, ксилитол, теофиллин, силденафил, леводопа, диазоксид, цитотоксические агенты.
Клиническая презентация
Г.А. Захарьин представил следующее описание потенциального больного подагрой: «Человек лет под 40, хорошего сложения, излишнего питания и с хорошим пищеварением, хорошо кушающий и телесно недеятельный, давно уже замечающий у себя красную мочу, словом, кандидат на подагру, но не представляющий еще ни единого местного ее симптома».
Основными клиническими проявлениями подагры являются:
– рецидивирующие атаки острого артрита;
– накопление кристаллов уратов в тканях с образованием тофусов;
– нефролитиаз;
– подагрическая нефропатия.
Стадии течения подагры включают:
– острый подагрический артрит;
– периоды между приступами подагрического артрита (межприступная подагра);
– хроническая тофусная подагра.
Острый подагрический артрит
Основным клиническим проявлением, позволяющим заподозрить подагру, является острый артрит. Приступ резчайшей нарастающей боли в суставе и воспаление, которые достигают максимума в течение 6-12 ч, особенно сопровождающиеся эритемой, высокоподозрительны в отношении микрокристаллического воспаления, хотя и не специфичны для подагры. В 50-80% случаев острая атака возникает внезапно на фоне полного здоровья через несколько лет бессимптомной гиперурикемии. Приступ, как правило, манифестирует в ночное время или в утренние часы. Интенсивность болевого синдрома делает невозможными движения в воспаленном суставе. Причем даже легкое прикосновение вызывает усиление боли. Для первого приступа подагры у мужчин характерен моноартрит с преимущественным поражением суставов стопы: большого пальца, плюснефаланговых, предплюсневых и др. Реже отмечается воспаление лучезапястных, локтевых суставов и очень редко вовлекаются плечевые и тазобедренные. У женщин часто отмечаются олиго- или полиартриты, примерно у 1/3 больных с вовлечением суставов кисти. В пожилом возрасте приступы подагры протекают менее остро, нередко наблюдается начало заболевания по типу олиго- или даже полиартрита. Ускорить или спровоцировать подагрический криз может целый ряд факторов: физические перегрузки, травма, в том числе хирургическая, эпизоды переедания, резкой потери жидкости (воздействие жаркого климата, сауны), употребление алкоголя, прием лекарств (главным образом диуретиков, цитостатиков), острая общая инфекция, инфаркт миокарда, стресс. Во время приступа обычно отмечаются увеличение СОЭ, умеренный нейтрофильный лейкоцитоз, повышение уровня сиаловых кислот в крови, серомукоида, фибрина, резко возрастает уровень С-реактивного белка. Характерной особенностью острого подагрического артрита является обратное развитие всех симптомов (в течение нескольких дней, как правило, без каких-либо остаточных явлений) и отсутствие симптомов между приступами до развития хронического подагрического артрита.
В начале болезни наблюдаются длительные межприступные промежутки. У 60-80% больных повторный приступ развивается уже в течение первого года. В дальнейшем заболевание неуклонно прогрессирует, вовлекая все большее количество суставов. Трудности в диагностике возникают, когда типичные острые суставные проявления появляются поздно или перестают носить характер острых атак (хронические подагрические артриты, которым свойственна неполная ремиссия).
Хроническая тофусная подагра характеризуется формированием тофусов, как подкожных, так и внутрикостных (часто множественных), развитием хронического артрита с появлением стойких деформаций суставов и поражением почек, мочекаменной болезни.
Подагрические узлы, содержащие ураты, окруженные соединительной тканью (тофусы), как правило, возникают при длительности заболевания более 5 лет и высоком неконтролируемом уровне гиперурикемии. Преимущественно они располагаются на ушных раковинах, локтях, в бурсах локтевых суставов, на стопах, пальцах кистей, разгибательной поверхности предплечий, бедер, голеней, на лбу, в области хрящевой перегородки носа. Возможно истончение кожи над тофусом с образованием свищей, из которых спонтанно выделяется пастообразная белая масса. Наряду с этим выявляются и другие характерные рентгенологические признаки (эрозивные изменения костных частей суставов), входящие в перечень критериев подагры, предложенный Американской ассоциацией ревматологов (см. ниже).
Помимо поражения почек возможно вовлечение в процесс сердца, нервной системы, вероятны и сопутствующие артериальная гипертония, ожирение, дерматозы, мигрени. Такой взгляд на подагру как на системное заболевание был известен и раньше, поскольку отложение уратов всегда признавалось условием развития висцеральных изменений. Так, описаны случаи отложения кристаллов в костной ткани позвонков с симптомом сдавления спинного мозга и развитием соответствующей неврологической симптоматики.
При подозрении на подагру схема обследования пациента включает:
– осмотр, в частности оценку суставного статуса, измерение артериального давления;
– антропометрические измерения (рост, масса тела, окружность талии и бедер, их соотношение);
– социальный анамнез (особенности питания и образа жизни);
– выявление семейной предрасположенности к подагрическому артриту, артериальной гипертензии, ожирению, сахарному диабету, ишемической болезни сердца;
– определение биохимических показателей: уровня мочевой кислоты в крови, мочевины, креатинина, скорости клубочковой фильтрации, глюкозы крови натощак, аспартатаминотрансферазы, аланинаминотрансферазы, билирубина, исследование липидного профиля (уровень общего холестерина, триглицеридов, холестерина липопротеидов высокой плотности);
– проведение ЭКГ, эхокардиографии.
Скорость клубочковой фильтрации является одним из основных показателей, который учитывают как при выборе противовоспалительной терапии, так и при мониторинге антигиперурикемической терапии.
Золотым стандартом диагностики подагры является обнаружение кристаллов моноурата натрия методом поляризационной микроскопии. В соответствии с рекомендациями Европейской антиревматической лиги (EULAR, 2006) определенный диагноз подагры ставится при обнаружении кристаллов моноурата натрия в синовиальной жидкости. Именно поэтому при подозрении на подагру в момент артрита необходимо провести пункцию пораженного сустава с исследованием синовиальной жидкости с помощью световой или поляризационной микроскопии. Причем кристаллы моноурата натрия в синовиальной жидкости обнаруживаются и в межприступный период.
Подчеркнем, что концентрация мочевой кислоты в сыворотке крови не является показателем, исключающим или подтверждающим подагру. Более того, во время приступа подагры содержание мочевой кислоты в сыворотке крови может снижаться, поэтому данное исследование следует проводить через некоторое время после разрешения артрита.
Для диагностики подагрического артрита применяют предварительные классификационные критерии, предложенные Американской ассоциацией ревматологов и одобренные ВОЗ.
Классификационные критерии острого подагрического артрита
А. Наличие характерных кристаллов мочевой кислоты в суставной жидкости
Б. Наличие тофусов, содержание кристаллов мочевой кислоты в которых подтверждено химически или поляризационной микроскопией.
В. Наличие 6 из 12 перечисленных ниже признаков:
1) более одной атаки острого артрита в анамнезе;
2) воспаление сустава достигает максимума в 1-й день болезни;
3) моноартрит;
4) гиперемия кожи над пораженным суставом;
5) припухание и боль в I плюснефаланговом суставе;
6) одностороннее поражение I плюснефалангового сустава;
7) одностороннее поражение суставов стопы;
8) подозрение на тофусы;
9) гиперурикемия;
10) асимметричный отек суставов;
11) субкортикальные кисты без эрозий (рентгенография);
12) отрицательные результаты при посеве синовиальной жидкости.
Рентгенологическое исследование суставов помогает в проведении дифференциальной диагностики и может демонстрировать типичные признаки хронической подагры, но бесполезно в ранней диагностике подагры. Характерные для подагры рентгенологические изменения развиваются обычно не ранее 3 лет от начала заболевания. Патогномоничным для подагры является выявление внутрикостных кистовидных образований различных размеров, обусловленных тофусами, расположенными как внутри сустава, так и рядом с ним и даже на некотором отдалении. Формирование внутрикостных тофусов часто происходит одновременно с образованием подкожных тофусов, в связи с чем рентгенологическое исследование используется для определения тяжести тофусного поражения.
При хроническом подагрическом артрите возможно обнаружение деструкции хряща (сужение щели сустава) и краевых костных эрозий. Рентгенологический феномен, типичный для поздней подагры, симптом «пробойника» представляет собой краевые костные эрозии или кистовидные образования правильной формы с четкими, иногда склерозированными контурами. Диагностируется в 10-40% случаев после повторных атак артрита и служит одним из поздних проявлений болезни. Причем на фоне специфической терапии редко наблюдается уменьшение костных изменений. Более того, со временем они даже несколько увеличиваются. Тофусы в мягких тканях с помощью рентгенографии выявляются лишь при их кальцификации, что бывает достаточно редко.
Выделяют следующие рентгенологические стадии подагры:
1-я стадия: периартикулярный отек;
2-я стадия: депозиты тофусов, эксцентричные или асимметричные узловатые образования в мягких тканях, иногда кальцифицированные;
3-я стадия: хрящевая или костная деструкция;
4-я стадия: появление внутрикостных депозитов кристаллов или костных анкилозов.
В начале заболевания рентгенологические изменения в суставах не обнаруживаются. Однако в ряде ситуаций выполнение рентгенографии может быть оправданным при проведении дифференциальной диагностики с травмами и пр. Алгоритм дифференциальной диагностики артрита по данным рентгенограмм представлен на рисунке.
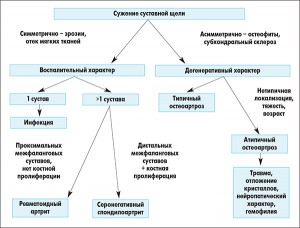 Рис. Схема рентгенологической оценки артрита. Алгоритм начинается с определения сужения суставной щели, и далее дифференциация проводится с учетом характера изменений (воспалительные или дегенеративные)
Рис. Схема рентгенологической оценки артрита. Алгоритм начинается с определения сужения суставной щели, и далее дифференциация проводится с учетом характера изменений (воспалительные или дегенеративные)
Ультразвуковое исследование суставов (УЗИ) позволяет обнаружить отложение уратов в мягких тканях, суставах, хрящах, а также определить костные эрозии, наличие синовита и повышенной васкуляризации. УЗИ является широко распространенным, безопасным, не требующим применения контрастных веществ и доступным диагностическим методом в нашей стране.
Отмечено, что УЗИ потенциально может применяться для диагностики подагры и оценки проводимой терапии. Так, с помощью этого метода возможно определение депонирования моноурата натрия на поверхности гиалинового хряща в виде дополнительной светлой линии, которая расположена параллельно линии перехода субхондральной кости в хрящ и носит название симптома «двойного контура». Он определяется при остром подагрическом артрите у больных с приступами подагры и бессимптомной гиперурикемией. Чувствительность данного признака при подагре варьирует от 25 до 95%. Предполагается, что симптом «двойного контура» можно рассматривать в качестве раннего проявления заболевания до развития эрозий. Однако необходимы дальнейшие исследования для определения его чувствительности и специфичности при ранней диагностике подагры и его прогностического значения при бессимптомной гиперурикемии.
Также УЗИ при подагре позволяет визуализировать тофусы. Определение тофусных структур способствует проведению ранних терапевтических мероприятий. Кроме того, УЗИ – более чувствительный метод, чем рентгенография, для диагностики краевых костных эрозий, однако возможна недооценка их размеров и количества по сравнению с магнитно-резонансной томографией (МРТ). Специфичность ультразвуковой диагностики эрозий возрастает в случае наличия синовита или тофусов.
В то же время при подозрении на септический артрит у больных с микрокристаллическими артритами EULAR рекомендует производить окраску по Граму и посев синовиальной жидкости.
Компьютерная томография (КТ) позволяет идентифицировать агрегаты кристаллов уратов и проводить дифференциальную диагностику с другими заболеваниями. Метод отличается высокой точностью в обнаружении тофусов, располагающихся как внутрикостно, так и в области сухожилий и мягких тканей; высокочувствителен при определении объема кристаллов уратов. В то же время необходимы дальнейшие исследования по определению чувствительности и специфичности КТ в выявлении наиболее ранней стадии подагры до образования агрегатов кристаллов (кристаллы размером менее 3 мм, микротофусы, отложения кристаллов на хряще и пр.). Метод КТ может быть полезен в диагностике пациентов с высокой вероятностью тофусной подагры по клиническим данным, когда результаты обычных диагностических тестов оказываются неубедительными. Более того, особую значимость метод имеет при атипичной локализации подагры (например, тофусное поражение позвоночника).
Компьютерная томография – высокочувствительный метод визуализации характерных для подагры эрозий и тофусов. Однако рутинное применение КТ ограничивают высокая стоимость и лучевая нагрузка.
Магнитно-резонансная томография позволяет визуализировать локализацию, размеры, структуру тофусов, изменения суставных хрящей, синовиальных оболочек, суставных сумок, которые не определяются при рентгенографии. Продемонстрировано, что в идентификации тофусов МРТ превосходит стандартную рентгенографию. Установлено, что чувствительность МРТ составляет 93,9%, специфичность – 80%, тогда как при рентгенографии – 80,6 и 66,7% соответственно. Имеются сообщения о развитии тофусов в дебюте подагры, вплоть до манифестации классических признаков артрита, однако существуют определенные трудности в трактовке результатов МРТ, поскольку изображение тофусов отличается вариабельностью. МРТ с гадолинием рекомендуется при проведении дифференциальной диагностики с остеомиелитом.
В таблице 1 представлена сравнительная оценка диагностической значимости методов визуализации.

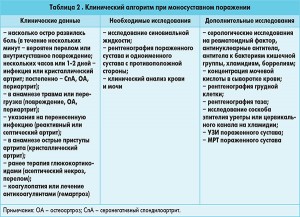
Клинический алгоритм обследования пациента при моносуставном поражении суммирован в таблице 2.
В 2014 г. были опубликованы международные рекомендации по лечению и диагностике подагры. В рамках 3Е инициативы (Evidence, Expertise, Exchange) были суммированы наиболее часто встречающиеся вопросы, возникающие в процессе диагностики и лечения пациентов с подагрой, и представлены ответы (табл. 3). Каждый пункт оценивался по уровню доказательности, по каждому пункту рассчитывался средний уровень согласия по 10-балльной шкале, где 10 баллов соответствовали полному согласию с окончательной формулировкой.
Клинические вопросы в рамках 3Е инициативы (Evidence, Expertise, Exchange)
1. В каких случаях диагноз подагры может быть выставлен на основании клинической картины с применением или без применения лабораторных тестов или методов визуализации и когда необходима идентификация кристаллов?
2. Должны ли мы проводить обязательный скрининг больных с гиперурикемией и/или диагнозом подагры на наличие сопутствующей патологии и факторов риска развития сердечно-сосудистых заболеваний?
3. Какова роль глюкокортикоидов, колхицина и нестероидных противовоспалительных препаратов, ингибиторов интерлейкина-1 и парацетамола в лечении острой подагры?
4. Какие изменения образа жизни (диета, ограничение потребления алкоголя, снижение массы тела, отказ от курения и/или занятия лечебной физкультурой) являются эффективными для лечения и профилактики подагры?
5. Каковы эффективность, соотношение стоимость/эффективность и безопасность уратснижающих препаратов (аллопуринола, фебуксостата, пегуриказы, бензбромарона и пробенецида) в лечении подагры? Какую последовательность или комбинацию уратснижающих препаратов рекомендовать?
6. Какое лечение является наилучшим в профилактике острой атаки при проведении уратснижающей терапии и как долго его следует проводить? Каково оптимальное время начала уратснижающей терапии после острого приступа подагры?
7. Как сопутствующие заболевания (например, метаболический синдром, сердечно-сосудистые заболевания, патология желудочно-кишечного тракта и поражение почек) влияют на выбор при подагре конкретных препаратов (в частности, колхицина, аллопуринола и других уратснижающих средств) при остром приступе артрита, хронической подагре и для профилактики острого приступа артрита?
8. Какова цель лечения и как пациенты с подагрой должны наблюдаться в динамике (например, сообщения пациентов о течении заболевания, клинические, биохимические данные и/или методы визуализации)?
9. Как следует справляться с тофусами?
10. Можно ли предупредить подагрический артрит, поражение почек и сердечно-сосудистые события, снижая сывороточный уровень мочевой кислоты у пациентов с бессимптомной гиперурикемией? Если да, то какими должны быть целевые уровни?
Заключение
Таким образом, диагностика подагры не так проста, как считалось ранее. Поздняя диагностика подагры объясняется несколькими факторами, прежде всего – недостаточным уровнем знаний, касающихся диагностики и лечения подагры, у врачей первичного звена. Однако нельзя не отметить и такой фактор, как позднее обращение пациентов к врачу и длительное самолечение, что демонстрирует представленный клинический случай. Кроме того, низкий комплайенс пациентов, зачастую пренебрегающих советами и рекомендациями врачей, приводит к частым и длительным обострениям подагры и длительной потере трудоспособности. Применение в клинической практике современных диагностических алгоритмов улучшает диагностику подагры, и, что особенно важно, – на ранних этапах ее развития. Кроме того, это позволяет использовать эффективные лечебные стратегии, направленные на улучшение качества жизни пациентов и исходов заболевания, а также снизить затраты на лечение.
Список литературы находится в редакции.