6 липня, 2015
Проблеми безпеки та ефективності сучасних протиподагричних препаратів
 Подагра – хронічне захворювання, пов'язане з порушенням сечокислого обміну, що полягає у підвищенні вмісту в крові сечової кислоти (гіперурикемії) і відкладенні її у вигляді моноурату натрію в тканинах опорно-рухового апарату й внутрішніх органах. Подагра є найпоширенішим запальним захворюванням суглобів у чоловіків: на неї страждає до 2% дорослого населення. Крім того, сьогодні спостерігається стрімке зростання кількості хворих на подагру. Незважаючи на розуміння патогенезу хвороби й можливості ефективної її терапії, подагру часто не діагностують або діагностують пізно, а ефективне лікування супроводжується низкою побічних ефектів.
Подагра – хронічне захворювання, пов'язане з порушенням сечокислого обміну, що полягає у підвищенні вмісту в крові сечової кислоти (гіперурикемії) і відкладенні її у вигляді моноурату натрію в тканинах опорно-рухового апарату й внутрішніх органах. Подагра є найпоширенішим запальним захворюванням суглобів у чоловіків: на неї страждає до 2% дорослого населення. Крім того, сьогодні спостерігається стрімке зростання кількості хворих на подагру. Незважаючи на розуміння патогенезу хвороби й можливості ефективної її терапії, подагру часто не діагностують або діагностують пізно, а ефективне лікування супроводжується низкою побічних ефектів.
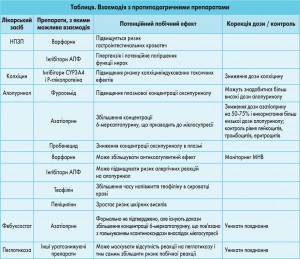
Водночас подагра є патологією з високим індексом коморбідності, вона пов’язана з низкою супутніх захворювань, включаючи артеріальну гіпертензію, серцево-судинні захворювання, ниркову недостатність, цукровий діабет, ожиріння та гіперліпідемію. Наявність цих супутніх захворювань і застосування препаратів для їх лікування натомість можуть сприяти розвитку подагри. Це також впливає на вибір терапії подагри у кожного конкретного пацієнта через можливість взаємодії з іншими лікарськими засобами і високим ризиком розвитку побічних ефектів. У таблиці наведено важливі взаємодії між протиподагричними препаратами та тими, що найчастіше використовуються в лікуванні коморбідних станів.
Загальновизнано, що головним предиктором розвитку подагри є гіперурикемія. При перевищенні певного рівня сечової кислоти в сироватці крові (>400 мкмоль/л) відбувається насичення тканин моноуратом натрію, створюються умови для його кристалізації, а отже, розвитку подагри. Європейська протиревматична ліга (EULAR) рекомендує вважати гіперурикемією стан, коли рівень сечової кислоти досягає >360 мкмоль/л, що ґрунтується на результатах досліджень, які продемонстрували 4-кратне збільшення ризику розвитку подагри у чоловіків і 17-кратне – у жінок при перевищенні вказаного рівня.
Багаторічний перебіг гіперурикемії може призвести до утворення депозитів уратів без симптомів, а іноді й пов’язаних із субклінічним запаленням; далі – інтермітуючі епізоди гострого запалення, викликані відкладанням кристалів моноурату натрію в порожнині суглоба; з часом відстані між цими атаками (спалахами запалення) зменшуються, артрит набуває хронічного перебігу, а запалення – персистуючого характеру; наступний етап – структурне пошкодження суглобів внаслідок хронічного запального процесу і руйнування суглобових структур тофусами (депозитами моноурату натрію).
Ведення подагри охоплює і об’єднує два напрями: по-перше, адекватне лікування гострих подагричних епізодів, по-друге, стійке зниження сироваткового рівня уратів до <360 мкмоль/л (6 мг/дл), щоб запобігти рецидивам і сприяти розсмоктуванню тофусів. Нестероїдні протизапальні препарати (НПЗП), колхіцин і глюкокортикостероїди (ГК) були основою лікування гострих подагричних епізодів упродовж багатьох років. Окрім того, алопуринол є лікарським засобом, який найчастіше використовують у довгостроковій уратзнижуючій терапії з моменту його першого застосування в 1960-х роках. В останні 5-7 років спостерігається відродження інтересу до ведення подагри, знайдено нові терапевтичні можливості як для лікування гострої подагри (інгібітори інтерлейкіну-1 – IL-1), так і для зниження рівня уратів (фебуксостат, пеглотиказа).
Терапевтичні можливості при гострому нападі подагри полягають у застосуванні НПЗП, колхіцину та ГК. При виборі препарату для купірування гострої подагри враховують супутню патологію, функцію нирок і відповідь на попереднє лікування.
Колхіцин. Цей препарат – один із найдавніших серед тих, що використовуються в лікуванні подагри. Протизапальний ефект колхіцину зумовлений дезінтеграцією мікротубул нейтрофілів і пригніченням їх міграції, підпорядкованої хемотаксису. Однак, незважаючи на видимість повної розшифровки протизапального механізму дії препарату, з’являється велика кількість доказів мультифасеточного характеру його ефектів. Колхіцин порушує розподіл молекул адгезії на поверхні нейтрофілів та ендотеліальних клітин, значно пригнічуючи взаємодію між лейкоцитами й ендотеліальними клітинами, втручаючись у процес трансміграції. Більше того, біологічна дія цього лікарського засобу залежить від його дози. У мікромолярних концентраціях він пригнічує інфламасомозалежну активацію каспаз-1NALP3, вивільнення інтерлейкіну-1β (IL-1β) та експресію L-селектину на нейтрофілах. У наномолярних концентраціях колхіцин блокує вивільнення хемотаксичних факторів нейтрофільними лізосомами, адгезію нейтрофілів до ендотелію шляхом зменшення молекул адгезії на ендотеліальних клітинах, пригнічує виділення супероксидних аніонів нейтрофілами. У високій концентрації препарат впливає на експресію генів HUVEC (клітини ендотелію), які відіграють велику роль у запаленні та міграції нейтрофілів.
Максимальний рівень колхіцину в сироватці крові досягається протягом 1-3 год незалежно від способу застосування (перорально чи парентерально), тому він є дієвим засобом при гострому нападі подагри. Рівень плазмової концентрації препарату знижується швидко, але його екскреція триває кілька днів, це пояснюється тим, що він тривалий час залишається у зв’язаному стані. Близько 20% усієї дози колхіцину екскретується нирками. Важливо пам’ятати, що препарат піддається інтенсивному метаболізму в печінці за участю системи цитохрому С450, у зв’язку з чим лікарські засоби, які також зв’язуються з цим білком, можуть впливати на його фармакокінетику й фармакодинаміку.
Колхіцин має вузький терапевтичний індекс і дозозалежну шлунково-кишкову токсичність, це зумовлює погану переносимість, особливо у пацієнтів літнього віку з нирковою й серцевою недостатністю.
У 2010 р. опубліковано дослідження AGREE (The Acute Gout Flare Receiving Colchicine Evaluation), в якому дані вибору дози колхіцину отримали трактування з позицій доказової медицини. Це багатоцентрове рандомізоване подвійне сліпе плацебо-контрольоване дослідження гострого подагричного артриту, в якому порівнювали ефект дози 1,8 мг колхіцину, прийнятої за 1 год, з дозою 4,8 мг, прийнятою за 6 год. Низькі дози препарату продемонстрували профіль небажаних явищ, аналогічний прийому плацебо. Висока доза асоціювалася зі значною діареєю у 76,9% хворих, нудотою та іншими побічними реакціями. Однак при прийомі низьких доз у 23% пацієнтів також розвинулася діарея, але вона була нетяжкою на відміну від такої у хворих, які отримували високі дози. Це вказує на те, що старі схеми лікування гострого нападу подагри, коли колхіцин призначали по 0,6 мг щогодини до повного купірування нападу, є надто токсичними, а за дієвістю не відрізняються від використання низьких доз. Саме у дослідженні AGREE продемонстровано співставну дію низьких і високих доз колхіцину.
У той час як прийом НПЗП і ГК може викликати серцево-судинний ризик, існують дані нещодавніх досліджень, у яких зазначено, що колхіцин може відігравати певну роль у вторинній профілактиці серцево-судинних захворювань. У ретроспективному дослідженні хворих на подагру (n=1288) використання колхіцину було пов’язане зі значно нижчою частотою інфаркту міокарда (1,2 проти 2,6%; р=0,03). У проспективному рандомізованому контрольованому дослідженні пацієнтів зі стабільною стенокардією (n=532) використання колхіцину 0,5 мг на день у комбінації зі статинами та інших стандартних стратегій вторинної профілактики асоціювалося зі зменшенням частоти гострого коронарного синдрому, позалікарняної зупинки серця та кардіоемболічного ішемічного інсульту (відношення ризиків 0,33; 95% довірчий інтервал – ДІ – 0,18-0,59; р<0,001). Отже, саме колхіцин може бути препаратом вибору при гострому епізоді подагри у пацієнтів із серцево-судинними ризиками та у випадках, коли застосування НПЗП протипоказане. Взаємодії між колхіцином та інгібіторами CYP3A4 і Р-глікопротеїну (наприклад, дилтіазем, верапаміл, еритроміцин, кларитроміцин, кетоназол, ітраконазол, циклоспорин А) добре відомі і були пов’язані з летальним наслідком. CYP3A4 бере участь у метаболізмі колхіцину, при цьому одночасне введення інгібіторів CYP3A4 може призвести до накопичення колхіцину й зростання його токсичності. При одночасному застосуванні з цими препаратами дозу колхіцину необхідно зменшувати. Звичайною схемою використання колхіцину є старт із дози 1,2 мг із подальшим прийомом у дозі 0,6 мг через 1 год. При застосуванні з інгібіторами CYP3A4 і Р-глікопротеїну дозу колхіцину знижують: 0,6 мг із подальшим прийомом через 1 год у дозі 0,3 мг.
Інгібітори інтерлейкіну-1. Головним індуктором розвитку гострого запалення у хворих на подагру є стимуляція кристалами сечової кислоти синтезу ІL-β, що опосередковується через систему Toll-подібних рецепторів, розташованих на поверхні моноцитів і мононуклеарних клітин синовіальної оболонки, шляхом активації цитозольного білка NLRP3 (кріопірину), що, у свою чергу, активує каспазу-1, під дією якої утворюється активна форма ІL-1β; залучаються різні типи клітин-ефекторів запалення, запускаючи каскад клітинних імунних реакцій, зокрема міграцію нейтрофілів у вогнище запалення й виділення зрілих форм прозапальних білків. Крім того, саме гіперпродукція ІL-1β у хворих на подагру може бути причиною розвитку у місцях відкладення кристалів моноурату натрію хронічного запалення й деструктивних процесів. Застосування інгібіторів ІL-1β при гострому нападі подагри є більш ефективним, ніж використання НПЗП і колхіцину, особливо у разі непереносимості чи високого ризику ускладнень. Більшість даних стосуються канакінумабу – повністю людського моноклонального антитіла IgG1 до ізотипу ІL-1β та рилонацепту, що зв’язується з IL-1, запобігаючи тим самим його взаємодії з рецептором. У дослідженнях продемонстровано переваги канакінумабу порівняно з колхіцином і ГК щодо зняття гострого нападу подагри, а рилонацепт виявився ефективним у профілактиці гострих атак при ініціації уратознижуючої терапії. Інфікування і реакції в місці введення були найбільш поширеними побічними ефектами, пов’язаними з канакінумабом і рилонацептом. У зведених даних 12-тижневого дослідження β-RELIEVED та β-RELIEVED II повідомляється про 20% випадків інфекцій, 1,8% випадків серйозних інфекцій, 4,9% випадків реакції в місці ін’єкції у пацієнтів, що отримували канакінумаб.
Застосування канакінумабу може мати пріоритетне значення для хворих на подагру в разі наявності в них ниркової недостатності, враховуючи, що корекції дози препарату у пацієнтів із порушенням функції нирок не вимагається. У таких хворих вибір протизапальної терапії до останнього часу обмежувався ГК, і дуже важливим було встановлення більш вираженого ефекту канакінумабу порівняно з ГК. У дослідженні P. Sunkureddi та співавт. проаналізовано порівняльну ефективність канакінумабу і тріамцинолону у хворих із нирковою недостатністю (показник швидкості клубочкової фільтрації – ШКФ – <60 мл/хв). Виявилося, що редукція ризику розвитку загострень артриту при застосуванні канакінумабу порівняно з тріамцинолоном була на 54% меншою при співставному впливі на показники ниркової функції й артеріального тиску (АТ).
Також перспективним видається використання канакінумабу у хворих на подагру з ризиком розвитку кардіоваскулярних катастроф, що є основною причиною їх смерті. Найважливішу роль в ґенезі атеросклерозу, в тому числі у хворих на подагру, відіграє хронічне запалення. Передбачається, що пригнічення запалення може зменшити цей ризик, тому оптимальні шляхи вибору протизапальної терапії є предметом пильної уваги і обговорення.
З метою визначення можливостей канакінумабу впливати на кардіоваскулярний ризик недавно стартувало плацебо-контрольоване дослідження CANTOS (Canakinumab ANti-inflammatory Thrombosis OutcomesStudy), в яке планується включити 17 200 хворих із сироватковим рівнем С-реактивного білка >2 мг/дл, незважаючи на терапію статинами. Введення канакінумабу буде здійснюватися кожні 3 міс у різних дозуваннях (50/150/300 мг); упродовж дослідження (планується 4 роки) будуть реєструвати випадки нефатальних інфарктів міокарда, інсультів і смерті, асоційованої з кардіоваскулярними катастрофами; випадки цукрового діабету 2 типу, венозного тромбозу.
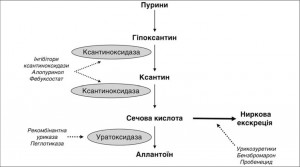
На відміну від лікування гострої подагри, препарати для якої використовуються періодично, запобігання рецидиву подагри потребує довготривалого й скрупульозного застосування уратознижуючої терапії. Зменшення концентрації уратів може досягатися шляхом зниження продукції сечової кислоти (інгібітори ксантиноксидази: алопуринол, фебуксостат), збільшення екскреції уратів нирками (урикозуретики: бензбромарон, пробенецид) або перетворення уратів на водорозчинний алантоїн (рекомбінантна уриказа: пеглотиказа). Механізм дії відомих уратознижуючих препаратів показаний на рисунку.
Алопуринол залишається препаратом, що найширше використовується для зниження рівня уратів. Терапія алопуринолом має розпочинатися з низьких доз (100 мг) і підвищуватися на 100 мг кожні 2-4 тиж за необхідності. Особливо ретельно слід підбирати дози у пацієнтів із хронічною нирковою недостатністю. Алопуринол зазвичай добре переноситься, можуть виникнути незначні шкірні реакції, які реєструються приблизно у 2% хворих. Препарат є безпечним, однак поява алергічних реакцій суттєво утруднює його використання. З практики багатьох експертів відомо, що спроби провести десенсибілізацію в більшості випадків є неефективними, а іноді й небезпечними, тому що алергія на алопуринол генетично детермінована.
У недавньому дослідженні за типом «випадок-контроль» розглянуто клінічні фактори ризику для розвитку побічних ефектів алопуринолу. Серед 1934 пацієнтів, що приймали алопуринол, у 94 зареєстровано побічні реакції, у тому числі висип (3% випадків), шлунково-кишкові розлади (2% випадків), алопуринол-асоційований синдром гіперчутливості (1% випадків), лихоманку (1% випадків). Статистичний регресивний аналіз встановив, що одночасний прийом колхіцину (р=0,012) і статинів (р=0,041) підвищує ризик побічних ефектів алопуринолу. Одним із найбільш серйозних і навіть потенційно смертельних побічних ефектів є алопуринол-асоційований синдром гіперчутливості, що характеризується висипом (наприклад, токсичний епідермальний некроліз, ексфоліативний дерматит), еозинофілією, лейкоцитозом, пропасницею, гепатитом і нирковою недостатністю. Захворюваність оцінюється приблизно в 0,1%. Факторами ризику цього ускладнення є супутня діуретична терапія, ниркова недостатність, висока доза алопуринолу, ранній початок терапії алопуринолом та носійство HLA-B*5801 гена. Носійство HLA-B*5801 стійко асоціюється з серйозними побічними шкірними реакціями у разі застосування алопуринолу в різних етнічних групах. Недавнє ретроспективне дослідження за типом «випадок-контроль» повідомило про 100% чутливість і 86,7% специфічність для HLA-B*5801 при прогнозуванні серйозних шкірних побічних реакцій. Клінічний фармакогенетичний консорціум (Clinical Pharmacogenetics Implementation Consortium) опублікував рекомендації, заявивши, що алопуринол протипоказаний при носійстві HLA-B*5801.
Чи існує зв’язок між дозою алопуринолу й побічними реакціями, залишається спірним питанням. Рекомендації К. Hande та співавт. на основі визначення кліренсу креатиніну були розроблені з урахуванням очевидного зв’язку між нирковою функцією, дозою алопуринолу й шкірними реакціями. Однак здебільшого пацієнти не могли досягти рекомендованих сироваткових концентрацій сечової кислоти, використовуючи рекомендовані дози. Підвищення доз викликало численні шкірні реакції, а також значне погіршення функцій печінки й нирок. Сьогодні проводяться численні дослідження щодо встановлення ефективної й безпечної дози алопуринолу, особливо при зниженій ШКФ.
У ще одному дослідженні за типом «випадок-контроль» продемонстровано, що висока стартова доза алопуринолу асоціюється з тяжкими шкірними реакціями. На підставі цього запропоновано стартувати з дози алопуринолу 1,5 мг на 1 мл ШКФ. Наприклад, при ШКФ 38 мл/хв стартова доза алопуринолу становитиме 38×1,5 мг = 57 мг. У практичному відношенні це відповідає нещодавнім рекомендаціям Американського коледжу ревматології (ACR), які передбачають початкову дозу алопуринолу 50 мг/день у пацієнтів з 4-ю або 5-ю стадією хронічного захворювання нирок і 100 мг/день для усіх інших когорт пацієнтів.
Окрім того, алопуринол за структурою подібний до гіпоксантину і бере участь у широкому спектрі пуринових і піримідинових реакцій, що позбавляє його селективності й адресного впливу на патологічний процес, який викликає хворобу.
Фебуксостат – це 2-(3-ціано-4-ізобутоксифеніл)-4-метилтіазол-5-карбоксильна кислота, нещодавно розроблений непуриновий інгібітор ксантиноксидази. Його молекулярна структура абсолютно відрізняється від структури алопуринола. Фебуксостат, як і алопуринол, інгібує фермент ксантиноксидазу шляхом приєднання до молібден-птеринового центру, єдиного у всіх пуринів. Однак є ціла низка відмінностей цієї взаємодії.
1. Пригнічення різних форм ензиму: алопуринол зв’язується тільки з редукованою формою ензиму, фебуксостат формує комплекс з обома формами ксантиноксидази – редукованою і оксидийованою. Переваги фебуксостату є особливими, зважаючи на те що дві різні форми ензиму можуть обмінюватися іонами молібдену («пінг-понг»-механізм) і, перетворюючись з однієї форми на іншу, «тікати» від дії алопуринолу.
2. Особливості формування кристалічного зв’язку з ензимом: фебуксостат практично повністю заповнює вузькі канали, що ведуть до молібденового центру, стійко пригнічуючи активність ферменту. Алопуринол є інгібітором механізму дії ензиму, тимчасово усуваючи його активність.
3. Щільність зв’язків: фебуксостат інгібує ксантиноксидазу шляхом утворення високоаффінних міцних зв’язків з обома формами ензиму, алопуринол має більш слабкий зв’язок лише з однією формою ферменту.
4. Реактивація ензиму: фермент, інгібований алопуринолом, реактивується швидко (Т1/2=300 хв при 25°C) під дією спонтанної реоксидації молібденового центру. Фебуксостат, навпаки, тривало пригнічує ензим внаслідок утворення досить стабільних зв’язків.
5. Селективність: фебуксостат практично не впливає на інші ферменти пуринового й піримідинового метаболізму, на відміну від алопуринолу, що дозволяє називати його селективним інгібітором ксантиноксидази.
У 2005 р. опубліковано результати рандомізованого подвійного сліпого 52-тижневого багатоцентрового дослідження III фази, в якому порівнювали безпеку й ефективність різних доз фебуксостату та алопуринолу (Febuxostat versus Allopurinol Controlled Trial – FACT). У дослідження було включено 760 хворих, частота небажаних явищ була однаковою у всіх групах. Найбільш часто відзначалися підвищення рівня печінкових ферментів, діарея, головний біль. Серйозні небажані явища з однаковою частотою спостерігалися у всіх групах – у 51 хворого, з них у 34 пацієнтів продовжили терапію.
Висловлювалися побоювання щодо серцево-судинної безпеки фебуксостату. Під час ІІІ фази клінічних досліджень, у яких порівнювали фебуксостат та алопуринол, повідомили про невелику кількість серцево-судинних побічних ефектів в обох групах лікування. У той час як більшість пацієнтів у цих дослідженнях мали й інші серцево-судинні фактори ризику, залишається неясним, чи пов’язаний підвищений ризик несприятливих серцево-судинних результатів із застосуванням інгібіторів ксантиноксидази. На сьогоднішній день продовжується ІІІВ фаза рандомізованого дослідження хворих (n=7500) на подагру з чітко визначеними серцево-судинними захворюваннями, у якому мають оцінити ризик серйозних несприятливих серцево-судинних подій (серцево-судинної смерті, нефатального інфаркту міокарда, нефатального інсульту й нестабільної стенокардії, що потребує реваскуляризації) у хворих, що приймають алопуринол і фебуксостат. Враховуючи широке визнання зв’язку між подагрою (а також часто важкою подагрою) й серцево-судинними захворюваннями в цій групі пацієнтів, необхідність проведення уратознижуючої терапії не викликає сумнівів. Водночас немає даних щодо необхідності обмеження дози інгібіторів ксантиноксидази у таких пацієнтів.
Клінічні дослідження показали, що фебуксостат є ефективним засобом для зниження рівня сечової кислоти. Фебуксостат у дозі 80 мг/добу продемонстрував більшу ефективність порівняно з алопуринолом у дозі 300 мг/добу. Переносимість препарату була доброю в усіх дослідженнях. Важливою в практичному відношенні є добра переносимість фебуксостату хворими з синдромом гіперчутливості до алопуринолу.
Є обмежені дані щодо терапії фебуксостатом у пацієнтів із нирковою недостатністю (ШКФ <50 мл/хв). Єдине спостереження використання фебуксостату у дозі 10-20 мг/добу було проведене у 5 пацієнтів, які перебували на гемодіалізі. У жодного з них не відзначено побічних ефектів, хоча тривалість терапії не повідомляється.
Пеглотиказа зменшує сироваткову концентрацію уратів унаслідок ферментативної деградації сечової кислоти в більш розчинні форми, зокрема в екскретований алантоїн.
У початкових (упродовж 6 міс) дослідженнях, у яких узяли участь 225 пацієнтів, найбільш поширеними побічними ефектами, окрім гострих нападів подагри, виявились інфузійні реакції, що були зареєстровані в 26% випадків у пацієнтів, які отримували інфузію двічі на тиждень, і у 42% випадків у тих, що отримували інфузію щомісяця. Інші побічні ефекти включали головний біль (11% випадків при щомісячному дозуванні) і нудоту (7% випадків). Серйозні несприятливі події реєструвалися значно частіше у пацієнтів, які отримували пеглотиказу 1 раз на 2 тиж (24%; 95% ДІ – 15-34%) та у тих, хто приймав 1 раз на місяць (23%; 95% ДІ 14-33%), порівняно з прийомом плацебо (12%; 95% ДІ 4-25%). Незначну кількість серйозних серцево-судинних побічних реакцій під час періоду дослідження зафіксовано у пацієнтів із наявністю факторів ризику серцево-судинних подій та тривалим анамнезом кардіоваскулярних захворювань.
Нещодавно опубліковано результати продовження відкритого етапу дослідження у 149 пацієнтів, які отримали в середньому 29±18 інфузій пеглотикази і яких спостерігали протягом наступних 25±11 міс. Інфузійні реакції займають друге місце (після спалахів подагри) серед найбільш поширених побічних ефектів, що зустрічалися в 44% хворих і вважалися важкими в 18%. Більшість пацієнтів з інфузійними реакціями мали сироватковий рівень уратів >360 мкмоль/л (6 мг/дл). Зважаючи на це, рекомендується припинити прийом інших уратознижуючих препаратів на період інфузій пеглотикази, оскільки вони можуть маскувати підвищений сироватковий рівень сечової кислоти й порушувати ідентифікацію пацієнтів, які мають ризик виникнення інфузійних реакцій.
Препарати, що застосовуються у веденні подагри, як правило, добре переносяться, але можуть бути пов’язані зі значними негативними наслідками. Ризик цих побічних ефектів залежить від коморбідності та прийому супутніх препаратів. Так, на сьогодні залишаються без відповіді питання про взаємозв’язок між серцево-судинними подіями та прийомом колхіцину й інгібіторів ксантиноксидази. Це питання активно досліджується, утім остаточних результатів і відповідних рекомендацій поки що не отримано. Тим часом лікарі мають пам’ятати про взаємодію між колхіцином і серцево-судинними препаратами. Проблеми залишаються також у лікуванні пацієнтів із порушеною функцією нирок. Є обмежені дані про використання фебуксостату при нирковій недостатності. Ретроспективні дослідження демонструють, що розрахунок дози алопуринолу залежно від кліренсу креатиніну є ефективним, утім значна частка пацієнтів не досягає цільових значень сечової кислоти, що нівелює ефекти уратознижуючої терапії. Роль визначення HLA-B*5801 у запобіганні випадкам серйозних шкірних реакцій ще належить з’ясувати. Економічну ефективність скринінгу на HLA-B*5801, зокрема в популяціях із низьким рівнем ризику, ще належить встановити, але цілком імовірно, що більш дешеві й більш доступні тести для широкого скринінгу будуть рекомендуватися.