1 квітня, 2015
Ревматология-2014: украинский и международный ракурс
 О.Б. Яременко, д.м.н., профессор, главный внештатный ревматолог МЗ Украины, заведующий кафедрой внутренних болезней стоматологического факультета Национального медицинского университета им. А.А. Богомольца, г. Киев
О.Б. Яременко, д.м.н., профессор, главный внештатный ревматолог МЗ Украины, заведующий кафедрой внутренних болезней стоматологического факультета Национального медицинского университета им. А.А. Богомольца, г. Киев
В 2014 г. ревматология продолжала оставаться одной из наиболее динамично развивающихся областей клинической медицины. В странах Европы, Америки и Азии проходили десятки многоцентровых клинических исследований по изучению эпидемиологии ревматических заболеваний, оценке эффективности и безопасности новых лекарственных средств; проводились масштабные высокотехнологичные исследования влияния генетических факторов на возникновение, прогнозирование течения и предсказание ответа на лечение наиболее распространенных и редких заболеваний; разрабатывались новые и пересматривались предыдущие диагностические и лечебные рекомендации. В Украине также произошли некоторые примечательные события, часть из них мы упоминаем в данной статье.
В апреле 2014 г. приказом № 263 Министерства здравоохранения (МЗ) Украины был утвержден унифицированный клинический протокол оказания первичной, вторичной (специализированной) и третичной (высокоспециализированной) медицинской помощи (УКПМП) и медицинской реабилитации при ревматоидном артрите (РА) – первый такого рода отечественный документ в области ревматологии. Вынесению протокола на рассмотрение МЗ Украины предшествовали многомесячная работа рабочей группы, презентация документа и его обсуждение на Академии ревматологии (Academy of Rheumatology; г. Лиссабон, Португалия) с участием вице-президента Европейской противоревматической лиги (EULAR) профессора Джозефа Смолена. Этот УКПМП был разработан на основе составленного рабочей группой адаптированного клинического руководства, базирующегося на лучших международных источниках доказательной информации о надлежащей медицинской практике при РА. Положения УКПМД и их обоснования нацелены на создание единой, комплексной, мультидисциплинарной, эффективной системы оказания медицинской помощи больным РА. Протокол охватывает все ее этапы, начиная с врача первичного звена; определяет содержание и последовательность мероприятий по раннему выявлению, диагностике, лечению и реабилитации пациентов в возрасте старше 18 лет. Одна из особенностей украинского УКПМП по сравнению с зарубежными аналогами – включение в один из его разделов алгоритма рационального применения нестероидных противовоспалительных препаратов (НПВП) с учетом желудочно-кишечного (ЖК) и сердечно-сосудистого (СС) рисков. Необходимость этого шага была продиктована тем, что правила безопасного использования этой наиболее распространенной в ревматологии группы препаратов до сих пор не регламентированы ни одним официальным отечественным документом. Если УКПМП – достаточно лаконичное изложение целесообразных практических действий, то в адаптированном клиническом руководстве можно найти доказательную базу каждого содержащегося в протоколе положения. Создание первого ревматологического украинского протокола именно по РА не случайно, поскольку это заболевание является наиболее распространенной и тяжелой воспалительной артропатией в нашей стране. Так, по данным официальной медицинской статистики за 2013 г., распространенность РА в Украине в абсолютных показателях составляла 115,5 тыс. больных, а заболеваемость – чуть более 4 тыс. На сегодня в медицинских учреждениях большинства областей Украины на базе УКПМП созданы локальные клинические протоколы оказания помощи пациентам с РА, учитывающие региональные особенности индивидуального «маршрута» пациента.
Серьезным шагом в ходе интеграции отечественной системы здравоохранения в европейское медицинское сообщество стал комплекс организованных МЗ Украины мероприятий по реализации положений принятого Верховной Радой Украины в апреле 2014 г. Закона Украины «О внесении изменений в Основы законодательства Украины о здравоохранении относительно обеспечения профилактики и лечения редких (орфанных) заболеваний». Орфанные («сиротские») заболевания – это патологии, затрагивающие небольшую часть популяции, которые угрожают жизни человека или хронически прогрессируют, приводят к сокращению продолжительности его жизни или инвалидности, их распространенность среди населения не превышает 1:2000. На пути реализации положений этого закона МЗ Украины с участием главных внештатных специалистов в прошедшем году были сделаны первые шаги: 1) подготовлен перечень редких (орфанных) заболеваний, в который вошли 38 ревматических заболеваний и синдромов (утвержден Приказом МЗ Украины № 778 от 27.10.2014 г.); 2) составлен список орфанных (разработанных для лечения орфанных заболеваний) препаратов с ориентировочными расчетами стоимости лечения таких больных в нашей стране (на стадии утверждения). В дальнейшем предусмотрены следующие шаги: создание государственных реестров граждан, страдающих орфанными заболеваниями; определение порядка обеспечения их орфанными препаратами; поиск источников финансирования. Последний вопрос на данном историческом отрезке, безусловно, является наиболее болезненным. Вероятно, проблема финансовой поддержки реализации указанного закона, как и в целом обеспечения больных тяжелыми ревматическими заболеваниями дорогостоящими препаратами, должна решаться комплексно, в рамках внедрения концепции страховой медицины, привлечения средств спонсорских организаций.
В прошлом году в Украине был зарегистрирован и стал доступным для клинического применения при иммуновоспалительных артропатиях еще один иммунобиологический препарат – голимумаб, который пополнил семейство уже присутствующих на нашем фармацевтическом рынке ингибиторов фактора некроза опухолей (ФНО) – адалимумаба, инфликсимаба, этанерцепта. Таким образом, из препаратов этой группы, имеющихся в распоряжении зарубежных специалистов-ревматологов, в Украине отсутствует только один – цертолизумаба пэгол. Голимумаб, представляющий собой полностью человеческие антитела к ФНО, прошел полный цикл клинических испытаний, по результатам которых утверждены показания для его применения, а именно: РА, анкилозирующий спондилоартрит и псориатический артрит. Его эффективность и безопасность изучены в более чем 36 интервенционных и не менее чем 5 обсервационных исследованиях. В рамках контролируемых клинических программ голимумаб получали свыше 11 тыс. больных, а в обычной клинической практике препарат применялся у 256 тыс. пациентов во всем мире. Продолжается изучение возможности его использования в лечении больных ювенильным РА и неспецифическим язвенным колитом. Интересно, что в то время, как другие фармацевтические компании, производящие иммунобиологические препараты с внутривенной формой введения, сконцентрировали усилия на разработке форм для подкожного введения (ритуксимаб, тоцилизумаб), разработчики голимумаба избрали прямо противоположный вектор: имея препарат для подкожного введения, они создали форму для внутривенного пути применения и инициировали проведение соответствующих клинических исследований, в которых принимают участие и несколько ревматологических центров Украины. Фирма-производитель сделала выводы из опубликованных результатов обсервационных исследований и опросов/анкетирования больных, согласно которым значительная часть пациентов с воспалительными артропатиями отдает предпочтение препаратам с внутривенной формой введения. Среди выделенных пациентами преимуществ внутривенного пути введения ингибиторов ФНО – меньшая частота введения лекарственного средства и посещения врачебного кабинета; отсутствие сложностей, связанных с проведением самостоятельных инъекций; независимость от помощи членов семьи или вспомогательного домашнего персонала. Такой точки зрения придерживаются прежде всего лица более пожилого возраста, больные с большим стажем артрита, нетрудоспособные пациенты или имеющие функциональные ограничения, испытывающие боязнь/тревогу относительно способности самостоятельно проводить инъекции. Время покажет, насколько оправданными будут усилия по разработке внутривенной формы препарата, хотя, безусловно, иметь возможность выбора (лекарственного средства, путей и частоты его применения) всегда лучше, чем отсутствие таковой.
Среди значительных, информационно-насыщенных событий в ревматологии в 2014 г. следует выделить очередной конгресс EULAR, на котором традиционно рассматривался широкий круг вопросов, касающихся этиопатогенеза, диагностики и лечения распространенных и редких ревматических заболеваний. Можно отметить результаты нескольких исследований, имеющих наибольшее прикладное значение. В последние годы в стадии активной разработки и клинического изучения находятся несколько иммунобиологических препаратов, блокирующих эффекты интерлейкина-6 (IL-6). На конгрессе были представлены результаты исследования ІІІ фазы (SARIL-RA-MOBILITY), в котором оценивалась эффективность и безопасность сарилумаба (полностью гуманизированного моноклонального антитела к рецепторам IL-6) у больных РА, у которых не был достигнут адекватный ответ при лечении метотрексатом. У пациентов, получавших сарилумаб (1 раз в 2 нед подкожно) в комбинации с метотрексатом, отмечено достоверное улучшение достижения всех комбинированных конечных точек по сравнению с больными, принимавшими метотрексат с плацебо. Так, на 24-й неделе лечения сарилумабом в дозе 200 мг зарегистрировано снижение показателей клинической активности артрита на 66% (в группе плацебо – на 33%), а на 52-й неделе – замедление структурного повреждения суставов. Наиболее частыми побочными явлениями были инфекции, повышение уровней холестерина и аминотрансфераз. После завершения еще трех клинических испытаний сарилумаб, вероятно, станет вторым после тоцилизумаба анти-IL-6-препаратом, имеющимся в распоряжении клиницистов.
Еще одним новым направлением в иммунобиологической терапии РА является разработка и уже начавшееся практическое применение ингибиторов янус-киназы (JAK-ингибиторов). В настоящее время проходят клинические испытания несколько лекарственных средств этой группы (барицитиниб, децернотиниб, тофацитиниб, филготиниб и др.), один из них (тофацитиниб) уже зарегистрирован в нескольких странах, включая США. На конгрессе EULAR были представлены несколько докладов, подтверждающих эффективность и приемлемый профиль безопасности JAK-ингибиторов. Привлекательность данного направления биологической терапии заключается в том, что янус-киназа – это семейство внутриклеточных ферментов, участвующих в инициировании синтеза различных цитокинов, ряда факторов роста. То есть при подавлении активности этих ферментов происходит блокада иммунопатологического процесса на более ранних, «проксимальных» этапах. Исходя из этого ожидается, что JAK-ингибиторы могут быть эффективными у больных, не отвечающих на терапию антицитокиновыми препаратами, например ингибиторами ФНО или IL-6, поскольку последние действуют только на уже синтезированные, внеклеточные молекулы цитокинов или на их рецепторы. Подтвердятся ли эти ожидания, покажут дальнейшие исследования. В одном из докладов были представлены результаты исследования, продемонстрировавшие хороший профиль безопасности адалимумаба при 4-летнем применении у больных ювенильным РА.
Достаточно большое количество докладов и постерных сообщений было посвящено биосимилярам – «копиям» иммунобиологических препаратов. Поскольку по технологическим причинам воспроизвести абсолютно идентичный оригиналу биологический препарат невозможно (именно поэтому они и называются биосимилярами, а не генериками), биосимиляры проходят полный цикл клинических испытаний и «под увеличительным стеклом» должны доказать свою схожесть с брендовыми препаратами как в отношении эффективности, так и безопасности. На конгрессе были представлены результаты прямых сравнительных исследований нескольких новых биосимиляров с оригинальными лекарственными средствами (инфликсимабом, этанерцептом, ритуксимабом), во всех случаях биосимиляры продемонстрировали свою схожесть/эквивалентность в отношении эффективности и профиля безопасности.
Следует также выделить обнародованную на конгрессе интересную информацию, касающуюся рутинной клинической практики. Несколько неожиданным был интерес к фармакологическому «долгожителю» ревматологии – метотрексату. В двух исследованиях были показаны достоинства парентеральной формы препарата: в одном из них продемонстрировано, что при недостаточной эффективности таблетированного метотрексата у пациентов с РА переход на такую же дозу в парентеральной форме увеличивает количество больных, у которых получен ответ на терапию; в другом установлено, что при использовании парентеральной формы метотрексата с самого начала лечения более половины больных РА достигают ремиссии или низкой активности заболевания, тем самым снижается доля пациентов, нуждающихся в биологической терапии.
Чрезвычайно важными следует признать результаты проведенного в Канаде исследования, в котором изучалась возможность прекращения иммуносупрессивной терапии (азатиоприном, метотрексатом, микофенолата мофетилом) у больных системной красной волчанкой. Ведь существующие рекомендации по лечению этого заболевания регламентируют только назначение, но не отмену иммуносупрессантов. В канадском ретроспективном исследовании было установлено, что при соблюдении методики постепенной отмены иммуносупрессанта (ступенчато, по 25% от исходной дозы) 56% больных смогли полностью прекратить их прием. Из них после отмены иммуносупрессанта 74% пациентов не имели обострений заболевания в течение 2 лет, а 50% – в течение 3 лет и оставались клинически стабильными еще на протяжении почти 5 лет. Наиболее значимым прогностическим фактором риска развития обострений была позитивность в отношении специфических для системной красной волчанки антиядерных антител. С учетом этих данных ревматологи по-новому могут рассматривать перспективы лечения иммуносупрессантами больных системной красной волчанкой. Мажорным аккордом конгресса EULAR-2014 стало представление первых рекомендаций по визуализации при спондилоартритах. Хотя рентгенологическое исследование сохраняет свое значение, прежде всего из-за невысокой стоимости, однако при небольшой продолжительности симптомов сакроилеита, при подозрении на спондилит, для объективизации теносиновитов, энтезитов и периферических артритов, мониторинга активности заболевания методом выбора является магнитно-резонансная томография.
В отношении наиболее широко применяемой в ревматологии группы лекарственных средств – НПВП – какого-либо существенного обновления информации в 2014 г. не было. Можно выделить только два новых документа, имеющих широкую и прочную доказательную базу. Это Кокрановский обзор, посвященный оценке эффективности и безопасности разовых доз пероральных аналгетиков для купирования острой послеоперационной боли у взрослых пациентов, который является обновленной версией аналогичного обзора 2011 г. Cогласно изложенным в этих обзорах результатам доля больных, у которых боль уменьшилась по крайней мере на 50% на период 4-6 ч, для разных препаратов составляла 30-70%, а период времени до повторного введения обезболивающего средства варьировал в пределах 2-20 ч (для плацебо и эторикоксиба соответственно). Побочные эффекты встречались редко, в целом не было различий в их частоте между активным препаратом и плацебо, за исключением аспирина и опиоидов. Следует отметить, что среди 46 изученных НПВП в разных дозах и комбинаций опиоидов с парацетамолом наилучшие (т.е. самые низкие) показатели NNT (количество пациентов, которых необходимо пролечить для достижения обезболивания на ≥50% в течение 4-6 ч) были получены для эторикоксиба 120 мг (NNT=1,9), далее следовали кетопрофен 25 мг и 100 мг (NNT=2,0 и 2,1 соответственно), кодеин 60 мг с парацетамолом 1000 мг (NNT=2,2) и такие популярные НПВП, как диклофенак 100 мг (NNT=2,3), целекоксиб 400 мг (NNT=2,5) и ибупрофен 400 мг (NNT=2,5). Парацетамол в дозах от 500 мг до 1000 мг оказался в конце списка с показателями NNT >3,6, что в очередной раз подтвердило низкую обезболивающую активность этого препарата.
Второй документ – это вышедшие в феврале 2014 г. под эгидой Национальной службы здравоохранения (NHS) Великобритании обновленные (пересмотр версии 2009 г.) рекомендации по назначению НПВП при артритах и остеоартрозе у взрослых пациентов, одобренные Wirral Drug and Therapeutics Committee (своеобразный формулярный комитет, осуществляющий контроль за допуском к практическому применению лекарственных средств и лечебных технологий, в том числе рекомендованных Национальным институтом здоровья и клинического совершенствования (NICE) Великобритании). Принципиально эти рекомендации мало отличаются от алгоритма рационального применения НПВП, изложенного в утвержденном национальном УКПМП «Ревматоидный артрит». Перед назначением НПВП британские рекомендации предлагают оценить гастроинтестинальный (ГИ) и кардиоваскулярный (КВ) риски и принимать решение в зависимости от их наличия. Так, при отсутствии риска развития ГИ и КВ осложнений могут применяться ибупрофен, напроксен или эторикоксиб. У лиц с повышенным ГИ риском следует отдавать предпочтение ибупрофену, целекоксибу, эторикоксибу, при подагре – также напроксену, во всех случаях – в сочетании с недорогими ингибиторами протонной помпы (ИПП). У больных с наличием факторов риска КВ осложнений (заболеваний коронарных, мозговых и периферических артерий, застойной сердечной недостаточности, артериальной гипертензии, гиперлипидемии, сахарного диабета, курения) без повышенного ГИ риска наиболее предпочтительным НПВП является напроксен, в качестве альтернативы используют целекоксиб или эторикоксиб. Оптимальная тактика при сочетании повышенных ГИ и КВ рисков – избегать назначения любых НПВП. При этом подчеркивается, что при необходимости длительного приема НПВП следует стремиться к использованию минимальных эффективных доз на протяжении наиболее короткого периода времени. Относительно актуальных в настоящее время рекомендаций по оптимальному применению НПВП уместно привести философское высказывание Ж.П. Сартра: «Я всегда могу выбрать, но я должен знать, что даже в том случае, если я не выбираю ничего, я тем самым все-таки делаю выбор».
В прошедшем году очередной виток совершила почти детективная история с отношением авторитетных международных медицинских сообществ к медленно действующим симптоматическим препаратам (SYSADOA) для лечения остеоартроза (ОА). В ней можно выделить два аспекта: 1) постепенное сокращение линейки препаратов этой группы; 2) маятникообразные изменения позиций касательно целесообразности применения глюкозамина и хондроитина сульфата.
Научно-идеологические истоки первого аспекта – общемировая тенденция к повышению требований к безопасности лекарственных средств, особенно в контексте соотношения с их эффективностью. Напомним, что согласно определению комитета экспертов Всемирной организации здравоохранения (M. Lequesne et al., 1994) и рекомендаций EULAR по лечению ОА коленного, тазобедренного суставов и кисти (2003; 2005; 2007) SYSADOA должны оказывать положительный эффект на боль и нарушения функции в течение нескольких месяцев от начала применения, и этот результат сохраняется некоторое время после прекращения лечения. Терапия этими средствами сопровождается снижением потребности в аналгетиках и НПВП. В данную группу препаратов входят хондроитина сульфат, глюкозамина сульфат, неомыляемые экстракты сои и авокадо, диацереин и гиалуроновая кислота. В последние годы была предпринята попытка пополнить группу SYSADOA (и даже стать первым препаратом в категории модифицирующих течение ОА – «структурно-модифицирующих») новым лекарственным средством – стронция ранелатом. Действительно, в исследовании SEKOIA с соблюдением современных требований к выявлению симптоммодифицирующего действия и рентгенологической оценке структуро-модифицирующего действия (Европейское медицинское агентство – EMA; 2010) была продемонстрирована способность стронция ранелата не только оказывать достоверное положительное влияние на боль и нарушение функции, но и замедлять по сравнению с плацебо сужение суставной щели у больных ОА коленных суставов. Это подтвердили и результаты анализа количественной магнитно-резонансной терапии – МРТ (J.-P. Pelletier et al., 2013). Однако до настоящего времени стронция ранелат не входит ни в одни международные рекомендации по лечению ОА. Кроме того, в феврале 2014 г. EMA приняло решение ограничить использование этого препарата из-за вероятного повышения сердечно-сосудистого риска (21 February 2014. EMA/84749/2014). В частности, отмечается, что «лечение препаратом должно быть остановлено в случае развития сердечных и циркуляторных проблем, таких как неконтролируемая артериальная гипертензия или стенокардия; больные, перенесшие инсульт и инфаркт миокарда, не должны использовать этот препарат». Существенные ограничения, связанные с безопасностью применения препарата, коснулись и диацереина. 4 сентября 2014 г. ЕМА обнародовало решение (EMA/544268/2014), согласно которому «не рекомендуется применение диацереина у пациентов в возрасте 65 лет и старше из-за рисков, связанных с тяжелой диареей. Лечение следует начинать с половины обычной дозы (т.е. 50 мг в день, а не 100 мг) и прекратить прием диацереина в случае развития диареи. Диацереин не должен использоваться пациентами с заболеваниями печени в настоящее время или в анамнезе». Таким образом, этим решением, которое является обязательным для исполнения во всех странах Европейского Союза, еще больше ограничен перечень препаратов, которые могут применяться для лечения ОА.
Анекдотически детективная же часть истории относится к оставшимся в линейке SYSADOA глюкозамину и хондроитина сульфату. Не является новостью, что в последние годы в целом, по мере повышения требований к качеству проведения клинических исследований, наметилась тенденция к более критичному отношению к эффективности SYSADOA («хондропротекторов»). Еще в 2000 г., по мнению европейских экспертов (A. Pendleton et al., 2000), применение этих препаратов занимало 11-ю позицию в рейтинге полезности различных лечебных мероприятий при ОА коленных суставов, на более высоких позициях находились физические упражнения, прием НПВП, внутрисуставные инъекции глюкокортикоидов, использование трости и др. С целью оценки симптоматического и болезньмодифицирующего действия глюкозамина и хондроитина сульфата с использованием современных стандартов организации клинических испытаний в США было проведено исследование GAIT. По его результатам (A.D. Sawitzke et al., 2008) и данным сетевого метаанализа предыдущих клинических испытаний, посвященных оценке эффективности глюкозамина и хондроитина сульфата при ОА коленного и тазобедренного суставов (S. Wandel et al., 2010), был сделан вывод, что ни один из этих препаратов по отдельности, ни их сочетание не обладают клинически значимым влиянием на суставную боль и скорость сужения суставной щели (потерю хряща). Авторы пришли к заключению, что специалистам в области здравоохранения и страховым компаниям не следует покрывать расходы на эти лекарственные средства; пациентам, еще не получавшим лечение, не следует назначать указанные препараты. Эти выводы нашли отражение в рекомендациях Американской коллегии ревматологов (ACR) по лечению ОА кисти, тазобедренного и коленного суставов (M.C. Hochberg et al., 2012): «ACR не рекомендует пациентам с ОА использовать хондроитина сульфат и глюкозамин». Такое отношение к указанным препаратам, хоть и в несколько смягченной формулировке, было продублировано в рекомендациях Международного общества исследования остеоартрита (OARSI; 2014) по нехирургическому лечению ОА коленных суставов (T.E. McAlindon et al., 2014): «Лечение неопределенной целесообразности для конкретных клинических субфенотипов включает иглоукалывание, неомыляемые экстракты авокадо/сои, хондроитин, костыли, диацереин, глюкозамин, внутрисуставное введение гиалуроновой кислоты, опиоиды (пероральные и трансдермальные), шиповник, чрескожную электрическую стимуляцию нервов и ультразвук».
Не прошло и нескольких месяцев после выхода рекомендаций OARSI, как были опубликованы Рекомендации по алгоритму лечения ОА коленного сустава в Европе и по всему миру: отчет специальной комиссии Европейского общества по клиническим и экономическим аспектам остеопороза и остеоартрита – ESCEO (О. Bruyere et al., 2014), в которых глюкозамина сульфат и хондроитина сульфат были реабилитированы – возвращены в разряд препаратов, относящихся к базовому лечению ОА (рис.).
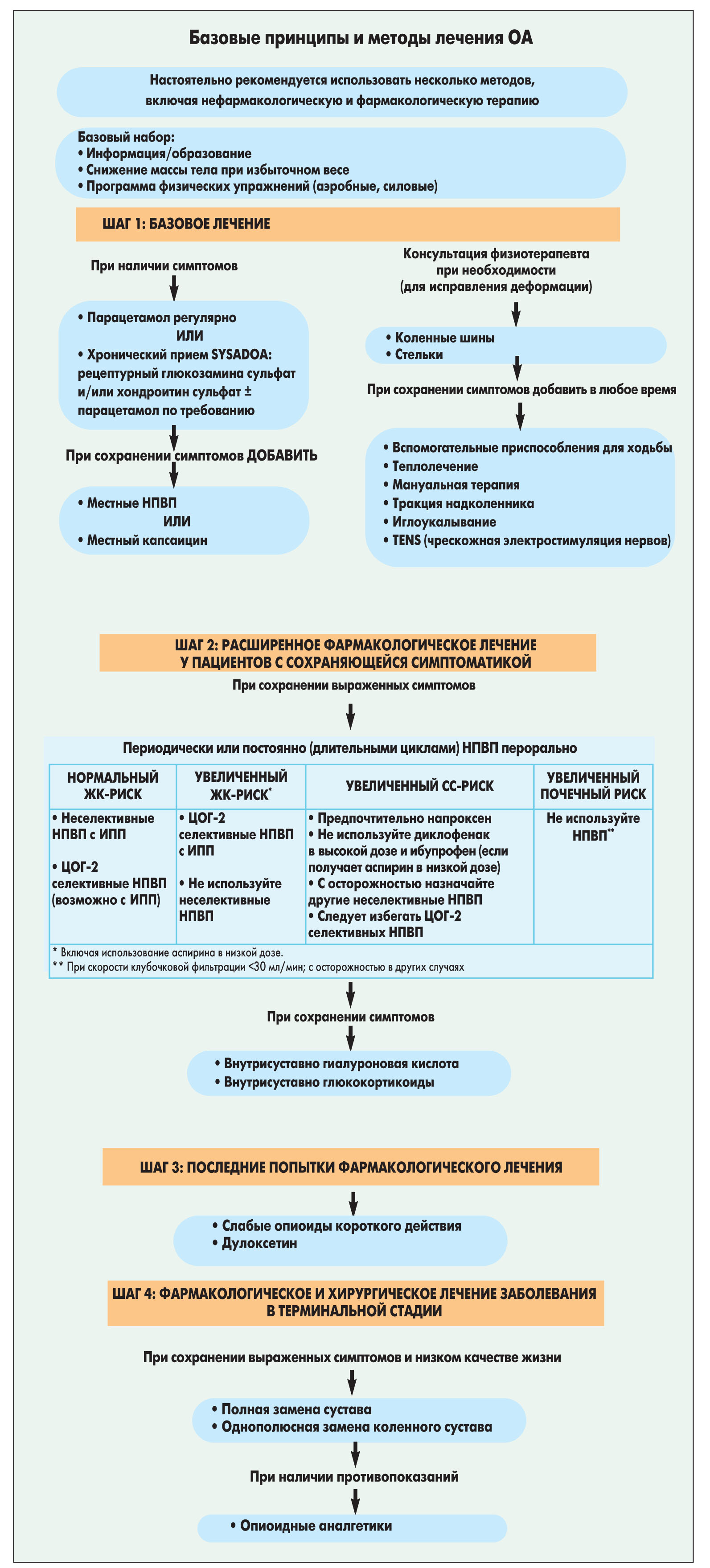 Рис. Рекомендации по алгоритму лечения ОА коленного сустава в Европе и по всему миру: отчет специальной комиссии Европейского общества по клиническим и экономическим аспектам остеопороза и остеоартрита (ЕSСЕО)
Рис. Рекомендации по алгоритму лечения ОА коленного сустава в Европе и по всему миру: отчет специальной комиссии Европейского общества по клиническим и экономическим аспектам остеопороза и остеоартрита (ЕSСЕО) Появлению этих рекомендаций предшествовал публичный отзыв редакцией журнала, опубликовавшего сетевой метаанализ S. Wandel и соавт. (2010), вывода статьи о неэффективности этих SYSADOA и нецелесообразности их применения. Было признано, что S. Wandel и соавт. неправомерно включили в обобщающий метаанализ результаты исследований двух разных препаратов – глюкозамина сульфата и глюкозамина гидрохлорида, так как в отношении второго из них уже давно сформировалась критичная позиция. Кроме того, было обращено внимание на методологическую оплошность исследования GAIT: в нем изучалась эффективность не рецептурных препаратов хондроитина и глюкозамина (они не зарегистрированы в США), а продающихся в супермаркетах пищевых добавок, якобы содержащих указанные молекулы. Поэтому не случайно в рекомендациях ESCEO по лечению ОА (2014) в разделе «Базовое лечение» прописано: «Хронический прием SYSADOA: рецептурный глюкозамина сульфат и/или хондроитина сульфат». Примечательно, что среди соавторов рекомендаций ESCEO (2014) значится едва ли не самый авторитетный в мире специалист по ОА – M.C. Hochberg, который возглавлял авторский коллектив рекомендаций ACR по лечению ОА (2012), категорически отрицавших целесообразность использования глюкозамина и хондроитина сульфата при лечении ОА. Таким образом, синусоида отношения ученых и клиницистов к этим двум препаратам группы SYSADOA после почти 4-летней отрицательной фазы вновь пошла на подъем. Принципиально важно еще раз подчеркнуть, что эта «реанимация» касается только технологически безупречно производимых в Европе препаратов.
Таким образом, 2014 год был отмечен рядом важных событий в ревматологическом сегменте медицины как в Украине, так и в международном масштабе. Наблюдающиеся в последние годы темпы развития теоретической и прикладной ревматологии дают основания полагать, что в наступившем году мы будем свидетелями и участниками новых впечатляющих достижений, которые позволят еще на один шаг продвинуться в направлении снижения медико-социального бремени этой группы заболеваний.


