29 вересня, 2015
Тромбоэмболия легочной артерии: анализ современных рекомендаций и возможности рутинной практики на основе клинического случая

Содержание статьи:
- Тяжесть ТЭЛА.
- Диагноз.
- Клинические проявления.
- Клиническая оценка вероятности ТЭЛА.
- Лабораторная диагностика: определение D-димера.
- Диагностическая стратегия.
- Стратегия оценки прогноза.
- Лечение ТЭЛА у пациентов высокого риска.
- Лечение ТЭЛА у пациентов невысокого (умеренного или низкого) риска.
- Тромболитическая терапия ТЭЛА.
- Клинический случай.
- Выводы.
>>__Тромбоэмболия легочной артерии (ТЭЛА) относится к относительно распространенным неотложным состояниям в кардиореаниматологии. ТЭЛА — трудный диагноз, который часто не ставят из-за неспецифичности клинических проявлений. Важнейшее значение имеют и ранняя диагностика, и своевременное начало интенсивной терапии, которая направлена на восстановление кровотока через закупоренные легочные артерии (ЛА).
Одними из первых и основных документов, стандартизирующих помощь пациентам с ТЭЛА, в Европе и мире были «ESC Guidelines of pulmonary embolism», опубликованные в 2000 и 2008 гг. На сегодняшний день одним из последних документов является «2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism».
К сожалению клиницистов, из-за неспецифичности клинических проявлений истинную встречаемость ТЭЛА трудно оценить. ТЭЛА обычно развивается через 3–7 суток после возникновения тромбоза глубоких вен (ТГВ) и у 10% больных приводит к смерти в течение первого часа после развития симптомов, из-за чего у большинства умерших пациентов остается нераспознанной. В 5–10% случаев первыми проявлениями ТЭЛА являются шок или артериальная гипотензия, еще примерно в 50% случаев при отсутствии шока отмечаются признаки дисфункции и/или повреждения правого желудочка (ПЖ), которые указывают на неблагоприятный прогноз. Большинство случаев смерти (>90%) наблюдается у нелеченых пациентов, у которых ТЭЛА осталась нераспознанной. На долю лечившихся больных приходится менее 10% случаев смерти.
В данной статье авторы хотели бы кратко охарактеризовать основные положения данных рекомендаций и сравнить их с реальной жизнью на основании клинического случая лечения пациента с тромбоэмболией легочной артерии.
Для оценки вероятности ТЭЛА в ходе ее диагностики важным вопросом являются так называемые предрасполагающие факторы венозной тромбоэмболии (ВТЭ) — результат взаимодействия состояния пациента с провоцирующими или ситуационными факторами. Связанные с пациентом предрасполагающие факторы обычно устойчивые, в то время как предрасполагающие, связанные с ситуацией, — чаще преходящие (табл. 1).
Таблица 1. Предрасполагающие факторы ВТЭ
|
Предрасполагающий фактор |
Связанный с пациентом |
Провоцирующий или ситуационный |
|
Сильные (увеличивают риск более чем в 10 раз) |
||
|
Переломы (бедра или голени) |
+ |
|
|
Протезирование тазобедренного или коленного суставов |
+ |
|
|
Крупное общехирургическое вмешательство |
+ |
|
|
Большая травма |
+ |
|
|
Повреждение спинного мозга |
+ |
|
|
Средней силы (увеличивают риск в 2–9 раз) |
||
|
Артроскопические хирургические манипуляции на коленном суставе |
+ |
|
|
Катетеризация центральных вен |
+ |
|
|
Химиотерапия |
+ |
|
|
Хроническая сердечная или дыхательная недостаточность |
||
|
Гормонзаместительная терапия |
||
|
Злокачественные новообразования |
||
|
Терапия пероральными контрацептивами |
||
|
Инсульт с параличом |
||
|
Беременность/послеродовой период |
+ |
|
|
Предыдущие ВТЭ |
||
|
Тромбофилия |
||
|
Слабой силы (увеличивают риск менее чем в 2 раза) |
||
|
Постельный режим более 3 суток |
+ |
|
|
Иммобилизация в положении сидя (в том числе при длительных автомобильных или авиапутешествиях) |
+ |
|
|
Пожилой возраст |
+ |
|
|
Лапароскопические хирургические вмешательства (в том числе холецистэктомия) |
+ |
|
|
Ожирение |
+ |
|
|
Беременность/предродовой период |
+ |
|
|
Варикозно расширенные вены |
+ |
|
Встречаемость ТЭЛА экспоненциально увеличивается с возрастом. Средний возраст больных с острой ТЭЛА составляет 62 года. Около 65% имеют возраст 60 лет и старше. ТЭЛА в 8 раз чаще наблюдается у пациентов старше 80 лет, чем у больных моложе 50 лет.
Ключевые последствия ТЭЛА — это нарушения гемодинамики. Крупные и/или множественные эмболы могут вызывать резкое увеличение легочного сосудистого сопротивления и постнагрузки ПЖ, с которой ПЖ уже не может справиться. Может наступить внезапная смерть, обычно — вследствие электромеханической диссоциации. В части случаев первым проявлением заболевания являются синкопе и/или системная артериальная гипотензия, которая может переходить в шок и впоследствии наступает смерть вследствие острой недостаточности ПЖ. Выпячивание межжелудочковой перегородки в полость левого желудочка (ЛЖ) может вызвать еще большее снижение сердечного выброса в результате диастолической дисфункции ЛЖ.
Вторичная дестабилизация гемодинамики может возникать в первые 24–48 часов в результате раннего рецидивирования ТЭЛА и/или ухудшения функции ПЖ. Такие ранние рецидивы часто встречаются у больных с нераспознанной или неадекватно леченной ВТЭ. Другая причина ухудшения гемодинамики — недостаточная эффективность компенсаторной инотропной и хронотропной стимуляции для поддержания функции ПЖ на длительное время, даже без новых эмболических эпизодов.
В результате неблагоприятного влияния комбинации увеличенной потребности миокарда ПЖ в кислороде и уменьшения градиента его коронарного перфузионного давления оба эти фактора содействуют ишемии и дисфункции ПЖ и могут инициировать порочный круг, способный приводить к фатальному исходу. Предшествующая сердечно-сосудистая патология может неблагоприятно влиять на эффективность компенсаторных механизмов и тем самым ухудшать прогноз. Дыхательная недостаточность при ТЭЛА является в основном следствием гемодинамических расстройств. Гипоксии, которая возникает при ТЭЛА, способствует низкий сердечный выброс и вентиляционно-перфузионное несоответствие.
Тяжесть ТЭЛА
Тяжесть ТЭЛА определяется риском ранней смертности, а не анатомическим расположением и распространенностью эмболов в ЛА. Исходя из этого, в рекомендациях вместо понятий «массивная», «субмассивная» и «немассивная» ТЭЛА с 2008 года принято использовать понятия степени риска раннего (в стационаре или в первые 30 суток) летального исхода, связанного с ТЭЛА (табл. 7).
Оценка риска основывается на наличии факторов риска, которые удобно классифицировать на три группы.
Клинические факторы:
- шок;
- гипотензия (систолическое артериальное давление [САД] <90 мм рт.ст. или резкое снижение АД на 40 мм рт.ст. и более в течение более чем 15 минут, не связанное с аритмией, гиповолемией или сепсисом).
Маркеры дисфункции ПЖ:
- дилатация ПЖ, гипокинезия или повышение давления в ПЖ при ЭхоКГ;
- дилатация ПЖ при спиральной компьютерной томографии;
- повышение BNP или NTproBNP в крови;
- повышение давления в правых отделах сердца при их катетеризации.
Маркеры повреждения миокарда:
- положительный сердечный тропонин Т или I.
Критерии высокого и невысокого риска ТЭЛА представлены в таблице 2. Эту классификацию следует применять также у больных с подозрением на ТЭЛА, так как она помогает в выборе оптимальной диагностической стратегии и начальной тактики ведения.
Таблица 2. Стратификация риска у больных ТЭЛА
|
Риск ранней смерти, связанной с ТЭЛА |
Маркеры риска |
|||
|
Клинические (шок или гипотензия) |
Дисфункция правого желудочка |
Повреждение миокарда |
Лечение |
|
|
Высокий (>15%) |
+ |
(+)* |
(+)* |
Тромболизис или эмболэктомия |
|
Промежуточный (3–15%) |
– |
+ |
+ |
Госпитализация |
|
+ |
– |
|||
|
– |
+ |
|||
|
Низкий (<3%) |
– |
– |
– |
Ранняя выписка или амбулаторное лечение |
Примечание: * — при шоке или гипотензии подтверждение дисфункции/повреждения правого желудочка для зачисления больного в группу с высоким риском не обязательно.
ТЭЛА высокого риска является угрожающим жизни неотложным состоянием и требует специфической стратегии диагностики и лечения (риск ближайшего летального исхода >15%).
ТЭЛА невысокого риска в зависимости от наличия маркеров дисфункции ПЖ и/или миокардиального повреждения может подразделяться на ТЭЛА с промежуточным и низким риском. Критерием промежуточного риска является наличие, как минимум, одного из маркеров дисфункции ПЖ или миокардиального повреждения. На низкий риск ТЭЛА указывает отсутствие маркеров дисфункции ПЖ и миокардиального повреждения (ранняя летальность, связанная с ТЭЛА, <1%).
Диагноз
Термин «подтвержденная ТЭЛА» используют в случаях высокой вероятности ТЭЛА, когда необходимо специфическое лечение, а термин «исключенная ТЭЛА» — в случаях с достаточно низкой вероятностью этого заболевания и низким риском летального исхода, что оправдывает отказ от специфического лечения.
Клинические проявления
Подозрение на возможность ТЭЛА обычно возникает при наличии одного или нескольких клинических симптомов, таких как одышка, боль в грудной клетке или синкопе. По данным нескольких исследований одышка, тахипноэ или боль в груди наблюдались более чем у 90% больных ТЭЛА. Синкопе — достаточно редкое, но важное проявление ТЭЛА, так как может указывать на серьезно уменьшенный гемодинамический резерв. В самых тяжелых случаях развиваются шок и артериальная гипотензия. Плевральная боль в грудной клетке (изолированная или в сочетании с одышкой) является одним из самых частых первых проявлений ТЭЛА (табл. 3). Внезапно возникшая одышка как единственный симптом заболевания обычно связана с ТЭЛА более проксимальной локализации, которая вызывает более значительные нарушения гемодинамики, чем синдром инфаркта легкого. Она может сопровождаться загрудинной болью, напоминающей стенокардию, которая может быть связана с ишемией миокарда ПЖ. Иногда одышка может прогрессивно нарастать в течение нескольких недель, и подозрение на возможность ТЭЛА возникает в связи с отсутствием других причин прогрессирующей одышки. У больных с предшествующей сердечной недостаточностью или заболеванием легких усиление одышки может быть единственным симптомом ТЭЛА.
Таблица 3. Частота встречаемости симптомов и признаков у пациентов с ТЭЛА, %
|
Проявление |
Подтвержденная ТЭЛА (n=219) |
Исключенная ТЭЛА (n=546) |
|
Симптомы |
||
|
Одышка |
80 |
59 |
|
Плевральная боль в груди |
52 |
43 |
|
Загрудинная боль |
12 |
8 |
|
Кашель |
20 |
25 |
|
Кровохаркание |
11 |
7 |
|
Синкопе |
19 |
11 |
|
Признаки |
||
|
Тахипноэ (≥20 в 1 минуту) |
70 |
68 |
|
Тахикардия (≥100 в 1 минуту) |
26 |
23 |
|
Признаки ТГВ |
15 |
10 |
|
Повышение температуры тела (>38,5°С) |
7 |
17 |
|
Цианоз |
11 |
9 |
Оценка отдельных клинических проявлений и симптомов не очень помогает в постановке диагноза, так как они имеют низкую чувствительность и специфичность (табл. 3). При рентгенографии грудной клетки обычно выявляют изменения, чаще всего — в виде дисковидных ателектазов, плеврального выпота или поднятия купола диафрагмы, однако они неспецифичны. Тем не менее, рентгенография грудной клетки очень полезна для исключения других причин одышки и боли в грудной клетке. ТЭЛА обычно приводит к гипоксии, но у 20% таких больных рО2 находится в пределах нормы. ЭКГ-признаки перегрузки ПЖ в виде инверсии зубцов Т в отведениях V1–V4, наличия QR в отведении V1, классического синдрома S1Q3T3 и неполной или полной блокады правой ножки пучка Гиса могут быть полезными, особенно в случаях их внезапного возникновения. Однако эти изменения связаны, как правило, с более тяжелой ТЭЛА и могут возникать при любой перегрузке ПЖ независимо от ее причины.
Таким образом, клинические признаки, симптомы и данные рутинных дополнительных методов исследования не позволяют исключить или подтвердить острую ТЭЛА, но указывают на большую или меньшую вероятность этого заболевания.
Клиническая оценка вероятности ТЭЛА
За последние несколько лет были предложены несколько шкал для клинической оценки вероятности ТЭЛА. Чаще всего используют Канадскую шкалу Wells, верифицированную результатами специальных методов диагностики ТЭЛА, которая предусматривает выделение как трех, так и двух степеней вероятности этого диагноза. В Европе используют также модифицированную Женевскую шкалу. Она включает в себя простые признаки, базирующиеся только на данных клинического исследования, и стандартизированные. Информативность этой шкалы также хорошо доказана, хотя она была предметом меньшего количества исследований, чем шкала Wells (табл. 4).
Таблица 4. Модифицированная Женевская шкала и шкала Wells
|
Женевская шкала |
||
|
Признак |
Балл |
|
|
Предрасполагающие факторы |
||
|
Возраст >65 лет |
1 |
|
|
ТГВ или ТЭЛА в анамнезе |
3 |
|
|
Хирургическое вмешательство или переломы в предыдущий месяц |
2 |
|
|
Активное злокачественное новообразование |
2 |
|
|
Симптомы |
||
|
Односторонняя боль в нижней конечности |
3 |
|
|
Кровохаркание |
2 |
|
|
Клинические признаки |
||
|
ЧСС 75–94 уд. за 1 минуту |
3 |
|
|
ЧСС ≥95 уд. за 1 минуту |
5 |
|
|
Боль по ходу глубоких вен нижней конечности при пальпации или односторонний отек |
4 |
|
|
Клиническая вероятность |
||
|
||
|
Шкала Wells |
||
|
Признак |
Балл |
|
|
Предрасполагающие факторы |
||
|
ТГВ или ТЭЛА в анамнезе |
1,5 |
|
|
Недавнее хирургическое вмешательство или иммобилизация |
1,5 |
|
|
Рак |
1 |
|
|
Симптомы |
||
|
Кровохаркание |
1 |
|
|
Клинические признаки |
||
|
ЧСС >100 уд. за 1 минуту |
1,5 |
|
|
Клинические признаки ТГВ |
3 |
|
|
Клиническая оценка |
||
|
Альтернативный диагноз менее вероятен, чем ТЭЛА |
3 |
|
|
Клиническая вероятность (3 категории): |
||
|
||
|
Клиническая вероятность (2 категории): |
||
|
||
Для обеих шкал у больных с низкой вероятностью ТЭЛА ее частота составляет около 10%, с умеренной — 30%, с высокой — 65%.
Таким образом, клиническая оценка — как субъективная, так и с использованием специальных шкал — позволяет отнести каждого пациента в одну из категорий вероятности ТЭЛА, которые соответствуют большей или меньшей распространенности заболевания.
Лабораторная диагностика: определение D-димера
Диагностическая значимость неоднозначна. Чаще рекомендуется использовать для исключения ТЭЛА у пациентов с низкой или умеренной вероятностью ТЭЛА. Отрицательный результат определения содержания D-димера в плазме крови с использованием высокочувствительных методов надежно исключает ТЭЛА у больных с низкой или умеренной вероятностью этого заболевания по данным клинической оценки, в то время как при использовании тестов с умеренной чувствительностью ТЭЛА можно исключить только у больных с низкой вероятностью ТЭЛА.
Рекомендуемые методы аппаратной диагностики
Компрессионная ультрасонография и КТ-венография
У 90% пациентов источником ТЭЛА служит ТГВ нижних конечностей. В настоящее время компрессионная венозная ультрасонография (КУС) нижних конечностей вытеснила венографию при диагностике ТГВ. Для диагностики ТГВ проксимальной локализации КУС имеет чувствительность выше 90% и специфичность около 95%.
В последнее время простым методом диагностики ТГВ у больных с подозрением на ТЭЛА была признана венография путем КТ, так как ее можно проводить одновременно с КТ-ангиографией грудной клетки с использованием только одной внутривенной инъекции контрастного вещества. К сожалению, выявить проксимальный ТГВ у больных с ТЭЛА с помощью КУС удается примерно у 20% пациентов. КУС можно использовать как резервную процедуру для уменьшения риска ложноотрицательного результата при однодетекторной КТ или при положительном результате, чтобы избежать проведения КТ при противопоказаниях к введению контрастного вещества и/или ионизирующему облучению. Одновременное использование КТ-ангиографии (венографии и КТ) не имеет существенных преимуществ и сопряжено с увеличением дозы ионизирующего облучения.
Вентиляционно-перфузионная сцинтиграфия
Вентиляционно-перфузионная сцинтиграфия (ВПС) легких — информативный метод диагностики ТЭЛА. Основной принцип исследования основан на внутривенной инъекции макрочастиц альбумина, меченных технецием-99 (99Tc), которые блокируют небольшую часть легочных капилляров и, таким образом, позволяют оценить перфузию легких. Цель дополнительного исследования вентиляции — увеличить специфичность метода путем документирования отсутствия в очагах гипоперфузии зон гиповентиляции (несоответствие вентиляции и перфузии). Лучевая нагрузка при таком исследовании в 255 раз меньше, чем при СКТ.
Анализ результатов исследования PIOPED II подтвердил информативность заключения о высокой вероятности ТЭЛА по данным ВПС и нормального результата для ее исключения. Ограничением метода является высокая частота результатов перфузионной сцинтиграфии, описываемых как «не имеющие диагностического значения» (умеренная вероятность ТЭЛА), потому что они указывают на необходимость в дальнейшем диагностическом поиске. Для получения точного результата предлагают учитывать вероятность ТЭЛА по данным клинической оценки и результаты однофотонной эмиссионной КТ (SPECT). Таким образом, отсутствие изменений при перфузионном сканировании позволяет исключить ТЭЛА с относительно высокой надежностью. Такой же вывод целесообразно делать при отсутствии диагностически значимых изменений при ВПС и низкой вероятности ТЭЛА при клинической оценке. Данных ВПС о высокой вероятности ТЭЛА в большинстве случаев достаточно для постановки диагноза, однако у отдельных больных, прежде всего с низкой вероятностью этого заболевания по данным клинической оценки, целесообразно продолжить обследование. Это же рекомендуют при других сочетаниях варианта заключения по ВПС и клинической вероятности ТЭЛА.
КТ-ангиография
Значение КТ-ангиографии для диагностики ТЭЛА после усовершенствования технологий претерпело существенные изменения. По данным нескольких исследований у больных с возможной ТЭЛА для однодетекторной спиральной КТ чувствительность составляет около 70%, специфичность — 90%. После появления мультиспиральной КТ (МСКТ) с высоким разрешением и качеством артериального контрастирования КТ-ангиография стала методом выбора для визуализации легочного кровотока при подозрении ТЭЛА в рутинной клинической практике. По данным исследования PIOPED II чувствительность МСКТ при диагностике ТЭЛА составила 83%, специфичность — 96%. У больных с низкой или средней клинической вероятностью ТЭЛА по шкале Wells отрицательный результат КТ имел высокую прогностическую ценность относительно отсутствия ТЭЛА (96% и 89% соответственно), тогда как у пациентов с высокой клинической вероятностью эти показатели оказались значительно ниже — около 60%. С другой стороны, у больных со средней или высокой клинической вероятностью прогностическая ценность положительного результата КТ была высокой (92–96%) и значительно ниже (58%) — с низкой вероятностью ТЭЛА. Поэтому клиницисты должны с большой осторожностью подходить к диагностике ТЭЛА в случаях расхождения клинической оценки вероятности ТЭЛА и результатов МСКТ, которых, к счастью, относительно немного. Таким образом, визуализация тромбов в проксимальных ветвях ЛА, включая те, которые обеспечивают кровью сегменты легких, с помощью одно и многоспиральной КТ является достаточной для диагностики ТЭЛА в большинстве случаев. По данным клинической оценки у больных с невысокой вероятностью ТЭЛА исключить данное заболевание позволяет сочетание отрицательного результата односпиральной КТ и КУС или отрицательный результат одной МСКТ. Целесообразность дальнейшего обследования у редких пациентов с отрицательным результатом МСКТ в сочетании с высокой вероятностью ТЭЛА, по данным клинической оценки, не определена.
Ангиография легких
Диагностические критерии острой ТЭЛА установлены почти 40 лет тому назад и включают прямые признаки тромба в виде дефекта наполнения или ампутации ветви легочной артерии. Ангиография позволяет визуализировать тромбы размером до 1–2 мм, однако их оценка в столь мелких ветвях ЛА не лишена субъективизма. Другие косвенные признаки ТЭЛА включают наличие медленного тока контраста, регионарную гипоперфузию и задержку или уменьшение кровотока в легочных венах, однако их диагностическая ценность точно не определена. Ангиопульмонография — инвазивная процедура и в силу этого не лишена риска. Летальность составляет 0,2%, преимущественно — за счет крайне тяжелых больных с нестабильной гемодинамикой или острой дыхательной недостаточностью. Хотя ангиопульмонография является золотым стандартом для диагностики или исключения ТЭЛА, этот метод сейчас редко используют, потому что аналогичную информацию позволяет получить неинвазивная КТ-ангиография. Правожелудочковая вентрикулография в целях оценки дисфункции ПЖ при острой ТЭЛА представляет сложности для интерпретации. Сейчас в повседневной практике ее заменили ЭхоКГ и определение биомаркеров. Кроме того, тромболизис у больных с ТЭЛА, диагностированной с использованием стандартной ангиопульмонографии, сопряжен с повышением риска местных геморрагических осложнений. Ангиография легких является надежным, но инвазивным исследованием. Ее используют лишь тогда, когда неинвазивные методы исследования дают неоднозначные результаты.
Эхокардиография
Дилатация ПЖ наблюдается как минимум у 25% больных с ТЭЛА, и ее обнаружение с помощью ЭхоКГ или КТ полезно для стратификации риска. В различных исследованиях для диагностики ТЭЛА использовали разные ЭхоКГ-критерии, однако все они основывались на скорости потока крови через трехстворчатый клапан и размерах ПЖ. Их чувствительность составляет около 60–70%, поэтому негативный результат не дает возможности исключить ТЭЛА. С другой стороны, признаки перегрузки или дисфункции ПЖ могут быть также проявлением сопутствующего заболевания сердца или легких при отсутствии острой ТЭЛА. ЭхоКГ-исследование не рекомендовано как часть диагностической стратегии при подозрении на ТЭЛА у больных с нормальным АД и стабильной гемодинамикой. У больных с подозрением на ТЭЛА высокого риска с шоком или артериальной гипотензией отсутствие ЭхоКГ-признаков перегрузки ПЖ или его дисфункции практически исключает ТЭЛА как причину гемодинамической нестабильности. ЭхоКГ может помочь в дифференциальной диагностике причины шока, позволяя выявлять тампонаду сердца, острую дисфункцию клапанов, острый инфаркт миокарда или гиповолемию. У отдельных больных можно дополнительно попытаться визуализировать эмболы в главных ЛА посредством чреспищеводной ЭхоКГ, выявление которых позволяет подтвердить диагноз. У 4–18% больных с острой ТЭЛА при чреспищеводной ЭхоКГ определяются также тромбы в правых отделах сердца, которые требуют соответствующего лечения.
Заключение: ЭхоКГ особенно полезна в принятии решения для безотлагательного определения лечебной тактики у больных с подозрением на ТЭЛА, которые находятся в критическом состоянии. У пациентов с шоком или артериальной гипотензией отсутствие ЭхоКГ-признаков перегрузки или дисфункции ПЖ практически исключает ТЭЛА как причину гемодинамической нестабильности. Главная роль ЭхоКГ при ТЭЛА невысокого риска — уточнение оценки прогноза между категориями промежуточного или низкого риска.
Диагностическая стратегия
Первоочередное разграничение предположительной ТЭЛА высокого и невысокого риска имеет важное значение, поскольку в этих случаях диагностическая стратегия отличается. Ангиопульмонография как золотой стандарт диагностики ТЭЛА является инвазивным и дорогостоящим методом, поэтому важно минимизировать ее использование путем оптимального применения неинвазивных методов диагностики, включая клиническую оценку, измерение плазменного уровня D-димера, КУС нижних конечностей, ВПС легких и КТ. Самые простые диагностические алгоритмы диагностики ТЭЛА представлены на рисунках 1 и 2. В таблице 5 и 6 приведена информация, необходимая для создания в специальных случаях альтернативных алгоритмов на основании данных доказательной медицины и рекомендации по диагностике ТЭЛА.
Таблица 5. Критерии диагностики ЛЭ у пациентов без шока и артериальной гипотензии (ЛЭ невысокого риска) в зависимости от вероятности ЛЭ по данным клинического обследования
|
Диагностический критерий |
Вероятность ЛЭ |
||
|
низкая |
средняя |
высокая |
|
|
Исключающий ЛЭ |
|||
|
Отрицательный результат ангиопульмонографии |
+ |
+ |
+ |
|
D-димер |
|||
|
Отрицательный результат при использовании высокочувствительного метода |
+ |
+ |
– |
|
Отрицательный результат при использовании метода со средней чувствительностью |
+ |
– |
– |
|
ВПС |
|||
|
Отрицательный результат |
+ |
+ |
+ |
|
Неопределенный результат |
+ |
– |
– |
|
Неопределенный или отрицательный результат проксимальной КУС |
+ |
+ |
± |
|
КТ-ангиография легких |
|||
|
Отрицательные результаты однодетекторной КТ и проксимальной КУС |
+ |
+ |
± |
|
Отрицательный результат МСКТ |
+ |
+ |
± |
|
Подтверждающий ЛЭ |
|||
|
Визуализация ЛЭ при ангиопульмонографии |
+ |
+ |
+ |
|
Высокая вероятность положительного результата ВПС |
± |
+ |
+ |
|
Проксимальный ТГВ при КУС |
+ |
+ |
+ |
|
КТ-ангиография легких |
|||
|
Визуализация ЛЭ при одно- или МСКТ (как минимум сегментарной) |
± |
+ |
+ |
|
Субсегментарная ЛЭ при одно- или МСКТ |
± |
± |
± |
Примечание: «+» — достаточно надежный критерий (дальнейшее обследование не нужно); «–» — недостаточно надежный критерий (дальнейшее обследование необходимо); «±» — спорный критерий (необходимо рассмотреть вопрос о целесообразности дообследования).
Подозрение на ТЭЛА высокого риска
Вероятность ТЭЛА у больных с шоком или артериальной гипотензией обычно высокая, и дифференциальный диагноз включает кардиогенный шок, острую клапанную дисфункцию, тампонаду сердца и расслоение аорты. Поэтому самый информативный начальный метод исследования в этой ситуации — это ЭхоКГ, которая обычно выявляет непрямые признаки острой легочной гипертензии и правожелудочковой перегрузки. Иногда при трансторакальной ЭхоКГ могут визуализироваться тромбы в правых отделах сердца. При чреспищеводной ЭхоКГ можно непосредственно визуализировать тромб в ЛА. Однако у больных с выраженной нестабильностью гемодинамики, а также когда другие методы исследования недоступны, диагноз ТЭЛА можно поставить только на основании совокупности косвенных ЭхоКГ — признаков (рис. 1). Если состояние пациента удается стабилизировать в ходе лечения — необходимо подтверждать диагноз. Из-за большого количества тромбов в сосудах легких КТ обычно подтверждает диагноз. Ангиопульмонографии нужно избегать, так как у пациентов с нестабильным состоянием она сопряжена с повышенным риском летального исхода и увеличивает риск кровотечения после проведения тромболизиса.
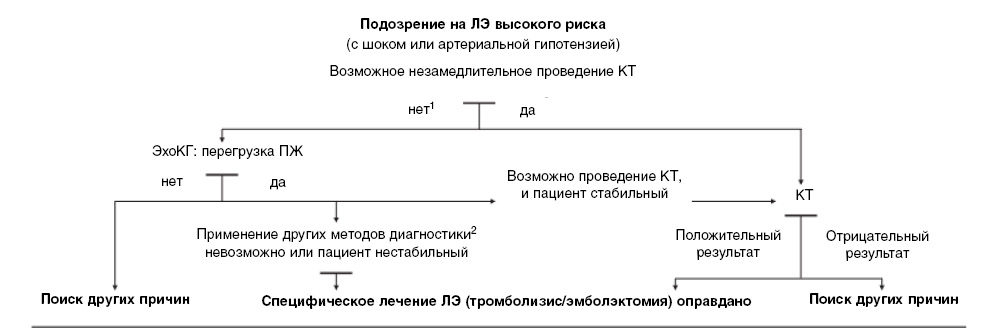 Рис. 1. Диагностический алгоритм для пациентов с подозрением на ЛЭ высокого риска,
Рис. 1. Диагностический алгоритм для пациентов с подозрением на ЛЭ высокого риска,т.е. в состоянии шока или артериальной гипотензии
Примечание: 1 — в том числе из-за тяжести состояния больного; 2 — чреспищеводная ЭхоКГ для выявления тромбов в ветвях легочной артерии, КУС для диагностики.
Таблица 6. Рекомендации по диагностике ТЭЛА
|
Рекомендации |
Класс |
Уровень |
|
Подозрение на ТЭЛА высокого риска |
||
|
При ТЭЛА высокого риска, т.е. при шоке или артериальной гипотензии, рекомендуют безотлагательно провести КТ или ЭхоКГ у постели больного (в зависимости от доступности обоих методов и особенностей в каждом конкретном случае) |
І |
С |
|
Подозрение на ТЭЛА невысокого риска |
||
|
Диагностическая стратегия должна быть основана на оценке вероятности либо по клиническим данным, либо эмпирической, либо с помощью специальных шкал |
I |
A |
|
У пациентов реанимационных отделений для уменьшения потребности в проведении инструментальных методов рекомендуют определять D-димер в плазме с помощью высокочувствительного метода |
I |
A |
|
КУС нижних конечностей в поисках ТГВ может быть полезна у отдельных больных с подозрением на ТЭЛА (во избежание потребности в дальнейших исследованиях) в случае ее положительного результата |
IIb |
B |
|
Систематическое использование ЭхоКГ для диагностики ТЭЛА у гемодинамически стабильных нормотензивных пациентов не рекомендовано |
III |
C |
|
Ангиопульмонография может быть полезной в случаях расхождения между клинической оценкой и результатами неинвазивных визуализирующих исследований |
IIa |
C |
|
Подозрение на ТЭЛА невысокого риска (низкая клиническая вероятность) |
||
|
Нормальный уровень D-димера, по данным высоко- или умеренно чувствительных методов его определения, исключает ТЭЛА |
I |
А |
|
Отрицательный результат ВПС легких исключает ТЭЛА |
I |
А |
|
Неинформативный результат (низкая или промежуточная вероятность) ВПС может исключать ТЭЛА, особенно в сочетании с отрицательным результатом проксимальной КУС |
IIa |
В |
|
Отрицательный результат МСКТ исключает ТЭЛА |
I |
А |
|
Отрицательный результат односпиральной КТ исключает ТЭЛА только тогда, когда сочетается с отрицательным результатом проксимальной КУС |
I |
А |
|
Положительный результат ВПС (высокая вероятность ТЭЛА) может подтверждать ТЭЛА, но у отдельных больных может быть полезным дообследование |
І |
А |
|
Проксимальный ТГВ, по данным КУС, подтверждает диагноз ТЭЛА |
IIa |
В |
|
При дистальном ТГВ, по данным КУС, необходимо дообследование для подтверждения ТЭЛА |
IIb |
В |
|
Односпиральная КТ или МСКТ, показывающие сегментарный или более проксимальный тромбоз, подтверждает диагноз ТЭЛА |
І |
А |
|
Если при односпиральной КТ или МСКТ виден только субсегментарный тромбоз, для подтверждения диагноза ТЭЛА необходимо дообследование |
ІІа |
В |
|
Подозрение на ТЭЛА невысокого риска (умеренная клиническая вероятность) |
||
|
Нормальный уровень D-димера, полученный при высокочувствительном методе исследования, исключает ТЭЛА |
I |
A |
|
При нормальном уровне D-димера, полученном при менее чувствительном методе исследования, необходимо дообследование |
IIa |
B |
|
Нормальная ВПС легких исключает ТЭЛА |
I |
A |
|
В случаях неинформативности ВПС рекомендуют дообследование для исключения или подтверждения ТЭЛА |
I |
B |
|
Отрицательный результат МСКТ исключает ТЭЛА |
I |
A |
|
Отрицательный результат односпиральной КТ исключает ТЭЛА только тогда, когда сочетается с отрицательным результатом проксимальной КУС |
I |
A |
|
Высокая вероятность положительного результата ВПС легких подтверждает ТЭЛА |
I |
A |
|
Проксимальный ТГВ при КУС подтверждает ТЭЛА |
I |
B |
|
Если при КУС выявлен только дистальный ТГВ, необходимо дообследование |
IIa |
B |
|
Сегментарный или более проксимальный тромбоз ЛА при односпиральной КТ или МСКТ подтверждает ТЭЛА |
I |
A |
|
В случае выявления субсегментарных тромбов для подтверждения ТЭЛА может потребоваться дообследование |
IIb |
B |
|
Подозрение на ТЭЛА невысокого риска (высокая клиническая вероятность) |
||
|
Определение D-димера не рекомендуется, так как отрицательный результат не исключает ТЭЛА даже при использовании высокочувствительных методов исследования |
III |
C |
|
У отдельных больных с отрицательным результатом КТ для исключения ТЭЛА может потребоваться дообследование |
IIa |
B |
|
Положительный результат ВПС легких с высокой вероятностью ТЭЛА подтверждает этот диагноз |
I |
A |
|
Проксимальный ТГВ при КУС подтверждает ТЭЛА |
I |
B |
|
Если при КУС выявлен только дистальный ТГВ, необходимо дообследование |
IIb |
B |
|
Сегментарный или более проксимальный тромбоз ЛА при односпиральной КТ или МСКТ подтверждает ТЭЛА |
I |
A |
|
В случае выявления субсегментарных тромбов для подтверждения ТЭЛА может потребоваться дообследование |
IIb |
B |
Подозрение на ТЭЛА невысокого риска
Стратегия, основанная на КТ-ангиографии. КТ-ангиография стала главным методом визуализации при диагностике предполагаемой ТЭЛА. ВПС сохраняет свое значение, но выполняют ее реже из-за высокой частоты неопределенных результатов. Поскольку у большинства пациентов с подозрением на ТЭЛА этот диагноз не подтверждается, КТ не должна быть методом исследования первой линии у больных, госпитализированных в приемное отделение.
Таблица 7. Клинические предикторы 30-суточной летальности при острой ТЭЛА
|
Показатель |
Балл |
|
Возраст |
1/год |
|
Мужской пол |
10 |
|
Рак |
30 |
|
Сердечная недостаточность |
10 |
|
Хронические заболевания легких |
10 |
|
ЧСС >110 уд. за 1 минуту |
20 |
|
САД <100 мм рт.ст. |
30 |
|
ЧДД ≥30 в 1 минуту |
20 |
|
Температура тела <36°С |
20 |
|
Нарушение ориентации, заторможенность, ступор, кома |
60 |
|
SaO2 <90% |
20 |
|
Категории риска (30 — суточная общая летальность):
|
|
Определение плазменного D-димера в комбинации с оценкой вероятности ТЭЛА, по данным клинического обследования, является логическим первым шагом и позволяет исключить ТЭЛА примерно у 30% пациентов, у которых без лечения риск тромбоэмболий в течение 3 месяцев ниже 1%. D-димер не должны измерять у больных с высокой клинической вероятностью, в том числе у госпитализированных, из-за низкой прогностической ценности негативного результата. В большинстве центров МСКТ является следующим шагом у больных с повышенным уровнем D-димера и методом исследования первого выбора — у больных с высокой клинической вероятностью ТЭЛА (рис. 2).
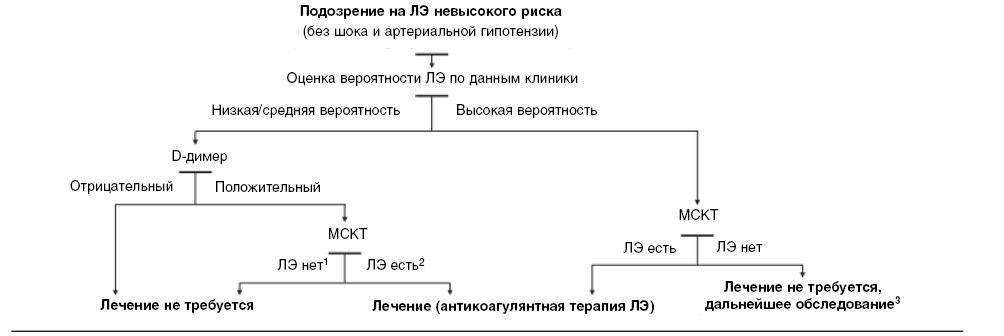 Рис. 2. Диагностический алгоритм для пациентов с подозрением на ЛЭ невысокого риска, т.е. без шока или артериальной гипотензии
Рис. 2. Диагностический алгоритм для пациентов с подозрением на ЛЭ невысокого риска, т.е. без шока или артериальной гипотензииПримечание: при использовании метода определения D-димера, обладающего средней чувствительностью, этот этап алгоритма следует применять только у пациентов с низкой вероятностью ЛЭ при трех градациях оценки вероятности (низкая, средняя, высокая) или при малой вероятности ЛЭ при двух градациях ее оценки, в то время как чувствительный метод исследования можно использовать у пациентов как с низкой, так и с промежуточной вероятностью ЛЭ. При подозрении на ЛЭ у стационарных пациентов определение плазменного D-димера следует использовать ограничено. 1 — КТ подтверждает ЛЭ, если сам проксимальный тромб находится, как минимум, в сегментарной ветви легочной артерии; 2 — если односпиральная КТ негативная, для окончательного исключения ЛЭ требуется негативный результат проксимальной КУС нижних конечностей; 3 — если МСКТ негативная у пациентов с высокой клинической вероятностью, перед отказом от применения специфической для ЛЭ терапии необходимо дообследование.
Результат одно- или мультиспиральной КТ является убедительным для диагноза ТЭЛА в том случае, когда визуализируется тромб, как минимум — на сегментарном уровне легочного артериального дерева. Отрицательный результат МСКТ надежно исключает ТЭЛА.
Из-за более низкой прогностической ценности отрицательного результата односпиральную КТ следует сочетать с венозной КУС для исключения ТЭЛА. Описаны случаи ложноотрицательных результатов односпиральной КТ и МСКТ у больных с высокой клинической вероятностью ТЭЛА. Однако они бывают редко, и 3-месячный тромбоэмболический риск у таких пациентов низкий. Поэтому необходимость выполнения дальнейшего обследования у таких пациентов остается спорной.
Стратегия оценки прогноза
Параллельно с верификацией диагноза ТЭЛА для стратификации риска и определения оптимальной тактики лечения необходимо оценивать прогноз (табл. 8).
Таблица 8. Оценка прогноза
|
Рекомендации |
Класс |
Уровень |
|
Начальную стратификацию риска при подозрении и/или подтверждении ТЭЛА, основанную на наличии шока и артериальной гипотензии, рекомендуют для разделения пациентов с высокой и невысокой ранней летальностью, связанной с ТЭЛА |
І |
В |
|
У пациентов с ТЭЛА невысокого риска дальнейшая стратификация на подгруппы промежуточного или низкого риска основана на наличии признаков дисфункции правого желудочка по данным методов визуализации или специального лабораторного исследования и маркеров повреждения миокарда |
ІІа |
В |
Стратификацию риска ТЭЛА начинают с оценки гемодинамического статуса, по данным клинического обследования, и продолжают с использованием результатов лабораторных исследований (табл. 2).
ТЭЛА высокого риска диагностируют при наличии шока или длительной артериальной гипотензии (САД <90 мм рт ст. или снижение давления >40 мм рт.ст. в течение >15 минут, если это не вызвано острой аритмией, гиповолемией или сепсисом), в этом случае необходимо немедленно начинать жизнеспасающее специфическое лечение.
У больных ТЭЛА с нормальным АД наличие маркеров дисфункции ПЖ и/или миокардиального повреждения указывает на умеренный или промежуточный риск ТЭЛА. Вероятно, что больные с промежуточным риском, у которых оба маркера дисфункции и повреждения положительные, имеют более высокий риск, чем больные, имеющие только 1 из 2 маркеров.
Пациенты со стабильной гемодинамикой без признаков дисфункции ПЖ или миокардиального повреждения имеют ТЭЛА низкого риска. Для зачисления пациентов с ТЭЛА в две последние группы необходимо определить, как минимум, один из признаков дисфункции миокарда ПЖ и как минимум — один из маркеров повреждения миокарда.
Основные направления интенсивной терапии острой фазы ТЭЛА состоят в следующих стратегиях:
- гемодинамическая и респираторная поддержка;
- антикоагулянты;
- тромболизис;
- хирургическая эмболэктомия.
Лечение ТЭЛА у пациентов высокого риска
1. Немедленно должна быть начата антикоагулянтная терапия нефракционированным гепарином (I, A).
2. Для профилактики дальнейшего прогрессирования правожелудочковой недостаточности необходимо устранить системную гипотензию. С этой целью рекомендуются вазопрессивные препараты (I, C). У пациентов с низким сердечным выбросом и нормальным АД могут быть использованы добутамин и допамин (IIa, B).
3. Не рекомендована агрессивная инфузионная терапия (III, B).
4. Пациентам с гипоксемией необходимо проведение оксигенотерапии (I, C).
5. У пациентов высокого риска с ТЭЛА, сопровождающейся кардиогенным шоком и/или артериальной гипотензией, показана тромболитическая терапия (I, A).
6. Если тромболизис абсолютно противопоказан или оказался неэффективным, альтернативным методом реперфузии является хирургическая эмболэктомия (I, C).
7. Если тромболизис абсолютно противопоказан или оказался неэффективным, в качестве альтернативного метода реперфузии может рассматриваться также чрескожная катетерная эмболэктомия или фрагментация тромба (IIb, C).
Лечение ТЭЛА у пациентов невысокого (умеренного или низкого) риска
1. Антикоагулянтная терапия должна быть начата немедленно у пациентов с высокой или средней вероятностью ТЭЛА еще в процессе диагностики, не дожидаясь окончательного подтверждения диагноза (I, С). Для большинства пациентов в качестве предпочтительного антикоагулянта рекомендуется препарат группы низкомолекулярных гепаринов или фондапаринукс (I, A), однако у больных с высоким риском геморрагических осложнений, а также в случае наличия тяжелой почечной дисфункции для стартовой антикоагулянтной терапии показан нефракционированный гепарин с удержанием активированного частичного тромбопластинового времени (АЧТВ) в пределах значений, в 1,5–2,5 раза превышающих нормальный показатель (I, С). Антикоагулянтная терапия нефракционированным гепарином, низкомолекулярным гепарином или фондапаринуксом должна продолжаться не менее 5 дней и может быть заменена на антагонист витамина К только после достижения целевого международного нормализованного отношения (МНО) и удержания его на протяжении как минимум 2 дней (I, С).
2. Рутинное использование тромболитической терапии у больных невысокого риска не рекомендовано, но ее целесообразность может быть рассмотрена у некоторых пациентов с умеренным риском (IIb, B). Тромболитическая терапия не показана у пациентов с низким риском (III, B).
Тромболитическая терапия ТЭЛА
1. Стрептокиназа:
а) обычная схема — нагрузочная доза 250 тыс. МЕ (на протяжении 30 минут), далее 100 тыс. МЕ в час на протяжении 12–24 часов;
б) ускоренная схема — 1,5 млн МЕ на протяжении 2 часов.
2. Урокиназа:
а) обычная схема — нагрузочная доза 4400 МЕ/кг массы тела (на протяжении 10 минут), далее 4400 МЕ/кг массы тела в час на протяжении 12–24 часов;
б) ускоренная схема — 3 млн МЕ на протяжении 2 часов.
3. rtPA (альтеплаза):
а) 100 мг на протяжении 2 часов;
б) ускоренная схема — 0,6 мг/кг массы тела на протяжении 15 минут (максимальная доза 50 мг).
Таким образом, суммируя рекомендации по диагностике, прогнозированию риска, лечению ТЭЛА, мы с сожалением должны констатировать, что материально-техническая база большинства лечебных учреждений не позволяет проводить и диагностику, и лечение ТЭЛА в полном предлагающемся объеме. Однако для демонстрации имеющихся возможностей мы хотели бы представить вниманию клинический случай лечения тромбоэмболии легочной артерии.
Клинический случай
Больной З., 64 года, поступил в отделение интенсивной терапии кардиологического профиля КУ «Днепродзержинская городская больница скорой медицинской помощи» ДОС с жалобами на одышку в покое, усиливающуюся при малейшей физической нагрузке, общую резкую слабость.
Из анамнеза — считает себя больным в течение 6 дней, когда после физической нагрузки появилась внезапная одышка, холодный липкий пот, тахикардия. В день поступления в стационар потерял сознание, что сопровождалось чувством нехватки воздуха, учащенным сердцебиением, потливостью, бледностью кожного покрова.
Длительно страдает гипертонической болезнью, гипотензивные препараты принимает нерегулярно. За 14 дней до момента заболевания у больного возникла боль в икроножной мышце слева, боль усиливалась при пальпации и ходьбе, усилился венозный рисунок — диагностирован тромбофлебит глубоких вен левой нижней конечности.
При объективном осмотре — состояние крайне тяжелое. Больной в ясном сознании. Кожный покров бледно-пепельный, акроционоз. Холодный, липкий пот. Грудная клетка правильной формы, перкуторно над легкими — легочной звук, аускультативно — дыхание везикулярное, хрипов нет. ЧДД — 24 в минуту. Область сердца без патологических изменений, при перкуссии — расширение левой границы сердца на 0,5 см кнаружи от левой среднеключичной линии, аускультативно тоны сердца приглушены, ритмичны. ЧСС — 100 уд. за 1 минуту, АД — 100/60 мм рт.ст.
Язык влажный. Живот при пальпации мягкий, безболезненный. Печень у края реберной дуги. Селезенка не увеличена. Симптом Пастернацкого отрицательный с обеих сторон. Физиологические отправления не нарушены.
Лабораторные исследования: в общем анализе крови при поступлении лейкоциты — 8,1 Г/л, палочкоядерные — 12%. D-димер — 1,5 мг/мл.
Инструментальные методы исследования. ЭКГ — синусовая тахикардия, ЧСС — 100 уд. за 1 минуту. Регистрируется Q-III S-I, отрицательный зубец Т в III, AVF, V1–4, признаки перегрузки правых отделов сердца.
Рентгенограмма органов грудной клетки: выявлено высокое стояние купола диафрагмы. Расширение тени сердца вправо, сглаженность талии сердца.
Эхокардиография — выявлены расширение и гипокинез правого желудочка, соотношение объемов правого и левого желудочков — изменения в пользу правого желудочка, проксимальная часть легочной артерии расширена.
Лечение: тромболитическая терапия стрептокиназой 1 500 000 МЕ на протяжении 2 часов (ускоренная схема). В качестве доступа использовалась периферическая вена. После тромболитической терапии налажена инфузия гепарина в дозе 30 000 ЕД в течение 24 часов. Антитромбоцитарные препараты — аспирин кардио в дозе 300 мг. Через 17 часов с момента поступления в стационар больной транспортирован в Институт сердца г. Киева, где в последующем пациенту успешно проведено оперативное лечение с установкой кава-фильтров.
Выводы
Раннее проведение тромболитической терапии с последующей инфузией антикоагулянтов улучшает прогноз заболевания и создает условия для успешности оперативного лечения.
Список литературы
1. Anderson F.A. Jr, Spencer F.A. Risk factors for venous thromboembolism // Circulation. – 2003. – Vol. 107 (23 Suppl. 1). – P. I9–16.
2. Becattini C., Vedovati M.C., Agnelli G. Prognostic value of troponins in acute pulmonary embolism: a meta-analysis // Circulation. – 2007. – Vol. 116. – P. 427–433.
3. British Thoracic Society guidelines for the management of suspected acute pulmonary embolism // Thorax. – 2003. – Vol. 58. – P. 470–483.
4. Geibel A., Zehender M., Kasper W., Olschewski M. et al. Prognostic value of the ECG on admission in patients with acute major pulmonary embolism // Eur. Respir. J. – 2005. – Vol. 25. – P. 843–848.
5. Goodman L.R., Stein P.D., Matta F. et al. CT venography and compression sonography are diagnostically equivalent: data from PIOPED II // AJR Am. J. Roentgenol. – 2007. – Vol. 189. – P. 1071–1076.
6. Guidelines on diagnosis and management of acute pulmonary embolism. Task Force on Pulmonary Embolism, European Society of Cardiology // Eur. Heart J. – 2014.
7. Guidelines on diagnosis and management of acute pulmonary embolism. Task Force on Pulmonary Embolism, European Society of Cardiology // Eur. Heart J. – 2000. – Vol. 21. – P. 1301–1336.
8. Kucher N., Goldhaber S.Z. Management of massive pulmonary embolism // Circulation. – 2005. – Vol. 112. – P. e28–e32.
9. Le Gal G., Righini M., Roy P.M. et al. Prediction of pulmonary embolism in the emergency department: the revised Geneva score // Ann. Intern. Med. – 2006. – Vol.144. – P. 165–171.
10. Le Gal G., Righini M., Sanchez O. et al. A positive compression ultrasonography of the lower limb veins is highly predictive of pulmonary embolism on computed tomography in suspected patients // Thromb. Haemost. – 2006. – Vol. 95. – P. 963–966.
11. Musset D., Parent F., Meyer G. et al. Diagnostic strategy for patients with suspected pulmonary embolism: a prospective multicentre outcome study // Lancet. – 2002. – Vol. 360. – P. 1914–1920.
12. Roy P.M., Meyer G., Vielle B. et al. Appropriateness of diagnostic management and outcomes of suspected pulmonary embolism // Ann. Intern. Med. – 2006. – Vol. 144. – P. 157–164.
13. Stein P.D., Fowler S.E., Goodman L.R. et al. Multidetector computed tomography for acute pulmonary embolism // N. Engl. J. Med. – 2006. – Vol. 354. – P. 2317–2327.
14. Ten Wolde M., Hagen P.J., MacGillavry M.R. et al. Non-invasive diagnostic work-up of patients with clinically suspected pulmonary embolism: results of a management study // J. Thromb. Haemost. – 2004. – Vol. 2. – P. 1110–1117.
15. van Belle A., Buller H.R., Huisman M.V. et al. Effectiveness of managing suspected pulmonary embolism using an algorithm combining clinical probability, D-dimer testing, and computed tomography // JAMA. – 2006. – Vol. 295. – P. 172–179.
16. Wells P.S., Anderson D.R., Rodger M. et al. Derivation of a simple clinical model to categorize patients probability of pulmonary embolism: increasing the models utility with the SimpliRED D-dimer // Thromb. Haemost. – 2000. – Vol. 83. – P. 416–420.
17. Wolfe M.W., Skibo L.K., Goldhaber S.Z. Pulmonary embolic disease: diagnosis, pathophysiologic aspects, and treatment with thrombolytic therapy // Curr. Probl. Cardiol. – 1993. – Vol. 18. – P. 587–633.


