9 липня, 2016
Основные принципы профилактики тромбоэмболических нарушений при беременности и в послеродовом периоде
Венозная тромбоэмболия (ВТЭ) включает в себя тромбоз глубоких вен и тромбоз легочной артерии, представляет собой одно из наиболее распространенных серьезных осложнений беременности и в настоящее время является ведущей причиной материнской заболеваемости и смертности в развивающихся странах мира. В последние два десятилетия появились новые данные, свидетельствующие о связи между ВТЭ и врожденными и приобретенными тромбофилиями, что, в свою очередь, осложняет проведение адекватной и доказательно обоснованной тромбопрофилактики.
Несмотря на все современные стратегии и методы профилактики сохраняется достаточно высокий уровень заболеваемости ВТЭ. Частота тромбоэмболии легочной артерии (ТЭЛА) у беременных с нелеченым тромбозом глубоких вен составляет 13-24%, смертность – 12-15%. При нелеченом тромбозе септических тазовых вен частота ТЭЛА достигает 33%.
В свою очередь, при своевременно и правильно назначенной терапии можно добиться снижения риска ТЭЛА до 0,7-4,5% и снижения риска материнской смертности до 0,7%.
Учитывая все вышеизложенное, необходимо ответить на несколько основных вопросов.
Почему в период беременности и в послеродовом периоде повышается риск тромбоэмболических осложнений?
Беременность и послеродовой период ассоциируются с повышенным риском развития ВТЭ – от 0,61 до 1,72 на 1000 родов. По сравнению с небеременными женщинами одного и того же возраста вероятность развития ВТЭ в 4-5 раз выше при беременности и после родов. Несмотря на различные данные, полученные в исследованиях, является очевидной связь между частотой ВТЭ и антенатальным и постнатальным периодом. Также следует отметить, что в послеродовом периоде частота ВТЭ повышается в 5 раз по сравнению с дородовым периодом.
Повышение риска развития ВТЭ во время гестации связано с тем, что во время беременности отмечаются все три элемента триады Вирхова: стаз, сосудистая травма и гиперкоагуляция.
Факторы, влияющие на повышение риска развития тромбоэмболии во время беременности:
- нарушения целостности сосудов таза (кесарево сечение);
- приобретенный дефицит антитромбина (нефротический синдром, преэклампсия);
- дисбаланс гормонов (синдром гиперстимуляции яичников, многоплодная беременность);
- тромбофилия;
- семейный анамнез ТЭ;
- возраст >35 лет;
- родов больше 3;
- ожирение;
- иммобилизация;
- курение;
- варикозная болезнь (флебиты);
- воспалительные заболевания кишечника (ВЗК);
- любое состояние, требующее введения постоянного катетера;
- повышение факторов свертывания (фибриноген, VII, VIII, IX, X);
- снижение протеина S;
- нарушение фибринолиза (плацента выделяет ингибиторы фибринолиза);
- венозный стаз и компрессия нижней полой вены.
Повышение внутрибрюшного давления и сдавление vena cava увеличенной маткой приводит к снижению скорости кровотока и повышению венозного давления в венах нижних конечностей. Кроме того, повышение концентрации циркулирующего в крови прогестерона наряду с усилением местного синтеза простациклинов и оксида азота приводит к увеличению емкости глубоких вен.
Описанные выше изменения вызывают относительное усиление венозного застоя, который нарастает с увеличением срока беременности. Кроме того, прослеживается тенденция к более выраженному застою в левой нижней конечности. Следует помнить, что снижение венозного тонуса в совокупности с поражением эндотелия и активация прокоагуляционной системы эндотелия могут сохраняться еще в течение 6 недель после родов.
Поражение эндотелия может произойти во время кесаревого сечения или в результате оказания оперативных манипуляций во время родов, также может ассоциироваться с такими осложнениями, как преэклампсия, в этиологии которой ведущая роль принадлежит эндотелиальной дисфункции. Наконец, даже физиологически протекающая беременность связана с прокоагуляционными изменениями системы гомеостаза. Активность большинства протромботических факторов возрастает, концентрация некоторых антикоагуляционных факторов снижается и одновременно снижается фибринолитическая активность.
Все вышеперечисленные изменения приводят к тому, что частота ВТЭ у женщин репродуктивного возраста возрастает с 1 случая на 10 000 в год до 1 на 1000 среди беременных и женщин после родов.
Как оценить риск тромбоэмболических осложнений при беременности и в послеродовом периоде?
 В августе 2014 г. в «Европейском кардиологическом журнале» (European Society of Cardiology) были опубликованы рекомендации по диагностике и ведению тромбоэмболии легочной артерии.
В августе 2014 г. в «Европейском кардиологическом журнале» (European Society of Cardiology) были опубликованы рекомендации по диагностике и ведению тромбоэмболии легочной артерии.
Кроме того, the Royal College of Obstetricians and Gynaecologists (RCOG), the American College of Obstetricians and Gynecologists (ACOG) опубликовали обновленные рекомендации по ВТЭ и беременности.
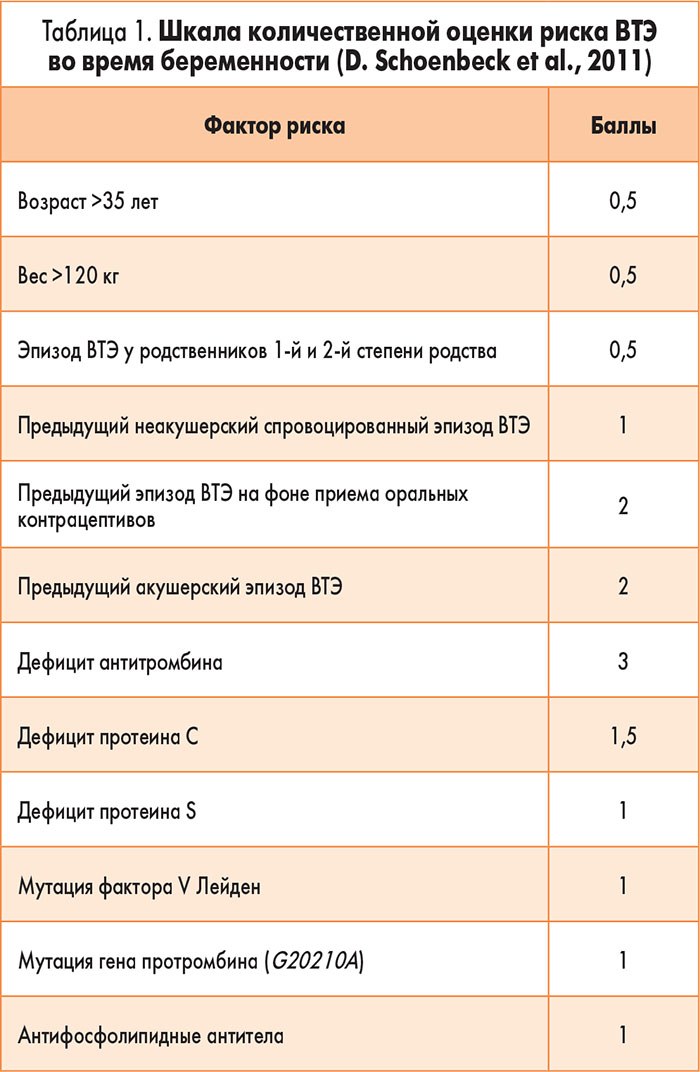
В 2011 г. D. Schoenbeck и соавт. разработали шкалу стратификации риска во время беременности.
<1 балла – без фармакологической тромбопрофилактики.
1-1,5 балла – применение низкомолекулярных гепаринов (НМГ) до 6 недель после родов.
2-2,5 балла – применение НМГ с 28-й недели беременности до 6-й недели после родов.
≥3 балла – применение НМГ в течение всей беременности и 6 недель после родов.
Особое значение стратификация риска и выделение наиболее значимых факторов, влияющих на увеличение риска ВТЭ, приобретают при наблюдении и родоразрешении беременных женщин, которые относятся к группе высокого перинатального риска.
К основным факторам риска в клинике экстрагенитальной патологии относят:
- тромбоз глубоких вен (ТГВ) в анамнезе;
- возраст >35 лет;
- ожирение;
- онкопатологию в анамнезе;
- вновь выявленную онкопатологию;
- химиотерапию;
- варикозное расширение вен;
- катетеризацию центральной вены;
- комбинированные оральные контрацептивы;
- прием эритропоэтина;
- ВЗК;
- нефротический синдром;
- антифосфолипидный синдром;
- системную красную волчанку, аутоиммунный гепатит, ревматоидный артрит;
- миелопролиферативные заболевания;
- врожденную тромбофилию;
- травму.
Что касается беременных с кардиальной патологией, то в отдельную группу следует выделить женщин, имеющих крайне высокий риск тромбозов с наиболее драматическим развитием.
К ним относятся пациентки, у которых:
- искусственные клапаны сердца;
- стенты коронарных сосудов;
- аритмии.
Каковы риски для матери и плода при проведении антикоагулянтной терапии во время беременности?
Принимая решение о проведении антикоагулянтной терапии во время беременности, необходимо помнить о балансе двух основных составляющих: риска для плода и эффективности/безопасности для матери. Поэтому начнем с антагонистов витамина К: метаболиты данных препаратов проникают через плаценту и могут оказывать тератогенный эффект, вызывать геморрагические осложнения у плода и неврологический дефицит в будущем. В связи с этим следует прекратить прием антагонистов витамина К до 6-й недели беременности и заменить его на более безопасные НМГ.
Наиболее эффективным и изученным в этом отношении является эноксапарин (Клексан). Он значительно уменьшает риск развития варфариновой эмбриопатии. Необходимо подчеркнуть, что беременные были исключены из участия в клинических исследованиях оценки влияния новых оральных антикоагулянтов (НОАК), дабигтрана, ривароксибана, апиксабана, эдоксабана, так как все эти препараты проникают через плаценту, и степень их отрицательного воздействия на плод неизвестна, равно как и другие репродуктивные риски. Опубликованы отдельные результаты работ по применению фондапаринукса во время беременности. Известно, что он проникает через плаценту в малых количествах, но большинство опубликованных работ включают данные о начале применения этого препарата во втором триместре, а иногда и позже.
Нефракционированный гепарин (НФГ), НМГ и данапароид (гепариноид) не проникают через плаценту и безопасны для плода. Несмотря на то, что НФГ давно используется для профилактики и лечения тромбоэмболических нарушений, НМГ имеют ряд преимуществ: лучший профиль безопасности, низкую частоту кровотечений, гепарин-индуцированной тромбоцитопении, гепарин-ассоциированного остеопороза.
Рекомендации
1. Врач любой специальности, консультирующий женщину репродуктивного возраста, которая получает длительную/пожизненную терапию антагонистами витамина К или новыми прямыми оральными антикоагулянтами, обязан предоставить ей информацию о возможных рисках для плода.
2. При профилактике и лечении женщин с ТГВ в перипартальный период предпочтение отдают НМГ. Исключение составляют женщины с тромбоцитопенией, индуцированной гепарином – ГИТ (при данной беременности или в анамнезе), а также с выраженными нарушениями функции почек (в этом случае предпочтительнее назначение НФГ).
3. Если женщина, получающая НОАК, планирует беременность, необходимо перевести ее на производные кумарина или НМГ до зачатия. В случае несвоевременности переход на другой препарат должен быть проведен сразу, как только беременность подтверждена.
4. Если у женщины имеет место тяжелая аллергическая реакция на НФГ или НМГ, а также ГИТ, необходимо назначить данапароид или фондапаринукс. Особое внимание должно быть уделено правильной дозировке этих препаратов перед родоразрешением.
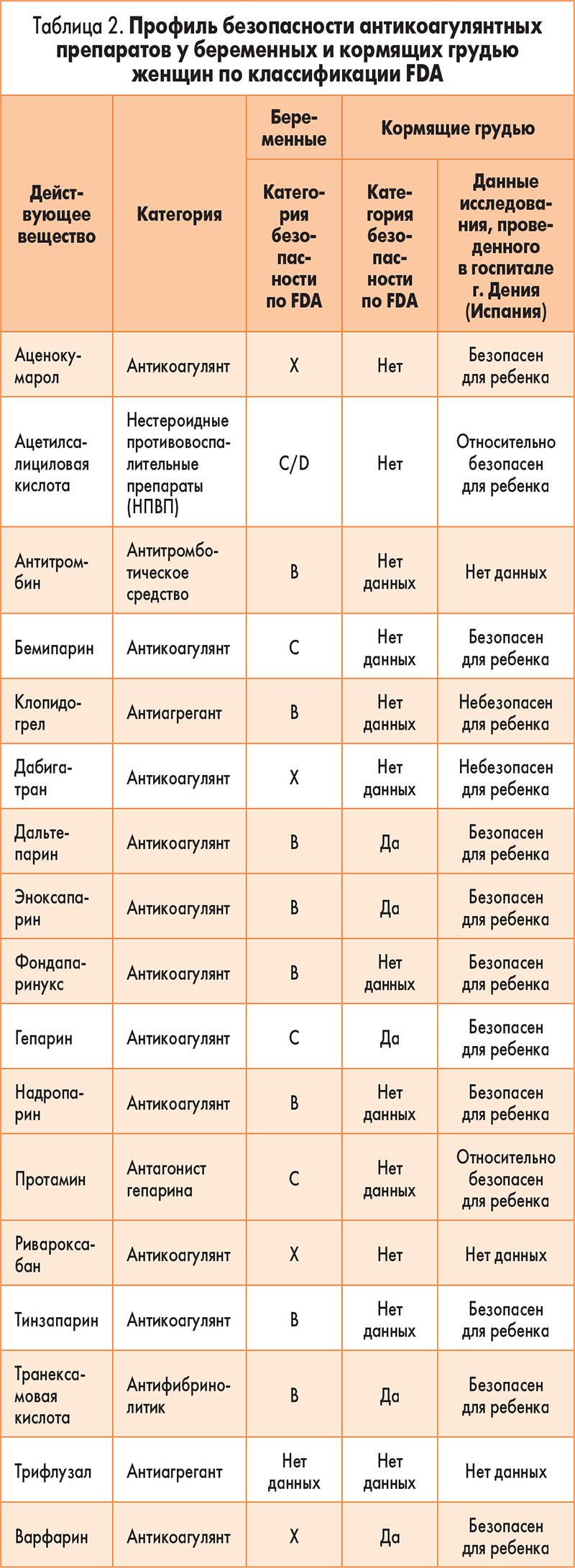
5. Всегда следует учитывать баланс двух основных составляющих: риска для плода и эффективности/безопасности для матери, основываясь на оценке безопасности антикоагулянтов по классификации FDA (табл. 2).
 Каковы риски при проведении антикоагулянтной терапии в период грудного вскармливания?
Каковы риски при проведении антикоагулянтной терапии в период грудного вскармливания?
Ни метаболиты варфарина, широко применяющегося в США и Великобритании, ни метаболиты аценокумарола, более часто применяющегося в ЕС, не определяются в грудном молоке. То есть назначение ни одного из этих препаратов не приводит к антикоагулянтным эффектам у новорожденного, мать которого получает данные антикоагулянты в период лактации. Небольшие количества НМГ определялись в грудном молоке, однако необходимо помнить, что биодоступность гепарина при пероральном применении минимальна, поэтому вряд ли присутствие метаболитов НМГ в молоке будет иметь клинический эффект для новорожденного.
До сих пор нет убедительных данных об экскреции метаболитов фондапаринукса в грудное молоко кормящих женщин, поэтому возможные эффекты для новорожденного неизвестны.
Тем не менее производитель настаивает на крайне осторожном применении фондапаринукса при грудном вскармливании, что означает его отличие от воздействия пероральных форм гепаринов.
В литературе не представлено данных о влиянии НОАК на новорожденного при грудном вскармливании, однако производители настаивают на невозможности применения этих препаратов в период лактации.
Согласно руководству по профилактике тромбозов (в отличие от полных схем антикоагулянтной терапии), в 2008 г. рекомендациями ACCP были выделены профилактические и средние дозы гепарина. Средние дозы НФГ вводят подкожно каждые 12 ч с учетом показателей анти-Xa, которые должны соответствовать 0,1-0,3 ед/мл, или НМГ в дозе 40 мг, которые назначаются каждые 12 ч.
В последних рекомендациях RCOG и ACCP определены принципы идентификации дозирования НМГ как профилактической и средней дозы и схемы дозирования НФГ в тех случаях, когда НМГ не могут быть использованы или когда предпочтительнее НФГ (например, у пациентов с нарушением функции почек). Напротив, в последних рекомендациях RCOG выделен «низкодозированный» режим НФГ и «профилактический» режим НФГ и НМГ. Полные режимы антикоагуляции называются скорректированной дозой по ACCP и лечебной или терапевтической по RCOG и ACOG.
На сегодняшний день есть результаты исследований последовательных уровней анти-Ха. Пиковые уровни анти-Ха были ниже у беременных женщин по сравнению с небеременными, различие было связано с увеличением клиренса эноксапарина. Хотя пиковые уровни анти-Xa на стабильной дозе 40 мг эноксапарина снизились с 0,47±0,13 МЕ/мл в I триместре до 0,32±0,08 МЕ/мл в III триместре беременности (p=0,002), оба этих средних значения находились в пределах рекомендованного диапазона руководства по профилактике тромбозов. В настоящее время не существует минимального значения анти-Ха активности с доказанным эффектом предотвращения тромбоза. В одной из публикаций представлены данные 321 анти-Ха у 77 пациентов, получавших НМГ в качестве профилактики ВТЭ. В группе, где 62% пациенток получали НМГ 2 р/день, только 59% находились в диапазоне профилактики (определяемой как 0,2-0,4 МЕ/мл), несмотря на корректировки последовательных доз, а 26% были ниже и 15% – выше необходимого уровня. Очевидно, что правильным подходом в группе высокого риска (механические искусственные клапаны сердца) является титрование доз НМГ под контролем анти-Ха, что было предложено в 2016 г. на 4-м Конгрессе «Кардиальные проблемы при беременности».
Рекомендации
1. НФГ, НМГ, варфарин и аценокумарол могут применяться у кормящих женщин.
2. НОАК не должны быть использованы в период лактации.
Как правильно проводить антикоагулянтную терапию во время беременности и в послеродовом периоде?
Решения, касающиеся профилактического применения антикоагулянтов во время беременности и послеродовом периоде, напрямую зависят от баланса риска развития ВТЭ и риска профилактики тромбоэмболических осложнений.
Для обеспечения успеха медикаментозной тромбопрофилактики необходимо определить группу высокого риска развития ВТЭ, так как именно у этих пациентов в соотношении польза/риск всегда будет превалировать польза.
В современных шкалах тромбоэмболических осложнений (Caprini, Khorana A.) учитываются факторы, необходимые для более точного расчета вероятного риска. К ним относятся: наличие ВТЭ в анамнезе; наличие ВТЭ в семейном анамнезе; наличие диагностированной тромбофилии и ее клинических факторов; кесарево сечение; длительная дородовая иммобилизация; увеличение индекса массы тела, а также значительные осложнения беременности и сопутствующие заболевания.
 Необходимо подчеркнуть, что тромбопрофилактика во время беременности, как правило, включает в себя подкожные инъекции НМГ в течение длительного времени, то есть имеет место «медикализация» беременности. Несмотря на то что профилактическая терапия НМГ является безопасной для плода и значительно снижает риск неблагоприятных исходов для матери, все-таки она остается достаточно затратной, требует инъекций, а порой и проведения планового родоразрешения, чтобы сделать возможной эпидуральную анестезию.
Необходимо подчеркнуть, что тромбопрофилактика во время беременности, как правило, включает в себя подкожные инъекции НМГ в течение длительного времени, то есть имеет место «медикализация» беременности. Несмотря на то что профилактическая терапия НМГ является безопасной для плода и значительно снижает риск неблагоприятных исходов для матери, все-таки она остается достаточно затратной, требует инъекций, а порой и проведения планового родоразрешения, чтобы сделать возможной эпидуральную анестезию.
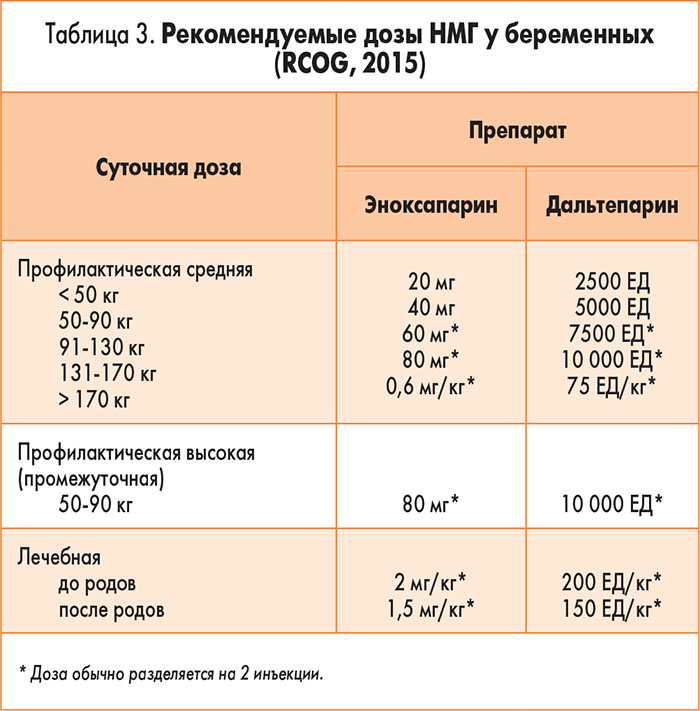
Особенно следует подчеркнуть, что во время беременности необходимая доза НМГ разделяется на два введения в сутки.
Нами предложен пошаговый подход к проведению тромбопрофилактики.
Шаг 1. Определить факторы риска ВТЭ.
Шаг 2. Определить метод тромбопрофилактики. Выявить наличие противопоказаний к проведению.
Шаг 3. Ввести необходимые препараты в адекватной дозе (табл. 3).
Шаг 4. Оценить эффективность, выявить необходимость дополнительных методов или препаратов.
Целесообразным является проведение аудита эффективности проведенной профилактики. Такой подход позволяет усовершенствовать и оптимизировать лечение, что, в свою очередь, приведет к уменьшению заболеваемости и смертности от ВТЭ.
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 2 (22) червень 2016 р.



