1 червня, 2020
COVID-19 і хронічне обструктивне захворювання легень: точки дотику та зони ризику
 Під час пандемії COVID-19 зростає увага клініцистів до респіраторних симптомів. Кашель і прогресуюча задишка є основними проявами тяжкої коронавірусної пневмонії [1]. Водночас не втрачає актуальності проблема хронічного обструктивного захворювання легень (ХОЗЛ), яка має в рази більші масштаби та медико-соціальні наслідки.
Під час пандемії COVID-19 зростає увага клініцистів до респіраторних симптомів. Кашель і прогресуюча задишка є основними проявами тяжкої коронавірусної пневмонії [1]. Водночас не втрачає актуальності проблема хронічного обструктивного захворювання легень (ХОЗЛ), яка має в рази більші масштаби та медико-соціальні наслідки.
Пацієнти з ХОЗЛ мають схильність до тяжкого перебігу COVID‑19, тому в цей непростий період вони потребують суворого дотримання протиепідемічного режиму та ретельного контролю базисної терапії для попередження загострень і госпіталізацій.
ХОЗЛ + COVID‑19 = РИЗИК × 6
G. Lippi та співавт. [2] виконали метааналіз 7 досліджень, проведених від початку 2020 року в Китаї в різних когортах хворих на COVID‑19 (загалом 1592 пацієнти).
Встановлено, що наявність ХОЗЛ асоціюється зі збільшенням ризику тяжкого перебігу COVID‑19 у 5,6 раза.
Уже підраховано, як ризик транслюється в смертність. За повідомленням Китайського центру контролю та профілактики захворювань [3], загальний показник смертності становив 2,3%, що відповідало 1023 смертельним випадкам із 44 672 підтверджених випадків COVID‑19.
В осіб із хронічними захворюваннями органів дихання показник смертності становив 6,3%, тобто був у 2,7 раза вищим.
У пацієнтів із ХОЗЛ тяжкому ураженню легень при пневмонії сприяють порушення місцевої та системної запальної відповіді, дисбаланс мікробіому, персистуюча гіперпродукція слизу з порушеним співвідношенням синтезу муцинів, структурні зміни легеневої тканини та бронхів [4]. Експериментально встановлено, що процес інфікування клітин хазяїна коронавірусом опосередкований зв’язуванням із рецепторами ангіотензинперетворювального ферменту-2 (АПФ‑2). Ці рецептори знаходяться на альвеолоцитах легень, у серці та судинах й експресуються в підвищеній кількості в пацієнтів із ХОЗЛ [5, 6].
Експерти Глобальної ініціативи з ХОЗЛ (GOLD) визнають загрозу COVID‑19 і закликають пацієнтів із цим захворюванням ретельно дотримуватися протиепідемічного режиму у зв’язку з підвищеним ризиком смерті в разі інфікування [7]. Під час епідемії закладам охорони здоров’я рекомендовано оптимізувати процеси надання медичної допомоги. Частина планових візитів може бути замінена телефонними консультаціями, а планові госпіталізації – відкладені.
Також в офіційній заяві GOLD звертає увагу на критичну необхідність пацієнтам із ХОЗЛ продовжувати раніше призначену базисну терапію для запобігання розвитку загострень і госпіталізацій. Незважаючи на занепокоєність щодо можливого негативного впливу кортикостероїдів на імунну відповідь і перебіг COVID‑19, GOLD не вбачає наукового обґрунтування для припинення інгаляційної чи системної терапії кортикостероїдами під час епідемії в пацієнтів із ХОЗЛ, якщо така терапія їм показана.
Виходячи зі статистики поширеності ХОЗЛ в Україні, а це близько 3 млн хворих і до 7% дорослого населення, за оцінками Національного інституту фтизіатрії і пульмонології [8], загострення хронічної бронхообструкції є найчастішою причиною задишки, з якою може стикатися лікар у клінічній практиці. Для таких пацієнтів своєчасна діагностика та лікування – це профілактика дихальної недостатності та врятовані роки життя. З іншого боку, пацієнт з інфекційним загостренням ХОЗЛ потребує ретельного обстеження на предмет виключення COVID‑19.
Клінічний сценарій
Чоловік 65 років, агроном на пенсії. Звернувся до сімейного лікаря зі скаргами на задишку. Під час навантажень задишка посилюється, поєднується з відчуттям «тиску в грудях», виникає кашель, інколи з виділенням мокротиння. Приблизно тиждень тому хворів на застуду, з підвищенням температури тіла, симптомами закладеності носа, ринореї, кашлем. Наразі не вважає, що повністю одужав, відзначає погіршення задишки після застуди. Контакт з іншими особами з ознаками респіраторної інфекції заперечує. Останнім часом задишка почала виникати навіть під час пересування в межах подвір’я та виконання звичних домашніх справ, що й стало причиною звернення. Анамнез життя та сімейний анамнез не обтяжені. Пацієнт стверджує, що ніколи не скаржився на здоров’я й за останні 20 років жодного разу не звертався до лікарів. При детальному розпитуванні зазначає, що його фізична витривалість при виконанні звичної роботи поступово зменшувалася впродовж останніх років, хоча момент появи задишки точно не пригадує. На пенсії 2 роки, але веде велике домашнє господарство. Курить по 1-1,5 пачки сигарет щодня протягом 30 років, шкодує, що не позбувся цієї звички, хоча намагався.
Дані об’єктивного огляду. Нормостенічної статури. Зріст – 188 см, маса тіла – 90 кг. Грудна клітка правильної форми. Температура тіла – 36,7 ºС. Шкіра суха, чиста. На язику білий наліт. Частота дихання – 28/хв. Залучення додаткової дихальної мускулатури не відзначається. Ціанозу немає. Аускультативно над усією поверхнею легень дихальні шуми ослаблені, з подовженням фази видиху. Вислуховуються свистячі хрипи над верхніми полями обох легень. Пульсоксиметрія: насичення крові киснем 95% при диханні кімнатним повітрям. Артеріальний тиск – 140/85 мм рт. ст. Пульс правильний, помірного наповнення, частота – 97 уд/хв. При аускультації серця тони ясні, без розщеплень, систолічного тремтіння, шуму тертя перикарда. Дещо посилений ІІ тон над легеневою артерією. На гомілках невиражені набряки.
Імовірний попередній діагноз:
- Емболія легеневої артерії?
- Хронічне обструктивне захворювання легень?
- Пневмонія (COVID‑19)?
- Ішемічна хвороба серця?
- Першочергове обстеження:
- Спірометрія?
- ЕКГ?
- Тест на SARS-CoV‑2?
- Рентгенографія грудної клітки?
Інтерпретація скарг і анамнезу
Наведений клінічний сценарій ілюструє типову маніфестацію ХОЗЛ у похилому віці. Під час епідемії COVID‑19 викликають настороженість будь-які респіраторні симптоми, що виникають уперше, особливо пов’язані з епізодом гострої вірусної інфекції. Проте в цьому випадку з анамнезу досить чітко вимальовується поступовий початок захворювання з прогресуючою задишкою. На користь хронічного бронхообструктивного синдрому свідчить і великий стаж куріння.
ВООЗ визначає підозрілі на COVID‑19 випадки за такими критеріями [9]:
- Пацієнт із гострим респіраторним захворюванням (гарячка та принаймні ще один симптом із таких, як кашель, задишка) та з історією подорожі (поїздки) чи прибуття з регіону, де зафіксовано групові випадки COVID‑19, упродовж 14 днів до початку симптомів.
- Пацієнт із будь-яким гострим респіраторним захворюванням, який контактував з особою з підтвердженою чи ймовірною COVID‑19 упродовж 14 днів до початку симптомів.
- Пацієнт із тяжким гострим респіраторним захворюванням (гарячка та принаймні ще один симптом із таких, як кашель, задишка, що спричиняли потребу в госпіталізації), за відсутності альтернативного діагнозу, який міг би пояснити клінічні прояви.
За даними ретроспективного дослідження 1099 пацієнтів із підтвердженою COVID‑19 у китайському місті Ухань [10], клінічні прояви коронавірусної інфекції є досить різноманітними, хоча загалом вписуються в симптомокомплекс гострої респіраторної вірусної інфекції. Гарячка як найчастіший симптом була присутня в 43,8% хворих на момент госпіталізації, але досягла показника 88,7% упродовж лікування в стаціонарі. Друге місце за частотою посів кашель (67,8%). У 33,7% хворих спостерігалося відходження мокротиння. До 40% пацієнтів скаржилися на загальне нездужання та виснаження. Частота задишки становила 18,7% у загальній когорті госпіталізованих пацієнтів, але зросла до 37,6% серед хворих із тяжким перебігом COVID‑19.
Ураховуючи анамнез і критерії ВООЗ, пацієнт із клінічного сценарію не потрапляє під підозру на COVID‑19. Пацієнти з ХОЗЛ дуже чутливі до дії різних чинників, зокрема респіраторних вірусів, які можуть призводити до загострення. Епізод ГРВІ може стати тригером погіршення задишки, що змушує хворого звернутися до лікаря, як в описаному сценарії. Але на момент звернення ознаки гострого респіраторного захворювання відсутні. Навіть якщо в подібному випадку ПЛР-тестування на SARS-CoV‑2 буде призначене, очікувати результату доведеться 2-3 дні. А підтвердити діагноз ХОЗЛ і розпочати лікування слід уже сьогодні.
Верифікація діагнозу
Згідно з Уніфікованим клінічним протоколом медичної допомоги (далі – УКПМД) [11], у первинній діагностиці та лікуванні типових випадків ХОЗЛ ключову роль відіграють лікарі первинної ланки (наказ Міністерства охорони здоров’я України від 27 червня 2013 року № 555). УКПМД ґрунтується на стратегічних настановах Глобальної ініціативи з хронічного обструктивного захворювання легень (GOLD), яке є галузевим стандартом і регулярно переглядається з урахуванням оновлень наукової бази [13].
Діагноз ХОЗЛ має бути підтверджений за допомогою спірометрії [11, 13]. Стандартний протокол передбачає виконання проби на максимальну швидкість потоку повітря за 1-шу секунду при форсованому видиху (ОФВ1) через 10-15 хвилин після інгаляційного введення швидкодіючого бронходилататора (сальбутамолу в дозі 400 мкг). Зменшення співвідношення ОФВ1/ФЖЄЛ <0,7 (70%) свідчить про наявність бронхообструкції, характерної для ХОЗЛ.
ЕКГ не входить до стандарту діагностики ХОЗЛ. Проте задишка й інші симптоми ХОЗЛ, такі як виснаженість, периферичні набряки, тахікардія, також часто зустрічаються при серцево-судинних захворюваннях (CCЗ). Вони становлять основну й, імовірно, найважливішу групу супутніх захворювань у пацієнтів із ХОЗЛ. Окрім того, прослідковується взаємообтяжливий патогенетичний зв’язок ССЗ із COVID‑19. Рецептори АПФ‑2, які експресуються у великій кількості на альвеолоцитах легень і вважаються точкою входу вірусу в клітини, також поширені в серці та судинах, де становлять ключову ланку ренін-ангіотензинової системи [5, 14]. Із перших місяців епідемії стало зрозуміло, що пацієнти з гіпертензією, цукровим діабетом й ожирінням, а також зі встановленими ССЗ є особливо вразливими та швидко поповнюють невтішну статистику смертності від COVID‑19. Підвищена вразливість пацієнтів із ХОЗЛ до інфекції COVID‑19 може бути також пов’язана з підвищеною частотою перерахованих коморбідних станів у цій групі хворих. З іншого боку, ССЗ можуть бути первинною маніфестацією COVID‑19, а також можуть розвиватися вторинно по відношенню до гострого ураження легень унаслідок збільшення навантаження на міокард. До найчастіших серцево-судинних проявів COVID‑19 відносять ішемічне ураження міокарда, міокардит і серцеві аритмії [14].
Тому в описаному клінічному сценарії ЕКГ є доцільним методом обстеження пацієнта на первинній ланці, що дозволяє провести швидку диференційну діагностику між гострими ураженнями міокарда та ХОЗЛ.
Електрокардіографічними ознаками, які свідчать на користь легеневого серця при хронічній бронхообструкції (проте не виключають іншого діагнозу), можуть бути: синусова тахікардія; зміщення електричної осі серця праворуч; легеневий зубець Р (амплітуда Р >2,5 мВ у нижніх відведеннях, частіше aVL); низький вольтаж комплексу QRS; блокада правої ніжки пучка Гіса. Крім того, у хворих на ХОЗЛ може відзначатися помірна депресія сегмента ST у нижніх відведеннях, що відображає аномалії реполяризації передсердь.
Прискорення серцевого ритму особливо часто зустрічається при загостреннях ХОЗЛ і виступає компенсаторним механізмом при гіпоксії чи дисфункції правого шлуночка серця (cor pulmonale). Найчастіше при ХОЗЛ зустрічається синусова тахікардія, але також можливі інші надшлуночкові аритмії: передсердна тахікардія, фібриляція чи тріпотіння передсердь. Останні дуже поширені в популяції віком понад 60 років [15].
P pulmonale часто можна побачити на ЕКГ у пацієнтів із ХОЗЛ. Збільшення вольтажу зубця Р відображає гіпертрофію правого передсердя, проте ця ознака є недостатньо чутливою [16]. Амплітуда може динамічно змінюватися й зазвичай досягає максимумів у періоди загострень ХОЗЛ [17].
За підозри на інші причини респіраторних симптомів можуть бути призначені додаткові обстеження: рентгенографія чи комп’ютерна томографія грудної клітки, мікробіологічне дослідження мокротиння, якщо воно має гнійний характер [11].
Оцінка ризику та призначення терапії
Згідно з настановами GOLD та УКПМД ХОЗЛ, наступним кроком після спірометричного підтвердження діагнозу є визначення групи ризику. Для цього проводиться комплексна оцінка з урахуванням вираженості симптомів, тяжкості бронхообструкції за даними спірометрії (табл. 1), а також частоти загострень. У результаті пацієнт відноситься до однієї з чотирьох груп ризику, що визначає подальшу тактику лікування (табл. 2).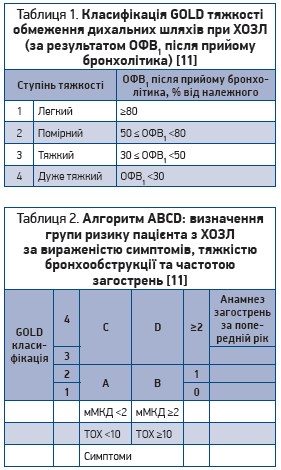
Процедура оцінювання ABCD та її інструменти деталізовані в УКПМД [11]. Зазначимо лише, що спірометрія й оцінювальні шкали (Модифікована шкала Міжнародного консиліуму дослідників – мМКД, тест з оцінки ХОЗЛ – ТОХ) доступні для використання на первинній ланці й не потребують значних затрат часу. Тому в типових випадках дебюту чи загострення ХОЗЛ діагностика та підбір базисної терапії можуть і мають бути виконані на первинному рівні. В умовах епідемії COVID‑19 це значно спрощує маршрут пацієнта (якщо він не потребує госпіталізації), зменшує ризик додаткових контактів й інфікування.
Пацієнт із клінічного сценарію, ймовірно, потрапить до групи А, беручи до уваги помірну вираженість симптомів при досить значних щоденних навантаженнях, і за умови, якщо результатом спірометрії буде ОФВ1 у межах від 50 до 80% від належного. До групи А відносяться малосимптомні хворі низького ризику (мМКД <2; ТОХ <10; ступінь бронхообструкції GOLD 1-2).
Приналежність до групи визначає раціональну терапію ХОЗЛ. Правильно підібрана та вчасно призначена базисна медикаментозна терапія може значно уповільнити прогресування бронхообструкції, зменшити тяжкість і частоту загострень, запобігти розвитку ускладнень і покращити якість життя пацієнтів [11, 13]. Окрім того, своєчасно попереджене ускладнення зменшує ризик додаткових контактів й інфікування SARS-CoV‑2, що надзвичайно важливо для пацієнтів із ХОЗЛ, зважаючи на високу смертність від COVID‑19.
Основу базисної терапії ХОЗЛ становлять інгаляційні засоби. Бронходилататори короткої дії – терапія першої лінії для пацієнтів групи А. До цієї групи належать β2-агоністи короткої дії (БАКД) та холінолітики короткої дії (ХКД). Інгаляційні бронходилататори при ХОЗЛ є центральним елементом контролю симптомів. Регулярне чи «за потребою» застосування БАКД/ХКД покращує ОФВ1 і полегшує симптоми (рівень доказів А).
У міру збільшення тяжкості захворювання та переходу до вищих клінічних груп акценти в терапії зміщуються в бік β2-агоністів тривалої дії (БАТД) і холінолітиків тривалої дії. БАТД забезпечують перевагу у вигляді 12-годинного контролю симптомів і мають докази позитивного впливу на прогноз при ХОЗЛ. Основу терапії груп В, С і D становлять комбіновані препарати – один або два бронходилататори тривалої дії в поєднанні з інгаляційними кортикостероїдами (ІКС).
При цьому не виключається додаткова користь для пацієнта від застосування БАКД за потребою [13]. Так, у перехресному рандомізованому дослідженні було встановлено, що після тривалого лікування БАТД (індакатеролом або формотеролом) у пацієнтів зі стабільним перебігом ХОЗЛ зберігається чутливість дихальних шляхів до дії БАКД сальбутамолу. При цьому інгаляції сальбутамолу забезпечували додаткове підвищення ОФВ1. Результати цього дослідження обґрунтовують застосування сальбутамолу як швидкодіючого засобу для усунення бронхоспазму навіть у тих пацієнтів, які лікуються бронходилататорами тривалої дії [18].
БАКД й ІКС у режимі повторюваних небулайзерних інгаляцій незамінні при лікуванні загострень ХОЗЛ. Небулайзерна терапія дозволяє доставити високі терапевтичні дози препаратів у легені в дрібнодисперсному аерозолі за короткий період часу, що недоступно для інших інгаляційних форм. Хворий з інтенсивною задишкою має серйозні труднощі при використанні дозованих інгаляторів. Щоби ввести 5 мг сальбутамолу через аерозольний інгалятор потрібно більше години, а в небулізованій формі – в середньому 10 хвилин. Завдяки винайденню більш селективних β2-aгоністів (сальбутамолу) вдалося значно знизити рівень небажаного впливу на міокард [19, 20].
Сучасні ІКС, наприклад флютиказон, при введенні за допомогою небулайзера забезпечують максимальний протизапальний ефект у мінімальній дозі та з мінімальним ризиком системної дії. Відомо, що флютиказону пропіонат характеризується вищою афінністю до глюкокортикоїдних рецепторів і меншою абсолютною біодоступністю, ніж будесонід [21].
Метилксантини (теофілін, доксофілін) є альтернативними засобами, які можуть застосовуватись окремо чи додаватися до препаратів першого та другого вибору при недостатньому контролі симптомів. Проте вони не замінюють інгаляційну терапію, якщо пацієнт не має до неї протипоказань [11]. БАКД (сальбутамол) порівняно з метилксантинами забезпечує селективну дію в дихальних шляхах і позбавлений небажаних системних, зокрема серцево-судинних, ефектів.
Антиоксиданти та муколітичні препарати. З цієї групи засобів найбільший досвід застосування має ацетилцистеїн (АЦ). Його рекомендується призначати пацієнтам із частими загостреннями, анамнезом тяжкого куріння. АЦ – відомий антиоксидант і дисульфідоруйнуючий агент, що було підтверджено багатьма дослідженнями. АЦ здатний поповнювати пул іншого важливого антиоксиданту глутатіону при його виснаженні, паралельно здійснюючи функції прямого антиоксиданту для деяких з’єднань. Нещодавно був відкритий новий механізм впливу АЦ – здатність руйнувати тіолізовані білки [12].
Не рекомендовано використовувати муколітичні препарати для запобігання загостренню в пацієнтів зі стабільним перебігом ХОЗЛ. При хронічному кашлі та виділенні мокротиння АЦ може зменшувати ці симптоми. Регулярна терапія муколітиками знижує ризик загострень в окремих групах пацієнтів (рівень доказів В) [11, 13].
Не слід забувати про немедикаментозні методи, які також деталізовані в УКПМД. Відмова від куріння є найбільш ефективним і рентабельним лікуванням ХОЗЛ у курців. Доведено, що припинення куріння уповільнює темпи зменшення ОФВ1. Тому обов’язок лікаря – надавати допомогу у відмові від куріння за будь-якої нагоди.
Довідка «ЗУ»
Небулізовані форми БАКД й ІКС у короткий час створюють високі терапевтичні концентрації в легенях, що сприяє швидкому полегшенню симптомів. Муколітики з різними шляхами введення допомагають підібрати оптимальну терапію кожному пацієнту з продуктивним кашлем і полегшити їхній стан.
 На сьогодні в Україні представлені розчини сальбутамолу сульфату (в 1 мл – 1 мг сальбутамолу) в однодозових контейнерах, які призначені для небулайзерної терапії, в тому числі для лікування хворих на ХОЗЛ. Сальбутамол – селективний бронхолітик, визнаний золотим стандартом БАКД. Бронхолітичний ефект від застосування небулізованого сальбутамолу розпочинається вже на 4-5-й хвилині після інгаляції та триває 4-6 годин. Нині на ринку України доступний небулізований сальбутамол з удосконаленим складом діючої та допоміжних речовин.
На сьогодні в Україні представлені розчини сальбутамолу сульфату (в 1 мл – 1 мг сальбутамолу) в однодозових контейнерах, які призначені для небулайзерної терапії, в тому числі для лікування хворих на ХОЗЛ. Сальбутамол – селективний бронхолітик, визнаний золотим стандартом БАКД. Бронхолітичний ефект від застосування небулізованого сальбутамолу розпочинається вже на 4-5-й хвилині після інгаляції та триває 4-6 годин. Нині на ринку України доступний небулізований сальбутамол з удосконаленим складом діючої та допоміжних речовин.
 Як ІКС у хворих із діагностованою бронхообструкцією при загостренні препаратами вибору можуть бути лікарські засоби у вигляді монодозових контейнерів із діючою речовиною флютиказону пропіонат (в 1 мл розчину – 1 мг флютиказону) для застосування зі струминним небулайзером. Флютиказону пропіонат має високу спорідненість і тривалий зв’язок із ГКС-рецепторами людини, що забезпечує потужну протизапальну дію (Bootsma et al. Fluticasone propionate does not influence bone metabolism in contrast to beclomethasone dipropionate. Am. J. Respir. Crit. Care Med. 1996; 153: 924-930. * Доза: 1500 мкг).
Як ІКС у хворих із діагностованою бронхообструкцією при загостренні препаратами вибору можуть бути лікарські засоби у вигляді монодозових контейнерів із діючою речовиною флютиказону пропіонат (в 1 мл розчину – 1 мг флютиказону) для застосування зі струминним небулайзером. Флютиказону пропіонат має високу спорідненість і тривалий зв’язок із ГКС-рецепторами людини, що забезпечує потужну протизапальну дію (Bootsma et al. Fluticasone propionate does not influence bone metabolism in contrast to beclomethasone dipropionate. Am. J. Respir. Crit. Care Med. 1996; 153: 924-930. * Доза: 1500 мкг).
 Як муколітична терапія хворим з інфекційним загостренням ХОЗЛ на госпітальному етапі може бути призначений ацетилцистеїн у формі ін’єкцій (внутрішньом’язовий або внутрішньовенний), муколітик із потужними антиоксидантними властивостями. Широко застосовується в лікуванні пацієнтів, які перебувають на стаціонарному лікуванні з інфекційно-запальними гострими захворюваннями чи загостреннями бронхолегеневих захворювань. Особливістю ацетилцистеїну серед муколітиків є його прямий муколітичний ефект без посилення секреції в дихальних шляхах, початок дії з перших годин уведення та здатність потенціювати дію антибактеріальної терапії (Bonanomi et al. Toxicological, pharmacokinetic and metabolic studies on acetylcysteineL. Eur. J. Respir. Dis. 1980; 61 (suppl. 111): 45-51).
Як муколітична терапія хворим з інфекційним загостренням ХОЗЛ на госпітальному етапі може бути призначений ацетилцистеїн у формі ін’єкцій (внутрішньом’язовий або внутрішньовенний), муколітик із потужними антиоксидантними властивостями. Широко застосовується в лікуванні пацієнтів, які перебувають на стаціонарному лікуванні з інфекційно-запальними гострими захворюваннями чи загостреннями бронхолегеневих захворювань. Особливістю ацетилцистеїну серед муколітиків є його прямий муколітичний ефект без посилення секреції в дихальних шляхах, початок дії з перших годин уведення та здатність потенціювати дію антибактеріальної терапії (Bonanomi et al. Toxicological, pharmacokinetic and metabolic studies on acetylcysteineL. Eur. J. Respir. Dis. 1980; 61 (suppl. 111): 45-51).
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 8 (477), квітень 2020 р.


