6 липня, 2020
R-альфа-ліпоєва кислота: інновації від природи
Близько 50 років тому була синтезована α-ліпоєва кислота, й уже невдовзі почали з’являтися перші результати її клінічного застосування. Дослідники відзначали позитивний вплив препаратів α-ліпоєвої кислоти на перебіг захворювань печінки та цукрового діабету. Згодом були виявлені універсальні антиоксидантні властивості α-ліпоєвої кислоти, після чого сфера її терапевтичного застосування суттєво розширилася.
Сьогодні найбільша кількість масштабних рандомізованих клінічних досліджень (РКД) із застосуванням α-ліпоєвої кислоти стосується лікування діабетичної периферичної та вегетативної полінейропатії. Ці РКД продемонстрували здатність α-ліпоєвої кислоти покращувати провідність нервових імпульсів, зменшувати больову симптоматику та неврологічний дефіцит, покращувати сон пацієнтів і якість їхнього життя.
Препарати α-ліпоєвої кислоти широко використовуються в гастроентерології для лікування хронічних дифузних захворювань печінки (гепатити різної етіології, гепатози, цироз і фібрози). Доведено, що застосування α-ліпоєвої кислоти в таких пацієнтів сприяє збільшенню запасів внутрішньоклітинного глутатіону, запобігає ураженню мітохондрій у процесі перекисного окислення ліпідів. Це дає змогу відновити рівновагу окисно-відновних процесів у гепатоцитах і знижує ушкоджувальну дію токсичних речовин.
Було отримано обнадійливі результати застосування α-ліпоєвої кислоти в лікуванні атеросклерозу та запальних захворювань судин (Zhang W.J. et al., 2008). Зокрема, встановлено, що α-ліпоєва кислота пригнічує утворення атеросклеротичних бляшок у середньому на 50%, сприяє суттєвому зниженню рівня холестерину ліпопротеїнів низької та дуже низької щільності. На сьогодні цей препарат вважається ефективним засобом профілактики та лікування атеросклеротичних уражень судин. У неврологічній практиці α-ліпоєву кислоту застосовують для лікування ішемічних захворювань головного мозку (транзиторні ішемічні атаки, ішемічний інсульт) і розсіяного склерозу.
Наведена вище інформація вже давно відома, й, на перший погляд, до неї нічого додати. Однак останнім часом з’являється дедалі більше даних щодо активності ізомерів α-ліпоєвої кислоти та схем її застосування, і саме про ці нові дані, котрі, поза сумнівом, корисно знати клініцисту, йтиметься в огляді.
Насамперед слід нагадати, що стандартні препарати α-ліпоєвої кислоти являють собою рацемічну суміш двох оптичних ізомерів – R(+) і S(-). Саме така суміш ізомерів дістала узагальнену назву «тіоктова кислота». У клітинах організму людини α-ліпоєва кислота присутня лише у формі свого активного ізомеру – R(+)-енантіомеру. (До речі, це стосується й усіх рослинних і тваринних клітин.) Саме з ним пов’язані її основні біологічні ефекти. S(-)-ізомер α-ліпоєвої кислоти є побічним продуктом її синтезу, котрий має певний антагоністичний вплив відносно R(+)-ізомеру.
Дослідники вважають, що системи транспорту α-ліпоєвої кислоти в клітину (зокрема, натрійзалежна система транспорту та трансмембранний білок SLC5A6) також відповідають за всмоктування α-ліпоєвої кислоти в кишечнику. При цьому R(+) і S(-) енантіомери конкурують за транспортні системи, тому можуть впливати на біодоступність і клінічну ефективність рацемічних сумішей α-ліпоєвої кислоти (Zehnpfennig B. et al., 2015). У результаті абсолютна біодоступність рацемічної α-ліпоєвої кислоти обмежується показником приблизно 30%.
На відміну від звичайної суміші, прийом лише R(+)-ізомеру α-ліпоєвої кислоти виключає конкуренцію між ізомерами, тож біодоступність R(+)-α-ліпоєвої кислоти є вищою порівняно з такою рацемічних сумішей. Доклінічні дослідження продемонстрували, що біодоступність R(+)-α-ліпоєвої кислоти підвищується в разі призначення лише цієї форми порівняно з показниками біодоступності при застосуванні рацемічних сумішей (Hermann R. et al., 1996).
Отже, природна форма α-ліпоєвої кислоти (R(+)-ізомер) дає змогу досягти вищої терапевтичної концентрації при меншій дозі порівняно зі звичною сумішшю R(+) і S(-) ізомерів, тобто тіоктовою кислотою.
Рекомендована доза тіоктової кислоти при лікуванні діабетичної нейропатії становить 600 мг, з яких на R(+) і S(-) ізомери α-ліпоєвої кислоти припадає по 300 мг. На основі результатів доклінічних досліджень очікується, що фармакокінетичні характеристики R(+)-α-ліпоєвої кислоти після застосування звичайного препарату тіоктової кислоти в дозі 600 мг будуть подібними до результатів застосування R(+)-α-ліпоєвої кислоти в дозі 200 мг.
Для перевірки цієї гіпотези J. Yoon і співавт. провели відкрите рандомізоване дослідження в паралельних групах здорових добровольців чоловічої статі. Метою цього випробування було порівняти фармакокінетичні властивості та переносимість R(+)- і S(-)-α-ліпоєвої кислоти після одноразового перорального застосування R(+)-α-ліпоєвої кислоти з аналогічними показниками після прийому тіоктової кислоти.
Учасники були розподілені методом рандомізації до однієї з 3 груп: R(+)-α-ліпоєвої кислоти 200 мг або 300 мг і тіоктової кислоти 600 мг. Після утримання від їжі протягом понад 10 год учасники приймали одноразову дозу тестового препарату, запиваючи його 240 мл води. Надалі їм заборонялося їсти й пити протягом 4 год після прийому препарату. Серійні відбори зразків крові для визначення концентрації R(+)-α-ліпоєвої кислоти та S(-)-α-ліпоєвої кислоти в плазмі крові проводили перед застосуванням препаратів і через 0,08; 0,17; 0,25; 0,33; 0,5; 0,67; 1; 1,5; 2; 3; 4; 6 і 8 год після цього.
Концентрації R(+)- та S(-)-α-ліпоєвої кислоти в плазмі визначали за допомогою валідованої системи рідинної хроматографії. Максимальну концентрацію (Cmax) і час для її досягнення (tmax) отримували шляхом безпосередньої перевірки індивідуальних профілів «концентрація – час». Площу під кривою «концентрація – час» від 0 до останнього показника концентрації, що піддається вимірюванню (AUClast), обчислювали за допомогою лінійно-логарифмічного методу трапецій.
Співвідношення середнього геометричного (GMR) і пов’язаного з ним 90% довірчого інтервалу (ДІ) для R(+)-α-ліпоєвої кислоти 200 мг і тіоктової кислоти 600 мг та R(+)-α-ліпоєвої кислоти 300 мг і тіоктової кислоти 600 мг обчислювали для логарифмічно перетворених значень Cmax й AUClast із метою вивчення фармакокінетичних параметрів досліджуваних препаратів.
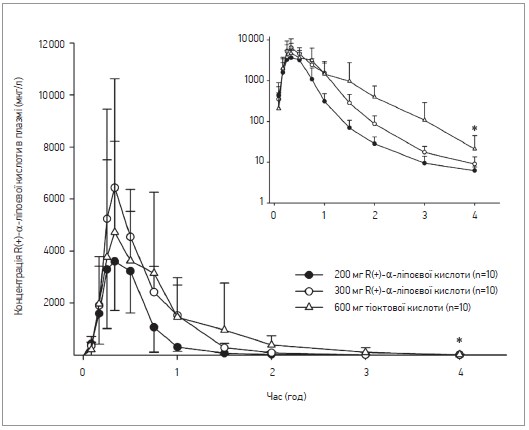
Фармакокінетичні характеристики після одноразового перорального застосування R(+)-α-ліпоєвої кислоти 300 мг були подібними до відповідного показника після одноразового перорального прийому тіоктової кислоти 600 мг. Показники tmax та t1/2 були зіставними в усіх трьох групах. Показник Cmax для 200 мг і 300 мг R (+)-α-ліпоєвої кислоти та 600 мг тіоктової кислоти становив 4186±1956, 6985±3775 і 6498±3575 мкг/л відповідно, а показник AUClast – 1893±759, 3575±1149 і 3790±1623 мкг×год‑1×л‑1 відповідно (рис. 1).
Рис. 1. Середнє значення площі під кривою «концентрація – час» після одноразового перорального застосування R(+)-α-ліпоєвої кислоти в дозі 200 мг чи 300 мг або тіоктової кислоти 600 мг
Показники на графіку відображені шляхом логарифмічно-лінійної моделі. Відрізками позначено стандартне відхилення.
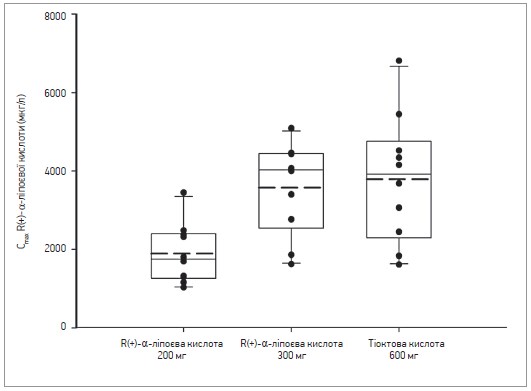
Надалі було проведено оцінку й порівняння параметрів фармакокінетики в кожній групі. Співвідношення середнього геометричного та пов’язаного з ним 90% ДІ для R(+)-α-ліпоєвої кислоти 200 мг відносно тіоктової кислоти 600 мг для Cmax та AUClast становило 0,71 (0,43-1,15) і 0,51 (0,37-0,70) відповідно. Значення для R(+)-α-ліпоєвої кислоти 300 мг і тіоктової кислоти 600 мг дорівнювало 1,11 (0,68-1,80) і 0,97 (0,71-1,34) відповідно (рис. 2).
Рис. 2. Порівняння максимальної концентрації (Cmax` верхня межа) та площі під кривою «концентрація – час» від 0 до останнього показника концентрації, що піддається вимірюванню (AUClast` нижня межа), R(+)-α-ліпоєвої кислоти після одноразового перорального застосування R(+)-α-ліпоєвої кислоти в дозі 200 мг чи 300 мг або тіоктової кислоти 600 мг
«Ящики» вказують інтерквартильний діапазон, «вуса» – 10-й і 90-й процентилі. Горизонтальні риски всередині «ящика» позначають медіану, довга пунктирна лінія – середнє значення.
Отримані результати свідчать, що фармакокінетичні характеристики R(+)-α-ліпоєвої кислоти після одноразового перорального застосування в дозі 300 мг подібні до показників, отриманих після одноразового перорального застосування тіоктової кислоти в дозі 600 мг.
Висновки
• У природі – в рослинних, тваринних і людських клітинах – α-ліпоєва кислота існує лише у формі R(+)-енантіомеру, і тільки R(+)-енантіомер чинить біологічну дію.
• Природна форма α-ліпоєвої кислоти (R(+)-енантіомер) дає змогу досягти вищої терапевтичної концентрації при меншій дозі, ніж звичайна ліпоєва кислота (рацемічна суміш R(+)- та S(-)-енантіомерів).
• На відміну від рацемічної суміші, застосування чистої R(+)-α-ліпоєвої кислоти виключає конкуренцію між енантіомерами, що підвищує біодоступність.
• Для пацієнтів важливими перевагами R(+)-α-ліпоєвої кислоти є менше медикаментозне навантаження, потенційно вища безпека та більша доступність терапії, що в довгостроковій перспективі покращить комплаєнс, а отже, й ефективність лікування.
• На сьогодні в Україні вже доступна перша пероральна форма R(+)-енантіомеру α-ліпоєвої кислоти – саплемент Райт, капсули 300 мг, № 30. Спосіб і тривалість застосування, показання та протипоказання в цього саплементу такі самі, як у звичайної α-ліпоєвої кислоти: приймати по 1 капсулі на добу натще за 30 хв до першого прийому їжі. Мінімальна тривалість курсу становить 2 міс.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 10 (479), травень 2020 р.