7 липня, 2020
Порушення коагуляції та тромбоз у пацієнтів із COVID-19
Здебільшого коронавірусна хвороба – 2019 (COVID‑19) зумовлює інфекційне ураження дихальних шляхів. Однак у частини пацієнтів захворювання прогресує та має тяжчий перебіг, що характеризується лихоманкою, стійкою до протизапальної терапії, гострим ушкодженням легень із розвитком гострого респіраторного дистрес-синдрому, шоковим станом і мультиорганною дисфункцією, котра асоціюється зі значним ризиком смерті [1]. У багатьох пацієнтів із тяжким перебігом COVID‑19 присутні порушення коагуляції, що імітують інші системні коагулопатії, пов’язані з тяжкими інфекціями, такі як синдром дисемінованого внутрішньосудинного згортання (ДВЗ‑синдром) або тромботична мікроангіопатія, але COVID‑19 має відмінні риси [2].
Коагулопатія у хворих на COVID-19 асоціюється з підвищеним ризиком летального наслідку [3]. Крім того, актуальність цієї проблеми зумовлена тим, що венозні й артеріальні тромбоемболічні ускладнення в пацієнтів із тяжким перебігом COVID-19 часто залишаються недіагностованими [4, 5]. У цьому огляді підсумовано характеристики COVID-19-асоційованої коагулопатії, результати досліджень коагулограм інфікованих пацієнтів, особливості прогемостатичного статусу та частоту тромбоемболічних ускладнень, а також представлено терапевтичні заходи, потенційно ефективні для лікування відповідних станів.
Найтиповішими знахідками в пацієнтів із COVID-19 є підвищення концентрації D-димеру, відносно помірне зниження кількості тромбоцитів і зростання протромбінового часу. Так, у дослідженні [6], проведеному в Китаї із залученням 1099 пацієнтів із COVID-19, зростання рівня D-димеру (>0,5 мг/л) спостерігалося в 260 (46%) із 560 учасників. Інше китайське обсерваційне дослідження [3] за участю 183 хворих на COVID-19 виявило, що в пацієнтів, які не вижили, середній рівень D-димеру становив 2,12 мг/л (діапазон – 0,77-5,27) порівняно з 0,61 мг/л (діапазон – 0,35-1,29) серед тих, хто вижив. Окрім того, за результатами випробування [7], в пацієнтів, які потребували лікування у відділенні реанімації й інтенсивної терапії (ВРІТ), відзначалися значимо вищі середні показники концентрації D-димеру (2,4 мг/л, інтерквартильний розмах (ІКР) – 0,6-14,4), ніж у хворих, які не потребували терапії у ВРІТ (0,5 мг/л, ІКР – 0,3-0,8). Автори ще одного дослідження [8] відзначили, що рівень D-димеру >1 мг/л при надходженні збільшував ризик смерті у 18 разів (95% довірчий інтервал 2,6-128,6; p=0,0033).
Цікавим також виявився той факт, що в пацієнтів, які померли внаслідок тяжкого перебігу COVID-19, попередньо відзначалося помірне зростання показника протромбінового часу (15,6 с, діапазон – 14,4-16,3) порівняно з тими, хто вижив (13,6 с, діапазон – 13,0-14,3) [3]. Однак такі зміни можуть залишитися невиявленими, якщо показник протромбінового часу надати як міжнародне нормалізоване відношення.
Варто звернути увагу на результати досліджень [6, 7], які виявили, що в 5% зі всіх госпіталізованих хворих на COVID-19 кількість тромбоцитів на момент надходження була меншою за 100×109/л. Натомість помірна тромбоцитопенія (кількість тромбоцитів <150×109/л) спостерігалася в 70-95% випадків тяжкого перебігу COVID-19. Незважаючи на це, деякі автори не вважають тромбоцитопенію важливим предиктором прогресування та несприятливого перебігу COVID-19 [5, 7].
Встановлено, що концентрація фібриногену на рівні верхньої межі норми, ймовірно, є одним із проявів гострофазової відповіді при COVID-19. Утім, у великої кількості інфікованих пацієнтів незадовго до їхньої смерті спостерігалося раптове зниження цього показника до рівня <1,0 г/л [3]. Окрім того, концентрація антитромбіну в плазмі крові у хворих, які не вижили, була значно нижчою порівняно з тими, хто залишився живим (84% від належної в тих, хто не вижив, проти 91% від належної в тих, які вижили). Проте зниження цього показника до <80% від належного спостерігається вкрай рідко [3].
Деякі автори зазначають, що наявність тромбоцитопенії в комплексі з подовженим протромбіновим часом і підвищеним рівнем D-димеру може свідчити про розвиток ДВЗ-синдрому крові. Проте такий патерн істотно відрізняється від ДВЗ, асоційованого із сепсисом [2]. Так, тромбоцитопенія при сепсисі зазвичай є вираженішою; натомість рівні D-димеру не досягають високих значень порівняно з такими в пацієнтів, які інфіковані SARS-CoV-2. Крім того, згідно зі шкалою діагностики ДВЗ Міжнародного товариства з вивчення тромбозу та гемостазу, більшість хворих на COVID-19 не будуть класифіковані як пацієнти з ДВЗ-синдромом [2, 3].
До інших лабораторних відхилень, які трапляються в пацієнтів із COVID-19 і можуть мати стосунок до коагулопатії, належать підвищений рівень лактатдегідрогенази й (у деяких хворих) істотно висока концентрація феритину, що нагадує таку в разі тромботичної мікроангіопатії [8]. При посмертному дослідженні пацієнтів із COVID-19 виявляють типові тромботичні маси в дрібних судинах легень й інших органів, при цьому ознак гемолізу чи наявності шизоцитів у мазках крові немає. До того ж фіксується значно вища кількість тромбоцитів порівняно з відповідним показником у хворих на тромботичну мікроангіопатію.
Зібрані дані свідчать про те, що коагулопатія, розвиток якої пов’язаний із COVID-19, – це поєднання слабко вираженого ДВЗ-синдрому та локальної легеневої тромботичної мікроангіопатії, що може мати суттєвий вплив на органну дисфункцію в найтяжчих пацієнтів.
У хворих із тяжкою формою COVID-19 може також спостерігатися підвищення концентрації прозапальних цитокінів, як-от фактора некрозу пухлини (TNF), і деяких інтерлейкінів (ІЛ-1 та ІЛ-6) [7]. Відомо, що ІЛ-6 властиво зумовлювати експресію тканинного фактора, розміщеного на поверхні мононуклеарних клітин, що надалі ініціює активацію коагуляції й утворення тромбіну. Натомість TNF й ІЛ-1 є основними медіаторами, здатними пригнічувати ендогенні антикоагуляційні механізми. Так, у субпопуляції найтяжчих пацієнтів із COVID-19 можуть спостерігати розвиток так званого цитокінового шторму, що характеризується зростанням рівнів прозапальних цитокінів і хемокінів [9].
Перебіг коронавірусних інфекцій також пов’язують зі значною активацією фібринолітичної системи, зокрема встановлено, що в пацієнтів, інфікованих коронавірусом SARS-CoV-1, плазмові концентрації тканинного активатора плазміногену (tPA) були більш ніж у 6 разів вищими, ніж у хворих без інфекції. Наявність високої концентрації D-димеру та продуктів деградації фібрину в пацієнтів із тяжким перебігом COVID-19 може бути пояснена розвитком індукованого запаленням ушкодження ендотелію, котре, своєю чергою, спричиняє масивний викид активаторів плазміногену.
Відомо, що виникнення тромботичної мікроангіопатії зазвичай пов’язане з появою в плазмі крові ультравеликих мультимерів фактора фон Віллебранда (ULvWF), що зумовлює патологічно посилену взаємодію між тромбоцитами та судинною стінкою. Зазвичай ULvWF викидаються з ушкоджених ендотеліальних клітин і в нормальних умовах розкладаються за допомогою плазмової металопротеїнази ADAMTS 13 (дизінтегрин і металопротеаза з повторами тромбосподину типу 1, член 13). Дефіцит останньої може спостерігатися на тлі багатьох тяжких запальних процесів, зумовлених системними інфекціями, проте поки що відсутні дані щодо концентрації ADAMTS 13 у тяжких хворих на COVID-19.
Коагулопатія, асоційована з COVID-19, свідчить про наявність у таких пацієнтів стану гіперкоагуляції, що безпосередньо збільшує ризик тромбоемболічних ускладнень. До інших факторів, які підвищують ризик тромбозу, належать іммобілізація й ушкодження судин. Наразі існують поодинокі повідомлення про розвиток тромбоемболії легеневої артерії (ТЕЛА) у хворих на COVID-19, а це дає змогу припустити наявність диспропорційно високого ризику венозних тромбоемболічних ускладнень і, можливо, артеріальних тромбозів у таких пацієнтів. Результати початкових когортних досліджень свідчать про те, що розповсюдженість тромбоемболій серед хворих на COVID-19 становить 35-45% [10]. Окрім того, деякі автори припускають роль легеневої емболії як однієї з причин швидкого погіршення легеневої функції [10]. Утім, на практиці далеко не завжди є можливість проведення адекватної об’єктивної діагностики (наприклад, КТ-ангіографії) цих патологічних станів.
Окремо варто звернути увагу на результати одного з ретроспективних досліджень [4], яке включало 449 пацієнтів, госпіталізованих із тяжкою формою COVID-19. У підгрупі хворих із тяжким перебігом COVID-19, які відповідали критеріям сепсис-індукованої коагулопатії (≥4 бали за шкалою SIC) або мали підвищені рівні D-димеру (в 6 разів вище за верхню межу норми), було виявлено, що рівень 28-денної смертності був нижчим у тих хворих, які отримували низькомолекулярний гепарин (НМГ) протягом ≥7 днів, порівняно з тими, кому тромбопрофілактику не проводили (40 (40%) із 99 пацієнтів проти 224 (64%) із 350 хворих; р=0,029). Однак, на думку авторів, дані цього дослідження слід інтерпретувати з обережністю, оскільки призначення НМГ не було рандомним, а висновки були зроблені на основі множинного ретроспективного та підгрупового аналізу. Отже, щоб установити ефективність профілактичної антикоагулянтної терапії в пацієнтів із COVID-19, необхідно провести додаткові проспективні рандомізовані контрольовані випробування.
На основі наявних даних моніторинг коагулопатії в пацієнтів із тяжким перебігом COVID-19 рекомендовано здійснювати за допомогою визначення протромбінового часу, кількості тромбоцитів і рівня D-димеру кожні 2-3 дні (табл.) [5]. Деякі автори припускають користь застосування профілактичних доз НМГ із метою профілактики венозних тромбоемболій у хворих, які перебувають у критичному стані. Гіперкоагуляційний стан і потенційно підвищений ризик тромбозів у пацієнтів із тяжким перебігом COVID-19 зумовлюють необхідність призначення профілактичної терапії НМГ усім госпіталізованим хворим (за відсутності медичних протипоказань). Окрім того, хворі з тяжким перебігом COVID-19 можуть потребувати застосування антикоагулянтів у вищих дозах (не так, як зазвичай). 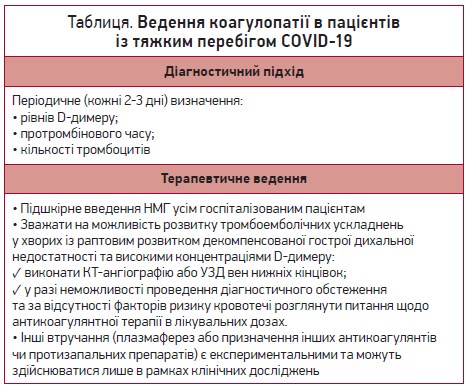
У ситуації, коли препарати НМГ є недоступними, можна призначити нефракціонований гепарин, хоча в такому разі виникне потреба в частому його введенні. Як альтернативу пропонують також застосування фондапаринуксу, проте поки що невідомо, чи має цей препарат постульовані протизапальні ефекти гепарину.
При проведенні диференційної діагностики в пацієнтів із високими концентраціями D-димеру та раптово декомпенсованою гострою дихальною недостатністю обов’язково варто врахувати ймовірність ТЕЛА, при цьому такий діагноз має бути підтвердженим візуалізаційними методами дослідження, що може спричинити деякі труднощі в клінічно нестабільних хворих. Як альтернативу можна виконати УЗД вен нижніх кінцівок, що може бути корисним для діагностики тромбозів вен нижніх кінцівок, які характерні для пацієнтів із ТЕЛА. У разі суттєвої підозри щодо наявності ТЕЛА та за неможливості проведення діагностики з метою підтвердження легеневого тромбозу слід розпочати антикоагулянту терапію в середніх терапевтичних дозах, зокрема за відсутності факторів ризику кровотечі чи наявності інших протипоказань до застосування антикоагулянтів. До того ж варто зазначити, що частота геморагічних ускладнень у пацієнтів із COVID-19 є низькою навіть за наявності тяжких порушень коагуляції [4].
Застосування інших методів антикоагулянтної терапії в пацієнтів із COVID-19 рекомендувати поки що не варто, адже ефективність такого лікування досі систематично не вивчалася, хоча проведення плазмаферезу може бути корисним для лікування тромботичної мікроангіопатії, оскільки здатне забезпечити компенсацію деяких втрачених речовин (наприклад, ADAMTS 13 або білків системи комплементу) та видалення надмірної кількості медіаторів запалення. Проте обмежена кількість даних зумовлює потребу подальшого вивчення ефективності цієї терапевтичної методики в таких хворих.
Список літератури знаходиться в редакції.
Levi M., Thachil J., Iba I., Levy J. Coagulation abnormalities and thrombosis in patients with COVID-19. Lancet Haematol. 2020; published online May 11, 2020. https://doi.org/10.1016/S2352-3026(20)30145-9.
Переклала з англ. Лілія Нестеровська
Медична газета «Здоров’я України 21 сторіччя» № 10 (479), травень 2020 р.


