8 липня, 2020
Роль пробіотиків у лікуванні дітей раннього віку з діарейним синдромом
Діарея інфекційної природи нині є одним із найпоширеніших захворювань у світі, що за частотою поступається лише гострим запальним респіраторним захворюванням. Провідне місце серед етіологічних чинників інфекційної діареї (ІД) у дітей в усьому світі займають віруси, на які припадає близько 70-80% усіх випадків ІД, на бактерії – 7-10% . За останні роки кількість випадків змішаних вірусно-бактеріальних діарей [1, 2] збільшилася до 15-17%.
Вибір методу лікування діареї у дітей залежить від її етіологічного чинника. В Україні принципи лікування гострих кишкових інфекцій (ГКІ) у дітей регламентовані наказом МОЗ України № 803 «Протокол лікування гострих кишкових інфекцій у дітей» [3] від 10.12.2007, у країнах Європейського регіону – рекомендаціями Європейського товариства педіатричної гастроентерології, гепатології та нутриціології (ESPHANG, 2014) [2], у США – рекомендаціями Товариства інфекційних захворювань (IDSA, 2017) [4].
Особлива роль у лікуванні та профілактиці діареї різної етіології у дітей належить пробіотикам. Згідно із сучасними уявленнями, які базуються на принципах доказової медицини, пробіотики допомагають скоротити тривалість діареї приблизно на 25 годин та вірогідність розвитку діареї тривалістю 4 та більше діб на 59% [5]. Сьогодні відомі механізми дії пробіотиків, що захищають шлунково-кишковий тракт (ШКТ) людини від інфекційних захворювань і є не лише простим заселенням кишечнику «корисними бактеріями», як це часто уявляють. Серед основних механізмів – посилення епітеліального бар’єру, пригнічення адгезії патогенних мікроорганізмів, конкурентне пригнічення росту патогенних мікроорганізмів, продукція антибактеріальних субстанцій та модуляція імунної відповіді [6].
Вважається, що пробіотики більш ефективні, якщо починати їх прийом на початку діареї, а також корисні для здорових немовлят і маленьких дітей із водянистими випорожненнями, які свідчать про наявність вірусного гастроентериту, а не інвазивної бактеріальної інфекції [7]. Отже, при гострому інфекційному гастроентериті рекомендується призначати пробіотикотерапію з першого дня захворювання [8]. При цьому треба взяти до уваги, що окремі штами пробіотичних мікроорганізмів проявляють певні патогенетичні властивості, які відрізняються одна від одної [2, 4, 9].
Найбільш складними у веденні пацієнтами з інфекційним гастроентеритом є діти раннього віку з затяжним перебігом діарейного синдрому (ДС, понад 7 діб) або його рекурентним перебігом. Основними причинами такого перебігу ГКІ у дітей є приєднання до провідних патогенетичних механізмів розвитку діареї (секреторного та осмотичного) двох інших – запального компоненту, який пов’язаний зі станами, що призводять до запалення та розвитку виразок слизової оболонки кишечнику (хвороба Крона, неспецифічний коліт тощо), та мальабсорбції, що є результатом осмотичної чи секреторної діареї, які призвели до зменшення площі функціонально активної слизової оболонки кишечнику або є результатом функціональної незрілості ентероцитів у дитини раннього віку [10]. Отже, у випадку затяжної діареї чи рекурентного перебігу ГКІ у дітей слід добирати такі пробіотичні препарати, які містять штами бактерій, що позитивно впливають на стан кишкової стінки: посилюють її бар’єрну здатність, зменшують прояви запалення тощо [11]. Одним із таких є Escherichia coli (E. Coli) штам Nissle 1917.
Непатогенна бактерія E. coli штам Nissle 1917 використовується в якості пробіотичного препарату для лікування як запальних, так і функціональних захворювань кишечнику. Цей пробіотик здатен попереджувати опосередковане цитокінами ушкодження слизової оболонки кишечнику. Так, відповідний штам не тільки запобігає руйнуванню бар’єра слизової оболонки ентеропатогенними кишковими паличками, але й відновлює цілісність слизової оболонки в клітинах Т84 та Сасо-2 [12]. Клінічно також був доведений антагонізм E. coli штам Nissle 1917 по відношенню до високоінвазивних штамів E. coli, ентеропатогенної E. coli 0112 ab, ентероінвазивної E. coli 0143:Н, уропатогенної E. Coli 06:К15:Н31, Candida albicans, Legionella pneumophilla strain Corbi, Listeria monocytogenes EGD, Proteus vulgaris, Salmonella enterica, Salmonella enteritidis, Shigella flexneri strain M90T, Shigella dysenteriae, Vibrio cholera, Yersinia enterocolitica [13, 14].
В якості лікувального засобу ДС непатогенна бактерія E. coli штам Nissle 1917 застосовується у живій та здатній до розмноження формі. Завдяки спеціальним адгезивним органелам (типу F-1A, F-1C і «в’юнких» фімбрій) штам має здатність прикріплятися до слизової оболонки товстої кишки та утворювати мікроколонії у вигляді біоплівки. Джгутики надають бактеріям мобільності, що є перевагою під час заселення товстої кишки, де E. coli штам Nissle 1917 виступає не тільки як антагоніст до патогенної та непатогенної мікрофлори, а й стабілізує слизовий бар’єр, впливає на метаболізм, володіє імуномодулювальними та прокінетичними властивостями. Анаеробне середовище у просвіті товстої кишки, яке створюється завдяки участі E. Coli штам Nissle 1917, підтримується тривалий час, що є надзвичайно важливим для стабільності екосистеми кишечнику та участі у багатьох метаболічних процесах зі здатністю каталізувати різні вуглеводи, цукрові спирти, амінокислоти та інші субстрати [15, 16].
Отже, непатогенна E. coli штам Nissle 1917 здатна як фізіологічна бактерія заселяти кишечник, де не всмоктується, не метаболізується, створює умови для реалізації пробіотичної і протизапальної дії і забезпечує відсутність патологічних реакцій організму на її введення.
Дослідження
Мета: оцінити ефективність пробіотика E. Coli штам Nissle 1917 у лікуванні дітей раннього віку з ІД із затяжним чи рекурентним перебігом.
Матеріали та методи. Для реалізації мети дослідження було проведено аналіз перебігу діарейного захворювання вірусної етіології у 72 дітей віком від 1 місяця до 5 років, які мали «діарейний анамнез» (тобто епізод діареї або нестійких випорожнень, чи тривалий перебіг наявного захворювання). Всі пацієнти отримували лікування в Обласній інфекційній клінічній лікарні Запорізької обласної ради. Критеріями включення до дослідження були вік дитини, наявність в анамнезі епізоду діареї або затяжний перебіг ДС під час наявного захворювання, згода батьків пацієнта на участь у дослідженні. Критеріями виключення були: наявність вроджених вад розвитку ШКТ, підтверджене хронічне захворювання ШКТ, імунодефіцит (первинний чи вторинний) та виділення із фекалій патогенної бактеріальної флори.
Усі діти були обстежені в умовах стаціонару третього рівня надання медичної допомоги (додаткові методи дослідження зстосовувалися за наявності показань). Для з’ясування етіології захворювання усім пацієнтам було проведене бактеріологічне дослідження калу на патогенну та умовно-патогенну флору (УПФ), зроблено ротатест. В усіх пацієнтів груп спостереження результати ротатесту були позитивними, отже, діти переносили ротавірусний гастроентерит.
Усі хворі з ДС отримували лікування згідно із сучасним протоколом лікування ГКІ у дітей [3]. Діти з групи спостереження випадковим методом були розподілені на дві підгрупи: в основній – 34 людини, які отримували додатково препарат Мутафлор (містить бактерії E. coli штам Nissle 1917), та 38 – у контрольній, які цей препарат не отримували. Діти груп порівняння були співставними за статтю: 15 дівчаток та 19 хлопчиків в основній групі та 18 дівчаток і 20 хлопчиків – у контрольній (рис. 1). В обох групах значна більшість учасників представлена віковою групою від 1 до 3 років.
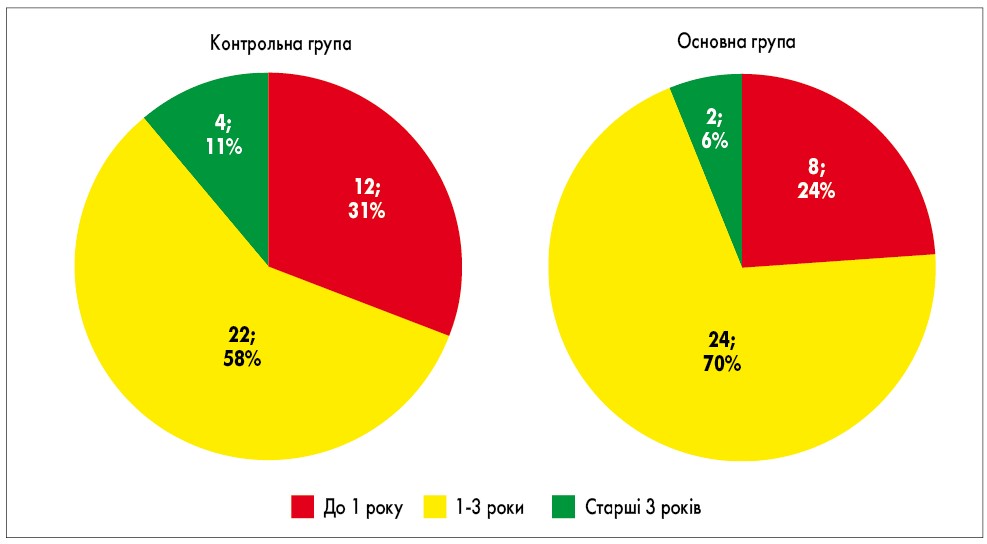 Рис. 1. Віковий скл ад пацієнтів груп порівняння
Рис. 1. Віковий скл ад пацієнтів груп порівняння
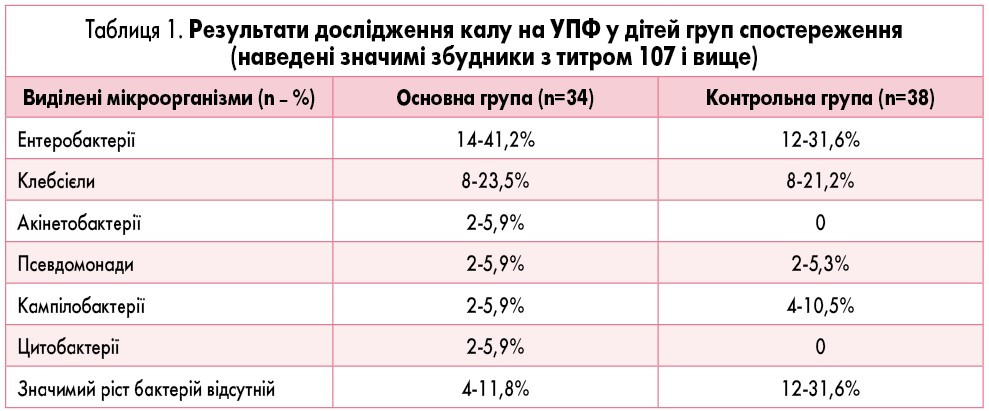
Додаткове обстеження на наявність УПФ у калі пацієнтів із високими титрами (107 та вище колонієутворювальних одиниць) показало, що у більшості (30-88,2% основної групи та 26-68,4% – контрольної) з калу були виділені відповідні бактерії. Результати цього дослідження наведені в таблиці 1.
Динаміку перебігу захворювання в обох групах оцінювали на момент потрапляння пацієнта до стаціонару, а потім на 3, 5 та 7 добу лікування. Фіксували вираженість діареї, блювання, проявів метеоризму, окремих показників загального аналізу крові (ЗАК) та копроцитограми.
Статистичну обробку отриманих результатів проведено за допомогою програмного забезпечення Excel (Microsoft, США) та Statistica for Windows 13 (StatSoft Inc., № JPZ804I382130ARCN10-J). Визначали середнє значення показника (М), стандартне відхилення середнього показника (m). Для оцінки достовірності відмінностей між кількісними ознаками застосовували критерій Стьюдента, між якісними ознаками – метод χ2.
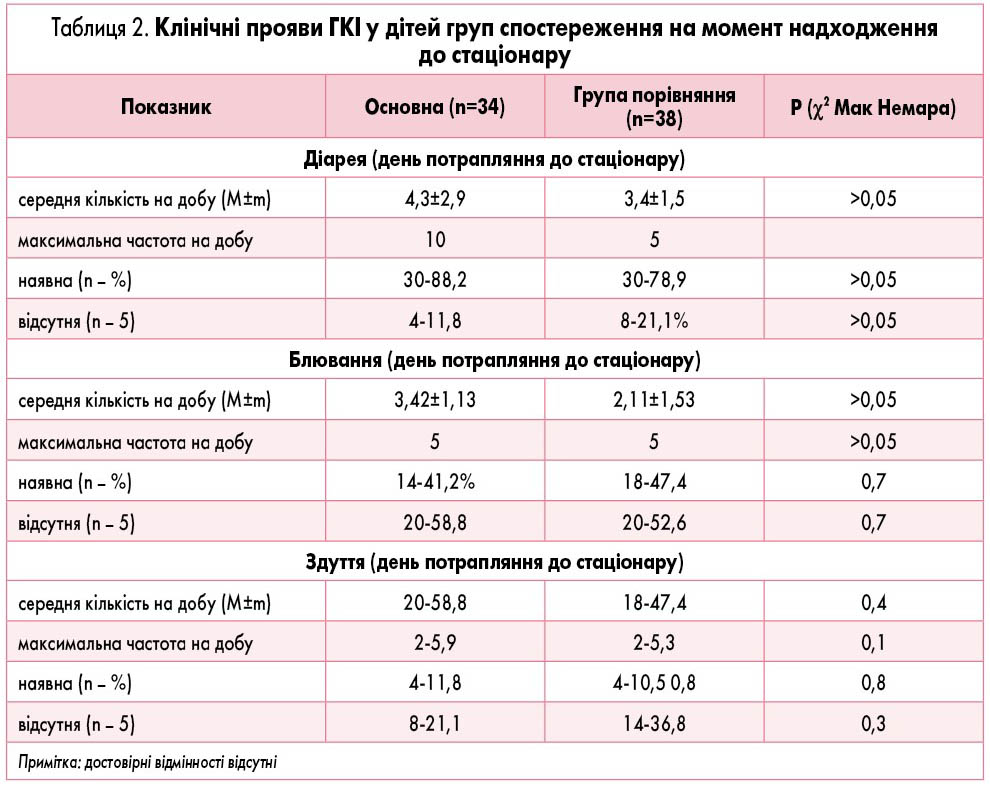
Результати та їх обговорення. Аналіз отриманих на момент госпіталізації даних показав, що діти в обох групах переважно (понад 76% в основній та 78% – у групі порівняння) потрапляли до стаціонару на 1-2 добу від початку захворювання (в середньому на 1,5±0,9 та 1,8±1,1 дня відповідно; р>0,05). Основними скаргами були діарея (таблиця 2), яка спостерігалася у 88,2% (30) хворих основної групи та у 78,9% (30) групи порівняння. Другим за частотою реєстрації був синдром здуття кишечнику із метеоризмом, який на день потрапляння до стаціонару був зареєстрований у 58,8% (20) дітей основної групи та у 47,3% (18) дітей з групи порівняння. Третім симптомом було блювання – у 41,2 та 47,4% відповідно (14 дітей з основної та 18 – із групи спостереження). Отже, на момент надходження до стаціонару за домінуючими клінічними ознаками ГКІ пацієнти в групах спостереження були співставними.
У подальшому ми оцінили частоту реєстрації основних симптомів (діареї, блювання, здуття) на 3, 5 та 7 добу перебування у стаціонарі дітей груп порівняння (кількість дітей із наявним симптомом).
Як виявилося, пацієнти із затяжною діареєю або рекурентним її перебігом позитивно реагували на додаткове введення до схеми лікування препарату, що включав бактерії E. coli штам Nissle 1917 (рис. 2-4). Так, вже на 3 добу лікування у дітей, що отримували додаткову пробіотичну терапію, у 2 і більше разів рідше реєстрували блювання (р<0,05). Також на 5 добу достовірно рідше спостерігався синдромокомплекс метеоризму (в 11,7% проти 26,3% відповідно; р<0,05). При цьому в групі дітей, які не отримували даний препарат, навіть до 5-7 доби лікування не вдалося досягти таких результатів.
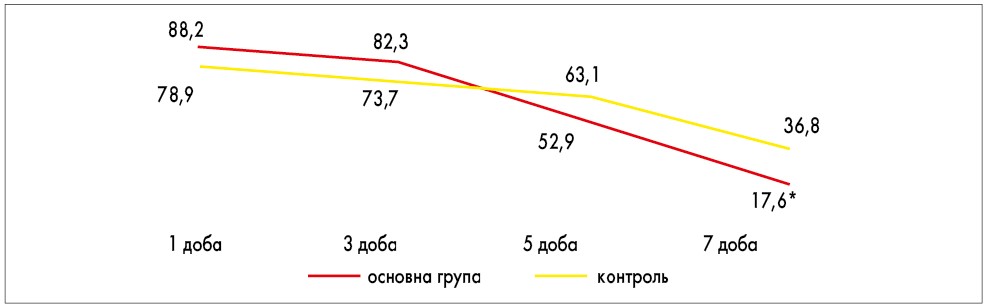 Рис. 2. Частота реєстрації діарейного синдрому в динаміці ГКІ у дітей груп порівняння (% серед обстежених)
Рис. 2. Частота реєстрації діарейного синдрому в динаміці ГКІ у дітей груп порівняння (% серед обстежених)
* достовірна різниця відносно контрольної групи
 Рис. 3. Частота реєстрації метеоризму в динаміці ГКІ у дітей груп порівняння (% серед обстежених)
Рис. 3. Частота реєстрації метеоризму в динаміці ГКІ у дітей груп порівняння (% серед обстежених)
* достовірна різниця відносно контрольної групи
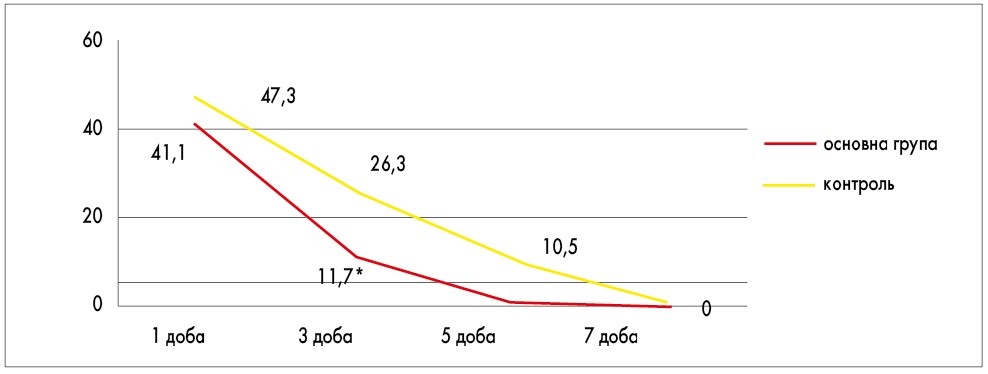 Рис. 4. Частота реєстрації блювання в динаміці ГКІ у дітей груп порівняння (% серед обстежених)
Рис. 4. Частота реєстрації блювання в динаміці ГКІ у дітей груп порівняння (% серед обстежених)
* достовірна різниця відносно контрольної групи
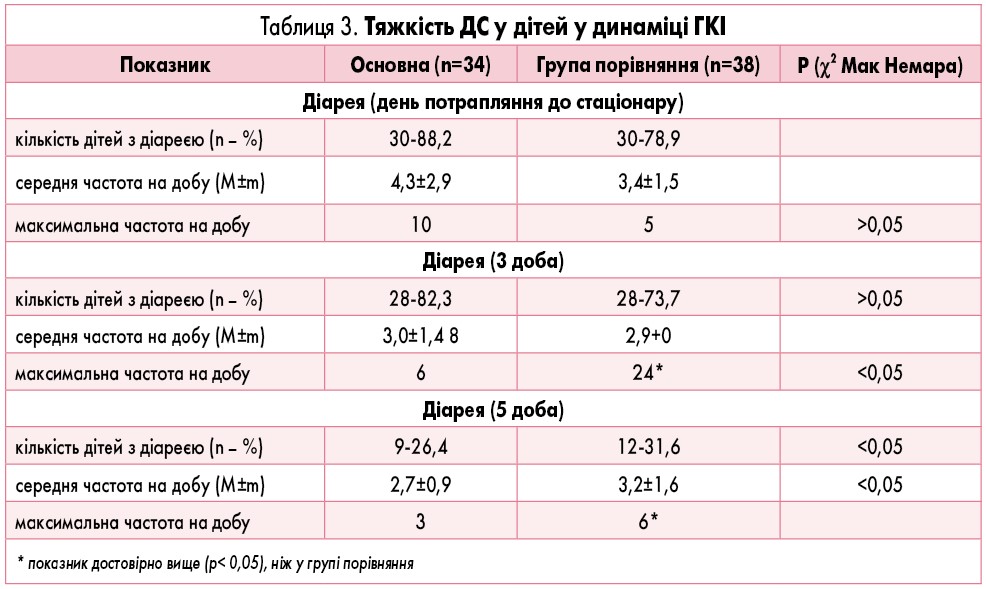
У таблиці 3 показано, що відмінності в групах порівняння стосувалися не лише динаміки частоти реєстрації основних симптомів ГКІ, а й їх виразності. Так, при додатковому введенні до схеми лікування препарату, що містить бактерії E. coli штам Nissle 1917, тяжкість ДС та здуття в переважної більшості хворих зменшувалися вже до 3 дня лікування, чого не відбувалося у групі порівняння.
Висновки
- Діарейні захворювання залишаються проблемою дитячого віку не лише через гострий перебіг із розвитком зневоднення, але й через можливість затяжного чи рекурентного перебігу.
- Визнаним терапевтичним заходом при ІД у дітей є призначення пробіотичних препаратів.
- Пробіотичний засіб, що містить бактерії E. coli штам Nissle 1917, продемонстрував свою ефективність у випадку затяжної та рекурентної діареї у дітей раннього віку, що проявилося зниженням частоти основних симптомів на 3-5 добу лікування і зменшенням їх інтенсивності.
Література
- S. Bicer, G.T. Sahin, B. Koncay et al. Incidence assessment of rotavirus and adenovirus associated acute gastroenteritis cases in early childhood. Infez Med. 2011; 19: 113-119.
- A. Guarino, S. Ashkenazi, D. Gendler, A. Lo Vecchio, R. Shamir, H. Szajewska European Society for Pediatric Gastroenterology, Hepatology and Nutrition/European Society for Pediatric Infectious Diseases evidencebased guidelines for the management of acute gastroenteritis in children in Europe: update 2014.
- Наказ МОЗ України від 10.12.2007 № 803 «Про внесення змін до Наказу МОЗ України від 09.07.2004 № 354 «Протокол лікування гострих кишкових інфекцій у дітей».
- Infectious Diseases Society of America Clinical Practice Guidelines for the Diagnosis and Management of Infection Diarrhea. – 2017.
- S.J. Allen, E.G. Martinez, G.V. Gregorio, L.F. Dans. Probiotics for treating acute infectious diarrhoea. Cochrane Database of Systematic Reviews 2010, Issue 11. Art. No.: CD003048. DOI: 10.1002/14651858. CD003048.pub3
- С.О. Крамарьов Пробіотики та інфекційні хвороби/Крамарьов С.О., Євтушенко В.В., Євтушенко О.М., Закордонець Л.В.//Актуальна інфектологія. – 2017. – Том 7, № 1. – С. 11-16.
- K. Muhsen, L. Shulman, U. Rubinstein et al. TAU-HCLVnRota Study Group. Incidence, characteristics and economic burden of rotavirus gastroenteritis associated with hospitalization of Israeli children.
Тематичний номер «Педіатрія» №3 (54) 2020 р.



.jpg)