9 червня, 2016
Лечение анемии при хронической болезни почек: роль препаратов железа
Длительное и тщательное изучение особенностей развития, течения и прогрессирования анемии при хронической болезни почек (ХБП) принесло свои плоды – в настоящее время опубликовано несколько руководств по лечению данной патологии. Наибольшую известность получили практические рекомендации, представленные медицинской общественности в 2012 г. известной международной организацией – «Болезни почек: улучшение глобальных результатов лечения» (Kidney Disease: Improving Global Outcomes, KDIGO). Несколько позже, в 2015 г., Национальный центр клинических исследований (National Clinical Guideline Centre, NCGC) по поручению Национального института здравоохранения и совершенствования медицинской помощи Великобритании (National Institute for Health and Care Excellence, NICE) опубликовал обновленное руководство по лечению анемии при ХБП. В указанных документах пристальное внимание уделяется диагностике железодефицита и эффективным способам восстановления запасов железа в организме.
Нюансы диагностики анемии при ХБП
Изучая положения вышеуказанных практических руководств, можно отметить сходства и различия мнений экспертов KDIGO и английских специалистов. В рекомендациях NCGC анемия при ХБП диагностируется на основании снижения уровня гемоглобина (Hb) ≤110 г/л (табл. 1), а по мнению экспертов KDIGO, анемию у пациентов с ХБП следует заподозрить гораздо раньше: при снижении концентрации Hb <130 г/л у мужчин или <120 г/л у женщин.
Представители KDIGO сходятся с экспертами NCGC во мнении, что первичное обследование пациентов с ХБП и анемией должно быть обширным и включать: клинический анализ крови с определением концентрации Hb, индексов эритроцитов, количества лейкоцитов и тромбоцитов, лейкоцитарной формулы, абсолютного числа ретикулоцитов, а также концентрации ферритина в сыворотке крови, НТС, содержания витамина В12 и фолатов.
Вопросы лечения
Эксперты NCGC и KDIGO единодушно настаивают на необходимости обсуждения с пациентами потенциальных преимуществ лечения препаратами железа и возможных рисков развития нежелательных реакций (анафилактический шок и др.) до назначения ферротерапии. В руководстве KDIGO указывается, что больным ХБП и анемией, не получающим ферротерапию и эритропоэз-стимулирующие препараты (ЭСП), следует рекомендовать внутривенное (в/в) введение препаратов железа, если необходимо добиться увеличения концентрации Hb, не начиная терапию ЭСП, при НТС и содержании ферритина в сыворотке крови, соответственно, ≤30% и ≤500 мкг/л. Пациентам, принимающим ЭСП, может быть также предложена в/в ферротерапия, если существует потребность в снижении дозы ЭСП, увеличении концентрации Hb при НТС≤30% и содержании ферритина ≤500 мкг/л. Эксперты KDIGO предусматривают возможность перорального приема препаратов железа для пациентов с додиализной стадией ХБП при отсутствии венозного доступа и хорошем ответе на предшествующую пероральную ферротерапию. Представители NCGC, предпочитая в/в введение препаратов железа, также допускают ситуации, в которых возможно проведение пероральной ферротерапии (табл. 2).
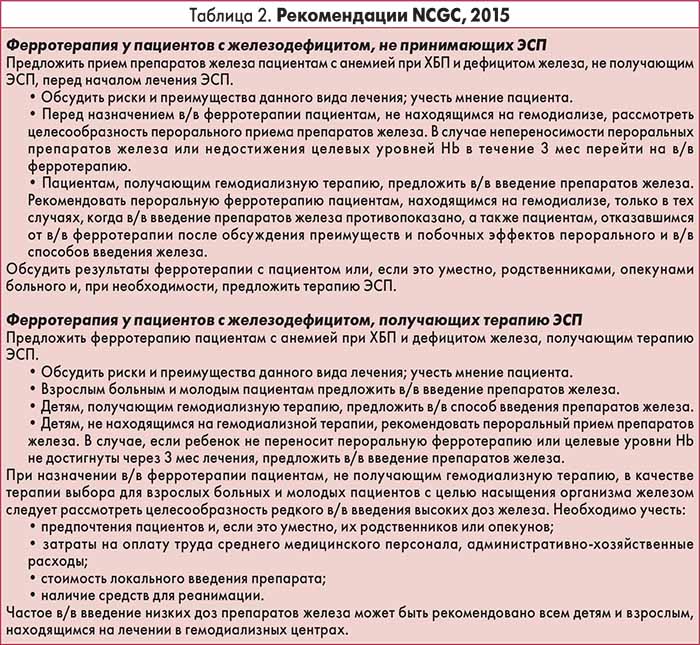
Еще одним отличием положений NCGC от рекомендаций KDIGO является разделение ферротерапии на 2 этапа: коррекцию выявленных нарушений и поддержание целевых значений показателей, характеризующих состояние обмена железа (табл. 3).

Большое внимание в рассматриваемых руководствах уделяется контролю эффективности терапии препаратами железа. Эксперты KDIGO рекомендуют оценивать состояние обмена железа (НТС, ферритин) каждые 3 мес терапии ЭСП. Представители этой авторитетной организации советуют чаще контролировать показатели обмена железа при начале терапии ЭСП или увеличении дозы этих препаратов, наличии кровопотери, оценке эффективности в/в ферротерапии. Подобного мнения придерживаются и специалисты NCGC (табл. 4).
Эксперты KDIGO и NCGC единодушно настаивают на соблюдении правил безопасности при в/в введении препаратов железа. В рекомендациях KDIGO значится: «При в/в ведении начальной дозы декстрана железа, а также при использовании других препаратов железа, синтезированных не на основе декстрана, мы рекомендуем, чтобы пациент наблюдался в течение 60 мин после инфузии; при этом должны быть доступны реанимационное оборудование и медикаменты, а также подготовленный медицинский персонал для диагностики и лечения серьезных побочных эффектов».
В рекомендациях NCGC приводится следующий алгоритм лечения анемии при ХБП (рис.).
Препараты железа для лечения анемии при ХБП
Положения рекомендаций KDIGO (2012), NCGC (2015) по лечению анемии при ХБП предусматривают проведение в/в или пероральной ферротерапии; однако в подавляющем большинстве случаев специалисты этих авторитетных организаций рекомендуют применять в/в формы препаратов железа. Наиболее приемлемым выбором с точки зрения количества проведенных исследований и наличия доказательной базы является трехвалентный гидроксид железа в виде сахарозного комплекса. Именно эта форма железа, предназначенная для парентерального введения, имеет высокую молекулярную массу, быстро транспортируется в костный мозг и эффективно восполняет дефицит железа. В отличие от лекарственных средств, содержащих железо в виде декстрана, сахарозный комплекс трехвалентного гидроксида железа лучше переносится, реже вызывает появление нежелательных реакций и более эффективно купирует проявления анемии.
В настоящее время клиницисты имеют уникальную возможность следовать международным рекомендациям по лечению анемии при ХБП, используя отечественный препарат трехвалентного железа – Суфер (производства компании «Юрия-Фарм»). Суфер представляет собой сахарозный комплекс гидроксида железа (III), в одной ампуле которого содержится 20 мг железа. Эффективность и безопасность его клинического применения неоднократно были проверены украинскими специалистами. Например, И. О. Дудар и соавт. (2014) назначали Суфер пациентам с ХБП 5D стадии, находящимся на гемодиализе и не получающим ЭСП. Препарат вводили в/в капельно в дозе 200 мг 3 раза в неделю, предварительно растворив его в 0,9% растворе хлорида натрия в соотношении 1:20. Неотъемлемым условием лечения являлось отсутствие нежелательных явлений на введение первой тест-дозы препарата. Исследователи установили, что ферротерапия с использованием Суфера сопровождалась достоверным увеличением уровня сывороточного ферритина (р<0,001) и ростом степени НСТ (р<0,001). В/в ведение сахарозного комплекса гидроксида железа (III) позволило в 76,67% случаев достичь у пациентов целевых значений ферритина и НТС, а в 40% – целевого уровня Hb. Анализируя результаты исследования, ученые подчеркнули хороший профиль безопасности препарата – при введении Суфера нежелательные реакции отсутствовали.
Подобные данные были получены в работе, выполненной под руководством А. В. Курята (2014). В этом исследовании приняли участие пациенты с ХБП I-III стадии и явлениями железодефицитной анемии (ЖДА), не получавшие ЭСП. Коррекцию явлений анемии проводили при помощи препарата Суфер, дозу которого рассчитывали индивидуально для каждого пациента. Ученые доказали, что парентеральное применение гидроксида железа (ІІІ) сахарозного комплекса способствует повышению уровней эритроцитов, Hb, ферритина, железа в плазме крови, а также сопровождается снижением концентрации креатинина (p<0,01 для всех показателей). Суфер безопасен при применении у пациентов с ЖДА, обусловленной ХБП, не вызывает существенных побочных эффектов, требующих изменения суточной дозы препарата или прекращения лечения.
Таким образом, современные рекомендации KDIGO (2012) и NCGC (2015) по лечению анемии при ХБП предусматривают в/в ведение препаратов железа. Препаратом выбора в терапии ЖДА может быть антианемическое средство отечественного производства – Суфер. Он содержит гидроксид трехвалентного железа в виде сахарозного комплекса, а его эффективность и безопасность подтверждены результатами нескольких клинических исследований.
Список литературы находится в редакции.
Подготовила Лада Матвеева





