26 червня, 2015
Инновации в урологии: устранение доброкачественной простатической обструкции посредством фотоселективной лазерной вапоризации

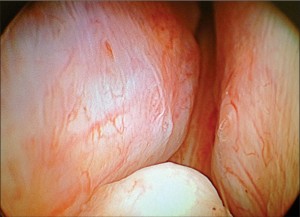
Гиперплазия парауретральных желез, гистологические признаки которой можно выявить у мужчины уже в возрасте 40 лет, способна со временем приводить к различным нарушениям мочеиспускания. Одним из них является инфравезикальная обструкция или, что более точно отражает сущность расстройства, доброкачественная простатическая обструкция (ДПО) – состояние, характеризующееся увеличением сопротивления оттоку мочи из мочевого пузыря вследствие сужения просвета уретры разрастающимися аденоматозными узлами (органический компонент) (рис. 1) и повышения тонуса гладкомышечных элементов шейки мочевого пузыря, предстательной железы и уретры (динамический компонент).
Субъективно ДПО проявляется ослаблением струи мочи, необходимостью напрягаться при мочеиспускании, ощущением неполного опорожнения мочевого пузыря. Объективно – снижением максимальной скорости мочеиспускания (Qmax) <15 мл/с, наличием остаточной мочи (ОМ) >30 см3 в сочетании с увеличением объема предстательной железы (Vпр.) >30 см3.
У большинства пациентов в течение продолжительного времени на динамический компонент ДПО можно эффективно влиять при помощи уроселективных α-адреноблокаторов. Тем не менее прогрессивное увеличение опухолевых узлов снижает восприимчивость к такого рода лечению, делая их удаление единственно возможным способом восстановления нормальной скорости мочеиспускания. С этой целью предлагаются различные трансуретральные методики, в том числе пользующаяся наибольшей популярностью и ставшая золотым стандартом электрорезекция. Однако даже она имеет ряд ограничений и не лишена недостатков. Наиболее существенный – необходимость использовать для ирригации не проводящую электрический ток жидкость. Ее попадание в системный кровоток через поврежденные в процессе процедуры венозные синусы сопряжено с риском развития угрожающего жизни состояния – ТУРП-синдрома, проявляющегося гиперволемией, нарушением электролитного баланса, гипонатриемией, гипераммониемией, гипотермией. Установлено, что при трансуретральной резекции простаты (ТУРП) всасывание ирригационной жидкости через венозные синусы происходит со скоростью около 20 мл/мин. Таким образом, вероятность возникновения ТУРП-синдрома зависит от продолжительности операции, на которую, в свою очередь, прямо влияют размер предстательной железы, необходимость прерывать процедуру для отмывания фрагментов резицированной ткани, интенсивность интраоперационного кровотечения. Указанные факторы вызывают необходимость поиска альтернативных методов хирургической коррекции ДПО.
Одним из претендентов на эту роль является фотоселективная лазерная вапоризация простаты (ФЛВП), при которой аденоматозная ткань удаляется лазерным излучением, которое подводится к месту операции по специальному волокну (световоду), предварительно введенному через функциональный канал цистоскопа. Эффект вапоризации заключается в моментальном испарении тканевой жидкости при поглощении энергии лазерного излучения. Возникающие при этом пузырьки пара, увеличиваясь в объеме, разрушают ткань с извержением продуктов деструкции в просвет мочеиспускательного канала. На месте вапоризации остается дефект в виде кратера (рис. 2).
Поскольку вместе с продуктами деструкции отводится тепловая энергия, глубоких термических повреждений ткани не возникает. Глубина коагуляционного некроза не превышает 3 мм. Избирательность поглощения энергии лазера («фотоселективность») достигается за счет использования монохромного излучения с длиной волны 532 нм, что придает ему характерный зеленый цвет. При такой длине волны энергия фотонов лазера поглощается преимущественно оксигемоглобином – красным пигментом, содержащимся в эритроцитах. Это обеспечивает сразу несколько преимуществ. Во-первых, отсутствуют потери энергии, связанные с ее поглощением в ирригационной жидкости. Во-вторых, одновременно с удалением ткани происходит герметизация сосудов, что снижает выраженность кровотечения.
Особый интерес представляют гистопатологические изменения в области лазерной раны и их эволюция. В исследованиях на собаках было продемонстрировано, что через 3 ч после аппликации литий-триборатного лазера мощностью 120 Вт в ткани предстательной железы можно выделить три отчетливые зоны: зону коагуляционного некроза толщиной 1,6 мм, которая непосредственно граничит с кратером, следующую за ней зону обратимых термических изменений (0,5 мм), где отмечается гиперемия, и, наконец, интактную область. В ходе эксперимента на третьи сутки регистрировалось частичное отторжение некротизированной ткани, а к 8-й неделе поверхность лазерной раны полностью эпителизировалась. Следует отметить, что в простатической ткани, граничащей с эпителием, не отмечалось увеличения количества коллагеновых волокон [1].
Для генерации зеленого лазерного излучения было разработано несколько систем. Во всех системах в качестве активной среды используются кристаллы. Система первого поколения PV®, основанная на кристаллах алюмоиттриевого граната, легированного неодимом (Nd:YAG), и титанилфосфата калия (KTiOPO4), характеризовалась небольшой мощностью (до 80 Вт), импульсным типом излучения и водяным охлаждением. Усовершенствование технологии генерации, в том числе замена KTiOPO4 на триборат лития, в современных системах HPS® и XPS® позволило получать квазинепрерывное излучение с оптимальной сходимостью лучей, мощность которого может достигать 120 Вт (система HPS®) и 180 Вт (XPS®). Кроме того, лазерное волокно для системы XPS® – MoXy имеет собственную систему охлаждения, что значительно повысило его устойчивость к термическим воздействиям.
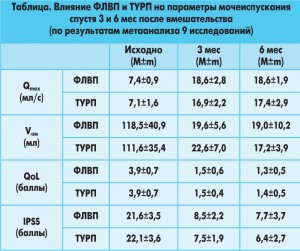
Каковы же результаты применения ФЛВП и насколько они сопоставимы с таковыми при ТУРП? Первая публикация, посвященная этому вопросу, появилась в 2000 г. [2]. Авторы оценивали кратко- (3 и 6 мес) и долгосрочные (спустя 2 года) результаты применения KTiOPO4 лазера мощностью 60 Вт в группе пациентов с доброкачественной гиперплазией предстательной железы (ДГПЖ) и средним объемом предстательной железы (43±14 мл). При этом было показано, что через 2 года после проведения ФЛВП среднее улучшение симптомов по шкале Американской урологической ассоциации составило 82%. Среднее значение Qmax на втором году наблюдения превысило исходный показатель на 278%. Среди осложнений отмечались преходящая дизурия (7%), контрактура шейки мочевого пузыря (2%), отдаленная гематурия (4%), ретроградная эякуляция (9%). С тех пор проведен целый ряд сравнительных исследований ФЛВП и ТУРП, результаты которых легли в основу нескольких метаанализов. J. Teng и соавт. [3], проанализировав 9 исследований, пришли к выводу, что эффекты ФЛВП и ТУРП, оцениваемые по динамике показателей IPSS (Международная система суммарной оценки симптомов при заболеваниях простаты), QoL (шкала, позволяющая оценить качество жизни пациентов), Qmax и Vом спустя 3 и 6 мес после вмешательства статистически достоверно не отличались (табл.).
К преимуществам ФЛВП исследователи отнесли отсутствие риска развития ТУРП-синдрома и перфорации капсулы предстательной железы, меньший уровень кровопотери, менее продолжительный период катетеризации и госпитализации, а к недостаткам – большую продолжительность вмешательства и более высокий уровень повторных операций. К таким же выводам пришли авторы другого метаанализа [4].
Влияние любой интервенционной технологии, затрагивающей предстательную железу, на сексуальную функцию должно всегда находиться под пристальным вниманием специалистов. В связи с этим интересен тот факт, что при использовании ФЛВП ретроградная эякуляция развивается реже, чем при ТУРП [5]. Кроме того, сообщается, что у некоторых пациентов этот феномен может самостоятельно разрешаться с течением времени [1].
С учетом имеющейся на сегодняшний день информации ФЛВП можно рассматривать в качестве реальной альтернативы ТУРП. Среди наиболее значимых преимуществ данной технологии следует отметить возможность продуктивно удалять аденоматозную ткань, не вызывая глубоких коагуляционных изменений в окружающих тканях, следствием которых в отдаленном периоде может стать рубцовый процесс, а также способность к термической герметизации сосудов, в основе которой лежит «тропность» хроматофоров оксигемоглобина к лазерному излучению в зеленой части спектра. Указанные особенности позволяют эффективно влиять на состояние больного, что наглядно иллюстрируется улучшением показателей IPSS, QoL, Qmax, Vом, исключить вероятность развития таких грозных осложнений, как ТУРП-синдром, а также сократить продолжительность катетеризации и пребывания больного в стационаре. Немаловажным является меньшая, чем при ТУРП, выраженность нарушений половой функции, в частности, меньшая частота развития ретроградной эякуляции. Что же касается актуальных проблем применения ФЛВП, то, несомненно, к ним относится более высокая частота повторных вмешательств и большая выраженность дизурических явлений в послеоперационном периоде. Хочется верить, что дальнейшие шаги по оптимизации генерации лазерного излучения и процедуры лазирования позволят решить их в ближайшее время.
Литература
1. Malek R.S., Kang H.W., Coad J.E., Koullick E. Greenlight photoselective 120-Watt 532-nm lithium triborate laser vaporization prostatectomy in living canines // J. of Endourology. – 2009. – 23(5). – Р. 837-845.
2. Malek R.S., Kuntzman R.S., Barrett D.M. High power potassium-titanyl-phosphate laser vaporization prostatectomy // J. Urol. – 2000. – 163(6). – P. 1730-3.
3. Teng J., Zhang D., Li Y., Yin L., Wang K., Cui X., Xu D. Photoselective vaporization with the green light laser vs transurethral resection of the prostate for treating benign prostate hyperplasia: a systematic review and meta-analysis // BJU Int. – 2013. – 111(2). – Р. 312-23.
4. Ding H., Du W., Lu Z.P., Zhai Z.X., Wang H.Z., Wang Z.P. Photoselective green-light laser vaporisation vs. TURP for BPH: meta-analysis // Asian J. Androl. – 2012. – 14(5). – Р. 720-5.
5. Capitan C., Blazquez C., Martin M.D., Hernandez V., dela Pena E., Llorente C. GreenLight HPS 120-W laser vaporization versus transurethral resection of the prostate for the treatment of lower urinary tract symptoms due to benign prostatic hyperplasia: a randomized clinical trial with 2-year follow-up // Eur.Urol. – 2011. – 60. – P. 734–9.