1 квітня, 2015
Обзор рекомендаций Европейского общества урологов (EAU) 2014 г. по диагностике и лечению синдрома сепсиса в урологии
Выводы и рекомендации
Уросепсис должен быть диагностирован на ранней стадии, особенно у пациентов с осложненными инфекциями мочевыводящих путей (ИМП). Синдром системного воспалительного ответа (ССВО), характеризующийся лихорадкой или гипотермией, гиперлейкоцитозом или лейкопенией, тахикардией, тахипноэ, является первым звеном в каскаде формирования полиорганной недостаточности.
При развитии тяжелого сепсиса или септического шока смертность пациентов значительно возрастает, однако прогноз для жизни больных при уросепсисе в целом более благоприятен по сравнению с сепсисом на фоне инфекционных очагов иных локализаций.
Лечение уросепсиса должно включать комплекс мер по поддержанию жизнеобеспечения организма, соответствующую и своевременную антибиотикотерапию, ряд вспомогательных процедур (симпатомиметики, гидрокортизон, контроль уровня гликемии) и коррекцию нарушений в работе мочевыделительной системы (уровень доказательств (УД) 1а, степень рекомендаций (СР) А). Восстановление проходимости мочевыводящих путей является основой первой линии терапии уросепсиса (УД 1b, СР А). Кроме этого, лечение больных уросепсисом должно проводиться урологом в сотрудничестве с реаниматологом и инфекционистом (УД 2a, СР B).
Уросепсис может развиваться как на фоне внебольничных, так и нозокомиальных инфекций. При этом большинство случаев уросепсиса нозокомиальной этиологии может быть предупреждено за счет мер, направленных на предотвращение персистенции внутрибольничной инфекции, например сокращения сроков пребывания пациентов в стационаре, раннего удаления катетера из мочевого пузыря, уменьшения количества эпизодов неоправданной катетеризации, рационального использования дренажных систем закрытого типа и соблюдения простых правил ежедневной асептики, позволяющих избежать перекрестного инфицирования (УД 2a, СР B).
Предпосылки
ИМП могут проявляться в виде бактериурии с ограниченной клинической симптоматикой, сепсиса или тяжелого сепсиса, в зависимости от распространенности инфекционного процесса. Диагноз «сепсис» констатируется в тех случаях, когда клинические признаки инфекционного поражения сопровождаются симптомами системного воспаления (лихорадка или гипотермия, тахикардия, тахипноэ, лейкоцитурия или лейкопения). Тяжелый сепсис определяется наличием симптомов органной дисфункции, а септический шок – упорной гипотонией, связанной с тканевой гипоксией.
Летальность при тяжелом сепсисе достигает 20-42% (по данным литературы, чаще всего эта патология связана с легочными (50%) или абдоминальными (24%) инфекциями), тогда как на долю ИМП приходится лишь 5% случаев данного заболевания. Также установлено, что сепсис более распространен среди лиц мужского пола. Несмотря на то что в последние годы заболеваемость сепсисом увеличилась на 8,7% в год, показатели обусловленной им смертности снизились, что свидетельствует о совершенствовании тактики ведения пациентов (всего с 1995 по 2000 год смертность в стационаре снизилась с 27,8 до 17,9%). За исключением уросепсиса в целом отмечается рост частоты встречаемости септических состояний, вызванных грибковой флорой, а грамположительные бактерии стали доминировать в этиологической структуре при септическом процессе, несмотря на то, что грамотрицательные микроорганизмы остаются ведущими патогенами, ответственными за формирование уросепсиса.
Тяжесть уросепсиса, как и других типов сепсиса, зависит главным образом от ответа организма. Наиболее часто уросепсис формируется у пожилых пациентов, людей с сахарным диабетом, ослабленным иммунитетом, получающих химиотерапию или кортикостероиды, больных СПИДом.
Течение уросепсиса также зависит от индивидуальных особенностей пациента, таких как камни в различных отделах мочевыделительной системы, непроходимость мочевыводящих путей на любом из уровней, наличие врожденной уропатии, нейрогенных расстройств мочевого пузыря или эндоскопических манипуляций. В то же время на него влияет специфика возбудителей, способных индуцировать воспаление в мочевыводящих путях. Кроме того, доказано, что ССВО может развиваться без участия инфекционного фактора (на фоне панкреатита, ожогов или несептического шока).
Определение и клинические признаки сепсиса в урологии
Помимо выявления симптомов заболевания, диагностика ИМП основывается на проведении физикального, ультразвукового и рентгенологического обследования, а также результатах лабораторного исследования, указывающих на наличие бактериурии и лейкоцитурии. Используются следующие определения:
• Сепсис является системным ответом организма на инфекцию. Симптомы ССВО, которые изначально считались патогномоничными для этого состояния, в настоящее время рассматриваются как сигнальные. Большинство других клинических или биологических признаков сепсиса требуют уточнения.
• Тяжелый сепсис ассоциируется с органной дисфункцией.
• Септический шок проявляется персистенцией гипоперфузии или гипотензии, несмотря на проведение инфузионной терапии.
• Рефрактерный септический шок характеризуется отсутствием положительного ответа на терапию.
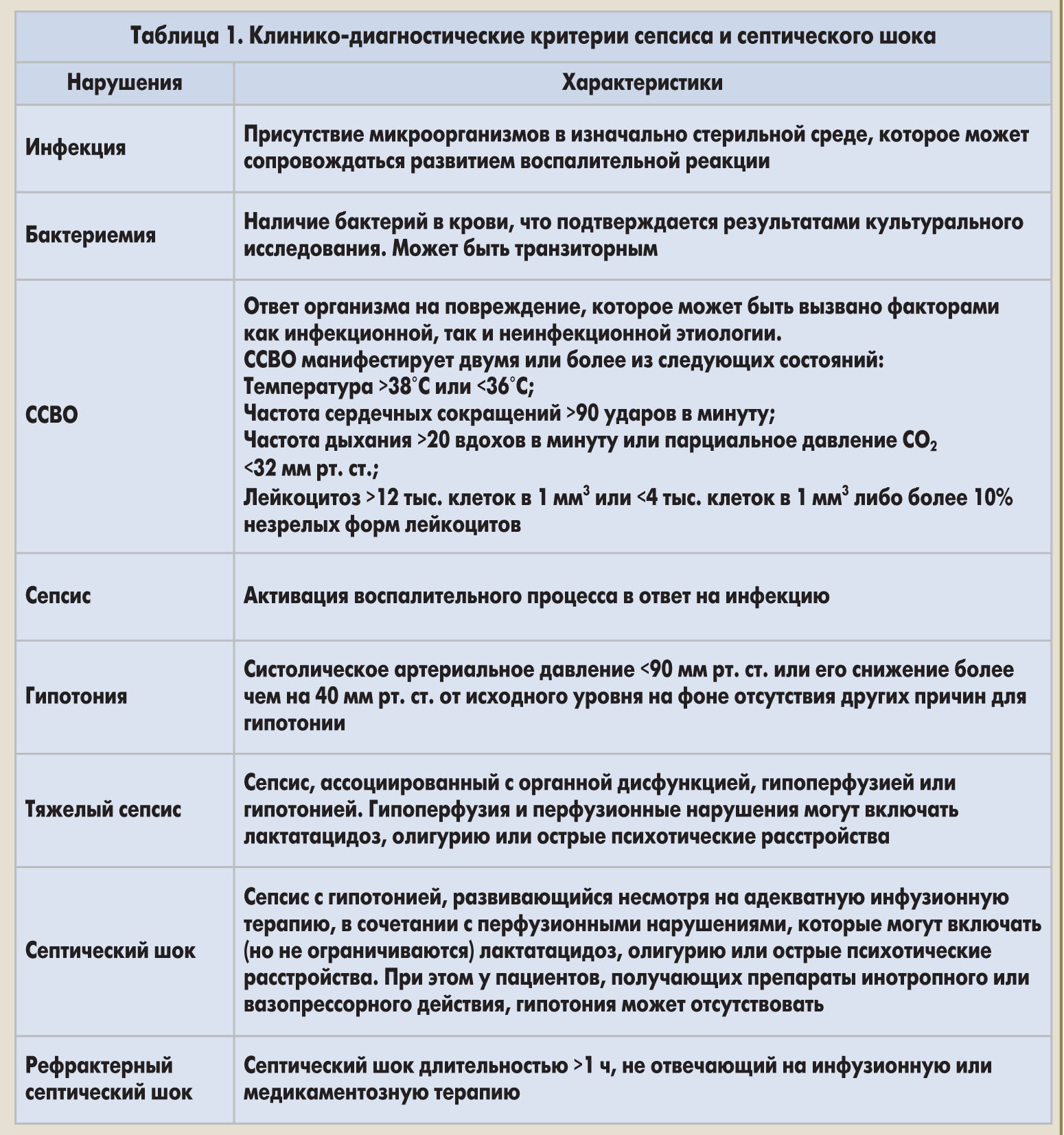
Клинико-диагностические критерии сепсиса и септического шока приведены в таблице 1.
Физиологические и биохимические маркеры
Микроорганизмы достигают мочевыводящего тракта по восходящему пути, а также за счет гематогенного и лимфогенного заноса.
В случае уросепсиса возбудители должны проникнуть в кровоток. Риск бактериемии увеличивается при тяжелых ИМП, таких как пиелонефрит и острый бактериальный простатит, облегчающих возникновение обструкции мочевыводящих путей. По-прежнему наиболее частым возбудителем сепсиса в урологии остается кишечная палочка. В ряде стран некоторые штаммы бактерий могут быть устойчивы к хинолонам или цефалоспоринам III поколения. Некоторые микроорганизмы (метициллинустойчивый золотистый стафилококк (MRSA), P. aeruginosa, Serratia spp. и др.) обладают множественной лекарственной резистентностью и трудно поддаются лечению. Чаще всего они встречаются у скомпрометированных пациентов (людей с сахарным диабетом или иммуносупрессией), обусловливая появление типичных симптомов генерализованного сепсиса, сочетающихся с местными признаками инфекции. По данным литературы, летальность при уросепсисе достигает 20-40%.
Цитокины как маркер септического ответа
Цитокины являются пептидами, регулирующими амплитуду и длительность персистенции воспалительной реакции в организме. Они продуцируются различными клетками, включая моноциты, макрофаги и эндотелиоциты, в ответ на инфекционные стимулы. При тяжелом сепсисе формируется дисбаланс в работе про- и противовоспалительной систем организма. В развитии сепсиса принимают участие такие цитокины, как интерлейкины 1, 6, 8 и фактор некроза опухоли. Сепсис является индикатором серьезных нарушений в иммунной системе, в частности ее неспособности обеспечить эрадикацию возбудителя и/или адекватный контроль над выраженностью воспалительной реакции. В ряде случаев тяжелый сепсис может быть объяснен генетической предрасположенностью.
Прокальцитонин
как потенциальный маркер сепсиса
Прокальцитонин является пропептидом кальцитонина, лишенным гормональной активности. Как правило, у здоровых людей его уровень не поддается определению. Во время тяжелых генерализованных инфекций (бактериальных, паразитарных и грибковых) с системными проявлениями уровень прокальцитонина может повышаться более чем до 100 нг/мл. В отличие от этого, при тяжелой вирусной инфекции или воспалительных реакциях неинфекционного генеза уровень прокальцитонина не изменяется или незначительно увеличивается.
Мониторинг концентрации прокальцитонина целесообразно проводить в группе пациентов, у которых существует риск развития ССВО инфекционной этиологии. Высокие уровни этого пропептида или резкое повышение его концентрации в крови у таких больных являются основанием для уточнения локализации очага инфекции в организме. В то же время определение концентрации прокальцитонина может помочь в установлении природы (инфекционной или неинфекционной) тяжелой воспалительной реакции.
Профилактика
Септический шок является наиболее частой причиной гибели пациентов, госпитализированных по поводу внебольничной и нозокомиальной инфекции (20-40%). Сепсис инициирует каскад реакций, обусловливающих развитие тяжелых форм ССВО, в том числе септического шока. В лечении уросепсиса используется комплексный подход, предусматривающий воздействие на причину заболевания (обструкцию мочевыводящих путей), мероприятия, направленные на поддержание жизнеобеспечения организма, и соответствующую антибиотикотерапию. В этой ситуации к курации пациента помимо уролога рекомендуется привлекать реаниматолога и инфекциониста.
Профилактические мероприятия с доказанной
или вероятной эффективностью
Наиболее эффективные методы предотвращения нозокомиального уросепсиса аналогичны используемым для предотвращения развития других нозокомиальных инфекций и состоят в следующем:
• изоляция всех пациентов, инфицированных мультирезистентными штаммами микроорганизмов, с целью профилактики перекрестного инфицирования;
• рациональное использование антимикробных препаратов для профилактики и лечения установленных инфекций, необходимое для предупреждения селекции резистентных штаммов. Выбор антибиотика должен зависеть от характеристик микроорганизма, преобладающего в очаге инфекции;
• сокращение сроков пребывания пациентов в стационаре (доказано, что долгое пребывание больных в стационаре перед операцией приводит к росту заболеваемости нозокомиальными инфекциями);
• максимально раннее удаление катетера из мочевого пузыря. Как известно, нозокомиальные ИМП часто обусловлены катетеризацией мочевого пузыря, а также стентированием мочеточников. Антибиотикопрофилактика не позволяет предупредить инфицирование стента, формирующееся у 100% пациентов с установленным постоянным мочеточниковым стентом и у 70% больных, перенесших временное стентирование;
• использование дренажных систем закрытого типа и минимизация рисков нарушения их целостности, в том числе при заборе проб мочи на анализ или промывании мочевого пузыря;
• использование наименее инвазивных методов устранения обструкции мочевыводящих путей до стабилизации состояния больного;
• внимание к соблюдению простых рутинных методов асептики, в том числе к регулярному использованию защитных одноразовых перчаток, частой дезинфекции рук, необходимых для профилактики перекрестного инфицирования.
Периоперационная антибиотикопрофилактика
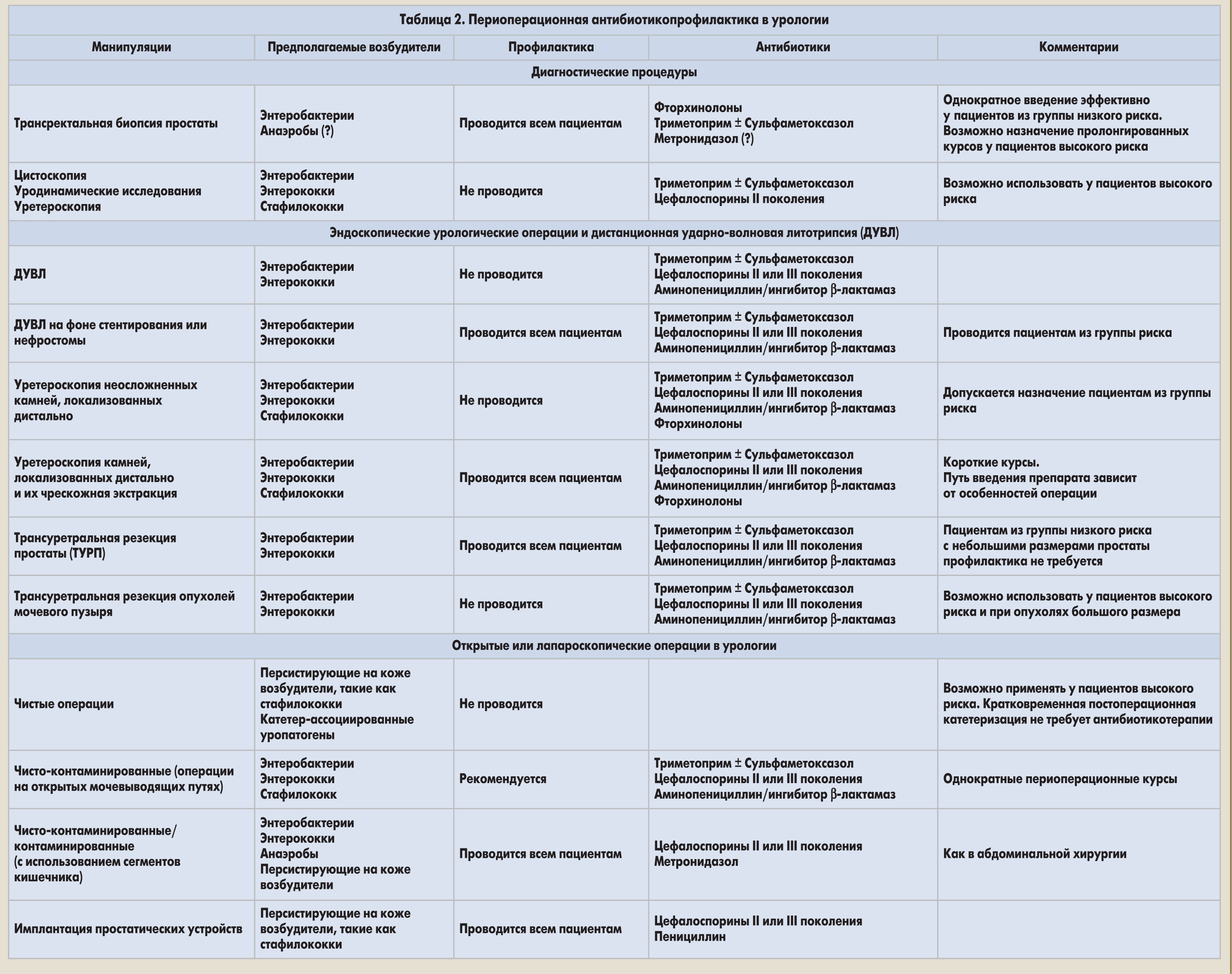
Потенциальные побочные эффекты антибиотиков должны быть учтены до их назначения. Рекомендации по использованию антибактериальных препаратов в периоперационном периоде представлены в таблице 2.
Профилактические мероприятия, эффективность которых дискутируется:
• Инстилляции антибиотиков или антисептиков в катетеры и дренажные мешки
• Использование мочевых катетеров, покрытых антибиотиками или серебром
Неэффективные меры:
• Непрерывные или периодические ирригации мочевого пузыря антибиотиками или антисептиками, которые увеличивают риск инфицирования антибиотикорезистентными бактериями
• Рутинное назначение антибактериальных препаратов катетеризированным пациентам, что на несколько дней уменьшает частоту бактериурии и увеличивает риск заражения мультирезистентными бактериями.
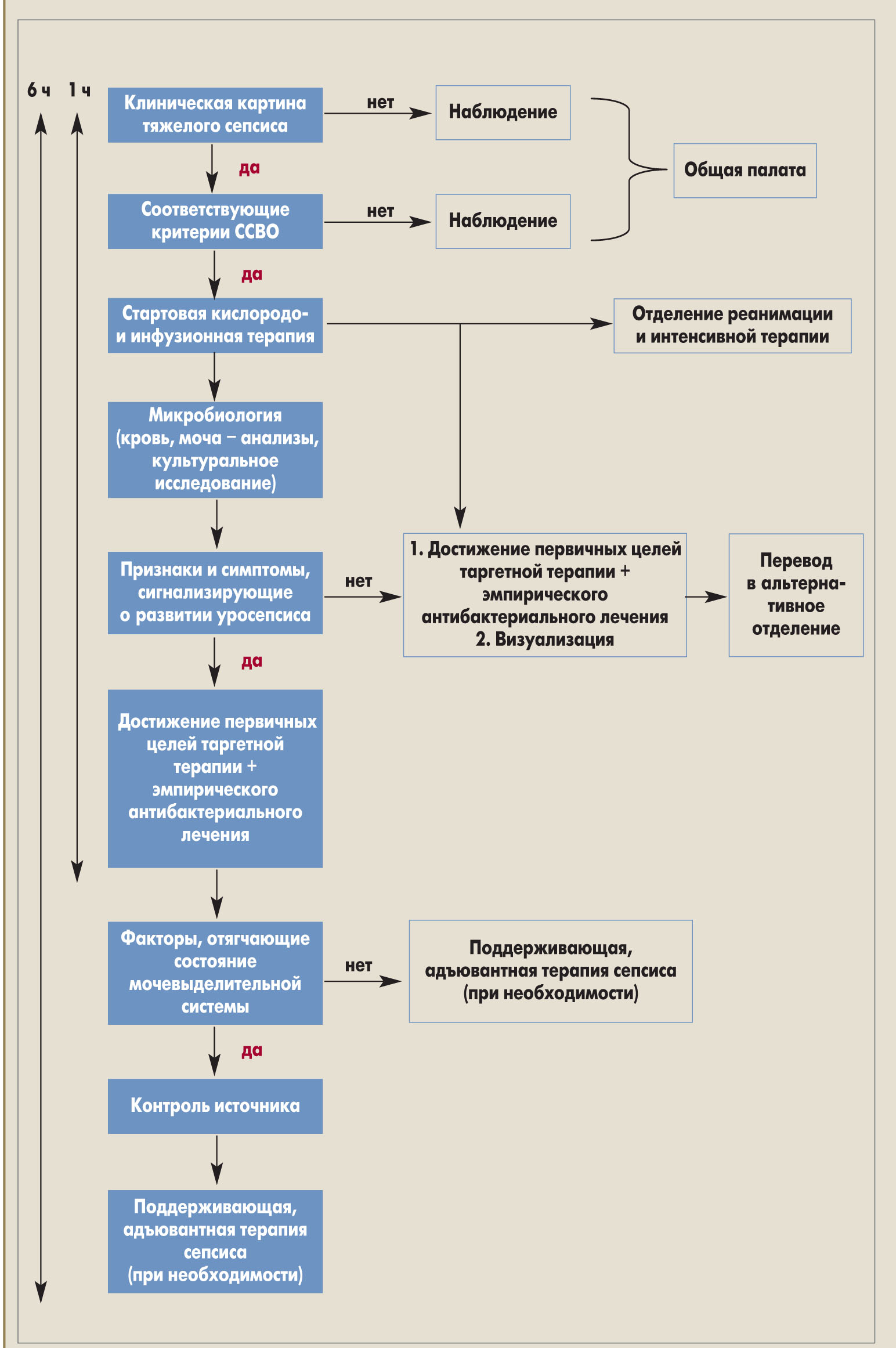
Алгоритмы лечения уросепсиса
Первичные цели таргетной терапии представлены в таблице 3.
Купирование обструкции в мочевыводящих путях
Устранение любой обструкции мочевыводящих путей с удалением инородных тел, таких как катетеры или камни, должно приводить к разрешению симптомов заболевания и выздоровлению. Восстановление проходимости мочевыводящих путей является ключевым компонентом стратегии лечения уросепсиса.
Антимикробная терапия
Стартовая эмпирическая антибиотикотерапия должна перекрывать широкий спектр потенциальных возбудителей септического процесса. Позже она модифицируется в зависимости от результатов культурального исследования. Дозировка антимикробных препаратов имеет первостепенное значение у пациентов с синдромом сепсиса, у которых, как правило, она бывает высокой, за исключением людей с почечной недостаточностью. Противомикробные средства должны быть назначены пациенту не позднее чем через 1 ч после постановки предварительного диагноза «сепсис».
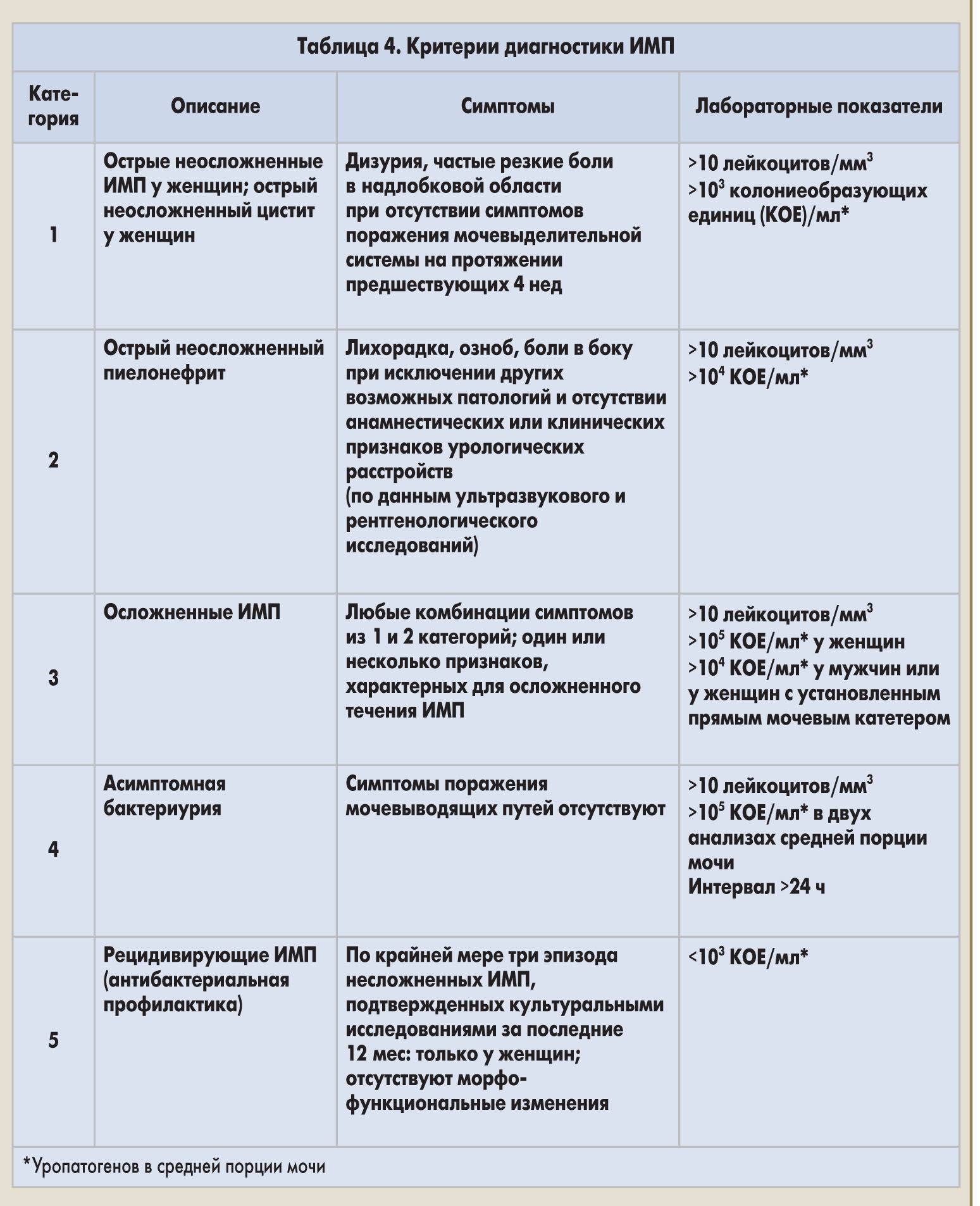
Критерии диагностики ИМП, модифицированные в соответствии с рекомендациями Американского общества инфекционных болезней / Европейского общества клинической микробиологии и инфекционных болезней, приведены в таблице 4.
Сопутствующая терапия
Контроль баланса жидкости и электролитов является одним из важнейших аспектов ухода за пациентами с синдромом сепсиса, особенно осложненного шоком. Целесообразность использования человеческого альбумина остается спорной. Доказано, что ранняя целенаправленная терапия приводит к снижению смертности пациентов. Коррекция объема циркулирующей крови и назначение препаратов вазопрессорного действия оказывают значительное влияние на исход заболевания. Раннее вмешательство в процессы тканевой перфузии и транспорта кислорода при помощи своевременной инфузионной терапии и стабилизации артериального давления являются весьма эффективными.
Гидрокортизон (оптимальная дозировка уточняется) оказывается полезным у пациентов с относительной недостаточностью системы гипофиз – кора надпочечников.
Жесткий контроль уровня глюкозы в крови с помощью введения инсулина в дозах до 50 ЕД/ч ассоциируется со снижением смертности.
Имеющиеся данные не подтверждают целесообразности использования человеческого рекомбинантного активированного протеина C у взрослых и детей с тяжелым сепсисом и септическим шоком.
Выводы
1. Синдром сепсиса в урологии представляет серьезную проблему, поскольку это состояние ассоциируется с высоким уровнем летальности (20-40% пациентов).
2. Ранняя диагностика симптомов сепсиса может снизить уровень летальности от данной патологии при условии своевременной коррекции нарушений в мочевыводящих путях, таких как обструкция или уролитиаз.
3. Рациональное использование подходов к поддержанию жизнеобеспечения организма и адекватная антибиотикотерапия создают наиболее благоприятные условия для улучшения выживаемости пациентов.
Сокращенный перевод с англ. Антона Пройдака
Полная версия руководства доступна на английском языке по адресу:
http://www.uroweb.org/