4 жовтня, 2016
Обзор рекомендаций по лечению пневмонии у детей
Успехи в лечении пневмонии у детей, без преувеличения, являются одними из значимых достижений медицины последних десятилетий. Пневмония с верхних строчек списка наиболее частых причин детской смертности переместилась в конец перечня. Однако, несмотря на заметный прогресс в этой области, проблема пневмонии детского возраста не стала менее актуальной. Высокая распространенность, диагностические ошибки, несвоевременность оказания медицинской помощи, возрастающая роль атипичной флоры в качестве этиологического фактора и, наконец, вопрос антибиотикорезистентности – все эти факторы не позволяют рассматривать пневмонию у детей в качестве рядовой и решенной проблемы.
Внедрение в отечественную практику принципа доказательной медицины, безусловно, не обошло стороной педиатрию. С одной стороны, систематизация накопленных врачами всего мира знаний об этиологии и эффективных методах терапии пневмонии призвана помочь практикующему врачу. Однако если этиология, патогенез и диагностические критерии пневмонии описаны в современных руководствах достаточно однозначно, то вопрос терапии оставляет для практикующего врача широкое поле выбора лекарственных препаратов, прежде всего антибактериальных. Важно помнить, что этиотропное лечение в случае пневмонии – ключ к выздоровлению, поэтому рациональный выбор антибиотика при бактериальных формах заболевания является важнейшей и первоочередной задачей.
Что же такое пневмония? Несмотря на изменившиеся в последние годы взгляды на многие фундаментальные вопросы этиологии, патогенеза и тактики лечения этой болезни, классическое определение родом из 80-х годов прошлого столетия остается востребованным и сегодня. Итак, внегоспитальная (внебольничная) пневмония (ВП) представляет собой острое инфекционное заболевание легких различной, преимущественно бактериальной, этиологии, развившееся вне больницы или в первые 48-72 ч госпитализации, сопровождаемое лихорадкой и симптомами поражения нижних дыхательных путей (одышка, кашель и физикальные данные), при наличии инфильтративных изменений на рентгенограмме. Важно отметить, что ВП – это острое инфекционное заболевание, поэтому определение «острая» перед диагнозом «пневмония» является излишним. В соответствии с классификацией МКБ-10 по этиологии выделяют следующие формы пневмонии: бактериальная, вирусная, грибковая, паразитарная, хламидийная, микоплазменная, смешанная (J12-J18). Низкая информативность и значительная продолжительность микробиологических исследований, а также практика приема антибактериальных препаратов (АБП) до обращения за медицинской помощью, широко распространенная в нашей стране ввиду безрецептурного отпуска любых антибиотиков в аптеках, становятся причинами фактического отсутствия этиологического диагноза у 70% и более детей с ВП. Несмотря на попытки многих авторов систематизировать дифференциальные признаки пневмонии той или иной этиологии, широкого применения такое разделение не получило. Тем не менее, ввиду необходимости эмпирического назначения антибиотика, этиология ВП – вопрос, который встает перед каждым врачом, имеющим дело с пневмонией.
Итак, фактом остается утверждение, что на момент назначения лечения возбудитель пневмонии почти всегда не идентифицирован. Исходя из этого утверждения, решение о назначении антибиотика должно определяться двумя факторами:
• распространенностью патогенов у детей различных возрастных категорий;
• определенными клиническими признаками, характерными для специфических патогенов.
Многие специалисты сегодня констатируют наличие определенной зависимости между возрастом ребенка и восприимчивостью к тем или иным возбудителям пневмонии. Так, по данным В. К. Таточенко (2008) и А. Г. Чучалина (2011), ВП у детей 6 мес – 5 лет чаще всего (70-88%) ассоциирована со Streptococcus pneumoniae. Haemophilus influenzae типа b выявляют значительно реже – до 10% случаев; вместе с пневмококком она обусловливает большинство случаев пневмоний, осложненных легочной деструкцией и плевритом. Стафилококки выделяют относительно редко. Атипичные пневмонии, вызванные Mycoplasma pneumoniae, наблюдают у 15% больных, а вызванные Chlamydia pneumoniae, – у 3-7%. Из вирусов в этом возрасте чаще всего выявляют респираторно-синцитиальный вирус (РС-вирус), вирусы гриппа и парагриппа, рино- и аденовирусы, часто в ассоциации с бактериальными возбудителями. При смешанной вирусно-бактериальной инфекции вирус, очевидно, выступает как фактор, способствующий инфицированию нижних дыхательных путей бактериальной флорой. Именно поэтому многие авторы сегодня рассматривают вирусную пневмонию в качестве более раннего этапа бактериальной ВП.
У детей старше 5 лет Streptococcus pneumoniae также остается ведущим возбудителем пневмонии – 35-40% всех случаев ВП, но в то же время возрастает роль и атипичной микрофлоры – атипичные пневмонии, вызванные M. pneumoniae и C. pneumoniae, выявляют у 23-44% и 15-30% соответственно. H. influenzae типа b практически не выявляют, в редких случаях пневмонию вызывает гемолитический стрептококк, распространяющийся лимфогенно из очага в миндалинах. По данным некоторых авторов, C. pneumoniae и M. pneumoniae чаще всего вызывают пневмонию у детей школьного возраста (Crawford S. E., Daum R. S., 2008; Бруснигина Н. Ф., Мазепа В. Н. и др., 2009; Чучалин А. Г. и др., 2011). К редким (3-5%) возбудителям ВП у детей этой возрастной группы относятся: H. influenzae, S. aureus и K. pneumoniae. В очень редких случаях ВП может вызывать Pseudomonas aeruginosa (у больных муковисцидозом). Значительная часть случаев ВП (8-40%) обусловлена смешанной вирусно-бактериальной инфекцией. Необычную этиологию ВП (Candida spp., Aspergillus spp., Pneumocystis jiroveci) следует предполагать у ВИЧ-инфицированных детей, а также у получавших иммуносупрессивную терапию или поступающих в тяжелом состоянии. Риск грамотрицательной этиологии или полирезистентного возбудителя высок при подозрении на аспирацию, антибактериальную терапию в предшествующие три месяца у детей, посещающих детские дошкольные учреждения, а также имеющих хронические заболевания респираторной системы. В целом независимо от тяжести больных в этиологии ВП доминирует S. рneumoniaе, однако по мере нарастания тяжести увеличивается удельный вес Staphylococcus aureus, Legionella рneumophila, H. influenzae и энтеробактерий, а значение M. pneumoniaе и C. pneumoniaе уменьшается (Don M., Canciani M., Korppi M., 2010). Резистентность патогенной флоры к антибиотикам является серьезной проблемой современной медицины. У больных с ВП этот вопрос особенно остро стоит в случаях наличия хронических заболеваний с частым применением антибиотиков в анамнезе, а также у детей, пребывающих в закрытых коллективах (интернат, дом ребенка). Говоря об уровнях устойчивости пневмококков к основным АБП (амоксициллин, амоксициллин/клавуланат, цефтриаксон, макролиды), важно отметить, что, несмотря на пристальное внимание к вопросу, резистентность не превышает 0,3-6,7% (Чучалин А. Г., Синопальников А. И. и др., 2010), при этом в большинстве случаев выявляются умереннорезистентные штаммы.
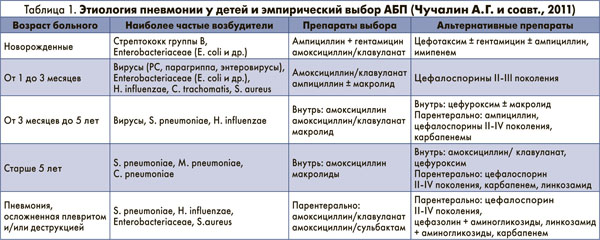
Переходя к вопросу эмпирического назначения АБП при ВП, важно подчеркнуть, что необходимо учитывать не только возраст ребенка и природную активность препаратов к предполагаемым патогенам, но и распространенность и характер резистентности возбудителей (табл. 1).
В руководстве «Внебольничная пневмония у детей: распространенность, диагностика, лечение и профилактика» (2011) содержится ряд рекомендаций по выбору АБП с учетом вышеописанных критериев. Так, препаратами выбора для лечения пневмококковой ВП являются β-лактамы: аминопенициллины (амоксициллин – внутрь, ампициллин парентерально только у новорожденных), в том числе ингибиторозащищенные (амоксициллин/клавуланат), а также цефалоспорины II-III поколения (цефуроксим, цефотаксим, цефтриаксон). Пневмококки лишены способности продуцировать β-лактамазы; механизм их резистентности к β-лактамным антибиотикам обусловлен модификацией пенициллиносвязывающего белка, в результате чего повышается минимальная подавляющая концентрация (МПК) этих препаратов и снижается клиническая эффективность. Карбапенемы и цефалоспорины III-IV поколения для парентерального применения в тяжелых и осложненных ситуациях, как правило, сохраняют высокую активность в стандартных дозах. Амоксициллин также сохраняет активность против пенициллинрезистентных пневмококков, но для надежного клинического эффекта целесообразно использование высоких доз препарата. Макролидные антибиотики являются альтернативными препаратами (в частности, при аллергии на β-лактамы). Респираторные фторхинолоны могут использоваться только с учетом возрастных ограничений. Аминогликозиды не имеют клинически значимой активности в отношении S. pneumoniae и не должны использоваться в стартовой терапии ВП у больных старше 6 месяцев. Препаратами выбора для лечения ВП, вызванной H. influenzae, являются аминопенициллины (амоксициллин внутрь) и АБП, активные в отношении штаммов, продуцирующих β-лактамазы (амоксициллин/клавуланат, амоксициллин/сульбактам, цефалоспорины II-III поколения), карбапенемы. Наибольшей природной активностью в отношении атипичных возбудителей ВП обладают макролиды. Тетрациклины (доксициклин) и респираторные фторхинолоны имеют возрастные ограничения и могут ограниченно использоваться лишь у подростков. Препаратом выбора при стафилококковых пневмониях является оксациллин, альтернативой могут быть амоксициллин/клавуланат, амоксициллин/сульбактам, цефалоспорины I поколения, линкозамиды.
Выбирая АБП, важно учитывать способ введения того или иного препарата. Сегодня, когда современные таблетированные формы препаратов не уступают по биодоступности парентеральным, безусловно, предпочтение следует отдавать средствам для приема внутрь. В тяжелых случаях ВП, требующих парентерального введения АБП, нельзя забывать о возможностях ступенчатой терапии, основная идея которой заключается в уменьшении длительности парентеральной антибиотикотерапии, что обеспечивает значительное уменьшение стоимости лечения и сокращение срока пребывания ребенка в стационаре при сохранении высокой клинической эффективности. Оптимальным вариантом ступенчатой терапии является последовательное использование двух лекарственных форм (для парентерального введения и приема внутрь) одного и того же антибиотика, что обеспечивает преемственность лечения. Однако абсолютно допустимо последовательное применение препаратов, близких по своим антимикробным свойствам и с одинаковым уровнем приобретенной устойчивости (например, ампициллин на амоксициллин; цефотаксим, цефтриаксон на цефиксим). Переход с парентерального на пероральный антибиотик осуществляют при стабилизации состояния пациента, нормализации температуры и улучшении клинической картины ВП, обычно через 2-3 дня после начала лечения.
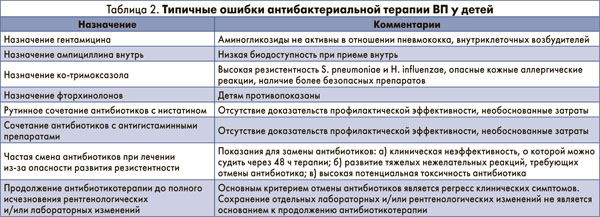
Оценка эффективности назначенного АБП проводится через 24-48 часов от начала терапии. Лечение пневмонии требует использования достаточных доз эффективного антибиотика в течение оптимального периода времени. В большинстве случаев продолжительность лечения колеблется в пределах от 7 до 14 дней. Длительность АБТ должна определяться наличием сопутствующих заболеваний и/или бактериемии, тяжестью и особенностями течения заболевания. При пневмонии, вызванной S. рneumoniae, оптимальная длительность терапии составляет 7-10 дней, M. рneumoniae – 10-14 дней (Community Acquired Pneumonia, Guideline 14, 2005). АБТ может быть завершена при устойчивой нормализации температуры тела на протяжении 3-4 дней (Чучалин А. Г., Синопальников А. И. и др., 2010). В последние годы наблюдается тенденция к сокращению сроков использования АБП даже при тяжелом варианте течения ВП (Таточенко В. К., 2005). Однако эксперты ATS/IDSA предлагают минимальную продолжительность потенциально эффективной АБТ в течение 5 дней. Индикаторами качества медицинской помощи у госпитализированных больных с ВП являются: у всех больных – обязательное рентгенологическое исследование в течение 24 часов с момента госпитализации, исследование мокроты; при тяжелой ВП до начала АБТ: бактериологическое исследование крови, введение АБП в первые два часа с момента госпитализации, ступенчатая терапия, рекомендации по вакцинации больных групп риска (Чучалин А. Г., Синопальников А. И. и др., 2010; 2011). Не рекомендуется для оценки качества использовать показатели летальности, длительности лечения, частоты осложнений (Community Acquired Pneumonia, Guideline 14, 2005). Типичные ошибки в назначениях АБП резюмированы в таблице 2.
В 2011 г. Британским торакальным обществом были опубликованы рекомендации по ведению детей с ВП (British Thoracic Society guidelines for themanagement of community acquired pneumonia in children).
Опорные рекомендации руководства:
• амоксициллин рекомендован в качестве перорального АБТ выбора в лечении ВП у детей, поскольку он эффективен в отношении большинства возможных патогенов, хорошо переносится, имеет невысокую стоимость. Альтернативой амоксициллину являются амоксициллина клавуланат, цефаклор, макролиды;
• макролиды могут быть включены в терапию ВП у детей любого возраста в случаях неэффективности препаратов первой линии;
• макролиды должны быть использованы при подозрении на наличие атипичных патогенов, а также в случаях тяжелого течения ВП;
• при смешанных ВП (бактериальные ассоциации с вирусами) препаратом выбора является амоксициллин/клавуланат;
• пероральные формы АБП эффективны и безопасны даже при тяжелых формах ВП, следовательно, предпочтение должно быть отдано именно таким формам;
• парентеральное использование АБП при ВП оправдано в случаях невозможности использования пероральных средств (например, нарушение всасывания, выраженная рвота), а также при наличии признаков септикемии или осложнений пневмонии;
• к парентеральному использованию при ВП могут быть рекомендованы амоксициллин, амоксициллина клавуланат, цефуроксим, цефотаксим, цефтриаксон;
• переход от парентеральных антибиотиков к пероральным должен быть осуществлен в клинически оправданные, но максимально ранние сроки.
Эксперты ВОЗ (бюллетень 2015 г.) предпочтительным антибиотиком для лечения пневмонии называют амоксициллин в диспергируемых таблетках. С клинической точки зрения диспергируемая лекарственная форма обеспечивает стабильное и прогнозируемое терапевтическое действие и снижает вероятность побочных реакций, в частности развитие диареи и диспепсических расстройств. Контролируемое высвобождение активного вещества обеспечивает также и маскировку его вкуса, что повышает приверженность пациентов лечению. Из состава наполнителей таблеток Солютаб исключены сахар, глютен, что снимает ограничения у пациентов с соответствующей патологией. Диспергируемые таблетки в форме Солютаб обеспечивают удобство применения: суспензия готовится из таблетки непосредственно перед каждым применением, в отличие от традиционных суспензий. Традиционно приготовленные суспензии зачастую требуют специальных условий хранения (в холодильнике, темном месте), что нередко не соблюдается родителями. Неправильное приготовление и хранение готовой суспензии может снижать эффективность антибактериальной терапии. Именно поэтому эксперты ВОЗ отдают предпочтение диспергируемым таблеткам: с их помощью антибактериальный препарат легко дозировать, готовить и хранить.
Национальные рекомендации, утвержденные МЗ Украины, по лечению ВП в качестве препаратов стартовой терапии ВП называют полусинтетические пенициллины – амоксициллин, в качестве альтернативы – амоксициллина клавуланат, макролиды. При этом макролидные антибиотики следует назначать не только в случаях аллергии на пенициллины, но и для лечения детей (прежде всего школьников и подростков) с признаками респираторной атипичной инфекции (микоплазмы, хламидии, легионеллы). С учетом рекомендованных сроков лечения (не менее 5 дней), вопросов безопасности и профилактики селекции резистентности макролидными антибиотиками выбора можно считать 16-членные препараты (прежде всего джозамицин).
Исходя из вышеизложенного, вполне логично, что в амбулаторной практике для лечения пневмонии наиболее применяемыми в Украине и Европе АБП являются амоксициллин, амоксициллин/клавуланат для перорального применения.
В заключение необходимо еще раз подчеркнуть, что определяющими для благоприятного течения и исхода ВП у детей являются ранняя диагностика заболевания, а также своевременно, обоснованно и разумно назначенный антибактериальный препарат, являющийся основой этиологического лечения пневмонии.
Подготовила Александра Меркулова
Медична газета «Здоров’я України» № 17 (390), вересень 2016 p.