11 грудня, 2020
Пацієнт із болем у спині під кутом 360 градусів: погляд невролога та гастроентеролога
26 листопада відбувся вебінар «Пацієнт із болем у спині – погляд на 360 градусів: невролог і гастроентеролог», який відвідали терапевти, сімейні лікарі та неврологи. Під час заходу було розглянуто проблему болю в спині, не лише аспекти діагностики та терапії, а й профілактику ускладнень такого стану. Біль у спині, зокрема в нижній її частині, є надзвичайно частою проблемою в щоденній практиці лікарів багатьох спеціальностей, тому актуальність точної диференційної діагностики й оптимального лікування складно переоцінити.
.jpg) Завідувач кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету, доктор медичних наук, професор Михайло Михайлович Орос присвятив свій виступ неспецифічним сакралгіям.
Завідувач кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету, доктор медичних наук, професор Михайло Михайлович Орос присвятив свій виступ неспецифічним сакралгіям.
Сакроілеальний суглоб (СІС) оточений однією з найбільших і найпотужніших груп м’язів тіла, але жоден з них безпосередньо не впливає на рух цього суглоба. Втім, унаслідок скорочення цих м’язів може відбуватися рух на стику СІС. На рухи в цьому суглобі впливають 22 м’язи, починаючи від найширшого м’яза спини та закінчуючи кравецьким. 8 із цих м’язів також прикріплені до крижів; деякі інші перетинають суглоб, але забезпечують ключову функцію у встановленні та підтримці осей руху чи стабілізації суглоба. СІС бере участь у підтримці рівного вертикального положення тіла та ходьбі. За наявності запалення або дегенеративних змін СІС з’являється кульгання, оскільки для уникнення болю пацієнт намагається розвантажити уражений суглоб. При дисфункції СІС біль є не лише в нозі, а й навіть у голові та шиї, що пояснюється переданням патологічного натягу по м’язах; для його зняття в таких випадках доцільно призначати міорелаксанти, наприклад, тизанідин, включений до американських і європейських рекомендацій з лікування неспецифічного болю в спині. На противагу толперизону, який показаний лише для симптоматичного лікування м’язового спазму в дорослих пацієнтів, що перенесли інсульт, показаннями до застосування тизанідину є болісний м’язовий спазм, спастичність унаслідок розсіяного склерозу й ушкоджень спинного та головного мозку. До лікування тизанідином доцільно додавати диклофенак (Диклак®, фармацевтична компанія «Сандоз»). Така комплексна терапія дозволяє усунути не лише спастичний компонент болю, а й запальний. Застосування препарату Диклак® насамперед є ефективним при залученні суглобів до патологічного процесу в м’язах.
СІС властиві значні зміни з віком. Так, у препубертаті СІС описуються як пласкі поверхні, на яких можуть відбуватися незначні ковзання у всіх напрямах. Після статевого дозрівання розвивається гребінь у формі півмісяця, що тягнеться всією поверхнею здухвинної кістки (з відповідним заглибленням на сакральному боці). Гребінь та паз існують для взаємної фіксації поверхонь й підвищення стабільності суглоба. Через подальші вікові зміни відбувається огрубіння суглоба внаслідок збільшення маси тіла та м’язових навантажень. За ненормальних умов навантаження в СІС створюється нове положення, за якого гребінь та паз більше не доповнюють один одного. Така аномальна позиція може розглядатися як блокований суглоб. Зміни здухвинної кістки послідовно проявляються зазвичай на третьому десятку життя в чоловіків і на четвертому-п’ятому – в жінок. До цього звуження суглобової щілини, склероз, кісти й ерозії суглобових поверхонь можна помітити на рентгенівських знімках і під час комп’ютерної томографії. На початкових стадіях ці зміни перебігають непомітно. Відсутність суглобової щілини на рентгенівських знімках є ознакою анкілозуючого спондиліту, який переважно виявляють у молодих людей; якщо його виявлено в старшому віці, ймовірно, він є наслідком захворювання в молодому віці.
Зростання тонусу m. erector spinae та напруження між тораколюмбальною фасцією і здухвинною кісткою створює силу СІС, що стабілізує таз. Унаслідок такого зв’язку будь-які проблеми з боку м’язів сприяють дисфункції суглобів (і навпаки). Аналіз причин болю в нижній частині спини (БНЧС) показав, що найчастішою з них є розлади з боку хребта (65%). Дисфункція СІС спричиняє БНЧС у 5%, а дисфункція кульшового суглоба – у 2,5%. На решту відсотків припадають комбіновані ураження, а в 10% випадків причину виявити не вдається.
Тактика сімейного лікаря при БНЧС передбачає насамперед рентген-діагностику, яка дає змогу виявити запальні та дегенеративні зміни. За дегенеративних змін суглобова щілина зберігається, а при запальних – звужується. Причинами БНЧС можуть бути вагітність, інфекції, пухлини, переломи, запальна артропатія, травми, хірургічні втручання, проблеми зв’язок і сухожилків. Часто зустрічається також ідіопатичний біль, що є наслідком адаптації рухового стереотипу при патології певної рухової ланки (СІС, лобкового симфізу, тазових органів) і при внутрішньо- та позасуглобових ураженнях кульшового суглоба. Під час збирання анамнезу необхідно звернути увагу на тривалість і перебіг вагітності, ураження поперека, кульшового суглоба та таза, гострі травми й активність, що вимагає рухів у тазових суглобах. Симптоми зазвичай є однобічними; біль зростає при прогулянковому темпі ходьби, а в разі бігу чи швидкої ходьби є меншим; сидіння частіше спричиняє біль, ніж стояння. Біль може локалізуватися в задній частині таза, стегні, паховій ділянці, нижніх кінцівках. У разі натискання на задню поверхню таза біль посилюється. Якщо він посилюється при флексії, екстензії, ротації та нахилах у сторони, має люмбалгічний характер. Для виявлення дисфункції кульшового суглоба використовуються зовнішня та внутрішня ротація кінцівки, FABER-тест і феномен Патріка.
Вертлюжний бурсит також може спричиняти біль, який іррадіює у СІС. У таких випадках біль зазвичай з’являється вночі, а при тендиніті сухожилля середнього сідничного м’яза – під час тривалої ходьби чи роботи в саду. В останніх двох випадках для лікування застосовуються ін’єкційні блокади, що є в цьому разі високобезпечними, оскільки поруч немає анатомічних структур, які легко ушкодити чи ушкодження котрих може бути критично небезпечним.
Окрім різного роду фізикальних проб, у діагностиці сакралгій широко застосовуються візуалізаційні методи дослідження: рентгенографія, комп’ютерна та магнітно-резонансна томографія, позитронно-емісійна комп’ютерна томографія.
При лікуванні пацієнтів із сакралгіями слід насамперед навчити цих хворих модифікувати своє фізичне навантаження. Крім усунення болю, лікування має бути спрямоване на ліквідацію тривоги та катастрофізації власного стану, порушень сну. Для цього може застосовуватися психотерапія. Що стосується болю, то важливим діагностично-лікувальним методом є блокади. Спочатку варто застосовувати звичайний анестетик (лідокаїн), оскільки включення до лікування бетаметазону може дати системний сприятливий ефект, який не дозволить зрозуміти справжньої причини болю.
Для зняття больового компонента хибного кола «біль – спазм – порушення функції – біль» доцільно застосовувати нестероїдні протизапальні препарати (НПЗП), антиконвульсанти, антидепресанти, а при хронізації болю – блокади місцевими анестетиками, іноді – в комбінації з пролонгованими стероїдами. Пацієнтам з вираженим запальним синдромом при артритах, артрозах, остеохондрозі та гнійно-запальних захворюваннях призначається диклофенак (Диклак®, фармацевтична компанія «Сандоз»). У разі помірної вираженості болю рекомендується застосовувати 1 таблетку препарату Диклак® ID 75 мг/добу протягом 7 днів, а при сильному болі – ступеневу терапію лікарським засобом Диклак® (1-2 дні – ін’єкції 2 р/добу, із 3-го по 14-й день – препарат Диклак® ID 150 мг 1 таблетка 1 р/добу). Масштабний метааналіз, який включав 58 451 пацієнта в 76 дослідженнях, виявив, що диклофенак дозою 150 мг є найефективнішим НПЗП у лікуванні болю та відновленні функції колінного й кульшового суглобів при остеоартриті (Da Costa et al., 2017). Пацієнтам з переважанням больового синдрому (після великих та малих оперативних втручань, травм і при остеохондрозах й радикулітах за неефективності інших НПЗП) призначається кетопрофен (Кетонал®, фармацевтична компанія «Сандоз»). Для місцевого нанесення використовується гель кетопрофену – Кетонал® (фармацевтична компанія «Сандоз»), оскільки він характеризується хорошим проникненням крізь шкіру. Додаткові способи лікування – масажі та тейпування. За неефективності терапевтичних методів призначається хірургічне лікування.
 Доцент кафедри внутрішньої медицини № 1 Національного медичного університету ім. О. О. Богомольця (м. Київ), кандидат медичних наук Олександр Аркадійович Мартинчук у своєму виступі охарактеризував мінімізацію ризиків застосування НПЗП з боку шлунково-кишкового тракту (ШКТ).
Доцент кафедри внутрішньої медицини № 1 Національного медичного університету ім. О. О. Богомольця (м. Київ), кандидат медичних наук Олександр Аркадійович Мартинчук у своєму виступі охарактеризував мінімізацію ризиків застосування НПЗП з боку шлунково-кишкового тракту (ШКТ).
Щодня понад 30 млн осіб приймають НПЗП для знеболювання, а також як протизапальні засоби та дезагреганти. Упродовж року НПЗП застосовують понад 300 млн осіб, однак лише ⅓ – за призначенням лікаря. Імовірність несприятливих явищ з боку ШКТ у пацієнтів, які приймають НПЗП, є учетверо вищою, ніж загальнопопуляційний показник. Смертність серед осіб, котрі вживають НПЗП, унаслідок уражень ШКТ є в 2-3 рази вищою, ніж серед осіб, які їх не вживають. У 20-40% випадків хворі, котрі приймають НПЗП, скаржаться на диспепсію, а в 10% випадків пацієнти самовільно припиняють їх вживати у зв’язку з появою побічних явищ. Дуже часто при НПЗП-гастропатіях відсутні клінічні симптоми та скарги, а приблизно в 70% випадків з’являються т. зв. «німі» виразки, першою маніфестацією яких є перфорація або тяжка гастродуоденальна кровотеча. Завдання лікаря – передбачити НПЗП-гастропатію та запобігти її розвитку.
Аналіз даних 1996-2005 рр. демонструє, що за цей період частота кровотеч з верхніх відділів ШКТ поступово знижується, а показник частоти кровотеч і нижніх відділів зберігається сталим і навіть дещо підвищується (Губська О. Ю., Кузьмінець А.А., 2018). Вважається, що таке зменшення частоти кровотеч зі шлунка та дванадцятипалої кишки обумовлене широким застосуванням інгібіторів протонної помпи (ІПП). Що стосується зростання показника кровотеч з нижніх відділів ШКТ, імовірно, це є наслідком покращення діагностичних методів, зокрема, застосування відеокапсульної ендоскопії та двобалонної ендоскопії. Поширення використання кишковорозчинних форм НПЗП має двозначний вплив: з одного боку, такі форми запобігають ураженню шлунка, з іншого – збільшують ризик ушкоджень тонкого кишечнику.
Шлунково-кишковий ризик пацієнта, якому планується призначення НПЗП, може бути високим (ускладнена пептична виразка в анамнезі, наявність ≥2 факторів ризику), помірним (вік >65 років, неускладнена пептична виразка в анамнезі, тривале (>7 днів) застосування високих доз НПЗП, одночасне вживання антикоагулянтів, кортикостероїдів, декількох НПЗП, у т. ч. низькодозових препаратів ацетилсаліцилової кислоти (НДАСК), супутні хронічні інвалідизуючі захворювання – серцева, печінкова та ниркова недостатність, цукровий діабет) і низьким (відсутність факторів ризику). Зазначені критерії ризику затверджені експертною групою Української гастроентерологічної асоціації (2017). Як окремі додаткові фактори ризику розглядаються наявність гелікобактерної інфекції, куріння, прийом селективних інгібіторів зворотного захоплення серотоніну.
Шлунково-кишковий ризик впливає на тактику ведення пацієнта. Крім того, ризик залежить від того, який саме НПЗП буде обрано. Так, ризик шлунково-кишкових ускладнень є найвищим на тлі застосування індометацину (відносний ризик (ВР) 2,25). Меншими показники ВР є для напроксену (1,83), диклофенаку (1,73), піроксикаму (1,66), теноксикаму (1,43), мелоксикаму (1,24) й ібупрофену (1,19). Ризик був пов’язаним із тривалістю лікування. Середня тривалість терапії до спостереження значного ризику побічних ефектів з боку ШКТ становила 84 дні, однак підвищений ризик спостерігався вже через 7 днів застосування індометацину (Richy F. et al., 2004). Необхідно також звертати увагу на дозу, оскільки негативний вплив НПЗП на ШКТ чітко залежить від дозування. Так, при застосуванні низьких доз ібупрофену ВР ураження ШКТ становить 1,16, високих – 4,2. Для напроксену аналогічні показники складають 3,7 та 6,0, для індометацину – 3,0 та 7,0 (Richy F. et al., 2004).
Інфекція Helicobacter pylori (HP) асоціюється зі збільшенням ризику неускладнених або ускладнених виразок шлунка та дванадцятипалої кишки в пацієнтів, які приймають НПЗП або НДАСК. Ерадикація НР знижує цей ризик за умов проведення до початку застосування НПЗП, однак не працює у хворих, котрі вже приймають НПЗП протягом тривалого часу. В цьому випадку, крім ерадикації, рекомендований тривалий прийом ІПП. Ерадикація абсолютно показана хворим з виразковою хворобою в анамнезі. Пацієнтам з виразковою хворобою в анамнезі, котрі приймають НДАСК, рекомендовано проведення тестів на наявність НР. За результатами тривалого спостереження після ерадикації частота виразкових кровотеч у таких хворих є низькою (навіть за відсутності гастропротекторного лікування).
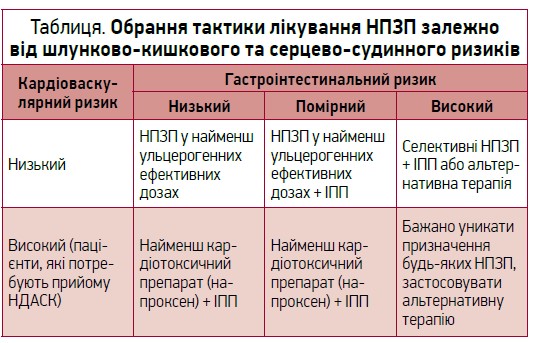 Після визначення шлунково-кишкового ризику слід перейти до первинної профілактики ушкоджень ШКТ. За умов застосування ІПП ВР появи симптоматичних виразок знижується до 0,09 (95% довірчий інтервал (ДІ) 0,02-0,47), мізопростолу – до 0,36 (95% ДІ 0,02-0,65). Заміна неселективних НПЗП на коксиби зменшує ризик до 0,49 (95% ДІ 0,38-0,65) (Raskin J. B. et al., 1995), однак слід пам’ятати про вплив коксибів на тромбогенез. Під час обрання НПЗП необхідно зважувати шлунково-кишковий та серцево-судинний ризики (табл.).
Після визначення шлунково-кишкового ризику слід перейти до первинної профілактики ушкоджень ШКТ. За умов застосування ІПП ВР появи симптоматичних виразок знижується до 0,09 (95% довірчий інтервал (ДІ) 0,02-0,47), мізопростолу – до 0,36 (95% ДІ 0,02-0,65). Заміна неселективних НПЗП на коксиби зменшує ризик до 0,49 (95% ДІ 0,38-0,65) (Raskin J. B. et al., 1995), однак слід пам’ятати про вплив коксибів на тромбогенез. Під час обрання НПЗП необхідно зважувати шлунково-кишковий та серцево-судинний ризики (табл.).
На тлі вживання мізопростолу дозою 200 мкг 4 р/добу в 15% пацієнтів з’являються ускладнення (діарея, дискомфорт у животі), а менші дози не є ефективними. Високі дози Н2-гістаміноблокаторів призначаються в разі непереносимості ІПП і мізопростолу та забезпечують профілактику виразок дванадцятипалої кишки, але не шлунка.
Ключові рекомендації стосовно профілактики та лікування НПЗП-гастропатій, розроблені експертною групою Української гастроентерологічної асоціації (2017):
- До призначення терапії НПЗП необхідно визначити ризик розвитку НПЗП-гастропатій.
- Діагностика НПЗП-гастропатій має бути своєчасною з використанням сучасних діагностичних можливостей.
- Пацієнтам, котрі приймають будь-які НПЗП, включаючи селективні препарати й безрецептурні форми традиційних НПЗП у невеликих дозах, додатково потрібно призначити гастропротекторні засоби (насамперед ІПП) залежно від ступеня шлунково-кишкового та серцево-судинного ризиків.
- Хворим з високим ризиком, котрі тривалий час (>6 місяців) отримують неселективні чи селективні НПЗП, рекомендована тривала (≥6 місяців) гастропротекторна терапія.
- Серед пацієнтів з вираженим ризиком НПЗП-гастропатій слід проводити просвітницьку роботу щодо зміни способу життя, зваженого прийому НПЗП, за можливості – переходу на селективні препарати.
- У НР-інфікованих хворих, які вперше планують тривале застосування НПЗП, рекомендовані своєчасне виявлення й ерадикація НР.
Пацієнтам, у яких з’явилася симптоматична виразка шлунка чи дванадцятипалої кишки на тлі лікування НПЗП або НДАСК, рекомендовано спочатку призупинити прийом цих препаратів. Після цього призначається лікування ІПП терміном 4-8 тижнів. Хворим, яким неможливо відмінити НПЗП або НДАСК, рекомендується розпочати тривалий прийом ІПП. Тривалість лікування залежить від розміру виразки та тяжкості первинних клінічних проявів. Зазвичай ІПП (омепразол 20-40 мг або еквівалентна доза іншого ІПП) призначають на 4-6 тижнів при виразках розміром до 1 см; на 6-8 тижнів – у разі наявності виразок розміром понад 1 см.
ІПП мають безперечну перевагу над іншими препаратами, що застосовуються із цією метою (ранітидином, мізопростолом, сукральфатом); це підтверджено в дослідженнях різноманітного дизайну, де тривалість лікування та характеристики пацієнтів також мали різні показники.
Призначаючи ІПП, слід зробити вибір між різними препаратами цього класу. Дослідження свідчать, що наприкінці лікування різноманітні ІПП демонструють практично однаковий результат за показником видужання. У випробуванні D. Otteanu та співавт. (2000) наприкінці періоду спостереження частка осіб, котрі видужали, була однаковою в групах омепразолу 20 мг і пантопразолу 40 мг, однак станом на 4‑й тиждень спостерігалася перевага пантопразолу.
Під час обрання ІПП необхідно звертати увагу на міжлікарські взаємодії. Пантопразол характеризується найнижчою афінністю до печінкової системи цитохрому Р450, не впливає на її активність та не має клінічно значимих перехресних реакцій із НПЗП (насамперед з диклофенаком – одним з найчастіше застосовуваних препаратів цієї групи). Саме тому за високого ризику розвитку НПЗП-гастропатій, коли існує потреба в додатковому превентивному призначенні ІПП або є необхідність у продовженні прийому диклофенаку (навіть за розвитку НПЗП-гастропатії), пантопразол – найоптимальніший ІПП (Bliesath et al., 1996). Пантопразол забезпечує швидкий, стабільний та тривалий контроль секреції соляної кислоти, що гарантує ефективне спостереження за симптомами упродовж 24 год і мінімальну кількість рецидивів після проведеного лікування. Пантопразол також є найбезпечнішим ІПП.
З тривалою кислотосупресивною терапією за допомогою ІПП асоціюються такі потенційні побічні ефекти, як хронічна хвороба нирок (у 0,1-0,3% пацієнтів на рік), деменція (в 0,07-1,5% хворих на рік), дефіцит мікронутрієнтів (у 0,3-0,4% пацієнтів на рік), спонтанний бактеріальний перитоніт (у 3-16% хворих на рік). Асоціації з пухлинами ШКТ, інфарктом міокарда та пневмоніями не були підтверджені в рандомізованих клінічних дослідженнях.
При призначенні НПЗП не слід забувати також про ентеропатії. Потрапляння до організму кишковорозчинних НПЗП наносить тонкому кишечнику особливий удар. По-перше, сама лікарська форма зумовлює розчинення фосфоліпідного шару клітин і руйнування міжклітинних зв’язків; по-друге, ентерогепатична циркуляція жовчних кислот спричиняє повторний вплив НПЗП на тонкий кишечник. Іншими потенційними механізмами несприятливої дії НПЗП на кишечник є інгібування циклооксигенази, зниження синтезу простагландинів, сприяння дисбіозу.
З метою профілактики та лікування НПЗП-ентеропатій можуть застосовуватися різні стратегії та медикаменти. Інгібітори циклооксигенази‑2 повністю не захищають від несприятливих подій на рівні нижніх відділів ШКТ і можуть мати такі самі переваги, як і стандартні неселективні представники цього класу. Основним способом лікування ушкоджень, спричинених застосуванням НПЗП, є припинення їх вживання. При ілеоцекальних ураженнях без стриктур припинення використання НПЗП зазвичай зумовлює швидке поліпшення. Для підтвердження часткового чи повного загоєння виразки та/або коліту через 6-8 тижнів має бути виконана повторна колоноскопія. Персистенція дефекту або погіршення стану є передумовами для появи підозри щодо хвороби Крона чи інших причин ураження. В разі утворення ендоскопічно доступних стриктур або діафрагм доцільно проводити їх балонну дилатацію. Діафрагмоподібні стриктури зазвичай є множинними, тому може знадобитися резекція та/або стриктуропластика ураженого відділу кишечнику. Хірургічне лікування показане у випадках значних кровотеч або перфорацій, а також за неможливості остаточно виключити карциному.
Доповідач підсумував свій виступ такими висновками:
- Ризик гастродуоденальної токсичності пов’язаний з наявними факторами ризику, НР-статусом і конкретним типом та дозою НПЗП.
- Значна шлунково-кишкова токсичність зазвичай проявляється через кілька тижнів лікування, однак при застосуванні деяких НПЗП (індометацин, кеторолак) може з’являтися й через тиждень.
- Слід намагатися використовувати найменші ефективні дози й тривалість лікування НПЗП та пам’ятати, що всі НПЗП пов’язані з підвищеним ризиком для ШКТ.
- Перед тривалою терапією НПЗП необхідно проводити ерадикацію НР.
- За наявності кількох факторів ризику гастродуоденальної токсичності, пов’язаної з НПЗП, потрібно призначати коксиби чи неселективні НПЗП у поєднанні з ІПП (ПанГастро®, фармацевтична компанія «Сандоз») або мізопростолом.
- Усі ІПП мають однакову ефективність, проте пантопразол (ПанГастро®) характеризується кращим профілем безпеки.
- Будь-які переваги коксибів щодо токсичного впливу на ШКТ елімінуються одночасним прийомом ацетилсаліцилової кислоти.
Підготувала Лариса Стрільчук
Інформація для спеціалістів сфери охорони здоров’я
3-21-АНП-РЕЦ-1220
Медична газета «Здоров’я України 21 сторіччя» № 22 (491), 2020 р.


