14 квітня, 2016
Биластин – новый антигистаминный препарат с оптимальным отношением «польза/риск» для безопасного вождения
Аллергический ринит (АР) может негативно влиять на когнитивную функцию и, следовательно, способность управлять автомобилем, отчасти вследствие сниженного качества ночного сна и сонливости в дневное время. В недавно проведенном исследовании было установлено, что у нелеченных пациентов с симптомами АР, вызываемыми пыльцой растений, водительские способности были значительно нарушены по сравнению с бессимптомными пациентами (Vuurman et al., 2014). Степень нарушений была сравнима с таковой, наблюдающейся при уровне алкоголя в крови 0,05%, легальном во многих странах. С помощью симптоматической терапии можно частично или полностью компенсировать негативное влияние АР на вождение.
Антигистаминные препараты (АГП; антагонисты или обратные агонисты гистаминовых Н1-рецепторов) являются основой лечения наиболее распространенных аллергических заболеваний, включая ринит и крапивницу. По оценкам, АР страдает около 30% мировой популяции, поэтому неудивително, что АГП остаются одними их самых назначаемых лекарственных средств. Терапевтической мишенью АГП являются периферические Н1-рецепторы.
Однако АГП I поколения, такие как хлорфенирамин, дифенгидрамин и гидроксизин, могут проникать через гематоэнцефалический барьер и связываться с Н1-рецепторами головного мозга, вмешиваться в нейротрансмиссию гистамина и вызывать сонливость. Из-за низкой селективности АГП I поколения ассоциируются с побочными эффектами со стороны центральной нервной системы (ЦНС), а также антихолинергическими и антисеротонинергическими эффектами. Центральные побочные эффекты, прежде всего сонливость и седация, нарушают когнитивную и психомоторную функции и могут иметь опасные последствия. В частности, эти эффекты могут нарушать способности человека управлять сложным оборудованием или автомобилем, таким образом повышая риск профессиональных травм и автокатастроф.
Осознание проблемы безопасности АГП I поколения привело к пересмотру рекомендаций Глобальной европейской сети по астме и аллергии, и сегодня предпочтение отдается препаратам II поколения. АГП II поколения являются более полярными и менее липофильными, что ограничивает их способность проникать в ЦНС. В целом АГП II поколения считаются неседативными, однако они существенно различаются по своим фармакодинамичес ким свойствам, эффективности и особенно безопасности, что имеет огромное значение для пациентов, деятельность которых требует ясного сознания (например, при управлении автомобилем).
Биластин – новый неседативный АГП II поколения, широко применяющийся в Америке и Европе для симптоматической терапии аллергического риноконъюнктивита (круглогодичного
и сезонного) и крапивницы у взрослых и у детей в возрасте старше 12 лет. После перорального приема в стандартной дозе 20 мг биластин быстро (через 1-1,5 ч) достигает пиковой концентрации в плазме, при этом период полувыведения составляет около 10 ч. В клинических исследованиях биластин, назначаемый перорально в дозе 20 мг 1 раз в день, как минимум не уступал другим АГП II поколения в облегчении симптомов аллергического риноконъюнктивита (цетиризин и дезлоратадин) и крапивницы (левоцетиризин). При этом биластин ассоциировался с повышением качества жизни пациентов, благоприятным профилем безопасности (отсутствие кардиальных и антихолинергических побочных эффектов, более высокая безопасность по сравнению с цетиризином) и отсутствием нарушения психомоторной функции.
Биластин – оптимальный АГП для тех, кто за рулем
Как и алкоголь, многие лекарственные препараты могут негативно влиять на способность управлять автомобилем. В руководстве, разработанном Международным советом по алкоголю, лекарствам и безопасности дорожного движения (ICADTS), препараты делятся на три класса в зависимости от способности нарушать вождение (табл.). В Испании в 2013 г. 43% водителей, погибших в автокатастрофах, незадолго до происшествия употребляли алкоголь и/или лекарства, включая психотропные препараты (III класс ICADTS), и у 23% пешеходов – участников фатальных ДТП определялись эти препараты в крови. АГП I поколения относятся ко II или III классу ICADTS, однако продолжают широко использоваться как дешевая альтернатива более современным АГП.
Консенсусная группа по АГП нового поколения (CGNGA) разработала критерии, которым должен соответствовать идеальный АГП. Новый АГП должен обладать высокой клинической эффективностью и безопасностью, хорошо переносится и иметь в целом благоприятный профиль «польза/риск». В частности, препарат должен быть лишен кардиотоксического действия, влияния на CYP и побочных эффектов со стороны ЦНС (минимальная субъективная сонливость или ее отсутствие; отсутствие связывания с церебральными Н1-рецепторами; отсутствие негативного влияния на когнитивную и психомоторную функции). Всем эти критериям в полной мере отвечает биластин.
Селективность в отношении Н1-рецепторов
При аллергических заболеваниях терапевтической мишенью являются периферические Н1-рецепторы; активность в отношении других рецепторов повышает риск нежелательных побочных эффектов, которые могут влиять на вождение. Биластин – высокоселективный обратный агонист Н1-рецепторов с минимальной или отсутствующей аффинностью к другим типам рецепторов. В исследованиях in vitro было убедительно продемонстрировано, что биластин обладает высокой специфичностью к Н1-рецепторам; на другие типы рецепторов гистамина (Н2, Н3, Н4) препарат не влияет (в целом показано отсутствие воздействия биластина более чем на 30 типов рецепторов, включая рецепторы серотонина, брадикинина, лейкотриена D4, М3-мускариновые рецепторы, α1-адренорецепторы, β2-адреноре цепторы). По аффинности к Н1-рецепторам биластин в 5 раз превосходит фексофенадин и в 3 раза – цетиризин.
Взаимодействие с системой цитохрома Р450 (CYP)
АГП относятся к наиболее используемым препаратам, вследствие чего часто назначаются с другими лекарственными средствами. Взаимо действие АГП с системой CYP (ингибирование или
индукция), посредством которой метаболизируются различные препараты, является нежелательным. Примером такого нежелательного взаимодействия является кардиотоксичность, наблюдавшаяся при одновременном назначении ингибиторов CYP3A4 с терфенадином или астемизолом.
В исследованиях in vitro было продемонстрировано, что биластин не оказывает значимого ингибирующего или индуцирующего влияния на различные изоферменты CYP, включая CYP1A3, 2A6, 2B6, 2C8, 2C9, 2C19, 2E1, 3А4 и др. Минимальный метаболизм биластина посредством CYP был также подтвержден in vivo и у здоровых добровольцев.
В частности, было установлено, что после приема однократной дозы 20 мг она выводится полностью в неизмененном виде (67% со стулом и 33% с мочой).
Антимускариновая активность
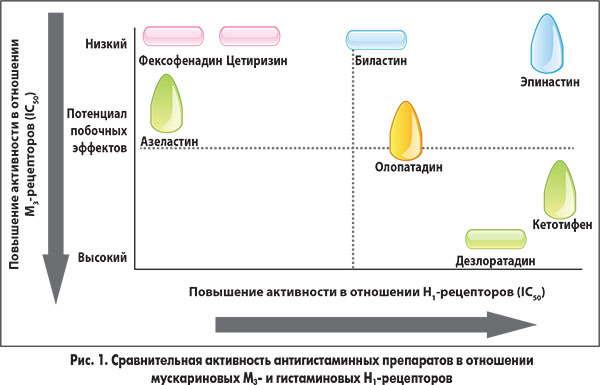
Антагонизм в отношении холинергических мускариновых рецепторов отвечает за такие побочные эффекты АГП, как сухость глаз, сухость во рту и носовой полости, нарушения зрения и тахикардия, которые как минимум доставляют дискомфорт, а зачастую приводят к серьезным последствиям. Эти побочные эффекты могут негативно влиять на вождение и повышать риск ДТП. В исследовании in vitro было установлено, что биластин даже в максимальной изученной концентрации (100 мкмоль) не обладает значимой антимускариновой активностью в отношении пяти подтипов рецепторов (М1-М5), тогда как АГП II поколения дезлоратадин показал наиболее высокую антихолинергическую активность со значениями IC50 от 21 нмоль (М2) до 218 нмоль (М4). При оценке сравнительной активности в отношении Н1-гистаминовых и М3-мускариновых рецепторов наиболее благоприятный профиль (сильное антигистаминное и слабое антимускариновое действие) продемонстрировали биластин и эпинастин (рис. 1).
Связывание с Н1-рецепторами головного мозга
Центральные побочные эффекты АГП, включая сонливость, когнитивную дисфункцию и подавленную бдительность, обусловлены способностью препаратов проникать через гематоэнцефалический барьер и связываться с центральными Н1-рецепторами. В исследованиях с применением позитронно-эмиссионной томографии (ПЭТ) была убедительно доказана корреляция между оккупацией церебральных Н1-рецепторов и степенью когнитивных/психомоторных нарушений. Поэтому минимальное связывание с Н1-рецепторами головного мозга является важнейшей характеристикой идеального для водителей АГП.
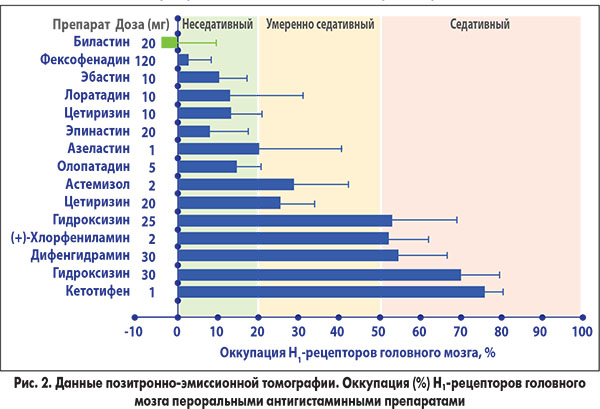
Биластин является субстратом для Р-гликопротеина, что снижает его способность проникать в ЦНС и связываться с центральными Н1-рецепторами. В двойном слепом исследовании с использованием ПЭТ было показано, что по оккупации Н1-рецепторов в различных областях коры биластин 20 мг (–3,92%) не отличался от плацебо, в то время как для гидроксизина соответствующий показатель составил +53,95% (Farre et al., 2014). В целом по сравнению с АГП I и II поколения биластин 20 мг демонстрирует самый низкий потенциал связывания с церебральными Н1-рецепторами (рис. 2).
Взаимодействие с алкоголем и лоразепамом
Алкоголь сам по себе способен вызывать седацию и другие эффекты со стороны ЦНС и часто становится причиной ДТП. Эти негативные эффекты могут усиливаться при взаимодействии алкоголя с лекарственными препаратами. Учитывая высокую распространенность употребления алкоголя и приема АГП, их одновременный прием трудно исключить. Бензодиазепины (диазепам, лоразепам), часто применяющиеся в лечении тревоги и нарушений сна, также могут негативно влиять на способность управлять автомобилем. Следовательно, для безопасности вождения важно, чтобы принимаемый АГП не взаимодействовал с алкоголем и бензодиазепинами.
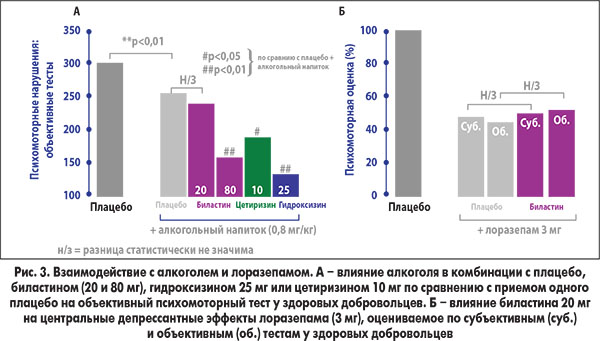
В рандомизированном двойном слепом исследовании с участием 24 здоровых добровольцев одновременный прием биластина 20 мг не потенцировал депрессантные эффекты алкоголя на ЦНС (Garcia-Gea et al., 2014). Объективные и субъективные тесты показали, что алкоголь в комбинации со всеми активными препаратами нарушал психомоторную функцию по сравнению с плацебо (р<0,01); в то же время биластин в дозе 20 мг единственный не оказывал дополнительного негативного влияния по сравнению с алкоголем + плацебо. Гидроксизин 25 мг, цетиризин 10 мг и биластин 80 мг (стандартная доза × 4) в комбинации с алкоголем индуцировали статистически значимое нарушение психомоторной функции по сравнению с одним алкоголем (рис. 3, А). В похожем двойном слепом перекрестном плацебо-контролированном исследовании результаты психомоторного тестирования показали, что биластин, назначаемый в дозе 20 мг однократно или в течение 8 дней, не потенцирует центральные депрессантные эффекты лоразепама 3 мг (рис. 3, Б).
Сонливость в дневное время
Сонливость и седация как центральные побочные эффекты АГП могут непосредственно ухудшать водительские навыки, нарушая когнитивную и психомоторную функции. В клинических исследованиях II и III фазы (>2000 пациентов) частота сонливости при лечении биластином 20 мг не отличалась от таковой при приеме плацебо. В то же время как цетиризин (10 мг), так и левоцетиризин (5 мг) ассоциировались с достоверно более высокой частотой сонливости по сравнению с плацебо (р<0,05), при этом частота сонливости для цетиризина 10 мг была значительно выше (р<0,001), чем для биластина 20 мг (Kuna et al., 2009).
Влияние на вождение
По влиянию на вождение АГП II поколения существенно различаются. В частности, для некоторых препаратов характерны ранние побочные эффекты со стороны ЦНС, которые могут проходить по мере продолжения лечения. Для оценки влияния таких побочных эффектов на способность управлять автомобилем был разработан тест, который проводится в реальных условиях на шоссе. Этот тест является более чувствительным по сравнению с лабораторными измерениями и считается стандартным при изучении лекарств. Во время теста водитель должен проехать 100 км, двигаясь с постоянной скоростью (90-95 км/ч) по центру крайней правой полосы (рис. 4). Управление автомобилем оценивается по стандартному отклонению латеральной позиции (СОЛП); чем больше СОЛП, тем сильнее нарушена способность управлять автомобилем.
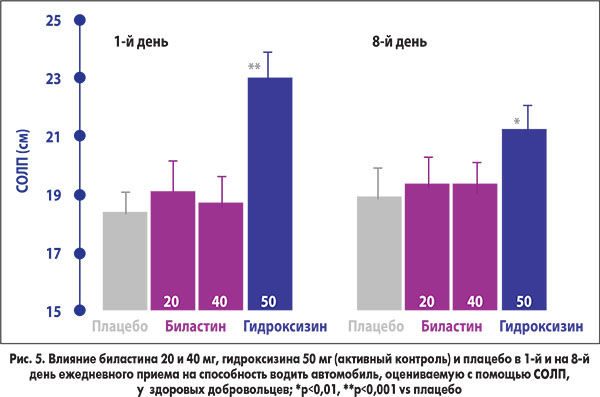
Влияние биластина на вождение в реальных условиях оценивалось в двойном слепом перекрестном исследовании с участием 22 здоровых добровольцев, которых рандомизировали для приема биластина 20 или 40 мг, гидроксизина 50 мг (активный контроль) или плацебо 1 раз в сутки в течение 8 дней (Conen et al., 2011). Первичной конечной точкой было СОЛП, оцениваемое в 1-й и на 8-й день. По этому показателю биластин в обеих дозах статистически не отличался от плацебо (рис. 5). Гидроксизин, напротив, ассоциировался с достоверным изменением СОЛП по сравнению с плацебо в 1-й и на 8-й день приема, то есть толерантность к его седативным эффектам не развивалась. Таким образом, биластин в дозах до 40 мг как при однократном, так и при повторных приемах не оказывает негативного влияния на вождение.
Перед тестом на вождение участники исследования с помощью визуальной аналоговой шкалы дали субъективную оценку ощущению седации и предполагаемому влиянию препарата на способность управлять автомобилем. Затем испытуемые и инструктор оценили качество вождения. Оказалось, что перед проведением теста респонденты не ощущали, что терапия может негативно повлиять на его результаты, и только после завершения теста они отметили значительное ухудшение способности управлять автомобилем (р<0,01). Таким образом, в реальной жизни пациенты, получающие гидроксизин, при принятии решения садиться или не садиться за руль могут не осознавать, что препарат негативно влияет на их способность управлять автомобилем.
Выводы
Накопленные на сегодня доказательства свидетельствуют о том, что у пациентов, которые водят автомобиль и нуждаются в антигистаминной терапии по поводу аллергического заболевания, среди всех антигистаминных препаратов биластин обладает оптимальным соотношением «польза/риск» и полностью соответствует критериям безопасности.
Список литературы находится в редакции.
Статья печатается в сокращении.
Jauregui I., Ramaekers J.G., Yanai K. et al. Bilastine: a new antihistamine with an optimal benefit-to-risk ratio for safety during driving. Expert Opin Drug Saf. 2016 Jan; 15(1): 89-98.
Перевел с англ. Алексей Терещенко