29 березня, 2016
Выбор антибиотика для лечения инфекций нижних дыхательных путей
Несмотря на то что этиология внебольничной (ВП) и госпитальной пневмонии сегодня хорошо изучена, а в арсенале врача имеется широкий выбор антибактериальных препаратов (АБП), уровни смертности от инфекций нижних дыхательных путей остаются высокими. Другой проблемой в лечении указанной группы заболеваний является возрастающая микробная резистентность к современным антибиотикам. В связи с этим не прекращается поиск оптимальных режимов антибиотикотерапии, которые позволят достичь полной эрадикации возбудителя при минимальных побочных эффектах и рисках развития антибиотикорезистентности.
Бактериальные инфекции респираторного тракта вносят весомый вклад в структуру заболеваемости и смертности от инфекционных заболеваний, особенно среди пациентов раннего детского и пожилого возраста. Трудности в лечении бактериальной инфекции дыхательных путей обусловлены тем, что врач должен принять немедленное решение о назначении больному АБП, не располагая данными об этиологически значимом инфекционном агенте. Основным возбудителем пневмоний является Streptococcus pneumoniae, который обусловливает от 30 до 80% случаев ВП у лиц всех возрастных групп (Зубков М.Н., 2002; Чучалин А.Г., 2006). Однако в последние годы отмечается повышение частоты атипичных пневмоний как среди взрослого населения, так и в детской популяции (Шихнебиев Д.А., 2014). Доля атипичных возбудителей (Mycoplasma pneumoniae, Chlamydophila pneumoniae, Legionella pneumophila) составляет 8-25% случаев. В связи с возрастанием числа больных с тяжелыми дефектами иммунитета (ВИЧ-инфекция, врожденный иммунодефицит, онкогематологические заболевания, длительная терапия кортикостероидами и иммунодепрессантами и др.) отмечается увеличение доли пневмоний, вызванных оппортунистическими инфекциями, Pseudomonas aeruginosa, Staphylococcus aureus (Ноников В.Е., Мышьяков В.И., 2011).
Инфекции нижних дыхательных путей в цифрах (Дзюблик А.Я., 2015; Островский Н.Н., 2015; Щербак И.Б., 2015; Юдина Л.В., 2015):
- заболеваемость пневмонией в Европе – 2-15 случаев на 1 тыс. населения в год;
- частота пневмонии в США – 5,6 млн случаев ежегодно, из них 60 тыс. – с летальным исходом;
- заболеваемость пневмонией в Украине в 2013 г. – 448,7 случая на 100 тыс. населения, летальность – 1,08%;
- ВП занимает 1-е место в структуре причин смерти по причине инфекционных заболеваний, 6-е и 4-е место – среди причин общей смертности и летальных исходов у пациентов старше 65 лет соответственно;
- в глобальном масштабе количество больных хроническим обструктивным заболеванием легких (ХОЗЛ) составляет более 64 млн;
- прогнозируют, что к 2030 г. ХОЗЛ станет 3-й по частоте причиной смерти в мировой популяции, уступая лишь инсульту и ишемической болезни сердца;
- смертность от обострения ХОЗЛ в стационаре – 8-11%;
- 22-43% больных, пролеченных в стационаре по поводу обострения ХОЗЛ, умирают в течение года после выписки;
- 5% пациентов с тяжелым обострением ХОЗЛ умирают в первые 30 дней после госпитализации, 39% – в течение последующих 5 лет.
Другой проблемой, с которой приходится сталкиваться врачу в практической деятельности, является возрастающая антибиотикорезистентность. Широкая доступность антибиотиков вследствие безрецептурного отпуска из аптек, профилактическое назначение при вирусных инфекциях, неправильный выбор стартового АБП, дозы и кратности его введения приводят к появлению и распространению антибиотикорезистентных штаммов микроорганизмов. Необходимым условием успешной антибактериальной терапии является полная эрадикация возбудителя. В условиях, когда лечение не обеспечивает полной ликвидаци патогенных микроорганизмов, возможны селекция устойчивых к применяемому препарату штаммов и возникновение антибиотикорезистентности (Жаркова Л.П. и соавт., 2011; Дзюблик Я.А., Дзюблик А.Я., 2014). На примере золотистого стафилококка показано, что некоторые возбудители способны вырабатывать резистентность всего за 2 года, так что проблема супербактерий представляет собой реальную угрозу. Выбор стартового АБП усложняется не только необходимостью эмпирического назначения и вероятной резистентностью возбудителя, но и необходимостью максимально сохранять препараты резерва.
Этиологическая структура ВП неоднородна, причинно значимые возбудители отличаются у пациентов разных возрастных и клинических групп, поэтому режим антибиотикотерапии следует подбирать в каждом случае индивидуально. Наиболее частым возбудителем ВП у пациентов I-II группы являются Streptococcus pneumoniae. Реже этиологическим фактором выступают Mycoplasma pneumoniae (13-37%), Chlamydophila pneumoniae (до 17%), Haemophilus influenzae (5-10%). В 10-13% случаев заболевание обусловлено вирусами. У пациентов III-IV группы среди возбудителей ВП также доминирует пневмококк, реже выделяется гемофильная палочка. В 3-7% случаев встречается легионеллезная ВП, а также обусловленная Moraxella catarrhalis, S. aureus и грамнегативными энтеробактериями (с большей частотой, чем при ВП с легким течением). Сохраняется роль M. pneumoniae и C. pneumoniae, вирусов, но в меньшей степени. У пациентов с тяжелым течением заболевания возрастает риск ВП, вызванной синегнойной палочкой (P. aeruginosa). Этот риск наиболее высок у больных с бронхоэктазами. Самостоятельная роль H. influenzae и M. рneumoniae в генезе тяжелой пневмонии незначительна, тем не менее они могут выступать копатогенами в полимикробной ассоциации, усугублять течение болезни и прогноз. Установлено, что практически у каждого второго больного с тяжелой пневмококковой ВП одновременно удается обнаружить серологические признаки активной микоплазменной или хламидийной инфекций. При тяжелой ВП наиболее высокий уровень летальности обусловлен S. aureus (31,8%) и Klebsiella pneumoniae (35,7%), несколько меньший – Legionella pneumophila (14,7%) и S. pneumoniae (12,3%). До 50% случаев ВП всех степеней тяжести остаются этиологически нерасшифрованными, даже несмотря на применение всех современных методов диагностики (Симонов С. С., 2011; Чучалин А. Г., Куценко М. А., 2012).
Для обострения ХОЗЛ легкой степени тяжести (ОФВ1>50%) наиболее характерными патогенами являются H. influenzae, S. pneumoniae, M. catarrhalis и C. pneumoniae. Роль M. pneumoniae в обострении ХОЗЛ определена неточно, однако в некоторых исследованиях частота ее обнаружения достигает 9%. Обострения средней степени тяжести (30% < ОФВ1 < 50%) сохраняют такой же спектр основных патогенов при снижении роли C. pneumoniae и M. pneumoniae. При тяжелых обострениях ХОЗЛ (ОФВ1<30%) и среднетяжелых обострениях с наличием отягощающих факторов имеет место высокий риск наличия синегной палочки или энтеробактерий в качестве действующего микробного агента (Чучалин А. Г., Куценко М. А., 2012).
Согласно приказу МЗ Украины от 19.03.2007 г. № 128 лечение ВП рационально начинать с аминопенициллинов или макролидов на догоспитальном этапе, аминопенициллинов в комбинации с макролидами или цефалоспоринами в условиях стационара (табл. 1).
Чувствительность пневмококка к β-лактамным антибиотикам, макролидам и фторхинолонам (ФХ) остается высокой. Однако рост доли атипичных возбудителей в этиологической структуре ВП ведет к тому, что аминопенницилины не всегда эффективны в качестве стартовой терапии. Нечувствительность к β-лактамным антибиотикам также могут проявлять 5-7% штаммов гемофильной палочки. Отдельно следует назвать M. catarrhalis – практически все штаммы (>90%) выделяют β-лактамазы, поэтому незащищенные пенициллины в таких случаях обычно неэффективны. (Симонов С. С., 2011). У пациентов с аллергией в анамнезе на β-лактамные АБП лечение начинают с препарата ряда макролидов. При неэффективности β-лактамного АБП на старте амбулаторного лечения нетяжелой ВП следует заменить АБП на макролид. У пациентов с ВП III группы лечение в условиях стационара начинают с комбинации β-лактамного АБП парентерально и макролида. ФХ показаны для лечения пациентов IV группы или при неэффективности препаратов первой линии.
Что касается лечения пациентов с ХОЗЛ, то в соответствии с приказом МЗ Украины от 27.06.2013 г. № 555 антибиотикотерапия показана только больным с инфекционным обострением указанной патологии. При этом Н.В. Щербенюк и О. А. Яковлева (2012) на основании проведенного анализа назначений АБП в госпитальных условиях установили, что 11,43% пациентов с инфекционным обострением ХОЗЛ не получали необходимую антибактериальную терапию. Систематический обзор клинических исследований показал, что назначение АБП при инфекционном обострении ХОЗЛ снижает риск ранней смерти на 77%, неудач при лечении на 53%, гнойность мокроты на 44%.
Следующие симптомы указывают на необходимость приема АБП при обострении ХОЗЛ:
- усиление гнойности мокроты;
- увеличение объема отделяемой мокроты;
- усиление одышки;
- потребность в механической вентиляции (инвазивной или неинвазивной).
Усиление гнойности мокроты в данном случае является ведущим симптомом, для назначения АБП достаточно сочетания усиления гнойности мокроты с повышением ее объема или усилением одышки.
В качестве стартовой эмпирической антибиотикотерапии следует назначать аминопенициллины, макролиды или цефалоспорины II-III поколений. Альтернативными препаратами служат ФХ (левофлоксацин, моксифлоксацин). Учитывая вероятный спектр возбудителей, у пациентов на амбулаторном этапе лечения АБП назначают эмпирически, бактериологическое исследование мокроты при этом проводить не обязательно. При выборе АБП стоит учитывать анамнез предыдущих обострений и приема АБП за последние 3 мес. У больных со среднетяжелым и тяжелым обострением ХОЗЛ, которые проходят лечение в условиях стационара, микробиологическое исследование мокроты необходимо из-за риска выявления антибиотикорезистентных штаммов и атипичных возбудителей.
Макролиды наряду с аминопенициллинами рекомендованы как стартовые препараты в комбинированной терапии благодаря их способности накапливаться и длительно сохранять эффективные концентрации в ткани легких, направленности спектра действия на атипичную и грамположительную флору. Назначение макролидов при ХОЗЛ может быть ограничено только в случаях, когда пациент параллельно получает препарат из группы теофиллинов. ФХ показаны при наличии факторов риска, подозрении на выявление синегнойной палочки, а также при указании на использование других АБП в предшествующие 3 мес или неэффективности пенициллинов при предыдущем обострении.
Показания к назначению макролидов при инфекциях нижних дыхательных путей (Перцева Т. А., Козлов Р. С., Симонов С. С. и соавт., 2011; Чучалин А. Г., Куценко М. А., 2012):
- неэффективность аминопенициллина при стартовой терапии ВП на амбулаторном этапе;
- стартовая амбулаторная терапия ВП при аллергии на β-лактамные АБП у пациента;
- в комбинации с β-лактамным АБП при стартовой терапии ВП на госпитальном этапе;
- альтернативное лечение тяжелой ВП IV группы в комбинации с АБП группы аминогликозидов, ФХ или карбапенемов;
- стартовая амбулаторная терапия обострения ХОЗЛ.
При выборе АБП группы макролидов особое внимание следует обратить на азитромицин – полусинтетический 15-членный макролид, который создает высокие концентрации в тканях и проявляет бактерицидный и бактериостатический эффекты в отношении многих возбудителей. Активность азитромицина в сравнении с другими макролидами выше в отношении наиболее частых возбудителей инфекций нижних дыхательных путей: H. influenzae (включая штаммы, продуцирующие β-лактамазы), M. catarrhalis, M. pneumoniae, L. pneumophila, и несколько меньше – в отношении C. pneumoniae, S. pneumoniae и Bordetella pertussis. Азитромицин известен и своим постантибиотическим эффектом, который по продолжительности в отношении гемофильной палочки и легионеллы превосходит соответствующий показатель для кларитромицина. Благодаря высокой липофильности азитромицин хорошо накапливается в различных органах и тканях. Внутриклеточные концентрации препарата в 10-100 раз превышают таковые в плазме крови. Наибольшие концентрации создаются в миндалинах, аденоидах, экссудате среднего уха, слизистой оболочке бронхов и бронхиальном секрете, а также в эпителии альвеол. Высокий уровень препарата в бронхах и легких поддерживается в течение нескольких суток после его отмены. Это свойство азитромицина выделяет его на фоне других АБП класса и позволяет рекомендовать в качестве препарата выбора среди макролидов для лечения инфекций дыхательных путей (Сарыгина О. Д., 2007; Чучалин А. Г., 2012).
Показания к назначению ФХ при инфекциях нижних дыхательных путей (Ноников В.Е., Мышьяков В.И., 2011; Сидоренко С.В., 2011; Лещенко С.И., 2009):
- тяжелая ВП, среднетяжелая пневмония у пациентов с риском выделения микробных ассоциаций (возраст старше 65 лет, тяжелая сопутствующая патология, муковисцидоз);
- нозокомиальная пневмония: в течение 5 дней от начала заболевания ФХ могут быть назначены в качестве монотерапии, после 5-7-го дня – в комбинации с антисинегнойными препаратами;
- среднетяжелое и тяжелое инфекционное обострение ХОЗЛ у пациентов старше 65 лет;
- безрезультатное применение β-лактамных антибиотиков и макролидов (в адекватных дозах) на догоспитальном этапе, подозрение на легионеллезную пневмонию;
- долевые и многодолевые пневмонии у пациентов с аллергией на β-лактамные АБП;
- отсутствие эффекта от лечения цефалоспоринами и макролидами в условиях стационара у пациентов с пневмонией или ХОЗЛ;
- случаи неэффективности стартовых АБП при смешанной инфекции (туберкулез, сепсис, эндокардит и т. д.).
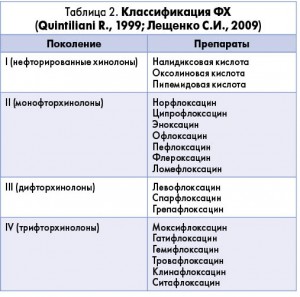
Механизм действия хинолонов принципиально отличается от такового других АБП. Эта особенность обеспечивает активность ФХ в отношении устойчивых, в том числе полирезистентных, штаммов микроорганизмов. Мишенью ФХ являются бактериальные топоизомеразы (топоизомераза IV и ДНК-гираза) – ферменты, осуществляющие изменение пространственной конфигурации молекулы бактериальной ДНК на различных этапах ее репликации. Хинолоны проявляют высокое сродство к комплексу «ДНК-фермент», а участок их связывания получил название «хинолоновый карман». В формировании последнего принимают участие все субъединицы фермента и молекула ДНК, для подавления жизнедеятельности микробной клетки достаточно ингибировать активность только одного фермента. Одна из классификаций ФХ, часто использующихся в практике, приведена в таблице 2.
Левофлоксацин – левовращающий изомер офлоксацина, представитель III поколения ФХ. Он хорошо всасывается в желудочно-кишечном тракте, обладает высокой биодоступностью (на уровне 99%). Около 5% этого АБП подвергается метаболизму в печени с образованием двух неактивных метаболитов. До 75-90% препарата выводятся почками путем клубочковой фильтрации и, частично, путем канальцевой секреции в неизмененном виде; до 4% элиминируются в течение 72 ч с фекалиями. Препарат обладает широким спектром антибактериальной активности, в том числе в отношении возбудителей внутрибольничных инфекций и патогенов, синтезирующих β-лактамазы. Левофлоксацин создает очень высокие концентрации (превышающие сывороточные) в альвеолярных макрофагах, слизистой оболочке бронхов и бронхоальвеолярной жидкости. Длительный период полувыведения, обеспечение высокой тканевой и внутриклеточной концентрации, а также наличие постантибиотического эффекта позволяют назначать левофлоксацин в режиме 1 р/сут (Галеева Ж. А., Зырянов С. К., 2012).
В случае лечения пациентов с респираторными инфекциями важно, что левофлоксацин проявляет высокую активность в отношении резистентных к ампициллину штаммов H. influenzаe, продуцирующих β-лактамазы штаммов M. catarrhalis, атипичных возбудителей (L. pneumophila, M. pneumoniae, C. pneumoniae). Ценным свойством левофлоксацина, принципиально отличающим этот АБП от ранних ФХ, является высокая активность в отношении грамположительных кокков – S. pneumoniae (включая пенициллинрезистентные), S. pyogenes, S. agalactiae, S. viridans. Левофлоксацин оказался наиболее активным АБП в отношении синегнойной палочки среди новых ФХ (Лещенко С.И., 2009). В настоящее время препарат считается одним из наиболее безопасных представителей класса. Частота развития кардио-, гепато- и фототоксичных реакций на фоне лечения левофлоксацином ниже, чем при терапии другими ФХ. Устойчивость патогенов к левофлоксацину и моксифлоксацину развивается реже, чем к другим ФХ. Спектр показаний к применению левофлоксацина, одобренных Управлением по контролю за качеством продуктов питания и лекарственных средств США (FDA), наиболее обширный в сравнении с таковым для других ФХ.
ФХ – препараты резерва, к назначению которых следует подходить взвешенно. Высокая активность ФХ в отношении респираторных патогенов и низкие уровни микробной резистентности позволяют использовать этот класс АБП в лечении тяжелых пневмоний и инфекционных обострений ХОЗЛ, а также при неэффективности других АБП. В качестве альтернативных препаратов для амбулаторного лечения ВП, а также стартовой терапии обострения ХОЗЛ и ВП в условиях стационара рекомендованы макролидные АБП.
На фармацевтическом рынке Украины представлены отечественные препараты азитромицина Азицин® и левофлоксацина Лефлок® («Дарница»). Азицин доступен в таблетированной форме по 500 мг в таблетке. Удобный прием препарата – всего одна таблетка в день – повышает приверженность пациентов к лечению без потери эффективности терапии. Лефлок® выпускается в двух лекарственных формах (раствор для инфузий и таблетки), что позволяет проводить ступенчатую терапию как на госпитальном этапе, так и амбулаторно. Высокая безопасность и приемлемая для украинского покупателя цена позволяют рекомендовать Азицин® и Лефлок® для лечения респираторных инфекций при наличии соответствующих показаний.
Подготовила Мария Маковецкая
Медична газета «Здоров’я України 21 сторіччя» №4 (377), лютий 2016 р.