22 лютого, 2016
Баланс эффективности и безопасности: подходы к антибиотикотерапии острого бактериального бронхита
Часто ли в ежедневной клинической практике встречаются «идеальные» пациенты – люди молодого возраста, не имеющие отягощающих факторов в виде вредных привычек и сопутствующей патологии? Конечно же, нет, скажете Вы – и будете абсолютно правы. При ближайшем рассмотрении обычно оказывается, что ситуация требует от врача клинического мышления и вдумчивого подхода в рамках утвержденных протоколов, ведь универсального «рецепта» антибиотикотерапии (АБТ) – для всех и каждого – не существует. Особую актуальность эта проблема приобретает при ведении больных с коморбидностью, у которых на первый план выходит вопрос безопасности терапии.
О том, как не навредить пациентам с инфекциями нижних дыхательных путей и тяжелой фоновой патологией, рассказала доцент кафедры фтизиатрии и пульмонологии Национальной медицинской академии последипломного образования им. П.Л. Шупика (г. Киев), кандидат медицинских наук Людмила Владимировна Юдина в ходе интерактивного мастер-класса «Новые возможности диагностики и лечения респираторных бактериальных инфекций» (симпозиум «Актуальные вопросы семейной медицины», который состоялся в рамках VIII Национального конгресса «Человек и лекарство – Украина»).
Свое выступление докладчик сопроводила презентацией показательного клинического случая.
Клинический случай
Больной Д., 64 лет, предъявляет жалобы на сухой приступообразный надсадный кашель, периодически приобретающий «лающий» характер; осиплость голоса, наличие скудного количества слизисто-гнойной мокроты, боль в нижних отделах грудной клетки и в области брюшной стенки (вследствие интенсивных приступов кашля), «свист» в груди.
Из анамнеза известно, что симптомы возникли 2 нед назад в виде резкого повышения температуры тела до 39,4 °С. Пациент лечился с помощью средств народной медицины, терапия обеспечила улучшение состояния и нормализацию температуры тела. В настоящее время обратился по причине повторного ухудшения самочувствия и возникновения дыхательных нарушений.
Анамнез жизни: страдает хронической сердечной недостаточностью, хронической венозной недостаточностью, перенес тромбоэмболию легочной артерии (ТЭЛА), транзиторную ишемическую атаку (ТИА), принимает дигоксин, варфарин, статины, антигипертензивные препараты.
Объективно: температура тела – 37,4 °С, аускультативно – дыхание жесткое, выслушиваются двусторонние сухие гудящие хрипы.
Данные лабораторных и инструментальных исследований: общий анализ крови – лейкоцитоз (10,8×109/л), СОЭ – 28 мм/ч; спирография – показатели функции внешнего дыхания в пределах возрастной нормы; рентгенография ОГП – инфильтративных изменений не обнаружено.
На основании данных клинического осмотра и результатов дополнительных методов диагностики установлен диагноз: «ОБ бактериальной этиологии. Варикозная болезнь, состояние после ТЭЛА (средних ветвей в средней доле справа). Гипертоническая болезнь, 2 ст. Непостоянная систолическая аритмия, НК I. Цереброваскулярная болезнь. ТИА в анамнезе».
Обоснование выбора терапевтической тактики:
экспертное мнение
Диагноз ОБ устанавливают при наличии остро возникшего кашля, продолжающегося ≥3 нед (вне зависимости от наличия мокроты), и других симптомов инфекционного поражения нижних дыхательных путей в отсутствие признаков пневмонии и хронической патологии легких, сопровождающейся кашлем. По сути, ОБ является диагнозом исключения.
Хотя ОБ лидирует среди причин назначения АБТ по поводу острых респираторных инфекций, известно, что в подавляющем большинстве случаев его провоцируют вирусы. Менее чем у 10% больных заболевание имеет бактериальную природу: в 45% случаев обнаруживаются типичные возбудители – Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Staphylococcus aureus; в 25% случаев выявляются атипичные патогены – Mycoplasma pneumoniae, Chlamydophila pneumoniae, Bordetella pertussis.
На бактериальную природу заболевания указывают снижение температуры тела до нормальных цифр после вирусной инфекции, наличие слизисто-гнойной или гнойной мокроты, выраженная интоксикация, измененные физикальные данные и показатели общего анализа крови, что соответствует клинической картине у данного пациента.
Согласно действующим рекомендациям в качестве стартовой терапии ОБ следует назначать амоксициллин или макролид перорально. В.Е. Ноников (2008) предлагает использовать в качестве средств первой линии доксициклин, макролиды, респираторные фторхинолоны (ФХ), в качестве альтернативных препаратов – β-лактамы в таблетированных формах.
Назначение тетрациклинов нежелательно в силу тяжелых побочных эффектов со стороны желудочно-кишечного тракта (боль, дискомфорт, тошнота, рвота, диарея) и нервной системы (головокружение и т. п.), гепатотоксичности, фотосенсибилизации, возможного поражения зубов (изменение цвета эмали на желтый или серо-коричневый, появление дефектов эмали), частых аллергических реакций (при этом существует высокая вероятность перекрестной аллергии к другим представителям класса). В то же время применение ФХ (вследствие их сверхширокого спектра действия) для лечения ОБ можно сравнить со стрельбой из пушки по воробьям.
При сочетанном наличии типичных и атипичных патогенов у пациентов с инфекцией нижних дыхательных путей оптимальным вариантом представляются макролиды. Это может быть спирамицин, обладающий высокой активностью относительно как внутриклеточных патогенов (M. pneumoniae, C. pneumoniae, B. pertussis), так и типичных возбудителей. Спектр активности препарата, помимо воздействия на атипичную флору, включает S. pneumoniae, S. pyogenes, Staphylococcus spp. (кроме метициллинпродуцирующих штаммов), M. catarrhalis, H. influenzaе (умеренная активность).
Интересный факт
В литературе описан т. н. парадокс спирамицина: несовпадение его эффективности в лабораторных условиях и в реальной клинической практике вызвало удивление и, как следствие, повышенный интерес специалистов. Суть этого феномена такова, что активность антибиотика in vitro умеренная, тогда как in vivo – гораздо выше.
Л.В. Юдина подчеркнула, что в качестве стартовой АБТ данному пациенту можно назначить макролиды, и перечислила аргументы в пользу выбора 16-членного макролида спирамицина:
- воздействие на типичную и атипичную флору;
- высокие концентрации внутри клеток, превышающие уровень в крови в 20-30 раз, сохраняющиеся длительно (69 ч – в альвеолярных макрофагах, 30 ч – в нейтрофильных гранулоцитах);
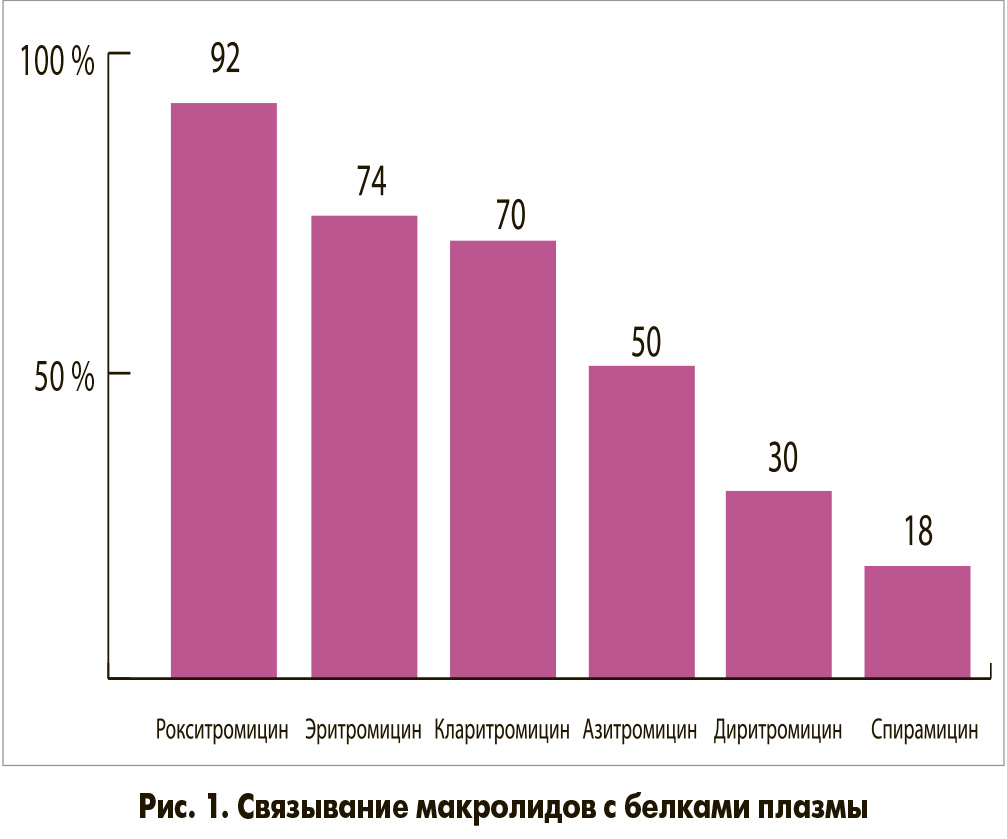
- способность накапливаться в тканях и секретах дыхательных путей в силу низкого (на уровне 10-18%) связывания с белками плазмы (рис. 1);
- более стойкое связывание и длительное антибактериальное воздействие (за счет взаимодействия с тремя доменами 50S-субъединицы рибосомы);
- постантибиотический эффект;
- низкий уровень резистентности;
- отсутствие прокинетической активности (сопряжено с уменьшением риска возникновения диареи);
- иммуномодулирующие свойства;
- отсутствие влияния на цитохром Р450 и, соответственно, минимальный риск лекарственных взаимодействий (рис. 2);
- отсутствие перекрестной резистентности с β-лактамами;
- хорошая переносимость;
- удобный режим приема;
- демократичная стоимость.
Интересный факт
Благодаря тому, что спирамицин не подвергается эффлюксу, он сохраняет активность в отношении ряда штаммов грамположительных кокков с приобретенной резистентностью к 14- и 15-членным макролидам.
Некоторые макролиды усиливают гипопротромбинемию при сочетанном использовании с непрямыми антикоагулянтами, повышают токсичность карбамазепина, сердечных гликозидов. В отличие от других представителей класса спирамицин можно применять у пациентов, получающих антациды, антиаритмические, антигистаминные средства, ксантины, оральные контрацептивы, преднизолон, рифампицин, статины. Спирамицин безопасно сочетается с непрямыми антикоагулянтами, сердечными гликозидами (что актуально для описываемой клинической ситуации) и, как уже указывалось, минимально угнетает цитохром Р450 печени.
«Эффективность и безопасность спирамицина подтверждены десятилетиями практического применения. Показательно, что спирамицин, полученный из Streptomyces ambofaciens еще в 1951 г., до сих пор не утратил актуальности и широко используется в ежедневной практике», – прокомментировала Л.В. Юдина.
Лечение: спирамицин (Ровамицин®) по 3 млн МЕ 2 р/сут курсом 5 дней, фиксированная комбинация ацетилцистеин/амброксол (ПульмоБРИЗ по 1 таблетке 3 р/сут в течение 7 дней).
Ответ на вопрос «Чего хотят пациенты?» лежит на поверхности: быстро и безопасно восстановить хорошее самочувствие. В то же время клиницисты стремятся иметь в арсенале антибактериальные средства, при выборе которых нет необходимости искать компромисс между эффективностью и безопасностью. Антибиотиком с уникальными фармакокинетическими характеристиками, который после более чем полувекового применения переживает «вторую молодость», является спирамицин.
Как отмечают профильные эксперты, с учетом катастрофического дефицита на рынке новых молекул и повышения угрозы антибиотикорезистентности не вызывает сомнений необходимость переоценки свойств данного препарата и более широкого его использования врачами первичного звена. Дейл Карнеги утверждал: «Есть только один способ воздействовать на другого человека – говорить с ним о том, что ему необходимо, и показать, как этого достичь». Именно демонстрация собственного положительного опыта – наиболее убедительный аргумент в медицинской практике.
Подготовила Ольга Радучич
| Медична газета «Здоров’я України» № 24 (373), грудень 2015 p. |