29 грудня, 2015
Антибиотики в лечении негоспитальной пневмонии: классика и современность
Не бойся, что не знаешь, бойся, что не учишься.
Китайская пословица
С наступлением сезона инфекционных заболеваний перед врачами общей практики, пульмонологами, педиатрами и другими специалистами все чаще возникает вопрос: нужно ли назначать антибактериальные препараты (АБП) таким пациентам? И если да, то какому классу антибиотиков и конкретному его представителю стоит отдать предпочтение? Изменяется ли терапевтическая тактика в случае наличия у больного коморбидной патологии, требующей приема других лекарственных средств?
Несмотря на прогрессивные достижения в мире медицины, непрерывное пополнение доказательной базы результатами новых исследований и, казалось бы, перенасыщенность специализированными ресурсами и профильными мероприятиями, предоставляющими исчерпывающую информацию касательно диагностики и лечения негоспитальной пневмонии (НП), многие вопросы остаются открытыми, а уровень смертности в мире вследствие НП недопустимо высок – 4 млн летальных исходов ежегодно.
Вопреки кажущейся простоте диагностика НП часто сопряжена с трудностями, а видимое «изобилие» антибиотиков, назначение едва ли не каждого из которых оправданно, – не более чем иллюзия, имеющая мало общего с реальностью. Всегда возникает вопрос о целесообразности назначения «лучшего» антибиотика.
 В показаниях к антибиотикотерапии (АБТ) при НП, тонкостях ее проведения и нюансах назначения так называемым сложным пациентам разбиралась доцент кафедры фтизиатрии и пульмонологии Национальной медицинской академии последипломного образования им. П.Л. Шупика (г. Киев), кандидат медицинских наук Людмила Владимировна Юдина. В ходе интерактивного мастер-класса «Новые возможности диагностики и лечения респираторных бактериальных инфекций» (симпозиум «Актуальные вопросы семейной медицины», который состоялся в рамках VIII Национального конгресса «Человек и лекарство – Украина») докладчик презентовала показательные клинические случаи, на примере которых проанализировала преимущества и недостатки часто использующихся групп АБП.
В показаниях к антибиотикотерапии (АБТ) при НП, тонкостях ее проведения и нюансах назначения так называемым сложным пациентам разбиралась доцент кафедры фтизиатрии и пульмонологии Национальной медицинской академии последипломного образования им. П.Л. Шупика (г. Киев), кандидат медицинских наук Людмила Владимировна Юдина. В ходе интерактивного мастер-класса «Новые возможности диагностики и лечения респираторных бактериальных инфекций» (симпозиум «Актуальные вопросы семейной медицины», который состоялся в рамках VIII Национального конгресса «Человек и лекарство – Украина») докладчик презентовала показательные клинические случаи, на примере которых проанализировала преимущества и недостатки часто использующихся групп АБП.
Один из них мы представляем Вашему вниманию.
Клинический случай
Пациентка Е., 22 лет, обратилась с жалобами на кашель с трудно отделяемой мокротой слизисто-гнойного характера, повышение температуры тела до 37,8 °С, заложенность носа (со слов больной, она возникала в течение последних 2 лет в весенний период во время цветения растений), затрудненное дыхание ночью, «свист» в груди. При аускультации над легкими выслушивались сухие свистящие двусторонние хрипы, справа в межлопаточной области – крепитация.
Из анамнеза известно, что пациентка неоднократно посещала медицинских специалистов и получала терапию по поводу «бронхита с астматическим компонентом» в амбулаторных условиях. На момент обращения принимала диазолин, теофиллин.
Лабораторные и инструментальные исследования: в общем анализе крови отмечаются лейкоцитоз (10,8×109/л), повышение уровня палочкоядерных нейтрофилов (14%) и эозинофилов (12%), увеличение СОЭ (32 мм/ч); при рентгенографии органов грудной полости (ОГП) в двух проекциях обнаружена инфильтрация верхней доли правого легкого. Учитывая указание GINA (2007) о том, что «все, что сопровождается свистящими хрипами, принято считать бронхиальной астмой, пока не будет доказано обратное», выполнена спирография. Исследование продемонстрировало выраженное нарушение функции внешнего дыхания, ощутимое снижение ОФВ1 (50,8%), признаки поражения мелких, средних и крупных бронхов, значительный прирост этих показателей после пробы с бронхолитиком.
На основании имеющихся данных установлен диагноз: «Негоспитальная пневмония верхней доли правого легкого, I клиническая группа, поллиноз, аллергический ринит, персистирующая неконтролируемая бронхиальная астма (БА)».
Обоснование выбора терапевтической стратегии: мнение эксперта
Оптимальным представляется назначение комплексной терапии, включающей АБП, антигистаминные средства, муколитики, ингаляционные кортикостероиды (ИКС), бронхолитики. Докладчик акцентировала внимание на необходимости назначения ИКС при БА и процитировала известного английского пульмонолога Питера Барнса, утверждавшего, что «лечить БА без глюкокортикоидов – все равно, что красить поверх ржавчины». Назначение антимикотиков с профилактической целью (показано только пациентам с тяжелой иммуносупрессией), равно как и использование иммуномодуляторов, пробиотиков и др., является нецелесообразным, т. к. не имеет доказательной базы.
При выборе АБП необходимо ориентироваться на следующие критерии:
• активность в отношении наиболее частых возбудителей заболевания;
• минимальное повреждающее действие на макроорганизм;
• способность создавать и длительно сохранять терапевтические концентрации в тканях и жидкостях организма.
Ключевым возбудителем НП являются Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis. Реже встречается атипичная флора.
Подходы к АБТ у пациентов с НП в амбулаторных условиях регламентированы приказом МЗ Украины от 19.03. 2007 г. № 128 (табл. 1).
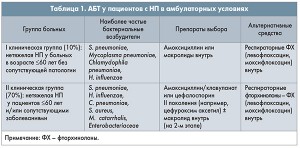 В соответствии с отечественным согласительным документом препаратом выбора для стартовой АБТ при НП является амоксициллин или макролид перорально. Применение ФХ у больных БА лимитировано широким спектром действия. С учетом наличия у пациентки атопии и БА предпочтителен макролид, так как представители этого класса реализуют противовоспалительное и иммуномодулирующее влияние, обладают хорошим профилем безопасности, оказывают постантибиотический эффект, создают высокие концентрации в клетках и тканях.
В соответствии с отечественным согласительным документом препаратом выбора для стартовой АБТ при НП является амоксициллин или макролид перорально. Применение ФХ у больных БА лимитировано широким спектром действия. С учетом наличия у пациентки атопии и БА предпочтителен макролид, так как представители этого класса реализуют противовоспалительное и иммуномодулирующее влияние, обладают хорошим профилем безопасности, оказывают постантибиотический эффект, создают высокие концентрации в клетках и тканях.
Кроме этого, при БА следует избегать назначения β-лактамных АБП даже при отсутствии аллергии на них в анамнезе, т. к. пенициллины и их производные занимают второе место в структуре причин астматических состояний.
Накоплен большой опыт применения 16-членного природного макролида спирамицина, который был получен в 1951 г. (условное разделение макролидов на ранние и новые представлено в таблице 2). Продуцирующий его микроорганизм – S. ambofaciens – был выделен из почвы на юге Франции.
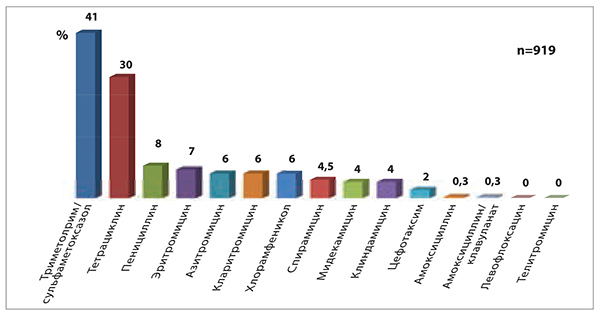
 Спектр активности препарата включает S. pneumoniae, S. pyogenes, Staphylococcus spp. (кроме метициллинпродуцирующих штаммов), H. influenzaе (умеренная активность), M. catarrhalis, Bordetella pertussis, внутриклеточных возбудителей. Несмотря на длительный опыт клинического применения спирамицина у ключевых патогенов, провоцирующих респираторные инфекции, он по-прежнему сохраняет актуальность: как показывают данные ПеГАС-II (Козлов Р.С., 2005), в РФ почти 96% штаммов S. pneumoniae сохраняют чувствительность к спирамицину (для сравнения: к триметоприму/сульфаметоксазолу и тетрациклину оказались устойчивы 41 и 30% штаммов соответственно, к эритромицину – 7%, кларитромицину и азитромицину – по 6%; рис.).
Спектр активности препарата включает S. pneumoniae, S. pyogenes, Staphylococcus spp. (кроме метициллинпродуцирующих штаммов), H. influenzaе (умеренная активность), M. catarrhalis, Bordetella pertussis, внутриклеточных возбудителей. Несмотря на длительный опыт клинического применения спирамицина у ключевых патогенов, провоцирующих респираторные инфекции, он по-прежнему сохраняет актуальность: как показывают данные ПеГАС-II (Козлов Р.С., 2005), в РФ почти 96% штаммов S. pneumoniae сохраняют чувствительность к спирамицину (для сравнения: к триметоприму/сульфаметоксазолу и тетрациклину оказались устойчивы 41 и 30% штаммов соответственно, к эритромицину – 7%, кларитромицину и азитромицину – по 6%; рис.).
Благодаря отсутствию влияния на Р450 указанный АБП отличается минимальным риском реакций с другими лекарственными средствами (в т. ч. антигистаминными препаратами и ксантинами, которые получает пациентка).
Способность макролидов к лекарственному взаимодействию (по убыванию; Страчунский Л.С. и соавт.): кларитромицин → эритромицин → джозамицин = мидекамицин → рокситромицин → азитромицин → спирамицин.
Многочисленные работы подтверждают отличный профиль безопасности препарата: он разрешен для применения у беременных, пациентов с почечной и печеночной недостаточностью, не обладает ото-, кардио- и гепатотоксичностью, не сопровождается нейросенсорными расстройствами, характеризуется минимальным риском побочных эффектов и низким аллергенным потенциалом. Спирамицин в незначительной степени (на 18%) связывается с белками плазмы, за счет чего способен создавать высокие концентрации внутри клеток и в тканях, и отличается длительным периодом полувыведения (36 vs 9 ч для эритромицина). Продолжительное пребывание внутри альвеолярных макрофагов (69 ч) и нейтрофильных гранулоцитов (30 ч) позволяет данному макролиду реализовать бактерицидное влияние в отношении внутриклеточных патогенов (Яковлев С.В., 1997).
Поскольку у пациентки наблюдается наличие вязкой трудноотделяемой мокроты, следует назначить препараты, облегчающие кашель и усиливающие выведение бронхиального секрета (некоторые из них, например амброксол, потенцируют действие антибиотиков – макролидов, β-лактамов, ФХ); с целью купирования проявлений аллергии показаны антигистаминные средства.
Лечение: спирамицин (Ровамицин®) в дозе 3 млн МЕ 2 р/сут курсом 5 дней; фиксированная комбинация лоратадин/амброксол (Пульмолор по 1 таблетке 2 р/сут курсом 7 дней); для купирования обострения БА – сальбутамол и флутиказон (2,0 мл 2 р/сут через небулайзер курсом 5 дней).
При повторном осмотре после проведенной терапии отмечены значительное улучшение показателей спирографии и нормализация рентгенологической картины (инфильтрации не выявлено).
«Спирамицин остается одним из немногих природных антибиотиков, которые выдержали испытание временем и сохраняют свое значение в новом тысячелетии, на фоне роста резистентности микроорганизмов и снижения скорости появления новых препаратов», – утверждал известный эксперт в области АБТ, профессор Л.С. Страчунский еще в 2005 г.
Ошибочное мнение, что в силу длительного присутствия спирамицина на фармацевтическом рынке уровень устойчивости основных возбудителей к данному АБП высок, абсолютно четко опровергают многочисленные научные исследования. Данный макролид по праву можно назвать «классикой, проверенной многими поколениями», не теряющей актуальности в современной АБТ.
Подготовила Ольга Радучич