5 листопада, 2016
Обзор международных рекомендаций относительно диагностики и лечения хронической крапивницы
Международные и американские руководства по диагностике и лечению хронической крапивницы (ХК) предписывают проведение тщательного сбора анамнеза, физикального обследования, рутинных лабораторных обследований и ступенчатый подход к лечению. Некоторые из этих рекомендаций отличаются по ряду позиций, например в отношении порядка диагностических процедур и лечения пациентов, не отвечающих на терапию антигистаминными препаратами (АГП) в стандартных дозах. Пациентам с ХК обычно назначают АГП второго поколения – рекомендованные препараты первой линии. При выборе лечения, отличного от АГП, следует принимать во внимание преимущества и недостатки каждого фармацевтического препарата.
Крапивница характеризуется наличием волдырей, ангиоотеком или двумя этими проявлениями и считается хронической, если симптомы сохраняются в течение ≥6 нед (Zuberbier T. et al., 2014; Bernstein J. A. et al., 2014). Понимание клинических проявлений, ассоциированных с ХК и ее подтипами, а также возможных методов лечения способно улучшить диагностику и оптимизировать клиническую тактику при этом заболевании. Целью этой статьи является освещение проблемы ХК, а также обзор рекомендаций относительно диагностики и стратегий лечения, основанных на доказательной базе.
Патогенез заболевания
Хроническую крапивницу можно условно разделить на характеризующуюся спонтанным началом симптомов и индуцированную/физическую крапивницу, когда симптомы возникают после контакта со специфическими факторами (давление, холод, тепло). Возможно сосуществование ≥2 форм ХК у одного пациента (Zuberbier T. et al., 2014; Bernstein J. A. et al., 2014).
Несмотря на то что патогенез ХК недостаточно изучен, установлено, что ключевую роль в нем играют тучные клетки и базофилы, гистамин, а также другие медиаторы (Kaplan A. P. et al., 1978; Chang T. W. et al., 2015; Jacques P. et al., 1992; Ying S. et al., 2002). Высвобождение гистамина и подобных провоспалительных веществ в результате дегрануляции тучных клеток считается окончательным общим путем возникновения и для ХК, индуцированной физическими факторами (ХКИФФ), и для спонтанной ХК (СХК). Этот элемент патогенеза является основанием для назначения АГП в качестве терапии ХК первой линии. Однако факторы, ведущие к дегрануляции тканевых тучных клеток или базофилов, менее ясны и, возможно, отличаются для ХКИФФ и аутоиммунной ХК. Считается, что при аутоиммунном ответе задействованы аутореактивные антитела IgE против аутоаллергенов, или аутореактивные антитела IgG против высокоаффинных рецепторов тучных клеток (или базофилов) FcεRI и/или IgE (Chang T. W. et al., 2015). Концепция центральной роли IgE и FcεRI в запуске дегрануляции тучных клеток стала поводом для испытаний новых средств лечения, например омализумаба. Некоторые авторы считают, что идиопатическая ХК в большинстве случаев вызвана аутоиммунной реакцией организма, другими причинами развития крапивницы могут стать инфекции, аутоиммунные заболевания, непереносимость пищевых продуктов или медикаментов (Bernstein J. A. et al., 2014; Chang T. W. et al., 2015; Zuberbier Т. et al., 2014).
Исследование, проведенное в Германии T. Zuberbier и соавт. (2010), выявило, что риск развития ХК на протяжении жизни составляет 1,8%. Большинство случаев ХК (по данным разных авторов, от 66 до 93%) – это спонтанный подтип болезни (Maurer М. et al., 2011). У многих пациентов симптомы сохраняются на протяжении года, а у 14% больных наблюдаются периодические вспышки симптомов в течение >5 лет (Toubi Е. et al., 2004; Gaig Р. et al., 2004).
Было установлено, что влияние ХК на качество жизни пациентов аналогично влиянию ишемической болезни сердца и превышает влияние респираторной аллергии, круглогодичного ринита и интермиттирующей астмы (Baiardini I. et al., 2003; O’Donnell B.F. et al., 1997). Негативное влияние ХК на качество жизни больных аналогично таковому при других заболеваниях кожи (псориазе, акне или атопическом дерматите), а иногда это влияние существенно больше (Grob J. J. et al., 2005; Poon Е. et al., 1999; Lennox R. D. et al., 2004).
ХК считается заболеванием с затратной экономической составляющей. Согласно данным за 2004-2006 гг., средние прямые и непрямые ежегодные расходы на СХК в США, по оценкам экспертов, составляют 244 млн долларов. Из них 62,5% – это траты на медикаменты, а 15,7% – утраченная заработная плата вследствие амбулаторного лечения или временной потери трудоспособности (Delong L. K. et al., 2008).
Кроме того, крупное популяционное исследование показало, что аутоиммунные заболевания (преимущественно болезни щитовидной железы) значительно чаще встречаются у пациентов с ХК, чем у участников в контрольной группе без этого диагноза (Confino-Cohen R. et al., 2010).
Роль специалистов
Многочисленные клинические исследования обеспечили доказательную базу для использования рекомендованных доз АГП второго поколения в качестве терапии ХК первой линии (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014). Тем не менее опрос 776 врачей (43,0% дерматологов, 28,7% педиатров и 27,5% врачей общей практики), проведенный в 2009 г. в Германии, обнаружил, что значительное число опрошенных использовали в качестве препаратов первой линии седативные антигистаминные препараты и оральные кортикостероиды (23,0 и 17,9% соответственно). Только треть докторов ответили, что они ознакомлены с международными рекомендациями; наиболее высокий уровень осведомленности продемонстрировали дерматологи (50,6%), для сравнения – у педиатров и врачей общей практики он равнялся 24,2 и 12,6% соответственно (Weller К. et al., 2013).
Авторы британского одномоментного исследования отметили, что из 64 дерматологов только 48 (75,0%) использовали рекомендации для диагностики и лечения ХК. У аллергологов и иммунологов этот показатель был выше: 50 специалистов из 55 (90,9%) (Wu С. Н.et al., 2015). В отличие от уже упомянутого немецкого исследования все врачи-участники сообщили об использовании АГП второго поколения в качестве терапии первой линии.
В онлайн-опросе, проведенном канадскими исследователями, АГП в качестве препаратов выбора применяли 96,8% респондентов. 16,1% участников исследования сообщили о количестве пациентов с рефрактерной ХК на уровне >50%. Значительные разногласия среди опрошенных вызвал вопрос о дополнительной терапии, а большинство респондентов (59,7%) не были ознакомлены с международными рекомендациями (Cheung L. Y. et al., 2016).
Низкий уровень осведомленности врачей в этой области иллюстрирует и датское исследование, в котором было отмечено, что пациенты, обращавшиеся в специализированную клинику в 2009-2011 гг., в основном получали лечение, заключающееся в недостаточных дозах АГП второго поколения (Kibsgaard L. et al., 2014).
В рекомендациях по лечению ХК прослеживается консенсус относительно увеличения дозы АГП второго поколения у пациентов с СХК, не отвечающих на стандартные дозы в достаточной мере (Weller К. et al., 2013), тем не менее даже в условиях назначения высоких доз этих препаратов некоторые пациенты остаются АГП-резистентными.
Диагностика
Характерными кожными проявлениями ХК являются отечные зудящие розовые (красные) волдыри разного размера и формы, не сопровождающиеся никакими эпидермальными изменениями (корка, десквамация). Отдельные элементы высыпания скоротечны и обычно исчезают в течение 24 ч. Ангиоотек охватывает нижние слои дермы и подкожную клетчатку с частым вовлечением в процесс слизистых оболочек (отек глаз или губ) или возникновением тяжелого периферического отека. Тяжелые отеки могут быть болезненными и сохраняться достаточно долго (до 72 ч) (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014).
Диагностика начинается с тщательного сбора анамнеза и физикального обследования (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014). При наличии соответствующих показаний согласно анамнезу рекомендуются провокационные тесты (холодовые пробы, использование дермографометра) для подтверждения наличия триггеров ХК у пациентов с ХКИФФ (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014). Следует отметить, что не всегда есть необходимость исследовать все возможные причинные факторы болезни (Zuberbier Т. et al., 2014). Например, попытки идентифицировать лежащие в основе крапивницы причины следует ограничить у пациентов с длительным и/или тяжелым течением ХК. Важно проинформировать пациентов о том, что в большинстве случаев СХК идентификация причин маловероятна (Bernstein J. A. et al., 2014).
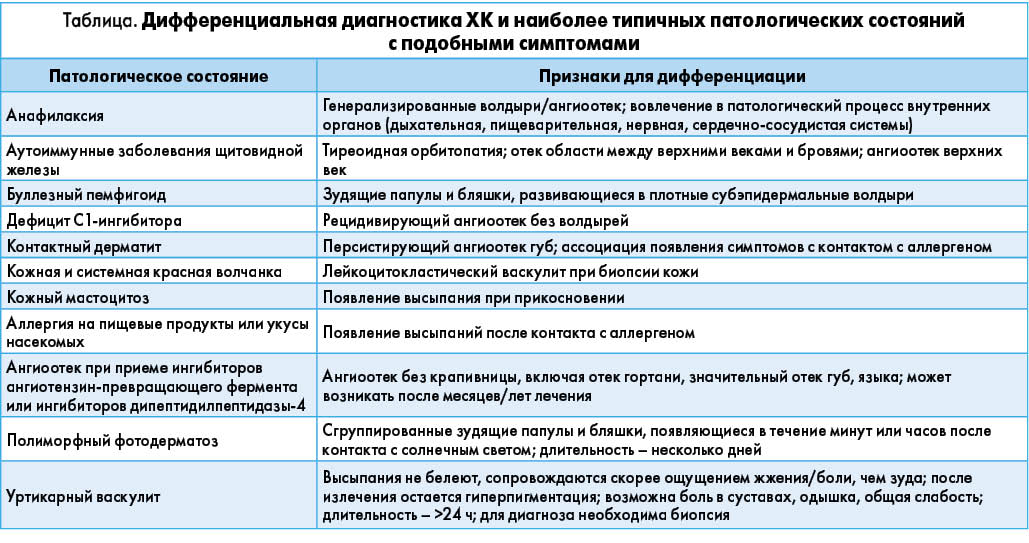
Рекомендованные диагностические обследования могут помочь идентифицировать подтипы ХК и облегчить дифференциальный диагноз (табл.). В большинстве случаев рефрактерной ХК потребности в биопсии кожи нет, этот метод обследования следует использовать только при подозрении на васкулит, аутоиммунное воспалительное заболевание или другое нарушение иммунного генеза, которое может проявляться подобными высыпаниями (например, буллезный пемфигоид) (Bernstein J. A. et al., 2014).
Лечение
Стандартные дозы АГП второго поколения являются терапией ХК первой линии, рекомендуемой во всем мире (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014) и основанной на эффективности, продемонстрированной в двойных слепых клинических исследованиях (Ortonne J. P. et al., 2007; Kapp А. et al., 2006; Kaplan А. Р. et al., 2005). Поскольку к настоящему времени проведено еще недостаточно сравнительных исследований для определения препарата выбора и каждый пациент может по-разному отвечать на лечение (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014; Greene S. L. et al., 1985), назначение конкретного препарата остается на усмотрение лечащего врача. У пациентов, не отвечающих на рекомендованные дозы, следует применить прогрессивное увеличение доз до 4 раз (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014). Исследования подтвердили, что увеличение дозы АГП может улучшить контроль симптомов ХК, хотя данные насчет некоторых препаратов являются ограниченными и противоречивыми (Stevska М. et al., 2010; Kameyoshi Y. et al., 2007; Metz М. et al., 2010; Jauregui I. et al., 2013; Siebenhaar F. et al., 2009).
Полученный нами опыт показывает, что ~50% всех пациентов с ХК отвечают на АГП в стандартных дозах, а 10-25% – в увеличенных. Тем не менее важно убедиться, что пациенты придерживаются назначенной дозы и режима приема препаратов (Maurer М. et al., 2009; Khan D. A., 2013). Для пациентов, не отвечающих на монотерапию, существуют дополнительные возможности лечения (Bernstein J. A. et al., 2014). Следует отметить, что американские руководства, в отличие от международных, советуют добавлять в схему лечения еще один препарат группы АГП второго поколения и/или H2-антагонист. Информации насчет эффективности и безопасности подобной комбинированной терапии достаточно мало (Schulz S. et al., 2009; Staevska М. et al., 2014), но очевидно, что подобрать соответствующую дозировку одного препарата безопаснее, чем усложнять лечение применением нескольких классов АГП (Zuberbier Т., 2012).
АГП первого поколения обладают хорошей эффективностью, но, учитывая более значительную седацию по сравнению с АГП второго поколения, должны использоваться с осторожностью (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014; Monroe E. W., 1992; Breneman D. L., 1996). Американские практические руководства предлагают принимать АГП первого поколения на ночь для уменьшения негативных проявлений в течение дня (Bernstein J. A. et al., 2014), однако и в этом случае они способны вызывать дневную сонливость, седацию, вялость, усталость и нарушения концентрации и памяти, особенно если препараты принимались поздним вечером или ночью (Church М. К. et al., 2009).
ХК считается рефрактерной при отсутствии клинического ответа на антигистаминную терапию. У пациентов с ХК, не контролируемой с помощью АГП, часто используются оральные кортикостероиды, хотя контролированных исследований по этому вопросу пока проведено не было (Bernstein J. A. et al., 2014; Asero R. et al., 2013). Крупное ретроспективное исследование показало, что у 50% пациентов с АГП-резистентной ХК, пролеченных одним курсом преднизона (3 дня по 25 мг/сут, 3 дня по 12,5 мг/сут и 4 дня по 6,25 мг/сут), наблюдалась ремиссия и еще 9% отвечали на лечение после второго такого же курса (Asero R. et al., 2013). Основной проблемой при использовании кортикостероидов является риск развития побочных эффектов, поэтому лечить обострения следует только кратковременными курсами терапии (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014).
Антагонисты лейкотриеновых рецепторов (АЛР), такие как монтелукаст и зафирлукаст, оказались эффективными для лечения ХК в качестве монотерапии или в комбинации с АГП. Наиболее убедительные доказательства имеются в отношении монтелукаста (10 мг/сут), хотя наблюдаемый эффект был малозначительным (Amin Р. et al., 2015; Ellis М. Н., 1998; Bagenstose S. E. et al., 2004; Erbagci Z., 2002; Nettis Е. et al., 2004). Результаты клинических исследований на эту тему несколько противоречивы: одни отмечают преимущество (Bagentstose S. E. et al., 2004; Nettis Е. et al., 2001; Pacor M. L. et al., 2001), другие – меньшую эффективность АЛР по сравнению с АГП (Di Lorenzo G. et al., 2004) или даже отсутствие эффекта по сравнению с плацебо (Reimers А. et al., 2002).
У пациентов с отсутствием ответа на АГП применяются также препараты с H1- и/или H2-антагонистическими свойствами (гидроксизин, ципрогептадин, доксепин), однако эти медикаменты имеют существенное седативное действие (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014).
Наиболее мощной доказательной базой в отношении эффективности лечения рефрактерной ХК обладает омализумаб – моноклональное антитело против IgE (Khan D. A., 2013), по состоянию на февраль 2016 г. это единственный препарат, одобренный FDA и Европейским агентством по лекарственным средствам, для лечения взрослых и подростков с рефрактерной спонтанной (идиопатической) ХК (European Medicine Agency, 2015). Хотя омализумаб, назначаемый в виде подкожных инъекций в дозе 150 или 300 мг каждые 4 нед, обладает хорошим соотношением польза/риск и хорошо переносился в клинических исследованиях (Kaplan А. et al., 2013; Maurer М. et al., 2013; Saini S. S. et al., 2015), была отмечена его связь с анафилаксией (Saini S. S. et al., 2015). Омализумаб также обеспечивает хороший эффект в качестве дополнительного препарата к АГП в сочетании с Н2-гистаминоблокатором и/или ЛМП у пациентов, не отвечающих на монотерапию АГП (Kaplan А. et al., 2013; Maurer М. et al., 2013; Saini S. S. et al., 2015). Однако его широкое использование может быть ограничено высокой стоимостью, необходимостью введения его в условиях медицинского учреждения и возможным развитием анафилаксии (Bernstein J. A. et al., 2014; Khan D. A., 2013).
Также у пациентов с рефрактерной ХК применяется циклоспорин А (Zuberbier Т. et al., 2014; Bernstein J. A. et al., 2014). При ХК эффективность приема этого иммуносупрессанта в дозе 3-5 мг/кг/сут в течение 4 нед была подтверждена в плацебо-контролированных исследованиях как в виде монотерапии, так и в комбинации с АГП второго поколения. Лечение циклоспорином А ассоциируется с относительно высокой частотой побочных эффектов умеренной силы, в том числе с нарушениями пищеварения, парестезиями и инфекционными процессами (Grattan С. Е. et al., 2000; Vena G. A. et al., 2006). Длительное применение циклоспорина А в низких дозах ассоциируется с нефротоксичностью (Isnard Bagnis С. et al., 2002). При назначении этого препарата особое внимание следует обратить на коморбидные состояния пациента, например лица с артериальной гипертензией и/или почечной недостаточностью не являются подходящими кандидатами для лечения циклоспорином А.
У пациентов с рефрактерной ХК можно применять дополнительные противовоспалительные препараты (ПВП) и иммуносупрессанты (Bernstein J. A. et al., 2014), хотя доказательная база по этому вопросу является недостаточной (Maurer М. et al., 2009; Bernstein J. A. et al., 2002; Asero R., 2005). ПВП, в т. ч. дапсон, сульфасалазин, гидроксихлорохин и колхицин, обладают небольшой доказательной базой касательно эффективности при ХК (Bernstein J. A. et al., 2014), но недавнее двойное слепое плацебо-контролированное исследование показало значительное уменьшение симптомов СХК на фоне приема дапсона в дозе 100 мг/сут (Morgan М. et al., 2014). Эффективность этих препаратов у пациентов с крапивницей, сопровождающейся высоким уровнем нейтрофилов, требует дальнейшего подтверждения. Открытое исследование установило, что среди пациентов с ХК с нейтрофильным воспалением кожи у 8 из 9 пролеченных колхицином и у 3 из 3 пролеченных дапсоном больных наблюдался ответ на лечение (Bernstein J. A. et al., 2014; Criado R. F. et al., 2008). Такие иммуносупрессанты, как такролимус, микофенолат и метотрексат, можно было бы рассматривать в качестве препаратов для лечения ХК, но клинических доказательств пользы их применения крайне мало (Bernstein J. A. et al., 2014). На данный момент существует потребность в новых, более эффективных, методах лечения рефрактерной ХК и проведении рандомизированных контролированных исследований для подтверждения клинической эффективности вышеперечисленных препаратов.
Оценка успешности лечения
Целью лечения ХК является достижение значительного уменьшения симптомов при минимальных побочных эффектах (Zuberbier Т. et al., 2014). Для объективной оценки ответа на терапию важно определить активность крапивницы у пациента в начале лечения и во время последующих визитов. Для определения и контроля активности заболевания в клинических исследованиях и повседневной практике используется индекс активности крапивницы – ИАК (Chakravarty S. D. et al., 2011; Mathias S. D. et al., 2012; Saini S. S. et al., 2015; Maurer М. et al., 2011). Рекомендованным подходом для оценки успешности лечения является сумма баллов ИАК (оценивается пациентом самостоятельно) за последние 7 дней (Zuberbier Т. et al., 2014; Mlynek А. et al., 2008). Можно также применять тест контроля крапивницы (Weller К. et al., 2014), визуальные аналоговые шкалы симптомов, сложно поддающихся объективному измерению, например интенсивности зуда (Izumi N. et al., 2008). Важным аспектом мониторинга активности заболевания является и оценка качества жизни (Zuberbier Т. et al., 2014): например, с помощью дерматологического индекса качества жизни (DLQI), который может значительно коррелировать с ИАК (Lennox R. D. et al., 2004; Mlynek А. et al., 2008), или опросника качества жизни для пациентов с ХК (CU-Q2oL), по сути единственного опросника, специфического для пациентов с СХК (Baiardini I. et al., 2011).
Выводы
ХК – комплексное заболевание, которое влечет за собой существенную экономическую нагрузку и значительное ухудшение качества жизни пациентов. Для точной диагностики ХК и определения объема необходимых лабораторных исследований следует тщательно собрать анамнез и провести физикальное обследование каждого больного.
Большинство пациентов адекватно отвечают на рекомендованные дозы АГП второго поколения, назначаемых в качестве терапии первой линии.
Пациентам, не достигшим значительного клинического улучшения, следует увеличить дозу этих неседативных АГП до 4 раз. По мнению авторов, увеличение дозы одного препарата в 4 раза является лучшим выбором, чем удвоение доз двух АГП второго поколения. Добавление седативного АГП для вечернего приема также может быть эффективным, но абсолютное большинство экспертов не рекомендуют комбинацию неседативного и седативного АГП.
Если изменение дозы АГП второго и первого поколения существенно не уменьшает симптомы ХК и/или побочные эффекты этих препаратов в высоких дозах являются неприемлемыми для больного, следует рассмотреть добавление омализумаба. В том случае, если он неэффективен, плохо переносится или недоступен, альтернативными препаратами являются циклоспорин А, дапсон, колхицин, микофенолат, сульфасалазин, ритуксимаб или АЛР. При выборе соответствующего лечения следует учесть преимущества и недостатки каждого препарата.
Beck L.A., Bernstein J.A., Maurer M. A Review of International Recommendations for the Diagnosis and Management of Chronic Urticaria.
Acta Derm Venereol 2016 Epub ahead of print Jun 28, 2016.
Перевела с англ. Лариса Стрильчук
Справка ЗУ
Алерзин (левоцетиризина дигидрохлорид) – антигистаминный препарат второго поколения производства Egis. В практике клинической аллергологии зарекомендовал себя как эффективное и безопасное средство. Алерзин влияет на гистаминзависимую стадию развития аллергической реакции, уменьшает миграцию эозинофилов, сосудистую проницаемость, ограничивает высвобождение медиаторов воспаления. Алерзин предупреждает развитие и облегчает течение аллергических реакций, обладает антиэкссудативным, противозудным, противовоспалительным действием и почти не оказывает антихолинергического и антисеротонинового действия. Показанием к примению Алерзина является симптоматическое лечение аллергического ринита (в том числе круглогодичного) и крапивницы. Препарат назначают взрослым и детям в возрасте от 6 мес внутрь 1 р/сут. Препарат можно применять без перерыва в течение 12 мес.
Медична газета «Здоров’я України 21 сторіччя» № 18 (391), вересень 2016