17 вересня, 2015
Дефіцит субкласів IgG: клініка, діагностика, лікування

Содержание статьи:
- Етіологія.
- Епідеміологія.
- Класифікація.
- Клінічні прояви.
- Клінічний перебіг.
- Діагностика.
- Диференційна діагностика.
- Лікування.
>>__Дефіцит субкласів (ДС) IgG – група поширених у популяції імунодефіцитних хвороб, пов’язаних зі зниженням сироваткової концентрації одного або кількох різновидів імуноглобулінів класу G [137]. Хоча частота цих порушень у світі достеменно не відома, ДС IgG вважається однією з найпоширеніших імунних дисфункцій. Марек Якобисяк засвідчує, що дефіцит одного з субкласів IgG має місце принаймні в 25% дітей, які перенесли щонайменше 7 інфекційних епізодів за 1 рік. Однак за результатами нещодавнього рандомізованого дослідження, проведеного Wågström P. зі співавт., частота інфекційних епізодів є недостатнім за валідністю критерієм ДС IgG, оскільки також має значення тяжкість, атиповість і пролонгованість інфекцій, а також розвиток автоімунних, алергічних і неопластичних ускладнень [176].
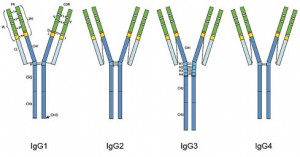
Виділяють 4 субкласи IgG, які позначають арабськими цифрами в порядку зменшення їх вмісту в сироватці крові (IgG1, IgG2, IgG3, IgG4; рис. 1). Субкласи різняться структурою константних ділянок, специфічністю до антигенів та функціональною активністю (див. таблицю). Клінічна картина дефіциту різних субкласів IgG дещо відрізняється відповідно до їх функціонального призначення. Якщо говорити про послідовність синтезу різних субкласів IgG під час імунної відповіді, то, згідно з останньою моделлю, запропонованою Collins A.M., Jackson K.J.L., при надходженні антигену спочатку виробляються низькоафінні IgE та IgG3, що є складовими негайної імунної відповіді, потім – високоафінні IgG1 та IgG2, що забезпечують кліренс середовищ від антигену, і зрештою – IgG4, що нарощують специфічність відповіді і реалізують блокувальний ефект щодо прозапальної активності інших імуноглобулінів [27].
Порівняльна характеристика субкласів IgG людини (за Bonilla F.A., 2008)
|
Назва |
% |
Активний транспорт через плаценту |
Активація комплементу |
Зв’язування з Fc-рецепторами фагоцитів |
Період напівжиття [7] |
|
IgG1 |
66% |
Так (1,47)* |
Висока, але нижча, ніж у IgG3 |
Високоафінне |
21 доба |
|
IgG2 |
23% |
Ні (0,8)* |
Помірна |
Дуже низька афінність |
21 доба |
|
IgG3 |
7% |
Так (1,17)* |
Найвища |
Високоафінне |
7 діб |
|
IgG4 |
4% |
Так (1,15)* |
Немає |
Помірна афінність |
21 доба |
Примітка: * співвідношення концентрацій пуповинна кров/материнська кров [58].
Етіологія
Добре відомі сімейні випадки ДС IgG вказують на генетичну основу цих розладів [31, 54, 102, 162]. Oxelius V.A. зі співавт. вивчили вміст субкласів IgG у матерів імуноскомпрометованих немовлят зі стрептококовою септицемією. У 13 з 19 матерів відзначався аналогічний імунодефіцит: 10 із них мали низьку концентрацію IgG2, 9 – IgG1, а 4 – IgG3. Відзначалася вірогідна різниця з контрольною групою здорових осіб [125].
Ці непрямі дані спонукали до проведення поглиблених генетичних досліджень при ізольованому ДС, завдяки яким встановили, що гомозиготні делеції генів константних ділянок імуноглобулінів 14-ї хромосоми є класичною причиною розвитку цього імунодефіциту в людей [90]. Так, Terada T. зі співавт. виявили делеції генів C alpha-1, psi C gamma, C gamma-2, C gamma-4 і C epsilon у пацієнта з дефіцитом IgG2, IgG4, IgA та IgE [164]. Тим не менше, Tashita H. зі співавт. ідентифікували інсерцію 1793insG в 4-му екзоні C gamma-2 у двох пацієнтів з ізольованим дефіцитом IgG2 [163]. Відомі транслокації генів субкласів IgG, що тісно пов’язані з непластичними ускладненнями [77].
Поліморфізми генів константних ділянок імуноглобулінів також можуть обумовлювати розвиток первинного імунодефіциту (рис. 2) [117]. Зокрема, алотип G3(g) є причиною ізольованого дефіциту IgG3 у людей, причому він часто поєднується з алотипом G2(n), що обумовлює комбінування з прихованим дефіцитом IgG2 [96]. У зв’язку з цим Miwa Y. зі співавт. не виявили делецій у структурних генах константної ділянки важких ланцюгів імуноглобулінів при сімейних формах ДС IgG, що вказувало на іншу генетичну природу хвороби [111].
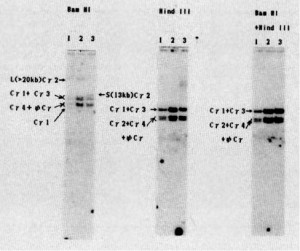 Рис. 2. Поліморфізм генів константних ділянок імуноглобулінів при проведенні гібридизації southern blot у пацієнта з первинним дефіцитом IgG2, IgG4 та IgE (за Ninomiya H. зі співавт.):
Рис. 2. Поліморфізм генів константних ділянок імуноглобулінів при проведенні гібридизації southern blot у пацієнта з первинним дефіцитом IgG2, IgG4 та IgE (за Ninomiya H. зі співавт.):1 – людська плацента; 2 – FLEB14-14; 3 – ДНК пацієнта
Seidel M.G. зі співавт. показали, що парціальна трисомія 19p13 призводила до комбінованого дефіциту IgG1 і IgG3 у одного пацієнта та вибіркового дефіциту IgМ – у іншого (рис. 3) [148]. Zhao Y. зі співавт. описали ізольований дефіцит IgG2 у пацієнта з точковою мутацією гена C gamma-2, що призводила до аномального сплайсингу [180]. Gallina R. зі співавт. у дослідженні за участю пацієнтів з верифікованим дефіцитом IgG4 та їхніх найближчих родичів показали тісну асоціацію цього імунодефіциту і структурного поліморфізму гена IGHC. Експресія алелю HLA-D сприяла розвитку дефіциту IgG4 в таких випадках [46].
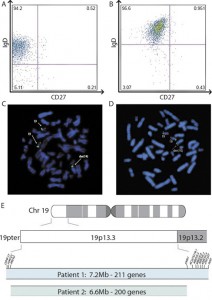 Рис. 3. Парціальна трисомія 19-ї хромосоми у пацієнтів з ізольованим ДС IgG або IgМ (за Seidel M.G. зі співавт.)
Рис. 3. Парціальна трисомія 19-ї хромосоми у пацієнтів з ізольованим ДС IgG або IgМ (за Seidel M.G. зі співавт.)ДС IgG може бути генетично детермінованим імунорегуляторним розладом, пов’язаним з утрудненням процесу переключення ізотипів антитіл під час імунної відповіді. Так, Péron S. зі співавт. описали гомозиготну мутацію гена PMS2, яка призводила до порушення переключення класів імуноглобулінів під час імунної відповіді і була причиною ізольованих дефіцитів класів та субкласів антитіл [132]. Kaneko H. зі співавт. виявили у пацієнтів з вибірковим дефіцитом IgG транскрипційний розлад у гамма-регіоні переключення ізотипів та гені інтерлейкіну-4 (IL-4) [73]. Відповідно до цього, аналіз northern blot виявив порушення механізму відкриття хроматинової структури в зоні переключення ізотипів константних ділянок важких ланцюгів імуноглобулінів при дефіциті IgA та субкласів IgG [84].
ДС IgG може бути наслідком субкомпенсації транзиторної гіпоімуноглобулінемії немовлят. Nettagul R. зі співавт. описали поступову зміну фенотипу транзиторної гіпоімуноглобулінемії немовлят, що проявлялась хронічною діареєю та 5 епізодами сепсису, до ізольованого дефіциту IgG2 з пом’якшенням клінічної картини і розвитком рецидивного середнього отиту і пневмоній [115]. ДС IgG може бути проявом субкомпенсованого загального варіабельного імунодефіциту. Так, Aghamohammadi A. зі співавт. встановили, що у родичів пацієнтів з загальним варіабельним імунодефіцитом у 30% випадків реєструється фенотип дефіцитів класів імуноглобулінів або субкласів IgG, здебільшого – IgG2 та IgG4 [3].
Cunningham-Rundles C. зі співавт. встановили, що алель HLA B38 асоційована з ДС IgG, особливо у разі поєднання цього розладу з дефіцитом IgА [28]. Алелі A*01-B*08, A*02-B*44 та A*29-B*44 тісно зв’язані як з ДС IgG, так і з загальним варіабельним імунодефіцитом, що вказує на спільність походження цих розладів [10]. Куріння може поглиблювати наявний ДС IgG, як це показали в спеціальному дослідженні Popa V. зі співавт. [135].
Епідеміологія
За даними Kuijpers T.W., у дітей, що страждають на рецидивні респіраторні інфекції, ДС IgG зустрічається в 20% випадків [86], однак поширеність імунодефіциту в загальній популяції залишається неуточненою. Як повідомляють Gallina R. зі співавт., серед італійців ізольований дефіцит IgG4 зустрічається з частотою 1 випадок на 400 мешканців [46].
У дітей ДС IgG зустрічається частіше, ніж у дорослих, хоча поширеність імунодефіциту серед дорослого населення також є високою.
Вважають, що чоловіки і жінки хворіють з однаковою частотою. Однак Hanson L.A. зі співавт. встановлили, що серед дітей на ДС IgG частіше страждають хлопчики (співвідношення хлопчики:дівчата – 3:1), тоді як серед дорослих імунодефіцит частіше реєструється у жінок (співвідношення чоловіки:жінки – 1:3) [59]. Feldman C. зі співавт. у спеціально спланованому дослідженні не виявили суттєвих відмінностей у клінічних проявах імунодефіциту серед представників білої і чорної раси [43].
Popa V. зі співавт. виявили гуморальний імунодефіцит у 58 із 136 дорослих пацієнтів з рецидивними респіраторними інфекціями. Дефіцит IgA відзначався в 3 випадках, дефіцит IgM – також в 3, тоді як 52 осіб мали дефіцит тотального IgG або субкласів IgG. Найчастіше зустрічався ізольований дефіцит певного субкласу IgG, особливо IgG3 або IgG4, а також помірне зниження концентрації тотального IgG (між 450 і 650 мг/дл) [136].
Stanford E. зі співавт. вивчили поширеність ДС серед 172 дітей з інвазивною пневмококовою інфекцією. Гуморальні імунні порушення виявлені в 11% випадків. Відзначалася кореляція між глибиною дефіциту IgG та кількістю серотипів пневмокока, до яких формувалась непротективна імунна відповідь після вакцинації. Невдачі вакцинації асоціювались з дефіцитом IgG вдвічі частіше, ніж у загальній групі. Було багато випадків субнормальних рівнів IgG або транзиторних порушень, які, однак, призводили до розвитку тяжких клінічних симптомів [155].
Kim J.H. зі співавт. провели ретроспективне дослідження за участю 55 дорослих з первинними імунодефіцитами, діагноз яких був виставлений у період між 1998 і 2009 р. у територіальному медичному центрі Кореї. ДС IgG зустрічалися найчастіше і мали місце в 67% випадків. Дефіцит тотального IgG діагностовано у 20%, IgМ – 7%, загальний варіабельний імунодефіцит – в 2% випадків, а Х-зчеплена агаммаглобулінемія – ще у 2 % випадків. Дефіцити IgG3 та IgG4 зустрічалися найчастіше (рис. 4) [80].
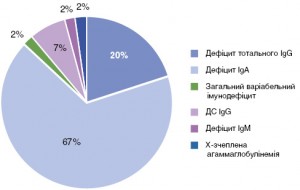 Рис. 4. Структура гуморальних імунодефіцитів у пацієнтів з рецидивними респіраторними інфекціями (за Kim J.H. зі співавт.)
Рис. 4. Структура гуморальних імунодефіцитів у пацієнтів з рецидивними респіраторними інфекціями (за Kim J.H. зі співавт.)Santaella M.L. зі співавт. встановили, що ДС IgG зустрічається щонайменше у 18,5% випадків серед пацієнтів з дефіцитом IgА, тоді як дефіцит манозозв’язувального білка – лише у 3,7% випадків. Додатковий субкласовий дефіцит поглиблював тяжкість інфекції та підвищував ризик розвитку атопії [145]. Водночас, компенсаторна гіпергаммаглобулінемія зустрічається щонайменше в 60% випадків при дефіциті IgА [97].
Vendrell M. зі співавт. показали, що ДС IgG відзначався щонайменше в 11% випадків серед пацієнтів з бронхоектазами невідомого походження. Особливо часто мав місце дефіцит IgG2, що обумовлював аномально слабку відповідь до Streptococcus pneumoniae і Haemophilus influenzae типу b. Імовірність дефіциту IgG2 становила 58%, якщо в клінічній картині паралельно відзначався рецидивний середній отит [171].
Thakar Y.S. зі співавт. у контрольованому дослідженні за участю 734 пацієнтів з інфекційним синдромом виявили ДС IgG у 38 випадках (5%), що було вірогідно вище, ніж серед 100 здорових осіб контрольної групи [166].
Martinot M. зі співавт. дослідили поширеність дефіциту класів антитіл серед 119 пацієнтів з інвазивними інфекціями, спричиненими S. pneumoniae і H. influenzae. У 18 випадках відзначалися менінгіти, у 79 – пневмонії, у 22 – інші тяжкі ураження. Гуморальні імунні порушення відзначалися у 37 із 119 пацієнтів (31% випадків). Серед них у 37,8% випадків мав місце дефіцит IgG1 [105].
Stead A. зі співавт., вивчаючи пацієнтів з множинними бронхоектазами, виявили ізольований дефіцит тотального IgG у 3 із 56 пацієнтів. Ще у 13 осіб мав місце ДС IgG, причому ізольований дефіцит IgG4 був найчастішим (9 випадків). Вакцинація демонструвала неможливість вироблення протективного титру антипневмококових антитіл у 1 із 29 випадків, при яких мав місце низький базальний рівень антиполісахаридних антитіл [156].
Ovesen T. зі співавт. виявили ізольовані гуморальні імунодефіцити у 5 із 18 дітей з хронічною посттимпанічною отореєю. Зокрема, тотальний і парціальний дефіцит IgА, дефіцит IgG та дефіцит манозозв’язувального білка. Ще у 8 пацієнтів гуморальні порушення комбінувалися з дефіцитом цитотоксичних Т-лімфоцитів або природних кілерів [123].
Karaca N.E. зі співавт. показали, що серед дітей з ДС IgG ізольований дефіцит IgG3 трапляється в 77% випадків, комбінований дефіцит IgG2 та IgG3 – в 14%, а ізольований дефіцит IgG2 – в 9% випадків. Основними клінічними проявами були рецидивні інфекції верхніх дихальних шляхів, пневмонії, гастроентерит та інфекції сечовивідних шляхів. Атопія розвивалася в 15% випадків [74].
Kutukculer N. зі співавт. спостерігали 87 дітей з дефіцитом класів імуноглобулінів і субкласів IgG. Найчастішим варіантом імунодефіциту був парціальний дефіцит IgA в комбінації із дефіцитом IgG3 (41%). Також діагностували ізольований парціальний дефіцит IgA (32%), вибірковий тотальний дефіцит IgA (8%), парціальний дефіцит IgA у комбінації з ДС IgG2-G4 (6%) та ізольований дефіцит субкласів IgG (13%). Показано, що траплялися як транзиторні порушення, котрі зазнавали спонтанної компенсації на тлі профілактичної антибіотикотерапїї (50–60%) протягом 50–60 міс, так і прогресуючі форми імунодефіциту, перебіг яких з часом погіршувався (30–40% випадків) [87].
Класифікація
При ізольованому ДС IgG відзначається зниження сироваткової концентрації одного з різновидів цього імуноглобуліну. Іноді трапляються комбіновані порушення субкласів IgG, здебільшого – дуальні. Найчастішою комбінацією є дефіцит IgG2 та IgG4, хоча можливі найрізноманітніші поєднання. Відомі також поєднані гуморальні порушення, при яких дефіцит одного чи кількох субкласів IgG асоційований з низькою концентрацією інших класів імуноглобулінів, здебільшого IgА, хоча існують повідомлення про зв’язок з дефіцитом IgМ, IgЕ або IgD.
Так, Miwa Y. зі співавт. описали в одного пацієнта комбінований дефіцит IgG2 та IgG4, у іншого – поєднане порушення, що включало дефіцит IgG2, IgG4 та IgА, а ще в двох – поєднання дефіцитів IgG2 та IgА [111]. При ширших порушеннях зазвичай говорять про дисімуноглобулінемію. При одночасному дефіциті IgG, IgА, IgЕ і IgD діагностують гіпоімуноглобулінемію (<7 г/л), а при зниженні сироваткового вмісту всіх класів імуноглобулінів – пангіпоімуноглобулінемію [166]. Часом ДС IgG супроводжується компенсаторною гіперімуноглобулінемією, що може зменшувати прояви інфекційного синдрому, однак асоціюється з вищим ризиком імунозапальних, автоімунних та алергічних ускладнень [172].
За тяжкістю можна розрізняти тотальні і парціальні ДС IgG, однак надійних критеріїв їх чіткого розмежування не запропоновано. Visitsunthorn N. зі співавт. пропонують діагностувати парціальний дефіцит при зниженні сироваткової концентрації субкласу більше, ніж на 2 стандартних відхилення від нижньої межі норми або на підставі аномально низького співвідношення вмісту конкретного субкласу до тотального IgG. При цьому автори діагностували парціальний ДС на підставі аномального співвідношення у 89,3% випадків, і лише у 12,7% – за низькою сироватковою концентрацією [175].
Можливе стійке і транзиторне зниження сироваткової концентрації субкласів IgG при первинних імунодефіцитах. В обох клінічних ситуаціях описаний розвиток тяжких симптомів. Так, Ohga S. зі співавт. описали рецидивний пневмококовий менінгіт, гепатит і гнійний артрит у дитини з транзиторним комбінованим дефіцитом IgG2 та IgG4 [118].
Імунодефіцит може бути первинним (генетично детермінованим) та вторинним (набутим). Винятком є випадки транслокацій генів імуноглобулінів, спричинені вірусом Епштейна–Барр, наприклад, у разі лімфоми Беркітта, при яких формується генетично детермінований набутий ДС IgG [192]. Вторинний дефіцит може бути проявом іншої хвороби. Так, дефіцит тотального IgG зустрічається при міотонічній дистрофії [143], дефіцит IgG2 – при серпоподібноклітинній анемії [114], а дефіцит IgG4 – при синдромі Ротмунда–Томсона [85]. Різні варіанти ДС можуть відзначатися при синдромі Кабукі [61] та гемохроматозі, обумовленому гомозиготною мутацією HFE C282Y [9].
Крім того, ДС може бути компонентом іншого імунодефіциту з ширшим фенотипом, наприклад синдрому Луї–Барр або дефіциту молекули CD19 [174]. Однак можливі випадкові комбінації незалежних імунних дисфункцій, особливо якщо ті часто зустрічаються у популяції. Зокрема, Resman F. зі співавт. описали некротичний міозит і септичний шок, спричинений H. influenzae типу f, у пацієнта з дефіцитом IgG3 та манозозв’язувального протеїну [141].
Іноді до вторинного імунодефіциту призводять антиконвульсанти. Так, карбамазепін може спричинити вторинний дефіцит IgG1 і IgG2 [50], фенітоїн – IgG2 та IgG4 [65], а зонізамід – дефіцит IgG2 та IgA [103]. Крім того, протизапальний препарат сульфасалазин може зумовлювати поєднаний дефіцит IgG2 та IgA [91].
Дефіцит IgG2 часом розвивається внаслідок спленектомії, однак Kavanaugh A.F., Huston D.P. описали парадоксальне зникнення передіснуючого дефіциту IgG2 після видалення селезінки з приводу портальної гіпертензії і гіперспленізму [76]. Спленектомія може сприяти декомпенсації прихованого ДС [41]. Scoular A. зі співавт. описали дефіцит IgG2 і пов’язану з цим бактеріємію, зумовлену Fusobacterium nucleatum, у ВІЛ-інфікованого пацієнта з нормальною кількістю CD4+- Т-лімфоцитів [147]. Вторинний ДС IgG розвивається при хронічному лімфолейкозі, визначаючи розвиток бактеріальних ускладнень при цьому новоутворенні [44], однак слід враховувати і зворотній зв’язок – розвиток лімфопроліферативних пухлин у пацієнтів з первинним ДС IgG [77]. Вважають, що перитонеальний діаліз може спричиняти вторинний ДС IgG [146], однак результати нещодавнього дослідження встановили, що саме дефіцит IgG2 і призводив у більшості випадків до ниркової недостатності внаслідок розвитку інфекційних та автоімунних уражень, що зумовлювало потребу в діалізі [79].
Слід враховувати, що іноді ізольований ДС IgG може супроводжуватися прихованим дефіцитом специфічних антитіл різних класів. Так, Van Kessel D.A. зі співавт. виявили серед 24 пацієнтів з дефіцитом IgG1 щонайменше 9 випадків дефіциту продукції специфічних IgG2 або IgA у відповідь на пневмококову вакцину, хоча загальні сироваткові рівні цих імуноглобулінів були нормальними [168]. Більше того, Lacombe C. зі співавт. описали 3 випадки трансформації ізольованого дефіциту IgG1 у дефіцит IgG2 [88].
Клінічні прояви
ДС IgG обумовлює розвиток клінічних симптомів інфекційних, алергічних, автоімунних і неопластичних уражень у людей. Загалом, тяжкість стану пацієнтів різниться у разі поєднаних, комбінованих та ізольованих порушень, однак ці відмінності можуть не справджуватися в конкретних випадках.
Поєднані форми. Якщо ДС IgG поєднується з парціальним або тотальним дефіцитом IgA, то зазвичай формуються тяжчі клінічні прояви, ніж при ізольованому ДС [29]. Так, Kutukculer N. зі співавт. виявили такі клінічні прояви поєднаних форм імунодефіциту: рецидивні інфекції верхніх дихальних шляхів (76%), пневмонія (14%), гострий гастроентерит (3%), інфекції сечовивідних шляхів (3%), синуїт (2%) і гострий середній отит (2%). Атопія траплялася в 24% випадків (n=87) [87].
DeBaets F. зі співавт. виявили гуморальний імунодефіцит серед дітей з хронічним бронхітом у 85% випадків. 9 (17%) пацієнтів мали дефіцит IgG2, 9 (17%) – IgG3, а 20 (38%) осіб – дефіцит IgG4. Ще 9 (17%) дітей страждали на дефіцит IgA, а 8 (15%) – на комбінований ДС IgG. Відзначалася вірогідна різниця у порівнянні з контрольною групою, яку склали здорові діти. Виявлено кореляцію між глибиною імунодефіциту і тяжкістю інфекційних проявів [33].
Saleem T. зі співавт. описали дефіцит IgА, IgG2 і IgG4 у 17-річної пацієнтки з анамнезом рецидивних бактеріальних інфекцій, у тому числі туберкульозу. Численні курси антибіотиків не зменшили кількості рецидивів інфекції. Найчастішими проявами були: пневмонія, гастроентерит та максилярний синуїт. Чотири рази вона успішно приймала внутрішньовенно імуноглобулін при загостренні стану, однак тривалої імуноглобулінотерапії не проводили. Через 5 років у неї розвинулася неходжкінська лімфома [144].
Ideura G. зі співавт. описали дефіцит IgМ та IgG4 у 37-річної пацієнтки з рецидивною бронхопневмонією та фіброепітеліальним поліпом у бронху. Згодом у неї розвинулася алергічна системна еритема у відповідь на антибактеріальні препарати. Відзначалося зниження кількості CD20+-В-лімфоцитів та відсутність В-клітин пам’яті [62]. Натомість Pengsaa K. зі співавт. повідомили про хронічний лямбліозний ентерит у 15-річного пацієнта з дефіцитом IgМ та IgG4 [131]. Ninomiya H. зі співавт. повідомили про рецидивні пневмонії (рис. 5) та множинні бронхоектази легень (рис. 6) у пацієнта з поєднаним дефіцитом IgG2, IgG4 та IgЕ, зумовленим поліморфізмом генів константних ділянок імуноглобулінів.
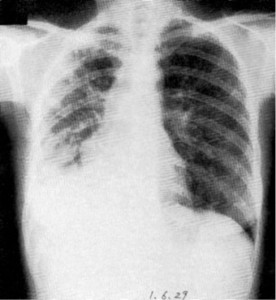 Рис. 5. Рентгенограма органів грудної клітки (ОГК) в прямій проекції, що демонструє ознаки правобічної пневмонії у пацієнта з первинним дефіцитом IgG2, IgG4 та IgЕ (за Ninomiya H. зі співавт.)
Рис. 5. Рентгенограма органів грудної клітки (ОГК) в прямій проекції, що демонструє ознаки правобічної пневмонії у пацієнта з первинним дефіцитом IgG2, IgG4 та IgЕ (за Ninomiya H. зі співавт.)Комбіновані порушення. Одночасний дефіцит кількох субкласів IgG призводить до дещо слабших клінічних проявів у порівнянні з поєднаними порушеннями, які, однак, зазвичай тяжчі, ніж при ізольованих дефіцитах. Слід враховувати, що тяжкість симптомів обумовлена не тільки глибиною імунодефіциту, але й реалізацією компенсаторних механізмів. De Gracia J. зі співавт. виявили ДС серед пацієнтів з множинними бронхоектазами в 48% випадків: 19 – дефіциту IgG2, 2 – дефіциту IgG3, 3 – дефіциту IgG4 і 7 – комбінованих порушень. При цьому в усіх осіб відзначалося зростання сироваткової концентрації тотального IgG, IgG1 і IgA [30]. Klingebiel T. зі співавт. описали пневмонію, спричинену Chlamydia trachomatis, у пацієнта з ДС IgG2 та IgG4. Ускладненням був пневмоторакс, що потребував виконання хірургічного втручання. Дитина також страждала на імпетиго [82].
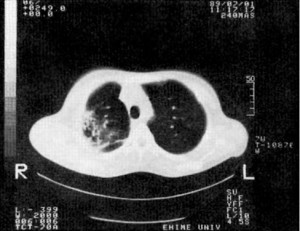 Рис. 6. КТ ОГК у горизонтальній проекції, що візуалізує ознаки бронхоектазів у правій легені у пацієнта з первинним дефіцитом IgG2, IgG4 та IgЕ (за Ninomiya H. зі співавт.)
Рис. 6. КТ ОГК у горизонтальній проекції, що візуалізує ознаки бронхоектазів у правій легені у пацієнта з первинним дефіцитом IgG2, IgG4 та IgЕ (за Ninomiya H. зі співавт.)Ізольовані форми дефіциту. У таких випадках частіше відзначають асимптомні варіанти перебігу хвороби, ніж у разі поєднаних і комбінованих порушень, оскільки має місце менша за глибиною імунна недостатність і ширші можливості для компенсації імунодефіциту. Kim J.H. зі співавт. вивчили структуру клінічних проявів ізольованого ДС IgG у дітей. Виявилось, що бактеріальні інфекції верхніх і нижніх дихальних шляхів зустрічалися в 76% випадків, а інфекції множинної локалізації, у тому числі ураження сечовивідних шляхів і коліт, – в 11% випадків. Бронхіальна астма (БА), алергічний риніт (АР) і декілька автоімунних хвороб також зустрічалися серед цих пацієнтів (рис. 7) [80].
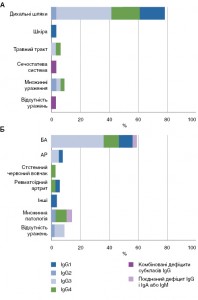 Рис. 7. Структура клінічних симптомів у дорослих пацієнтів з ізольованим, комбінованим і поєднананим ДС IgG
Рис. 7. Структура клінічних симптомів у дорослих пацієнтів з ізольованим, комбінованим і поєднананим ДС IgG(Kim J.H. зі співавт.)
Feldman C. зі співавт. у спеціально спланованому дослідженні показали асоціацію ізольованого ДС IgG з рецидивними респіраторними інфекціями, атопією та бронхоектазами у дорослих пацієнтів [43]. Faller J.P. зі співавт. продемонстрували асоціацію ДС IgG і фульмінантної форми менінгококової пурпури [40].
Barton J.C. зі співавт. у спеціально спланованому дослідженні за участю 212 дорослих показали тісну асоціацію ДС IgG і оперізувального герпесу. У таких пацієнтів аномально часто відзначалися алелі HLA-A*01 та B*08. Протягом 7,5 року спостереження частота рецидивів оперізувального герпесу в пацієнтів з ДС IgG була в 5 разів вища, ніж у імунокомпетентних осіб [8, 12].
Popa V. продемонстрував зв’язок ДС IgG, так само як і загального варіабельного імунодефіциту, з епізодами обструкції дихальних шляхів у дорослих, які розвиваються на тлі рецидивних респіраторних інфекцій (n=42) [135].
Тотальний IgG. Під дефіцитом тотального IgG розуміють паралельне зниження сироваткової концентрації всіх субкласів за умови нормального вмісту інших ізотипів імуноглобулінів. Може бути субкомпенсованою формою загального варіабельного імунодефіциту. Зумовлює неінформативність серологічних тестів при діагностиці інфекцій. Johnston S. L. зі співавт. описали редицивні шкірні і пульмональні інфекції, нефротичний синдром, цукровий діабет 1-го типу у дорослого пацієнта з тотальним дефіцитом IgG. У сечі не виявляли молекули IgG, тому втрата IgG через нирки була виключена. Досягнута компенсація клінічного стану завдяки внутрішньовенному імуноглобуліну [67]. Pardillos Tomé A. зі співавт. описали класичну саркому Капоші, зумовлену вірусом герпесу 8-го типу, у пацієнта з ізольованим дефіцитом тотального IgG [128].
Дефіцит IgG1. Цей субклас розпізнає переважно білкові антигени і складає основу пулу тотального IgG у сироватці крові людини. Клінічні прояви ізольованого дефіциту IgG1 можуть нагадувати загальний варіабельний імунодефіцит. Зазвичай відзначається зниження рівня тотального IgG у сироватці крові, тому цей імунодефіцит можна виявити в рутинній імунограмі. Частіше за інші ДС поєднується з дефіцитами інших ізотипів антитіл. Деякі автори вважають дефіцит IgG1 різновидом загального варіабельного імунодефіциту [112].
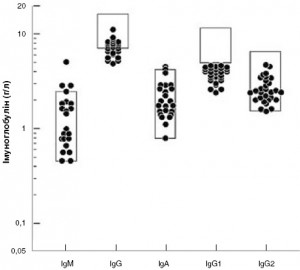 Рис. 8. М’які форми ізольованого дефіциту IgG1 у пацієнтів з рецидивними бактеріальними синуїтами і пневмоніями
Рис. 8. М’які форми ізольованого дефіциту IgG1 у пацієнтів з рецидивними бактеріальними синуїтами і пневмоніями(за van Kessel D.A. зі співавт.)
Lacombe C. зі співавт. верифікували дефіцит IgG1 в 119 випадках серед 3 005 пацієнтів. Клінічні симптоми у вигляді рецидивних бактеріальних інфекцій відзначалися в 83,2% випадків. Також реєструвалися атопічний дерматит (АД), природжені вади серця та автоімунні розлади, однак найчастіше виявляли БА (кожен п’ятий пацієнт). У більшості випадків відзначалися сімейні форми імунодефіциту [88]. Van Kessel D.A. зі співавт. повідомили про 24 випадки м’якого ізольованого дефіциту IgG1. Основними клінічними проявами були рецидивні бактеріальні синуїти і пневмонії (рис. 8) [168].
Kallio-Laine K. зі співавт. у спеціально спланованому дослідженні продемонстрували, що сироваткова концентрація IgG1 була нижчою (p = 0,009), а частота виявлення ізольованого дефіциту IgG1 – більшою (p <0,001) у пацієнтів з рецидивним менінгітом Молларе, спричиненим вірусом простого герпесу 2-го типу, у порівнянні з контрольною групою. Ризик нового епізоду менінгіту зростав зі зниженням концентрації IgG1 (показник інциденту 2,05). Експресія алелей HLA-DRB1*01 і -B*27 була асоційована з дефіцитом IgG1 і високим ризиком нейроінфекції [70].
Hassett J. зі співавт. описали рецидивний ентероколіт, спричинений Clostridium difficile, у пацієнта з дефіцитом IgG1 [60].
IgG2. Ці антитіла виробляються проти полісахаридних антигенів, тому в пацієнтів з дефіцитом IgG2 знижується резистентність передусім до S. pneumoniae та H. influenzae, що створює подібність з дефіцитом специфічних антитіл [64]. Це найчастіша форма ДС IgG у дітей.
Shackelford P.G. зі співавт. виявили дефіцит IgG2 в 7 випадках серед 30 дітей з рецидивними бактеріальними інфекціями, у тому числі бактеріальними синуїтами, пневмоніями та пневмококовим менінгітом [150], хоча Beck C.S., Heiner D.C. ідентифікували цю імунну дисфункцію лише в 4 з 422 пацієнтів з тяжкими синупульмональними інфекціями [15]. Inoue R. зі співавт. описали дефіцит IgG2 у поєднанні з дефіцитом продукції гамма-інтерферону [63]. Gordon C.L. зі співавт. у когортному дослідженні з використанням мультиваріативного аналізу показали тісну асоціацію тяжких форм грипу, спричиненого штамом H1N1, з ізольованим дефіцитом IgG2 [51]. Escobar-Pérez X. зі співавт. описали 4 випадки бактеріального менінгоенцефаліту, викликаного S. pneumoniae та H. influenzae типу b, у пацієнтів з ізольованим дефіцитом IgG2. Показана користь від внутрішньовенного застосування імуноглобуліну в таких випадках [38]. Gottsegen D.N. зі співавт. описали розвиток пневмококового остеомієліту [53], а Bass J.L. зі співавт. – рецидивної менінгококцемії у пацієнтів з ізольованим дефіцитом IgG2 [13].
IgG3. Цей субклас IgG проявляє специфічність до білкових антигенів, тому при його дефіциті знижується резистентність насамперед до Streptococcus pyogenes, що експресує М-протеїн, та Moraxella catarrhalis. Це найчастіша форма ДС IgG серед дорослих. Зазвичай розвиваються хронічні стрептококовий тонзилофарингіт та бронхіт, зумовлений моракселою. Також знижена резистентність до вірусних агентів, які містять багато білкових антигенів, що є особливістю імунодефіциту.
Visitsunthorn N. зі співавт. показали, що ізольований дефіцит IgG3 зустрічався у 56,4% випадків серед тайських дітей з ДС IgG. Клінічний дебют припадав на період від народження до 5 років. Основним клінічним проявом був рецидивний бактеріальний синуїт, який траплявся у 83,6% випадків [175].
Oxelius V.A. зі співавт., вивчаючи структуру дефіциту IgG3, діагностували ізольовану форму дефіциту IgG3 в 59,5% випадків серед 313 пацієнтів. Крім того, в 36,5% випадків мав місце комбінований дефіцит IgG1 та IgG3, а ще в 5% – IgG2 та IgG3. Пацієнти з ізольованим дефіцитом IgG3 страждали на рецидивні інфекції верхніх дихальних шляхів, бронхіти, бронхопневмонії та БА. Особи з комбінованим дефіцитом IgG1 та IgG3 частіше хворіли на хронічне обструктивне захворювання легень (ХОЗЛ) і пневмонії. Крім того, у пацієнтів з ізольованим дефіцитом IgG3 відзначали непоодинокі випадки цукрового діабету 1-го типу, пурпури Шенлейна–Геноха, рецидивної інфекції, спричиненої вірусом герпесу 1-го типу, і бешихи. Цікаво, що у деяких родичів пацієнтів з дефіцитом IgG3 відзначався загальний варіабельний імунодефіцит та дефіцит IgA, що вказує на спільність походження цих розладів [124].
Vehapoglu A. зі співавт. описали рецидивний бактеріальний менінгіт у 6-річного хлопчика з ізольованим дефіцитом IgG3 [170]. Abrahamian F. зі співавт. показали асоціацію ізольованого дефіциту IgG3 з рецидивними бактеріальними респіраторними інфекціями, АР і БА [2]. Snowden J.A. зі співавт. повідомили про ізольований дефіцит IgG3 у 35-річної пацієнтки з рецидивними інфекціями верхніх дихальних шляхів, синуїтами і генералізованою лімфаденопатією. Продемонстрована компенсація стану після призначення внутрішньовенного імуноглобуліну [153]. Armenaka M. зі співавт. в контрольованому дослідженні виявили асоціацію дефіциту IgG3 з хронічним рефрактерним синуїтом у людей [7].
Mitsui H. зі співавт. повідомили про розвиток хронічної активної інфекції, зумовленої вірусом Епштейна–Барр, яка проявлялася рецидивними оральними і генітальними виразками, некротичними папулами на обличчі, спалахами високої температури тіла та індурованою еритемою на шкірі тулуба. Показана користь від комбінованої терапії з використанням внутрішньовенного імуноглобуліну та альфа-інтерферону [110]. Linde A. зі співавт. описали серію випадків реактивованих інфекцій, спричинених вірусом Епштейна–Барр і вірусом герпесу 6-го типу, у пацієнтів з дефіцитом IgG3. Автори показали, що клінічно маніфестне ураження розвивається лише в тому разі, коли в контексті дефіциту загального IgG3 відзначається дефіцит специфічних IgG3 до вірусу. Паралельно з цим нерідко мав місце дефіцит IgG2 до полісахаридних антигенів при нормальному загальному пулі IgG2, що пояснює тісну асоціацію вірусу Епштейна–Барр зі стрептококовою інфекцією у деяких хворих [96]. Snowden J.A. зі співавт. описали рецидивний ентеровірусний серозний лімфоцитарний менінгіт у пацієнта з ізольованим дефіцитом IgG3 [152]. Kallio-Laine K. зі співавт. описали серію випадків часто рецидивуючого лабіального герпесу, спричиненого вірусом простого герпесу 1-го типу, у пацієнтів з ізольованим дефіцитом IgG3 та комбінованим порушенням, шо охоплювало дефіцит IgG1 і IgG3 [71].
Maes M. зі співавт. повідомили про синдром хронічної втоми і транслокацію ендотоксинів грамнегативних бактерій через стінку кишечника у 13-річної дівчинки з вибірковим дефіцитом IgG3 [107]. Ambrozic J. зі співавт. повідомили про рецидивний бактеріальний сепсис та серонегативний олігоартрит у пацієнта з ізольованим дефіцитом IgG3 [5].
IgG4. Ізольований дефіцит цього субкласу часто має безсимптомний перебіг у зв’язку з малою нормальною концентрацією IgG4 в сироватці крові, що обумовлює широкі можливості для компенсації. Імуноглобулін має протизапальні властивості і у разі атопії виступає в ролі блокувального антитіла. Moss R.B. зі співавт. виявили ізольований дефіцит IgG4 в 17% випадків серед дітей з рецидивними респіраторними інфекціями, що становило разючий контраст з контрольною групою, до якої увійшли здорові діти (n=250). Додатковими клінічними проявами були АД, БА, рецидивний гастроентерит [113]. Rawat A. зі співавт. описали ізольований дефіцит IgG4 у дитини з бронхоектазами, зумовленими частими випадками бактеріальних бронхопульмональних інфекцій [139]. Раніше повідомляли про розвиток хронічної діареї і рецидивного лямбліозу при дефіциті цього субкласу. Pavone P. зі співавт. показали, що у пацієнтів з синдромом Дауна ішемічний інсульт асоційований з дефіцитом IgG4, що пов’язали зі зниженою резистентністю до Mycoplasma pneumoniaе і Streptococcus oralis [130].
Karaman O. зі співавт. виявили ДС в 31,6% випадків серед немовлят зі свистячим диханням, причому переважно відзначався дефіцит IgG4 [75]. Castro R. зі співавт. описали тяжкий зовнішній отит і мастоїдит у дитини з ізольованим дефіцитом IgG4. Пацієнту виконано декілька мастоїдектомій і пластичних операцій з приводу рецидивів інфекційного ураження. Резидуальним дефектом було зниження слуху з іпсилатерального боку [25].
Levendoglu F. зі співавт. повідомили про спінальний епідуральний абсцес з прогресуючою параплегією у 16-річного пацієнта з ізольованим дефіцитом IgG4 [94].
Автоімунні прояви. У пацієнтів з ДС IgG може розвиватися цукровий діабет 1-го типу і пурпура Шенлейна–Геноха [124], первинний біліарний цироз [161], автоімунна тромбоцитопенічна пурпура [164], тиреоїдит Хашимото і гемолітична анемія [47], комбіновані автоімунні цитопенії [41], синдром Евана [173]. Зокрема, Rahiminejad M.S. зі співавт. виявили ДС IgG у 11% випадків серед пацієнтів з автоімунною тромбоцитопенічною пурпурою [138]. Про асоціацію з цим автоімунним розладом повідомляли також Shackelford P.G. зі співавт. [150]. Натомість Villiger P.M. зі співавт. описали синдром Евана у дорослого пацієнта, що страждав на комбінований ДС IgG2 та IgG4 [173].
Suyama K. зі співавт. описали розвиток системного червоного вовчака (СЧВ) у пацієнта з поєднаним дефіцитом IgA та IgG2, причому автоімунне ускладнення призвело до поглиблення імунної дисфункції до фенотипу загального варіабельного імунодефіциту [160]. Tamura A. зі співавт. повідомили про розвиток СЧВ у пацієнта з сімейним дефіцитом IgG2 і IgG4. У дитини розвинулася тампонада серця у зв’язку з ексудативним перикардитом [162]. Düzgün N. зі співавт. описали розвиток у 31-річної пацієнтки з дефіцитом тотального IgG спочатку СЧВ, а потім – екстрапульмонального туберкульозу з ураженням шкіри, суглобів та менінгеальних оболонок мозку [36]. Kamei K. зі співавт. повідомили про 2 випадки автоімунного імунокомплексного ураження нирок у пацієнтів з ДС IgG. У першому випадку мав місце дефіцит IgG2, IgG3 і IgG4. У нирках виявляли депозити, представлені IgG1. Було встановлено діагноз мембранозної нефропатії. У другому випадку виявили діагноз дефіциту IgG2 та IgG4. Мали місце депозити з IgG1 та IgG3. Був встановлений діагноз мембранопроліферативного гломерулонефриту [72].
Hassani R.T. зі співавт. описали розвиток спочатку неспецифічного виразкового коліту, а потім – автоімунного васкуліту сітківки у пацієнта з ізольованим дефіцитом IgG1. Паралельно пацієнт страждав на рецидивні бактеріальні інфекції [59].
Venuta A. зі співавт. повідомили про гіпергаммаглобулінемічну пурпуру у 12-річної пацієнтки з ізольованим дефіцитом IgG2 і анамнезом частих інфекційних епізодів [172]. Eriksson P. зі співавт. описали 6 випадків ізольованого ДС IgG, що призводив до розвитку синдрому Шегрена та гіпергаммаглобулінемічної пурпури [37]. Про подібний випадок повідомили Matter L. зі співавт. [106].
Нерідко розвиваються неврологічні автоімунні ускладнення. Likosky D.J. зі співавт. описали 3 випадки мультифокальної демієлінізуючої полінейропатії у пацієнтів з ізольованим дефіцитом IgG1 і/або IgG3 [95]. Meyts I. зі співавт. повідомили про оптичний нейромієліт у пацієнта з сімейним парціальним дефіцитом IgA та IgG3 [108]. Frohman L.P. зі співавт. діагностували рецидивний стероїд-залежний оптичний неврит у пацієнта з комбінованим дефіцитом IgG2 та IgG3 [45]. Bertoli L.F. зі співавт. виявили ДС IgG1 та IgG3 в 46,4% випадків серед пацієнтів з автоімунною сенсоневральною приглухуватістю. Дефіцит IgG1 зустрічався в 10,7%, дефіцит IgG3 – в 21,4%, а комбіноване порушення – в 14,3% випадків. Поширеність імунодефіциту була вірогідно вищою, ніж у контрольній групі, до якої увійшли 275 здорових європейців. Поширеність можливої автоімунної сенсоневральної приглухуватості при ДС становила 0,74%. У 21,4% випадків у таких пацієнтів відзначали інші автоімунні розлади та був підвищеним вміст автоантитіл до колагену ІІ типу [17].
Як показали Jiménez A. зі співавт., ізольований дефіцит IgG2 може бути причиною синтезу автоантитіл до IgА, що призводить до розвитку вторинного дефіциту IgА. Також у таких пацієнтів підвищена частота синтезу антикардіоліпінових автоантитіл [66].
Алергічні прояви. У пацієнтів з ДС IgG описані випадки БА [2], АР [80], АД [149], хронічного рефрактерного синуїту [169] та медикаментозної алергії [62]. Серед 62 пацієнтів із системними проявами атопії Bozkurt B. зі співавт. виявили дефіцит IgA, тотального IgG, IgM та IgG3 у 12,9%, 8%, 6,5% і 1,6% випадків відповідно, що вірогідно частіше, ніж у загальній популяції [20].
Серед пацієнтів з БА de Moraes Lui C. зі співавт. діагностували такі форми ДС IgG: дефіцит IgG3 (10/41), IgG4 (3/41), IgG2 (2/41), IgG1 (1/41), IgG3–IgG4 (4/41), IgG1–IgG3 (1/41), IgG1–IgG3–IgG4 (1/41). При цьому у пацієнтів з комбінацією БА і рецидивних респіраторних інфекцій переважав дефіцит IgG3, а серед осіб тільки з проявами БА – дефіцит IgG4 [32]. У деяких пацієнтів розвивається стероїд-залежна БА [39]. Outschoorn I.M. зі співавт. в контрольованому дослідженні показали асоціацію БА у дорослих з ДС IgG2 і IgG3 [122]. Loftus B.G. зі співавт. виявили ДС IgG в 28 випадках серед 82 дітей з БА на відміну від контрольної групи. Частіше за все зустрічався дефіцит IgG2. Глибина імунодефіциту корелювала зі швидкістю наростання сироваткової концентрації IgE [99].
O’Keeffe S. зі співавт. діагностували ДС IgG в 25,9% випадків серед 58 пацієнтів з ХОЗЛ. Найчастіше зустрічався ізольований дефіцит IgG2. Відзначалася вірогідна різниця з контрольною групою. ДС був асоційований з поступовим погіршанням результатів спірометричних досліджень і виступав у ролі чинника прогресування ХОЗЛ [120]. Löck K. зі співавт. діагностували ДС IgG в 26 з 99 пацієнтів з БА і ХОЗЛ. Глюкокортикостероїди поглиблювали наявний імунодефіцит, однак не були причиною його розвитку [98].
Tran Khai Hoan N. зі співавт. виявили ДС IgG у 13,7% випадків серед 161 пацієнта з поліпами носової порожнини [167]. Vanlerberghe L. зі співавт. діагностували серед пацієнтів з хронічним рефрактерним риносинуїтом ДС IgG3 в 17,9%, субкласу IgG2 – в 2%, а комбіновані порушення – в 2,9% випадків [169]. May A. зі співавт. виявили серед 220 пацієнтів з хронічним рефрактерним риносинуїтом такі гуморальні імунні порушення: дефіцит тотального IgG (n=3), IgG2 (n=10), IgG1 (n=6), IgG3 (n=1) та IgG4 (n=1) [107]. Chinratanapisit S. зі співавт. повідомили про одночасний розвиток рефрактерного риносинуситу і назальних поліпів у 2 пацієнтів. У першого з них ідентифікували ізольований дефіцит IgG3, а у другого – комбіноване порушення, що включало дефіцит IgG2 та IgG3 [26].
Ojuawo A. зі співавт. діагностували дефіцит IgA, IgG2 і IgG4 в 43,3%, 75,0% і 55,0% випадків відповідно серед дітей з алергічним колітом і менше ніж в 5% випадків – у контрольній групі [119].
Онкологічні ускладнення. У пацієнтів з ДС IgG розвиваються переважно мікроб-індуковані лімфопроліферативні пухлини [179]. Zenone T. зі співавт. описали 2 випадки лімфоми Ходжкіна у пацієнтів з ДС IgG. Також повідомляли про розвиток неходжкінських лімфом і аденокарциноми шлунка [144], саркоми Капоші [128], лімфоми Беркітта [192]. Дефіцит IgG4, найімовірніше, відповідальний за розвиток остеосарком при синдромі Ротмунда–Томсона [85]. Відомі описи лімфопроліферативних пухлин при транслокаціях і делеціях в генах субкласів IgG: гострого пре-В-лейкозу [77] і лімфоми, асоційованої зі слизовими оболонками [158], – при дефіциті IgG1; різних форм лейкозу – при дефіциті IgG2 [180]; хвороби важких ланцюгів – при дефіциті IgG3 [4]; В-клітинної лімфоми – при дефіциті IgG4 [81].
Інші прояви. У дітей з ДС можуть відзначатися ознаки затримки розвитку [151]. Pauly E. зі співавт. повідомили про розвиток синдрому нетримання пігменту у новонародженого з ізольованим ДС IgG [129]. Hahn-Zoric M. зі співавт. показали, що пацієнти з дефіцитом IgG3 не формують протективної гуморальної імунної відповіді після імунізації кон’югованою вакциною, що містить капсулярний антиген H. influenzae типу b і правцевий токсоїд [57]. У деяких пацієнтів з ДС може розвиватися некласифікована ентеропатія [48]. Layward L. зі співавт. в контрольованому дослідженні показали асоціацію IgA-нефропатії і комбінованого ДС IgG1 та IgG4. Аномальне підвищення сироваткової концентрації IgA пояснили аберантною компенсацією ДС IgG [89].
Нерідко спостерігають неврологічні ускладнення. Так, Wakefield D. зі співавт. продемонстрували асоціацію ДС IgG з синдромом хронічної втоми у людей [177]. Подібні результати отримали Komaroff A.L. зі співавт. [83] та Read R. зі співавт. [140] незалежно одні від одних. У дітей з ДС можуть формуватися рефрактерні форми епілептичних синдромів, які позитивно реагують на введення внутрішньовенного імуноглобуліну [133]. Caksen H. зі співавт. продемонстрували зв’язок дефіциту IgG4 і фебрильних судом у дітей [23]. Натомість Lenti C. зі співавт. у дослідженні сімей показали асоціацію ізольованого дефіциту IgG2 з фебрильними судомами у дітей [93]. Nieto M. зі співавт. виявили кореляцію між тяжкою міоклонічною епілепсією і дефіцитом IgA або IgG2 [116]. Натомість Bos-Veneman N.G. зі співавт. у контрольованому дослідженні показали асоціацію синдрому Туретта і дефіциту IgG3 [19].
Mikhak Z. зі співавт. повідомили про геміфаціальну мікросомію в сім’ї з гуморальним імунодефіцитом, обумовленим низькою сироватковою концентрацією IgG1, IgG2, IgA та специфічних антипневмококових антитіл [109]. Garg V. зі співавт. описали нодулярну лімфоїдну гіперплазію кишечнику у пацієнта з дефіцитом IgG2 [47]. Farmer J.R. зі співавт. повідомили про розвиток пульмональної артеріовенозної мальформації в контексті рецидивних респіраторних інфекцій у пацієнта з поєднаним дефіцитом IgA, IgG2 та IgG4, у зв’язку з якою було виконано білатеральну трансплантацію легень [41]. ДС зустрічається в 19,6% випадків серед пацієнтів з інтерстиційною хворобою легень, за даними дослідження Popa V. зі співавт. (n=148) [136].
Клінічний перебіг
У деяких пацієнтів може мати місце безсимптомний перебіг, принаймні протягом певних проміжків часу. Компенсація імунодефіциту може здійснюватися різними шляхами: за рахунок гіпергаммаглобулінемії [151], посиленого вироблення інших ізотипів антитіл, наприклад IgA [89] або IgE [100], і навіть шляхом посиленої продукції інших, неуражених субкласів IgG. Так, Layward L. зі співавт. показали, що у пацієнтів з дефіцитом IgG1 відзначається атипове компенсаторне вироблення IgG2 до білкових антигенів тетанічного токсоїду [89]. Depiero A. зі співавт. продемонстрували, що посилене вироблення IgG3 компенсувало дефіцит IgG1, IgG2, IgG4 і IgA1 у пацієнта з великою делецією генів важких ланцюгів імуноглобулінів [35]. За даними Plebani A. зі співавт., підвищена продукція IgG1 та IgG3 компенсувала поєднаний дефіцит IgA1, IgG2, IgG4 та IgE у пацієнта з гомозиготною делецією генів константних ділянок імуноглобулінів A1-E [134].
Оскільки в таких випадках відмічається сурогатне заміщення функції втраченого субкласу, така компенсація не завжди досягає ефекту, не усуваючи прояви інфекційного синдрому, а часом призводить до розвитку імунозалежних побічних ефектів. Так, гіперпродукція тотального IgG обумовлює розвиток гіпергаммаглобулінемічної пурпури та автоімунних ускладнень [172], гіперпродукція IgE призводить до алергічних уражень, у тому числі БА [32], а посилене вироблення IgA або IgM – до так званих IgA- [89] та IgM-нефропатій [126] відповідно.
Кореляція між глибиною ДС і тяжкістю клінічних симптомів виражена слабше, ніж при гіпогаммаглобулінемії [112].
Навіть субнормальні рівні субкласів можуть бути асоційовані з тяжкими клінічними проявами [155].
Іноді ДС IgG зазнає декомпенсації з розвитком фенотипу загального варіабельного імунодефіциту [6]. Часом ДС зазнає тимчасової псевдокомпенсації під впливом тяжкої інфекції, найімовірніше, за рахунок її потенціюючої дії на імунну відповідь [69].
Karaca N.E. зі співавт. продемонстрували, що дефіцит IgG3 зазнавав спонтанної компенсації у 30% випадків, а комбінований дефіцит IgG2 та IgG3 – в 35,7% випадків протягом 6 років. Однак ізольований дефіцит IgG2 не зазнавав компенсації протягом всього періоду спостереження [74].
Carvalho Neves Forte W. зі співавт. описали еволюцію ізольованого дефіциту IgA до поєднаного порушення з дефіцитом IgG2 та IgG4 в одному випадку і до фенотипу загального варіабельного імунодефіциту – в іншому. В обох випадках показана очевидна користь від застосування внутрішньовенного імуноглобуліну [24].
Діагностика
Jolles S. зі співавт. в спеціально спланованому дослідженні показали, що визначення калькульованого глобуліну (<18 г/л) може бути скринінговим тестом при діагностиці рівнів гуморальних імуноглобулінів, однак такий підхід є неінформативним при дефіциті міноритарних субкласів IgG [68].
Золотим стандартом діагностики ДС IgG вважають ELISA [171], хоча деякі автори застосовували радіальну імунодифузію, яка відома ще з 60-х років минулого сторіччя [38]. Наразі вважають, що за допомогою простої радіальної імунодифузії можна коректно діагностувати лише тотальний дефіцит IgG та дефіцит IgG1 [166]. Твердофазний імуноферментний аналіз застосовується як альтернатива ELISA [142]. Деякі автори використовували нефелометрію [94], однак точність результатів цього методу поступається ELISA. Bozkurt B. зі співавт. застосовували зворотній імуноферментний аналіз з сендвічною технікою ELISA [20]. Радіоімунний метод вважається найточнішим, однак він є недоступним у багатьох клінічних центрах [32].
У разі превалювання пневмококової інфекції рекомендовано додатково вивчати поствакцинальний імунітет після введення полівалентної антипневмококової вакцини (діагностичний рівень <0,035 мг/мл) [155]. Depiero A. зі співавт. рекомендують одночасне використання кількох лабораторних методів при верифікації діагнозу, зокрема нефелометрії, імуноферментного аналізу та радіальної імунодифузії [35].
Наразі превалює формальна діагностика – за відхиленням виміряної сироваткової концентрації субкласу IgG від нормативних діапазонів. Так, для 7-річної дитини встановлено такі референтні значення: IgG1=280–1120 мг/дл, IgG2=30–630 мг/дл, IgG3=40–250 мг/дл, IgG4=11–620 мг/дл [178]. Натомість Shackelford P.G. зі співавт. пропонують діагностувати ДС при зниженні вмісту імуноглобулінів на 3SD від медіани вікової географічної норми [150]. Іноді існує потреба у розрахунку індексу IgG2/IgG для діагностики прихованого дефіциту IgG2. Southern blot може застосовуватися для виявлення делецій в генах важких ланцюгів імуноглобулінів у разі первинного ДС IgG [164].
Диференційна діагностика
При комбінованому ДС IgG2 та IgG4 слід проводити диференційну діагностику з синдромами Луї–Барр та Віскотта–Олдрича, особливо у разі поєднання з дефіцитом IgА [112].
При переважанні у клінічній картині пневмококової інфекції здійснюють диференційну діагностику з дефіцитом специфічних антитіл [118].
Brägger C. зі співавт. описали дефіцит IgG2 і IgG4 у пацієнта з хронічним слизовошкірним кандидозом і гіпотиреоїдизмом. Замісна внутрішньовенна імуноглобулінотерапія призвела до припинення рецидивних пневмоній у цієї дитини [22]. Слід враховувати, що при ДС IgG, особливо поєднаних ураженнях, може мати місце прихований дефіцит специфічних антитіл до полісахаридних антигенів. Зокрема, Braconier J.H. зі співавт. виявили дефіцит специфічних IgM до пневмококових капсулярних антигенів у пацієнта з рецидивною пневмококовою інфекцію, у якого відзначався дефіцит IgG2, IgG4 та IgA, однак був нормальний рівень загального IgM [21]. У пацієнтів з тяжким ДС IgG слід подумати про субкомпенсовану форму загального варіабельного імунодефіциту та хвороби Брутона. Клінічна картина загального варіабельного імунодефіциту і ДС IgG дуже подібна, хоча в першому разі відзначається вірогідно щільніша асоціація з автоімунними ускладненнями, особливо синдромом Шегрена та тиреоїдитом Хашимото, як показали Barton J.C. зі співавт. [11].
Лікування
Як зазначає Fadal R.G., пацієнти з м’якими формами імунодефіциту можуть мати користь від профілактичної антибіотикотерапії, тоді як особи з глибоким зниженням сироваткової концентрації субкласів IgG, що супроводжується тяжкими клінічними симптомами, мають отримувати внутрішньовенну імуноглобулінотерапію [39].
Karaca N.E. зі співавт. показали користь від профілактичної антибіотикотерапії пролонгованим бензилпеніциліном та антибіотиками короткої дії у дітей з ДС IgG у ретроспективному дослідженні. Частота інфекційних епізодів знизилася з 12,4 до 5,7 випадку на рік [74]. Kutukculer N. зі співавт. застосовували бензатин пеніциліну, оральні антибіотики і препарати бактеріальних лізатів для профілактики інфекційних епізодів у пацієнтів з поєднаними формами імунодефіциту (n=68) і показали однакову ефективність трьох превентивних стратегій [87]. Існують поодинокі клінічні повідомлення про компенсацію антипневмококового гуморального імунітету у дітей з ДС IgG після імунізації полівалентною пневмококовою вакциною [118].
Del-Río-Navarro B.E. зі співавт. провели подвійне сліпе плацебо-контрольоване випробування OM-85 BV у дозі 3,5 мг щодня впродовж 10 діб поспіль кожного місяця протягом 3 міс при рецидивних інфекціях верхніх дихальних шляхів, асоційованих з субнормальними рівнями субкласів IgG. Показано вірогідне зменшення частоти інфекційних епізодів у групі терапії [34]. Genel F., Kutukculer N. провели рандомізоване проспективне дослідження, результати якого показали однакову клінічну ефективність OM-85 BV і профілактичної антибіотикотерапії при ДС IgG, однак 10 із 99 пацієнтів потребували проведення внутрішньовенної імуноглобулінотерапії, оскільки не відповідали на обидві терапевтичні стратегії [49].
Навіть низькодозова терапія глюкокортикостероїдами призводить до поглиблення імунодефіциту і унеможливлює спонтанну або індуковану компенсацію імунної дисфункції, хоча і послаблює прояви алергічних або автоімунних ускладнень [42].
Імуноглобулінотерапія має бути призначена тяжким пацієнтам з ДС IgG як засіб лікування першої лінії та як компонент терапії другої лінії після невдачі профілактичної антибіотикотерапії у пацієнтів з легкими і помірними клінічними проявами. Запропоновано застосовувати імуноглобуліни для внутрішньом’язового та внутрішньовенного введення, причому останні мають більшу доказову базу ефективності.
Повідомлення про клінічні випадки вказують на очевидну користь від внутрішньом’язового застосування нормального імуноглобуліну при ДС IgG [128]. Söderström T. зі співавт. провели проспективне дослідження, присвячене оцінці ефективності препарату імуноглобуліну для внутрішньом’язового введення в дозі 25 мг/кг на тиждень протягом 1 року у дорослих пацієнтів з дефіцитом окремих субкласів IgG (n=43). Показано, що під впливом проведеної імунотерапії досягли вірогідного зменшення кількості днів за рік, під час яких відзначалися інфекційні епізоди. Сироваткові концентрації всіх субкласів IgG нормалізувались у 24 з 43 пацієнтів. Інші 19 хворих надалі отримували внутрішньом’язовий імуноглобулін у дозі 50 мг/кг на тиждень, що забезпечило досягнення клініко-лабораторної ремісії [154].
Повідомлення про клінічні випадки вказують на очевидну користь від застосування внутрішньовенного імуноглобуліну при ДС IgG [115, 144, 151, 165]. Препарат застосовується в дозі 300–400 мг/кг маси тіла кожні 3–4 тиж [112]. Виключення становить лише дефіцит IgG3, коли внутрішньовенний імуноглобулін слід вводити в дозі 100 мг/кг на тиждень, зважаючи на короткий період напівжиття цього субкласу IgG [121].
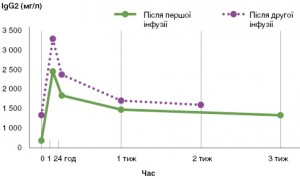 Рис. 9. Зростання сироваткової концентрації IgG2 у пацієнта з дефіцитом цього субкласу IgG після першої і другої інфузії внутрішньовенного імуноглобуліну (за Chou C.C. зі співавт.)
Рис. 9. Зростання сироваткової концентрації IgG2 у пацієнта з дефіцитом цього субкласу IgG після першої і другої інфузії внутрішньовенного імуноглобуліну (за Chou C.C. зі співавт.)Клінічна ефективність замісної внутрішньовенної імуноглобулінотерапії продемонстрована в кількох контрольованих та неконтрольованих випробуваннях [1, 2, 14, 18, 54]. Внутрішньовенний імуноглобулін покращує якість життя, знижує кількість інфекційних епізодів та потребу в антибіотиках, а також відновлює сироваткову концентрацію субкласів IgG у пацієнтів з цією імунною дисфункцією (рис. 9) [1].
Bernatowska-Matuszkiewicz E. зі співавт. провели проспективне контрольоване випробування двохрічної замісної внутрішньовенної імуноглобулінотерапії в дозі 400 мг/кг на місяць у пацієнтів з ДС IgG, що проявлявся рецидивними респіраторними інфекціями. Показано скорочення тривалості перебування у стаціонарі (перший рік – 27,8 дня, другий рік – 4,9 дня), використання антибіотиків (132,8 проти 30,9 дня) та стероїдів (21,4 проти 0,7 дня) [16]. Gordon C.L. зі співавт. у спеціально спланованому дослідженні продемонстрували ефективність внутрішньовенного імуноглобуліну для лікування пневмонії, спричиненої вірусом грипу H1N1, у пацієнтів з ізольованим дефіцитом IgG2 [52]. Olinder-Nielsen A.M. зі співавт. провели ретроспективний аналіз застосування внутрішньовенного імуноглобуліну в дозі 100 мг/кг на тиждень у 350 пацієнтів з ДС IgG, які страждали на рецидивні респіраторні інфекції. Досягнута редукція кількості інфекційних епізодів, що потребували призначення антибіотиків, при дефіциті IgG1 – на 57%, IgG2 – на 59%, IgG3 – на 63% та при комбінованих порушеннях – на 61% (p<0,001) [121].
Імунотерапія ефективна також при автоімунних і алергічних ускладненнях імунодефіциту.
Bertoli L.F. зі співавт. продемонстрували покращення слуху після призначення внутрішньовенного імуноглобуліну в 60,7% випадків серед пацієнтів з ДС IgG1 і IgG3, які страждали на автоімунну сенсоневральну приглухуватість [17]. Frohman L.P. зі співавт. вилікували рецидивний стероїд-залежний оптичний неврит у пацієнта з дефіцитом IgG2 та IgG3 за допомогою внутрішньовенної імуноглобулінотерапії [45]. Chinratanapisit S. зі співавт. усунули прояви рефрактерного риносинуїту і назального поліпозу в більшості пацієнтів з ДС IgG під впливом внутрішньовенного імуноглобуліну [26]. Як зазначають May A. зі співавт., ендоназальна хірургія має застосовуватися тільки при неефективності консервативних підходів до лікування, у тому числі внутрішньовенного імуноглобуліну [107]. Згідно з результатами дослідження Page R. зі співавт., відзначається суттєве зменшення клінічних проявів БА під впливом внутрішньовенного імуноглобуліну у пацієнтів з ДС IgG [127]. Loza Cortina C. усунув прояви стероїд-залежної астми під впливом високодозової імуноглобулінотерапії у пацієнта з ізольованим дефіцитом IgG2 [101]. Натомість Plebani A. зі співавт. продемонстрували послаблення симптомів рефрактерної епілепсії у дітей з цим імунодефіцитом після призначення внутрішньовенного імуноглобуліну [135]. Відповідно до цього, Sterio M. зі співавт. повідомили про купірування епілептичного синдрому у 2 дітей з дефіцитом IgG2 після призначення внутрішньовенного імуноглобуліну в дозі 400 мг/кг на місяць [157]. Popa V. зі співавт. продемонстрували усунення проявів хронічної інтерстиційної хвороби легень, зумовленої ДС IgG, під впливом внутрішньовенного імуноглобуліну [136].
Suga S. зі співавт. повідомили про успішну пересадку кісткового мозку 8-річному хлопчику з тяжким дефіцитом IgG1 від HLA-ідентичної MLC-негативної сестри, оскільки ні профілактична антибіотикотерапія, ні внутрішньовенний імуноглобулін не зменшили частоту інфекційних епізодів. Після трансплантації відзначалося відновлення сироваткової концентрації IgG1 і повна компенсація клінічного статусу [159]. Однак, як показали Kelsey S.M. зі співавт. у спеціально спланованому дослідженні, вторинні ДС IgG можуть персистувати більше 1 року після пересадки алогенного кісткового мозку у людей і зумовлювати розвиток ускладнень [78]. Hammarström L., Smith C.I. повідомили про перенесення реципієнту, що раніше не страждав на первинний імунодефіцит, генетично детермінованого дефіциту IgG2 від донора внаслідок проведення трансплантації алогенного кісткового мозку [56].
Список літератури – у редакції