26 січня, 2017
Рак мочевого пузыря

Руководство Национальной онкологической сети США (NCCN), 2016 г.
(аспекты терапии инвазивного заболевания)
Обзор
В 2015 г. в США было выявлено 74 000 новых случаев заболевания раком мочевого пузыря (РМП) – у 56 320 мужчин и 17 680 женщин. В структуре онкологической заболеваемости РМП занял 6-е место по распространенности, встречаясь в три раза чаще у мужчин, чем у женщин. За этот же период зарегистрировано 16 000 смертельных исходов (у 11 510 мужчин и 4490 женщин). РМП редко диагностируется у лиц моложе 40 лет, и поскольку средний возраст пациентов составляет 65 лет, их лечение сопряжено с наличием сопутствующих заболеваний.
Клинически пациентов с РМП можно разделить на 3 категории в зависимости от прогноза, лечения и терапевтических целей. К первой группе относятся пациенты с неинвазивным РМП, лечение которых направлено на уменьшение риска рецидива и предотвращение прогрессирования. Вторая группа – пациенты с инвазивным РМП, у которых обсуждается вопрос о сохранении органа без влияния на продолжительность жизни. Пациентам с высоким риском отдаленных метастазов необходима системная терапия с целью повысить вероятность излечения. Главной задачей в третьей группе пациентов с метастатическими поражениями является продление жизни и повышение ее качества.
Гистологические особенности
Более 90% всех уротелиальных опухолей происходят из мочевого пузыря, еще 8% развиваются из клеток почечной лоханки, остальные 2% – из мочеточника и мочеиспускательного канала. Уротелиальная (переходноклеточная) карцинома – наиболее распространенный гистологический подтип РМП – может развиться на любом участке, где присутствует переходной эпителий (почечная лоханка, мочеточник, мочевой пузырь, а также проксимальные 2/3 уретры). В дистальной 1/3 уретры преобладает плоскоклеточный эпителий. Плоскоклеточный рак диагностируется в 3% случаев (определяется по наличию кератинизации в биоптате). Среди других гистологических типов аденокарциномы составляют 1,4% и 1% – мелкоклеточный рак (с паранеопластическим синдромом или без такового). Аденокарциномы чаще встречаются в верхушке мочевого пузыря, урахусе и периуретральных тканях. В классификацию Всемирной организации здравоохранения входят 13 гистологических типов, наиболее распространенные варианты – плоскоклеточный, железистый, саркомоподобный и микропапиллярный рак. При уротелиальных опухолях часто наблюдаются смешанные формы, например, комбинация уротелиального и плоскоклеточного или железистого подтипа, недавно определили комбинацию папиллярного и саркомоподобного подтипов. Подходы к терапии такие же, как и при уротелиальной карциноме.
Системные режимы химиотерапии (ХТ), применяемые для лечения пациентов с уротелиальными карциномами, как правило, неэффективны для опухолей с чистым, неуротелиальным (непереходно-клеточным) гистологическим подтипом – аденокарциномы или плоскоклеточного рака. В некоторых случаях после системного лечения больных со смешанным гистологическим типом опухоли остается только ее неуротелиальный компонент.
Патоморфология
Приблизительно в 70% случаев впервые выявленный РМП является неинвазивным – это «экзофитный папиллярный рак» (опухоль ограничена слизистой оболочкой – Ta – 70-75% или, реже, подслизистым слоем – T1 – 20-25%) либо плоскоклеточные высокодифференцированные новообразования (CIS 5-10%). Для всех этих опухолей характерны рыхлая структура и склонность к кровоточивости, при рецидиве возможно их возникновение на том же или другом участке мочевого пузыря в аналогичной исходной или более поздней стадии.
У 31-78% пациентов при РМП с прорастанием в слизистый или подслизистый слой возникает в течение 5 лет рецидив или новая уротелиальная карцинома. Развитие рецидива коррелирует со степенью дифференцировки, начальной стадией, размером опухоли и множеством поражений.
Инвазивный РМП
Диагностика и первичное хирургическое лечение
Перед началом лечения рекомендуется провести общий и биохимический (щелочная фосфатаза – ЩФ) анализ крови. Осуществляется оценка на предмет наличия регионарных и отдаленных метастазов: цистоскопия, рентгенография или компьютерная томография (КТ) органов грудной клетки, остеосцинтиграфия (при повышенном уровне ЩФ), обследование верхних мочевых путей с визуализацией брюшной полости и таза посредством КТ или магнитно-резонансной томографии (МРТ). МРТ и КТ дают возможность оценить степень инвазии и ее распространение на лимфатические узлы (ЛУ) и отдаленные органы, но не определяют истинную глубину инвазии.
Начальным в терапии РМП является проведение трансуретральной резекции (ТУР). ТУР позволяет определить стадию заболевания, поэтому мышцы мочевого пузыря должны быть включены в биоптат. Большей частью инвазивный РМП – карцинома с высокой степенью злокачественности. После проведения ТУР при инвазивном РМП необходимо дальнейшее лечение, которое может включать: радикальную или частичную цистэктомию, неоадъювантную или адъювантную терапию, органосохраняющие операции и ХТ на поздних стадиях заболевания.
Радикальная цистэктомия
У мужчин проводится цистопростатэктомия, у женщин – цистэктомия и расширенная гистерэктомия с последующей деривацией мочи. Деривация мочи осуществляется путем формирования подвздошного кондуита или создания внутреннего резервуара с отведением мочи на переднюю брюшную стенку или через уретру. Относительные противопоказания для формирования уретрального дренажа: Tis в протоках предстательной железы или позитивный хирургический край уретры. Неоцистис или ортотопическая реконструкция мочевого пузыря обеспечивают те же функции, но с повышенным риском ночного недержания мочи или задержки мочи с необходимостью периодически ставить катетер.
Неотъемлемой частью хирургического лечения является диссекция тазовых лимфатических узлов (ДТЛУ). Расширенная ДТЛУ (общие подвздошные, нижние парааортальные или паракавальные ЛУ) ассоциируется с лучшей выживаемостью и меньшим риском рецидива. Факторы, которые могут препятствовать проведению ДТЛУ: грубые постхирургические рубцы, пожилой возраст и наличие тяжелых сопутствующих заболеваний.
Неоадъювантная ХТ
Результаты двух рандомизированных исследований продемонстрировали преимущество в выживаемости пациентов при проведении неоадъювантной ХТ, особенно с клинической картиной Т3 стадии заболевания.
В рандомизированном исследовании с участием 307 пациентов с инвазивным РМП сравнивалась эффективность радикальной цистэктомии с неоадъювантной ХТ и без нее. В рандомизированном исследовании с участием 307 пациентов с инвазивным РМП сравнивалась эффективность радикальной цистэктомии и 3 курсов режима MVAC (метотрексат, винбластин, доксорубицин и цисплатин) с последующей цистэктомией. Пациенты в группе неоадъювантной ХТ продемонстрировали увеличение медианы выживаемости (77 мес против 46) и более низкий уровень остаточной опухоли (15 против 38%) (Grossman et al., 2003).
В другом исследовании у 196 пациентов с инвазивным РМП сравнивалась эффективность цистэктомии с неоадъювантной ХТ и без нее (2 цикла – схема MVAC). Проведение ХТ привело к большему увеличению числа пациентов, достигших рT0 стадии: 34 против 9% при одной лишь цистэктомии. Общая выживаемость (ОВ) была незначительно выше при проведении неоадъювантной ХТ. Метаанализ данных 11 исследований с участием 3005 пациентов показал увеличение 5-летней общей и безрецидивной выживаемости на 5 и 9% соответственно у больных, получавших неоадъювантную ХТ на основе препаратов платины (2005 год).
В ходе многоцентрового проспективного исследования II фазы пациенты с cТ2 и cT4a и N0 или N1 инвазивным РМП получили 3 цикла «уплотненной» ХТ (ddMVAC) с пэгфилграстимом и последующую радикальную цистэктомию с лимфодиссекцией. Режим ddMVAC обладает лучшим профилем безопасности, сокращает время до операции и приводит к сопоставимому достижению патологического полного ответа в сравнении со стандартной ХТ на основе цисплатина. У пациентов, получавших ddMVAC, не зарегистрировано смертельных исходов, связанных с токсичностью. Побочные эффекты 1-й или 2-й степени наблюдались у 82% пациентов. Среднее время до цистэктомии составляло 9,7 недели.
Предварительные данные демонстрируют ценность режима ddVAC в качестве неоадъювантной ХТ при инвазивном РМП, однако эти данные следует интерпретировать с осторожностью из-за небольшого размера выборки (n=44).
По результатам рандомизированного исследования с участием 976 больных (медиана наблюдения – 8 лет) альтернативный режим ХТ с использованием цисплатина, метотрексата и винбластина (CMV) перед операцией снижает риск смертности на 16%.
Адъювантная ХТ
В настоящее время ведутся дискуссии относительно необходимости применения адъювантной ХТ. Метаанализ 6 исследований показал снижение смертности на 25% на фоне адъювантной ХТ, но авторы отметили несколько ограничений и заключили, что результаты недостаточны для принятия решения о лечении. Исследования показали улучшение выживаемости при применении комбинации циклофосфамида, доксорубицина и цисплатина (CAP), режима MVAC или комбинации метотрексата, винбластина, эпирубицина и цисплатина (MVEC). Тем не менее вопрос о возможности проведения данной терапии для всех пациентов с уротелиальными опухолями остается открытым. В исследовании MVEC пациенты с рецидивом заболевания в контрольной группе не подвергались ХТ, что не является типичным для более современных исследований.
В рандомизированном исследовании III фазы с участием 194 пациентов отсутствовала разница в ОВ или безрецидивной выживаемости между пациентами, получавшими гемцитабин и цисплатин (GC) адъювантно, и теми, кто проходил курс ХТ при рецидиве.
Тем не менее адъювантная ХТ оправданна при высоком риске рецидива. Необходимо не менее 3 курсов терапии, основанной на цисплатине, такой как MVAC, или чаще GC. Карбоплатин не следует заменять на цисплатин в периоперационном периоде. У пациентов со стадией pT2 и менее при отсутствии поражения ЛУ или лимфоваскулярного прорастания необязательно проведение адъювантной ХТ, так как они относятся к группе пониженного риска рецидива.
Некоторые ученые рекомендуют стратифицировать пациентов в зависимости от статуса p53, так как опухоли с более чем 20% p53-положительных клеток имеют более высокий риск системного рецидива. Определение статуса р53 опухоли по-прежнему считается экспериментальной процедурой и не является частью обязательной диагностики.
Адъювантная лучевая терапия
Рандомизированное исследование с участием 236 пациентов с pT3a-pT4a стадиями РМП продемонстрировало улучшение 5-летней безрецидивной выживаемости на фоне адъювантной лучевой терапии (ЛТ) по сравнению с только хирургическим лечением. Ретроспективные исследования также демонстрируют улучшение онкологической выживаемости после адьювантной ЛТ у пациентов с рТ2-рТ4а стадиями РМП. Поскольку риск развития местных рецидивов после цистэктомии высок для некоторых групп пациентов (32% для пациентов рT3-Т4 и 68% для пациентов с положительным хирургическим краем), целесообразно рассматривать применение ЛТ у таких больных. Может быть использована ЛТ в дозе 40-45 Гр с одновременным применением цисплатина или без такового. Более низкие дозы ЛТ обладают меньшей токсичностью, но необходимо дальнейшее изучение безопасных доз, особенно у пациентов с неоцистисом.
Органосохраняющие опции
У определенной группы пациентов с уротелиальной карциномой стадий Т2 и T3а может быть рассмотрена стратегия сохранения мочевого пузыря. Она заключается в проведении только эндоскопической ТУР, мочевого пузыря самостоятельно или ТУР с последующей ХТ, ЛТ или ЛТ в сочетании с ХТ.
Подход с сохранением мочевого пузыря является разумной альтернативой радикальной цистэктомии у пациентов, которым противопоказано хирургическое лечение или которые отказываются от цистэктомии. Решение о сохранении мочевого пузыря должно быть основано на данных о локализации, глубине инвазии, размере опухоли, состоянии уротелия и функциональном статусе пациента (емкость и функциональность мочевого пузыря, сопутствующие заболевания).
Если нет противопоказаний, проводится максимально полная ТУР; бимануальное исследование и диагностика метастазирования выполняются до начала терапии.
После максимально полной ТУР потенциальными вариантами терапии являются ХТ, ЛТ, химиолучевая терапия (с регулярным цистоскопическим мониторингом и дальнейшим лечением при необходимости). Тем не менее только сочетание ХТ и ЛТ было оценено в проспективных рандомизированных исследованиях, другие варианты до сих пор исследуются. Контрольная цистоскопия с биопсией проводится после индукционной фазы лечения. Оценка при других методах осуществляется через 2-3 мес после терапии. При наличии опухоли как можно быстрее проводится цистэктомия.
Химиотерапия при распространенном РМП
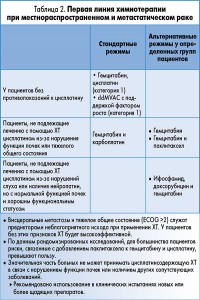
Выбор режима ХТ зависит от функционального статуса пациента, наличия сопутствующих заболеваний, таких как сердечная и почечная дисфункция, наряду с оценкой рисков, связанных с основным заболеванием. В целом длительная выживаемость при одной лишь комбинированной ХТ наблюдалась только у пациентов с низким риском без висцерального (печень, легкие) и костного поражения, нормальным уровнем ЩФ или лактатдегидрогеназы. У пациентов с повышенным риском (плохим общим состоянием или висцеральным поражением) отмечалась очень низкая переносимость комбинированной терапии и незначительная частота достижения полной ремиссии.
К первой линии терапии при метастатическом РМП относятся цисплатин, таксаны и гемцитабин. В международном рандомизированном исследовании III фазы сравнивался режим GC со стандартным MVAC у 405 пациентов с местнораспространенным или метастатическим РМП. При медиане наблюдения 19 мес ОВ и время до прогрессирования оказались одинаковыми в обеих группах. Меньшее количество смертельных исходов, связанных с токсичным действием, зарегистрировано в группе GC (1 против 3%). Анализ обновленных данных подтвердил, что GC не уступает MVAC с точки зрения выживаемости (ОВ 13 против 15,3%; выживаемость без прогрессирования – 9,8 против 11,3% соответственно). В другом крупном рандомизированном исследовании III фазы по сравнению ddMVAC со стандартной MVAC при медиане наблюдения 7,3 года ОB в группе ddMVAC составила 24,6% против 13,2% в группе MVAC. У пациентов с метастазированием режимы GC и ddMVAC с поддержкой фактором роста относятся к рекомендациям первой категории; режим GC обладает меньшей токсичностью. Альтернативные режимы первой линии включают карбоплатин и таксаны или монохимиотерапию.
Режимы с более низкой токсичностью рекомендованы пациентам с нарушением функции печени и почек или наличием серьезных сопутствующих заболеваний. У больных со скоростью клубочковой фильтрации менее 60 мл/мин карбоплатин может быть заменен на цисплатин. Исследования ІІ-ІІІ фазы оценивали 2 карбоплатинсодержащих режима у пациентов, не подлежащих лечению с помощью ХТ (функциональный статус 2). Частота общего ответа составила 42% в группе гемцитабина с карбоплатином и 30% в группе метотрексата, карбоплатина и винбластина. Тем не менее уровень ответа снизился соответственно до 26 и 20% с увеличением токсичности лечения у пациентов с нарушеной функцией почек (скорость клубочковой фильтрации <60 мл/мин).
Таксаны эффективны как в первой линии терапии, так и в ходе паллиативного лечения. Альтернативные режимы терапии, в том числе цисплатин/паклитаксел, гемцитабин/паклитаксел и другие, продемонстрировали незначительный эффект у больных с РМП в исследованиях І-ІІ фазы. Рандомизированное исследование III фазы по сравнению режимов GC и GC+паклитаксел с участием 626 пациентов с местнораспространенным или метастатическим раком мочевыводящих путей показало, что добавление паклитаксела приводит к увеличению частоты ответа и ОВ. Однако в группе intention-to-treat они не были статистически достоверными. Анализ данных только подходящих пациентов (92%) продемонстрировал небольшое (3,2 мес), но статистически значимое преимущество ОВ при использовании 3-компонентной терапии. Не отмечено влияния на выживаемость без прогрессирования. Нейтропеническая лихорадка наблюдалась чаще у пациентов на фоне 3-компонентной терапии (13,2 против 4,3%).
Независимо от режима терапии, повторная оценка пациентов с метастазами проводится после 2 до 3 циклов ХТ, у пациентов с регрессией или стабилизацией заболевания лечение продолжается еще 2 цикла. Хирургическое лечение или ЛТ могут быть рассмотрены у пациентов с высоким частичным ответом при первично неоперабельной опухоли или с единичным остаточным участком опухоли, резектабельным после ХТ. В одельных случаях этот подход позволяет улучшить выживаемость.
При полной резекции опухоли возможно проведение 2 дополнительных циклов ХТ в зависимости от их переносимости пациентом. Пациенты, для которых хирургическое вмешательство или ЛТ не рассматриваются как основные варианты терапии, могут получать ХТ в течение максимум 6 циклов. Смена терапии рекомендуется для пациентов с системным рецидивом после адъювантной ХТ.
Данные по второй линии ХТ весьма разнообразны, стандарты до сих пор не разработаны. Эксперты NCCN настоятельно рекомендуют включение в клинические исследования. В зависимости от препаратов, используемых в первой линии, для паллиативной терапии предпочтительно применение доцетаксела, паклитаксела или гемцитабина в монотерапии. Другие варианты включают цисплатин, карбоплатин, доксорубицин, 5-фторурацил, ифосфамид, пеметрексед, метотрексат и винбластин на основании скромных преимуществ, полученных в небольших исследованиях II фазы.
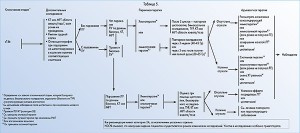
Т2, Т3 и T4a стадии
Первичным методом терапии пациентов со стадиями Т2, сТ3 и сT4a без поражения ЛУ является радикальная цистэктомия и тазовая лимфаденэктомия. Неоадъювантная ХТ рекомендована для лечения больных с опухолями Т3 и определенных групп пациентов с Т2 стадией. Если неоадъювантная ХТ не проводилась, адъювантная ХТ или ЛТ подбирается на основе патоморфологических данных (вовлечение ЛУ, позитивный край резекции, высокая степень злокачественности, рT3-T4 поражения).
Частичная цистэктомия наряду с неоадъювантной ХТ может рассматриваться только у пациентов с единичной опухолью стадии Т2 определенной локализации и без Tis. Частичная цистэктомия не является вариантом выбора для T3 или T4a стадий.
Органосохраняющая тактика допустима у тщательно отобранных пациентов без гидронефроза при наличии опухоли, которая хорошо визуализируется и позволяет проведение ТУР в полном объеме (категория 2B). Переоценка проводится через 3 недели после ЛТ (40-45 Гр) или 2-3 мес после полной дозы облучения (60-65 Гр). Если опухоль не обнаружена, проводится наблюдение или завершение ЛТ на уровне 66 Гр, при наличии опухоли – цистэктомия.
У пациентов с сопутствующими заболеваниями или плохим функциональным статусом вариантом выбора является ТУР в комбинации с ХТ и ЛТ. Только монотерапия цисплатином или 5-фторурацилом в комбинации с митомицином показали радиосенсибилизирующий эффект и преимущество по сравнению с одной лишь ЛТ. Повторная оценка проводится через 2-3 мес, при наличии опухоли предпочтительно проведение цистэктомии. Пациентам, которые не являются кандидатами на хирургическое вмешательство, возможно назначение ЛТ с альтернативной радиосенсибилизирующей ХТ и/или альтернативной ХТ.
T4b стадия, или пациенты с поражением ЛУ
Для пациентов без признаков поражения ЛУ (что подтверждено данными МРТ, КТ и биопсии) рекомендуется проведение 2-3 курсов ХТ с ЛТ или без таковой с последующими ТУР, цистоскопией и КТ брюшной полости и таза. Для тщательно отобранных пациентов со стадией T4a и без поражения ЛУ одним из вариантов терапии является цистэктомия с ХТ или без таковой. Если после первичной ХТ признаки опухоли не обнаружены, может быть рассмотрено применение консолидирующей ХТ с или без ЛТ, если же они есть, то целесообразно будет сменить режим терапии. Если проведение цистэктомии возможно, оно будет обязательным независимо от ответа на первичное лечение.
Пациентам с поражением ЛУ, выявленным методом визуализации, проводится биопсия, если она возможна, для подтверждения распространения опухоли. Пациенты с поражением ЛУ получают ХТ с ЛТ или без таковой с оценкой при помощи цистоскопии, ТУР, КТ, МРТ брюшной полости и таза. Если заболевание не исчезло после первичной терапии, его следует лечить по алгоритму для пациентов с метастазами.
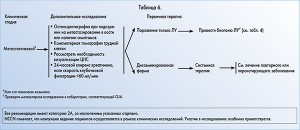
Метастатический РМП
Приблизительно у половины пациентов возникает рецидив заболевания после цистэктомии, развитие которого зависит от стадии и поражения ЛУ. На локальные рецидивы приходится 10-30% от всех рецидивов, отдаленные метастазы возникают еще чаще.
При наличии метастазов необходимо углубленное исследование с выполнением КТ грудной клетки и остеосцинтиграфии (при повышении уровней ферментов или наличии характерных симптомов, указывающих на вовлечение скелета). Если распространение ограничено только ЛУ, выполняется биопсия; лечение таких пациентов осуществляется по алгоритму для Т4 стадии. Если у пациента диагностировано диссеминированное метастатическое поражение, проводится системная терапия с включением ХТ, ЛТ и их комбинации. Особенности выбора режима терапии находятся на стадии обсуждения.
Публикуется в сокращении, полный текст на www.nccn.org.
Перевели с англ. Екатерина Марушко и Катерина Котенко