24 січня, 2017
Торемифен в терапии рака молочной железы: 20 лет исследований
Эндокринная терапия является краеугольным камнем лечения эстроген-рецептор-положительного (ЭР+) рака молочной железы (РМЖ). Открытие более 40 лет назад селективных модуляторов рецептора эстрогена стало революционным прорывом в лечении этого заболевания. Торемифена цитрат создан более 20 лет назад с целью улучшения профиля безопасности терапии по сравнению с тамоксифеном при аналогичной ее эффективности. Рассмотрим обобщенный анализ данных, отражающих возможности применения торемифена при РМЖ.
Хотя явные преимущества в переносимости торемифена по сравнению с тамоксифеном не выявлены, во всех исследованиях подтверждены эффективность и безопасность торемифена у пациенток с РМЖ в постменопаузе.
Фармакокинетический профиль и путь метаболизма торемифена отличаются от таковых для тамоксифена. Выявление генетических различий в метаболизме лекарственных препаратов позволило взглянуть на торемифен по-новому как на значимую терапевтическую опцию для конкретных категорий пациенток.
Определение генетического полиморфизма все чаще используется для оценки индивидуальной способности организма усваивать лекарственный препарат. В отличие от тамоксифена торемифен не является пролекарством и не требует преобразования с помощью ферментов семейства цитохрома Р450, таких как CYP2D6 (тогда как концентрации активных метаболитов тамоксифена значительно изменяются в зависимости от генотипа CYP2D6). Австрийская исследовательская группа ABCSG‑8 обнаружила связь между полиморфизмом CYP2D6 и рецидивированием РМЖ в первые 5 лет терапии тамоксифеном; эта связь отсутствовала, если через 2 года лечения пациенток переводили на анастрозол.
Из-за потенциальных проблем с нарушением метаболизма и лекарственных взаимодействий (например, с ингибиторами CYP2D6) тамоксифен может уступать по эффективности торемифену. Кроме того, в связи с отличиями в профиле побочных эффектов по сравнению с ингибиторами ароматазы торемифен является возможной их альтернативой для некоторых пациенток.
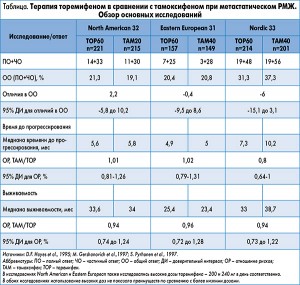
Торемифен утвержден для лечения метастатического РМЖ (мРМЖ) у женщин в постменопаузе с ЭР+ или неизвестным рецепторным статусом. Оценка эффективности и безопасности торемифена по этому показанию проводилась в трех основных проспективных рандомизированных контролируемых исследованиях.
В исследовании North American пациентки в пери- и постменопаузе получали торемифен (60 мг/сут) или тамоксифен (20 мг/сут). В исследованиях Eastern European и Nordic пациентки в постменопаузе получали торемифен в стандартной дозе 60 мг или тамоксифен в дозе 40 мг (стандартная доза за пределами США).
Параллельно изучались повышенные дозы торемифена – 200 мг в исследовании North American и 240 мг в исследовании Eastern European. Результаты этих исследований представлены в таблице.
Эффективность торемифена по сравнению с тамоксифеном в адъювантной терапии РМЖ у женщин в постменопаузе оценивали 4 масштабных исследования. Два из них проведены в 1990-х гг. международной исследовательской группой IBCSG (их результаты объединены), еще одно – финской исследовательской группой FBCG. Кроме того, в 2000 г. в США проведено исследование NAFTA.
В первых 2 исследованиях у женщин в перименопаузе и постменопаузе с РМЖ и поражением лимфоузлов сравнивалась эффективность стандартных суточных доз торемифена и тамоксифена в сочетании с химиотерапией. В первом исследовании IBCSG (Trial 12-93) сравнивались 3 адъювантных режима: 4 курса химиотерапии (доксорубицин или эпирубицин + циклофосфамид) и гормонального препарата одновременно, последовательно либо в качестве монотерапии. Во втором исследовании (Trial 14-93) сравнивали 2 режима (циклофосфамид 4 курса и далее режим CMF 3 курса) с 16-недельным перерывом между курсами и без такового. Общий анализ данных этих исследований (n=1035) показал сходные результаты 5-летней выживаемости без признаков заболевания: 72% для торемифена, 69% для тамоксифена; общая выживаемость (ОВ) составила 85% для торемифена, 81% для тамоксифена. У пациенток с ЭР+ РМЖ (n=773) на фоне торемифена 5-летняя выживаемость без признаков заболевания составила 76% (72% для тамоксифена), а 5-летняя ОВ – 90 и 86% соответственно.
В исследовании FBCG сравнивалась терапия торемифеном (40 мг) и тамоксифеном (20 мг) в течение 3 лет у 1480 женщин с инвазивным, преимущественно ЭР+, РМЖ и поражением лимфоузлов. В этом исследовании не выявлено существенных различий в показателях ОВ между двумя группами.
В исследование NAFTA включили 1813 пациенток с гормон-рецептор-положительным первичным РМЖ I-II стадии, которые получали торемифен (60 мг) или тамоксифен (20 мг) ежедневно в течение 5 лет; также использовалась адъювантная химио- и лучевая терапия. При медиане наблюдения 59 мес 5-летние показатели существенно не отличались (ОВ 93,7 и 92,7% для торемифена и тамоксифена соответственно).
Метаанализ исследований, включающий данные 3709 женщин, в целом не выявил различий в ОВ (относительный риск – ОР – 1,07; 95% доверительный интервал – ДИ – 0,97-1,19; p=0,99) или выживаемости без признаков заболевания (ОР 1,05; 95% ДИ 0,95-1,17; p=0,43) между группами торемифена и тамоксифена; авторы заявили об их одинаковой эффективности.
В соответствующих клинических испытаниях торемифен показал равную эффективность с ингибиторами ароматазы при мРМЖ. В одном из исследований сравнивали эффективность торемифена (60 и 240 мг), тамоксифена (20 мг) и летрозола (2,5 мг) в монорежиме у 451 женщины в постменопаузе с мРМЖ. Примерно 30% пациенток имели гормон-рецептор-отрицательный статус. Для всех конечных точек исследования было выявлено сходство торемифена и летрозола в суточных дозах 60 и 2,5 мг соответственно; эффективность лечения была одинаковой независимо от рецепторного статуса. Оба эти препарата показали более высокую эффективность по сравнению с тамоксифеном в суточной дозе 20 мг (р<0,05) (R. Zeynalov et al., 2006). Поскольку все пациентки в этом исследовании ранее получали адъювантную гормональную терапию тамоксифеном при лечении первичной опухоли, преимущество других препаратов перед тамоксифеном неудивительно. Тем не менее (по мнению исследователей) сходство в эффективности между торемифеном и летрозолом интригует.
Получены также свидетельства, что высокие дозы торемифена могут быть эффективным и безопасным решением после неудачного лечения ингибиторами ароматазы. В исследовании II фазы Hi-FAIR у 91 пациентки с ИА-резистентным РМЖ, лечение которых с помощью нестероидных ингибиторов ароматазы оказалось неэффективным, сравнивали воздействие торемифена (120 мг) и экземестана (25 мг). При медиане наблюдения 16,9 мес отмечено значительное преимущество торемифена по сравнению с экземестаном в уровне клинического ответа – 47,5 и 27% соответственно (р=0,046) – и выживаемости без прогрессирования (ВБП) (ОР 0,62; 95% ДИ 0,38-0,99; p=0,047), но не отмечено разницы в ОВ. Оба препарата одинаково хорошо переносились.
Y. Yamamoto и соавт. (2010) ретроспективно оценили эффективность торемифена (120 мг) в терапии РМЖ у 83 женщин, перенесших рецидив на фоне ингибиторов ароматазы. Эффект торемифена наблюдался в 45% случаев: 12 пациенток (15%) достигли частичного ответа и 24 (30%) – стабилизации заболевания в течение 24 недель.
Что немаловажно, торемифен может быть эффективен при РМЖ, резистентном к тамоксифену. В исследовании II фазы (28 пациенток с первично-рефрактерным РМЖ, 43 пациентки с рецидивом после терапии тамоксифеном и 31 – с рецидивом на фоне тамоксифена) объективный ответ и стабилизация заболевания достигнуты в 5 и 23% случаев соответственно. Статистическая обработка данных показала достоверно лучшую выживаемость у пациенток с наличием эффекта торемифена даже в случае стабилизации заболевания (p=0,02).
В 2002 г. R. Gams представил обобщенные данные исследований, изучающих эффективность торемифена в повышенных дозах (более 60 мг/день). В первой группе исследований 366 женщин с прогрессированием РМЖ на фоне тамоксифена получали торемифен в дозах от 120 до 240 мг ежедневно. Из них 37 (10,1%) достигли объективного ответа; дополнительный эффект у 60 пациенток (16,4%) обусловливался длительной стабилизацией заболевания. В другой группе исследований 146 женщин с мРМЖ, резистентных к тамоксифену, до начала терапии торемифеном получали дополнительное лечение, включая цитотоксические препараты.
На фоне торемифена в 3-й линии терапии был достигнут объективный ответ у 17 (11,6%) больных и у 35 (24,0%) наблюдалась стабилизация заболевания, обеспечив общее клиническое преимущество у 35,6% пациенток. Профиль токсичности в этих исследованиях был аналогичен таковому при применении стандартных доз тамоксифена или торемифена.
Безопасность торемифена изучалась в целом ряде клинических испытаний, охватывающих более 500 000 человеко-лет общего клинического опыта. В исследовании North American для торемифена и тамоксифена установили сходную частоту распространенных токсических эффектов, которые считаются связанными с терапией: приливы (35%), потливость (20%), тошнота (14%), выделения из влагалища (13%), головокружение (9%), отеки (5%), рвота (4%) и вагинальное кровотечение (2%). Около 1% пациенток, получавших торемифен или тамоксифен, прекратили лечение из-за серьезных побочных эффектов. Профиль безопасности этих препаратов похож; только исследование Nordic показало значительную разницу в частоте развития катаракты в группах торемифена (0%) и тамоксифена (2,5%; р=0,026). Также метаанализ показал отсутствие статистически значимой разницы в риске тромбоэмболических осложнений с незначительной тенденцией в пользу торемифена (рис.).
 Рис. Метаанализ показал отсутствие статистически значимой разницы в риске тромбоэмболических
Рис. Метаанализ показал отсутствие статистически значимой разницы в риске тромбоэмболическихосложнений на фоне торемифена по сравнению с тамоксифеном при их применении в адъювантном
режиме (W. B. Zhou et al. , 2011)
Таким образом, торемифен (Фарестон®) обладает большой доказательной базой и может считаться актуальной альтернативой тамоксифену у женщин в постменопаузе с ЭР+ метастатическим РМЖ, особенно у определенных категорий пациенток. Дальнейшие исследования могут выявить другие потенциально полезные качества торемифена.
По материалам: Ch.L. Vogel, M.A. Johnston, Ch. Capers, D. Braccia. Toremifene for Breast Cancer: A Review of 20 Years of Data. Clinical Breast Cancer, Vol. 14, 2014.
Подготовила Катерина Котенко