9 липня, 2016
Бевацизумаб при раке шейки матки
Первый за последние десять лет метод лечения, позволяющий увеличить продолжительность жизни женщин [1]
Основанием для включения бевацизумаба в схемы ведения пациенток с распространенным раком шейки матки (РШМ) стали результаты рандомизированного исследования III фазы GOG 240. Окончательный анализ результатов исследования подтвердил увеличение выживаемости пациенток при добавлении бевацизумаба к стандартным режимам химиотерапии (ХТ). В результате он стал первым таргетным препаратом, получившим одобрение регулирующих органов США для лечения распространенного РШМ, и первой за несколько лет новой терапевтической опцией, способной увеличить выживаемость у этой категории пациенток. Сегодня данное показание зарегистрировано также и в Украине.
Наиболее распространенной причиной РШМ является вирус папилломы человека (ВПЧ), который распространяется через сексуальный контакт и провоцирует злокачественное перерождение клеток эпителия шейки матки. ВПЧ обнаруживается в 95% образцов опухолей, удаленных при хирургическом вмешательстве. В настоящее время известно 80 типов ВПЧ, из которых 30 инфицируют аногенитальную область и только пять (HPV 16, 18, 31, 33, 45) считаются вирусами высокого онкогенного риска.
Распространенность РШМ в развитых странах резко сократилась благодаря внедрению цитологического скрининга и ДНК-тестирования на наличие инфицирования онкогенными штаммами ВПЧ. Дальнейшее снижение заболеваемости и смертности от РШМ связывают с проведением вакцинации.
Несмотря на наличие лицензированных вакцин для профилактики заражения онкогенными типами ВПЧ и пропаганду профилактических осмотров, случаи выявления запущенных стадий заболевания все еще распространены. Только в США ежегодно диагностируется около 12 тыс. новых случаев РШМ [2]. Для малообеспеченных групп населения, а также в странах с низким доходом РШМ остается серьезной проблемой.
Ежегодно в мире регистрируют более 600 тыс. первичных пациенток с РШМ [2]. Более 7 тыс. случаев первичного РШМ выявляется среди украинских женщин (данные 2013 г.), около 2,5 тыс. женщин умирают от этого заболевания, причем многие – в трудоспособном возрасте. По обновленным данным Национального канцер-регистра за 2014 г., зарегистрирован 4101 случай РШМ [3]. Это заболевание остается одним из наиболее распространенных в онкологической практике, занимая 4-е место в общей структуре смертности онкологических больных и 1-е – в структуре смертности от злокачественных новообразований репродуктивной системы у женщин [3]. С 1997 по 2006 г. рост смертности от РШМ среди женщин в возрасте 20-24 лет составил 70%, а в возрастной группе 30-34 года – почти 30%. В 20% рак шейки матки диагностируется в запущенных стадиях (ІІІ-ІV), что в первую очередь связано с нерегулярными профилактическими осмотрами [3].
Для женщин репродуктивного возраста на начальных этапах заболевания актуален вопрос органосохраняющего лечения. С другой стороны, РШМ характеризуется более агрессивным течением по сравнению с другими гормонозависимыми опухолями, специфические особенности связаны с непосредственным участием вируса в патогенезе заболевания.
На ранней стадии и при местнораспространенном опухолевом процессе РШМ успешно подвергается хирургическому лечению, ХТ и лучевой терапии (ЛТ) либо комбинированному лечению, тогда как пациентки с метастазами или рецидивами, развившимися после ХТ на основе препаратов платины, имеют ограниченные возможности для лечения. Кратковременный ответ на ХТ у больных с распространенным РШМ указывает на относительную химиорефрактерность заболевания. Как самостоятельный метод лечения ХТ используется при рецидивах и первично распространенной опухоли. Одним из важных моментов, лимитирующих использование цитостатиков, является наличие побочных токсических проявлений, связанных с их введением.
Предпосылки для применения таргетной терапии при РШМ
Сосудистый эндотелиальный фактор роста (VEGF) представляет собой ключевой медиатор ангиогенеза опухоли, процесс которого в свою очередь непосредственно связан со стадией заболевания и обратно пропорционален выживаемости. Сосудистые маркеры являются отличительными чертами для инвазивного РШМ, причем увеличение плотности микроскопических сосудов при опухолях шейки матки коррелирует с плохим прогнозом. VEGF участвует в процессах митогенеза, ангиогенеза, обеспечивает выживание эндотелиальных клеток и индукцию гематопоэза. У пациенток с дисплазией шейки матки и инвазивным раком увеличивается экспрессия VEGF и гипоксия-индуцибельного фактора 1α (HIF‑1). При инвазивном фенотипе РШМ отмечается только повышенная регуляция VEGF. Сверхэкспрессия онкогенных подтипов ВПЧ приводит к накоплению белка HIF‑1 и повышенной экспрессии VEGF.
В нативном состоянии ВПЧ существует в виде эписом, состоящих из циркулярной двухцепочечной ДНК. При интеграции генетического материала онкогенного вируса в ДНК клетки-хозяина смещается рамка считывания ДНК, нарушается экспрессия генов и инициируется неопластический процесс в результате деградации или инактивации туморсупрессорного протеина р53 и белка ретинобластомы соответственно. Показано, что стимуляция избыточной выработки VEGF осуществляется благодаря прямому воздействию вируса через р53‑независимый механизм.
Бевацизумаб представляет собой гуманизированное VEGF-нейтрализующее моноклональное антитело, обладающее самостоятельной противоопухолевой активностью. С момента появления этот таргетный препарат исследуется в лечении опухолей разных локализаций, рост и распространение которых тесно связаны с VEGF.
14 августа 2014 г. Управление по контролю качества пищевых продуктов и лекарственных препаратов США (FDA) одобрило принципиально новое показание к применению бевацизумаба (Авастин®) для лечения пациенток с персистирующим, рецидивирующим или метастатическим РШМ. Основанием для утверждения послужили результаты исследования, проведенного Гинекологической онкологической группой (GOG), посвященного изучению эффективности ХТ с добавлением бевацизумаба или без него при распространенном РШМ. В этом базовом исследовании III фазы GOG 240 продемонстрировано значительное увеличение выживаемости в группе, получавшей лечение с добавлением бевацизумаба, по сравнению с группой ХТ [4]. Результаты исследования были предварительно представлены в рамках пленарного заседания Американского общества клинической онкологии (ASCO) в 2013 г. и опубликованы в The New England Journal of Medicine за 20 февраля 2014 г. Также в 2014 г. проведен подробный обновленный анализ токсичности на основе протокола, включающего 346 событий. Эти результаты были впервые озвучены доктором Krishnansu Tewari (кафедра акушерства и гинекологии, University of California, Irvine Medical Center, Orange, США) в рамках конгресса ESMO в сентябре 2014 года в г. Мадриде.
В апреле 2015 г. на основании результатов исследования GOG 240 бевацизумаб в сочетании с ХТ был одобрен Европейской комиссией для применения в странах ЕС по аналогичному показанию (у пациенток с персистирующим, рецидивирующим или метастатическим РШМ).
Дизайн исследования GOG 240
В рандомизированное исследование III фазы GOG 240 были включены 452 пациентки с рецидивирующим или метастатическим РШМ из 164 медицинских центров США и Испании. После рандомизации пациентки были распределены в две группы, получавшие только ХТ или ХТ с добавлением бевацизумаба. Средний возраст пациенток составил 49 лет, группы были рандомизированы по клиническим показателям (70-73% рецидивирующий РШМ), предварительной химиолучевой терапии (74-75%) и количеству рецидивов в области таза (53-54%) [2].
Первичной конечной точкой исследования была общая выживаемость (ОВ). Снижение риска смерти на 30% считалось клинически значимым. Как вторичные конечные точки рассматривались выживаемость без прогрессирования (ВБП) и ответ на лечение. Кроме того, тщательно исследовалась токсичность.
В исследовании также сравнивались два режима ХТ. Первый состоял из цисплатина в дозе 50 мг на 1 м2 поверхности тела и паклитаксела в дозе 135 или 175 мг на 1 м2. Второй режим включал в себя топотекан в дозе 0,75 мг на 1 м2 в дни с 1-го по 3-й плюс паклитаксел в дозе 175 мг на 1 м2 в день 1-й. Каждый из этих режимов был изучен отдельно, а также с добавлением бевацизумаба в дозе 15 мг на 1 кг массы тела на 1-й день каждого цикла). Циклы терапии повторялись через каждые 21 день до прогрессирования заболевания, развития неприемлемых токсических эффектов либо подтвержденного полного ответа на лечение.
Исследование GOG 240 проводилось с использованием 2×2 факторного дизайна, позволяющего определить, способствует ли сочетание ХТ с бевацизумабом и/или комбинация, не содержащая препаратов платины (топотекан + паклитаксел), улучшению ОВ у женщин с рецидивирующим/персистирующим и метастатическим РШМ.
Среднее количество курсов лечения для пациенток, получавших только ХТ, составило 6 (диапазон от 0 до 30); среди получавших ХТ в комбинации с бевацизумабом этот показатель составил 7 (диапазон от 0 до 36). Прекратили лечение в рамках исследования 97% пациенток; наиболее распространенной причиной было прогрессирование заболевания (у 51% больных, получавших ХТ, и у 38%, получавших ХТ в комбинации с бевацизумабом).
Эффективность лечения
К моменту проведения первичного анализа 62% пациенток были живы, средняя продолжительность периода наблюдения составляла 12,5 мес. По сравнению с комбинацией цисплатин-паклитаксел (с бевацизумабом или без него), применение комбинации топотекана и паклитаксела было связано со значительно более высоким риском прогрессирования (относительный риск – ОР – 1,39; 95% доверительный интервал – ДИ – 1,09-1,77), но не оказывало существенного влияния на ОВ (ОР смерти 1,20; 99% ДИ 0,82-1,76). Кроме того, у пациенток, получавших только ХТ, не наблюдалось значительных различий в смертности между подгруппой, ранее получавшей препараты платины (ОР 1,18; 95% ДИ 0,84‑1,65) и без предшествующего воздействия препаратов платины (ОР 1,35; 95% ДИ 0,68-2,69).
При медиане наблюдения 20,8 мес был зарегистрирован 271 случай смерти (60% от общего объема популяции, включенной в исследование). Добавление бевацизумаба значительно улучшало медиану ОВ как по сравнению с ХТ (17 мес по сравнению с 13,3 мес; ОР смерти 0,71; 98% ДИ 0,54‑0,95) (рис. 1А). Также наблюдалось значительное улучшение ВБП (8,2 против 5,9 мес; ОР прогрессирования заболевания 0,67; 95% ДИ 0,54-0,82) (рис. 1Б).
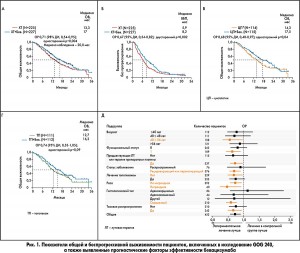
Частота ответа на лечение была значительно выше среди пациенток, получавших бевацизумаб, чем в группе, не получавшей таргетную терапию (48 против 36%) (относительная вероятность ответа 1,35; 95% ДИ 1,08-1,68; р=0,008, двухсторонний тест).
Полный ответ на лечение в группе, получавшей бевацизумаб, отмечен у 28 пациенток, в группе ХТ – у 14 (р=0,03). Лечение было прекращено у 21 пациентки. Применение схемы цисплатин-паклитаксел-бевацизумаб, по сравнению со схемой цисплатин-паклитаксел, было связано с ОР смерти 0,68 (95% ДИ 0,48-0,97) (рис. 1В). Общий ответ на лечение составил 50% (цисплатин-паклитаксел-бевацизумаб) и 45% (цисплатин-паклитаксел) (р=0,51, двусторонний тест), полный ответ имели 17 и 9 пациенток соответственно.
Режим топотекан-паклитаксел-бевацизумаб, по сравнению с режимом топотекан-паклитаксел, был связан с ОР смерти 0,74 (95% ДИ 0,53-1,05) (рис. 1Г). Уровень ответа составлял 47% (топотекан-паклитаксел-бевацизумаб) и 27% (топотекан-паклитаксел) (р=0,002, двухсторонний тест), полный ответ отмечен у 11 и 5 пациенток соответственно.
В ходе исследования было выявлено несколько значимых прогностических факторов. Преимущество лечения бевацизумабом также наблюдается при анализе подгрупп в зависимости от возраста, функционального статуса, расы, плоскоклеточного гистологического типа, статуса в отношении предварительного получения препаратов платины, рецидивирующего или распространенного заболевания и тазового расположения опухоли (рис. 1Д).
Следует отметить: дальнейший анализ результатов исследования показал, что преимущества, предоставляемые включением бевацизумаба в схему лечения, оказались устойчивыми и после 50 мес наблюдения, о чем свидетельствует сохраняющееся разделение кривых выживаемости.
Безопасность
Безопасность лечения отслеживали в течение каждого цикла. Дозу бевацизумаба в процессе лечения изменяли только в том случае, если масса тела пациентки изменялась более чем на 10%. Если проведение ХТ задерживалось из-за низкого абсолютного количества нейтрофилов или тромбоцитопении, бевацизумаб также не применялся. Терапия бевацизумабом могла быть отложена или прекращена в зависимости от возникновения, продолжительности и тяжести неконтролируемой артериальной гипертензии (систолическое артериальное давление >150 мм рт. ст. или диастолическое >100 мм рт. ст.), протеинурии (соотношение белок-креатинин ≥3,5), артериального или венозного тромбоза, коагулопатии, нарушения кишечной проходимости или непроходимости.
В таблице представлена частота побочных эффектов, которые потенциально могут быть связаны с терапией бевацизумабом. Гипертензия 2-й степени или выше была наиболее распространенным нежелательным эффектом у пациенток, получавших бевацизумабсодержащий режим, по сравнению с пациентками, получавшими только ХТ (25 против 2%, р=0,001), но ни одна пациентка не прервала лечение бевацизумабом из-за гипертензии.
В группе, получавшей бевацизумаб, отмечена достоверно большая частота развития гастроинтестинальных фистул (6% против 0 в группе сравнения) и тромбоэмболических осложнений (8% против 1 в группе сравнения). Не было достоверных различий по частоте развития нейтропении и болевого синдрома между группами. Кровотечения в желудочно-кишечном тракте и мочеполовой системе были редкими, признаков кровотечения в центральной нервной системе не обнаружено. Фатальные побочные эффекты развились у 4 пациенток (1,8%), которые получали ХТ и бевацизумаб (р=0,1). В целом наблюдаемые побочные эффекты были подобны таковым, отмечавшимся в других исследованиях с применением бевацизумаба.
О препарате Авастин®
Ингибирование VEGF с помощью бевацизумаба эффективно в сочетании с широким спектром химиотерапевтических препаратов и других видов противоопухолевого лечения с ограниченным дополнительным воздействием на побочные эффекты. Благодаря этому препарату антиангиогенная терапия стала одной из фундаментальных основ современного лечения рака.
С момента первоначального утверждения в США для лечения распространенного колоректального рака в 2004 г. бевацизумаб стал первым препаратом антиангиогенной терапии, получившим широкое распространение для лечения онкологических пациентов.
Продолжается расширение показаний к его применению на основании новых полученных доказательств его эффективности (увеличение ОВ и/или ВБП) при ряде опухолей. Авастин® одобрен в ЕС при поздних стадиях рака грудной железы, колоректального рака, немелкоклеточного рака легкого, рака почки, яичников, РШМ. Помимо аналогичных показаний, данный препарат одобрен в США и более чем 60 других странах для лечения пациентов с прогрессирующей глиобластомой (после предшествующей терапии). Сегодня исследуются возможности применения бевацизумаба при более чем 50 типах опухолей в рамках около 500 текущих клинических испытаний, и уже свыше 1,5 млн пациентов во всем мире прошли лечение этим препаратом.
В Украине Авастин® утвержден к применению по шести показаниям:
• лечение метастатического колоректального рака в сочетании с ХТ на основе препаратов фторпиримидина;
• лечение метастатического рака грудной железы;
• лечение распространенного нерезектабельного, метастатического или рецидивирующего немелкоклеточного рака легкого, за исключением преимущественно плоскоклеточного рака легкого, в сочетании с ХТ на основе препаратов платины;
• лечение распространенного и/или метастатического почечноклеточного рака, чувствительного к препаратам платины, в качестве 1-й линии терапии в комбинации с интерфероном альфа‑2а;
• лечение распространенного эпителиального рака яичника, фаллопиевой трубы и первичного рака брюшины в качестве 1-й линии терапии в комбинации с карбоплатином и паклитакселом. Лечение рецидивирующего эпителиального рака яичника, фаллопиевой трубы и первичного рака брюшины у взрослых, которые получили не более двух предшествующих режимов ХТ и ранее не получали анти-VEGF терапии;
• лечение персистирующего, рецидивирующего или метастатического РШМ в комбинации с паклитакселом и цисплатином, или паклитакселом и топотеканом в качестве альтернативы – для пациентов, которые не могут получать терапию препаратами платины. Это показание утверждено в Украине 18 мая текущего года.
Распространенность злокачественной опухоли является главным фактором, определяющим прогноз, интенсивность и продолжительность лечения РШМ. Авторы ключевого исследования GOG 240, основываясь на полученных результатах, говорят о том, что добавление бевацизумаба к ХТ снижает риск смерти пациенток с распространенным или рецидивирующим РШМ даже в тех случаях, когда они ранее получали препараты платины или ЛТ. Достигаемые благодаря назначению бевацизумаба преимущества (рис. 2) не сопровождаются существенным снижением качества жизни. Также показано, что сочетание топотекана и паклитаксела не превышало по эффективности комбинацию цисплатина и паклитаксела даже у тех пациенток, которые получали цисплатин прежде. В настоящее время бевацизумаб входит в международные руководства по ведению пациенток с РМЖ – рекомендуется его применение вместе с ХТ при рецидивирующих и первично-распространенных формах заболевания. Так, в обновленном руководстве Национальной онкологической сети США (NCCN) 2016 г. рекомендовано использование бевацизумаба в сочетании с двумя режимами химиотерапии: комбинацией паклитаксела и цисплатина либо паклитаксела и топотекана [5]. Отмечено, что цисплатин является наиболее эффективным химиопрепаратом при метастатическом РШМ. Большинство пациенток с метастатическим или рецидивирующим заболеванием получают в качестве первичного лечения цисплатин/ЛТ и впоследствии могут терять чувствительность к препаратам платины. Поэтому во второй линии терапии комбинация топотекана с паклитакселом (хотя в исследованиях и показала меньшую эффективность) рассматривается в качестве альтернативного режима для пациенток, теряющих чувствительность к цисплатину. При назначении таргетной терапии бевацизумабом необходимо учитывать соотношение пользы и риска у конкретной пациентки.
Литература
1. http://www.roche.com/media/store/releases/med-cor-2015-04-08.htm
2. Tewari K.S., Sill M.W., Long H.J. et al. Improved Survival with Bevacizumab in Advanced Cervical Cancer. New England Journal of Medicine, 2014; 370: 734-43. DOI: 10.1056/NEJMoa1309748.
3. Бюлетень Національного канцер-реєстру № 17 – «Рак в Україні, 2014-2015».
4. www.fda.gov.
5. NSSN Guidelines Version 1.2016, Cervical Cancer.
Подготовила Катерина Котенко



