20 травня, 2021
COVID‑19: сучасні принципи лікування і вакцинопрофілактики від провідних фахівців
 Минув рік з оголошення масового локдауну в Україні, і за цей час пандемія COVID‑19 внесла суттєві зміни в життя кожної людини і систему охорони здоров’я. Упродовж року медична спільнота перебувала в пошуках найбільш оптимальних і ефективних шляхів подолання пандемії.
Минув рік з оголошення масового локдауну в Україні, і за цей час пандемія COVID‑19 внесла суттєві зміни в життя кожної людини і систему охорони здоров’я. Упродовж року медична спільнота перебувала в пошуках найбільш оптимальних і ефективних шляхів подолання пандемії.
12-13 березня 2021 року відбувся один із наймасштабніших інформаційних медичних онлайн-заходів – ІІ Міжнародний конгрес «Pandemic STOP!», присвячений обговоренню найважливіших питань ведення хворих на COVID‑19 в амбулаторних і стаціонарних умовах, проблем вакцинації, правового захисту лікаря під час пандемії тощо. Провідні закордонні і вітчизняні експерти галузі поділилися з учасниками заходу найактуальнішою інформацією і власним досвідом щодо клінічних аспектів діагностики й лікування коронавірусної інфекції.
Ключові слова: COVID‑19, пандемія, коронавірусна інфекція, діагностика і лікування коронавірусної інфекції
Одна зі спікерів конгресу, лікар-інфекціоніст, медичний експерт дитячого фонду Організації Об’єднаних Націй (UNICEF) Катерина Булавінова (Україна), розповіла про стан проблеми з COVID‑19 в Україні.
 Пандемія COVID‑19 серйозно вплинула на систему охорони здоров’я в нашій країні, оскільки призвела як до позитивних, так і до негативних змін. Серед позитивних експерт передусім зазначила справедливе підвищення заробітної плати і збільшення поваги населення до роботи медичного персоналу. Іще одним позитивним моментом стало покращення оснащеності лікарень киснем. Раніше він здебільшого був у відділеннях реанімації, нині ж розведення кисню відбувається у стаціонарах багатьох лікарень великих міст. Кисень став доступнішим і в амбулаторній практиці: користуватися ним можуть не лише пацієнти, які потребують паліативної допомоги, усе частіше лікарі амбулаторної практики мають можливість лікувати пацієнтів із COVID‑19 у домашніх умовах із використанням кисневих концентраторів.
Пандемія COVID‑19 серйозно вплинула на систему охорони здоров’я в нашій країні, оскільки призвела як до позитивних, так і до негативних змін. Серед позитивних експерт передусім зазначила справедливе підвищення заробітної плати і збільшення поваги населення до роботи медичного персоналу. Іще одним позитивним моментом стало покращення оснащеності лікарень киснем. Раніше він здебільшого був у відділеннях реанімації, нині ж розведення кисню відбувається у стаціонарах багатьох лікарень великих міст. Кисень став доступнішим і в амбулаторній практиці: користуватися ним можуть не лише пацієнти, які потребують паліативної допомоги, усе частіше лікарі амбулаторної практики мають можливість лікувати пацієнтів із COVID‑19 у домашніх умовах із використанням кисневих концентраторів.
Спікер К. Булавінова зазначила, що кількість нових захворювань на COVID‑19 очевидно не відображає реальну кількість захворювань – остання є значно більшою. Проте важливішим є не абсолютне значення, а тренди захворюваності – кількість випадків захворювань збільшується щодня, тоді як кількість ліжко-місць і доступ до кисню зменшується. На жаль, і досі нема підстав стверджувати, що інфекційний контроль на тлі пандемії COVID‑19 здійснюють належним чином.
Сьогодні для виявлення COVID‑19 застосовують як ПЛР-тести, так і тестування на антиген. Проблемою є відсутність забезпечення лікарів-ФОПів тестами на антиген, а також поширене побоювання щодо обмеженої кількості цих тестів. Спікер зазначила, що, за словами Головного державного санітарного лікаря України В.К. Ляшка, тестів достатньо і буде ще більше, тож їх необхідно широко використовувати для своєчасного виявлення нових випадків зараження на COVID‑19.
Серед лікарів і пацієнтів побутує хибна думка, що тестування на COVID‑19 має проводитися виключно для визначення тактики подальшого лікування. Експерт наголосила, що тестування не є ланкою терапії і здійснюється з метою своєчасної ізоляції та обмеження поширення інфекції.
Основні проблеми інфекційного контролю:
- Неповне розділення стаціонарів медичних закладів на чисту й брудну зони.
- Некоректне використання захисних масок.
- Відсутність регулярних провітрювань приміщень лікарень і поліклінік.
Усе це вкрай негативно впливає на процес вакцинації в Україні. Часто люди очікують своєї черги на вакцинацію в тісному непровітрюваному приміщенні, не дотримуючися соціально безпечної дистанції, у неправильно одягнених масках, що суттєво підвищує ризик зараження на COVID‑19.
Щодо ситуації з вакцинацією від COVID‑19 в Україні, спікер повідомила, що з 24 лютого по 10 березня цього року в Україні вакциновано 29 378 осіб. Багато хто з лікарів публікують у соціальних мережах дописи про власний досвід щеплення, закликаючи населення наслідувати їх приклад. Аби підтримати ініціативу своїх колег, Катерина Булавінова також вакцинувалася публічно. На жаль, не лише деякі пересічні громадяни, а й навіть дехто з лікарів вважають, що необхідності у вакцинації після перенесеної інфекції COVID‑19 немає. Це хибна думка, оскільки на COVID‑19 можна захворіти повторно, і таких випадків більш ніж достатньо.
Ще однією проблемою є відсутність у певної частини населення довіри стосовно необхідності проведення вакцинації проти COVID‑19 взагалі. Мали місце випадки знищення препаратів через відмову від вакцинації, що є неприпустимим – усі залишкові дози мають бути запропоновані населенню. На щастя, Міністерство охорони здоров’я (МОЗ) розширило доступ населення до вакцинації, тож на сьогодні певна кількість осіб, зокрема громадських діячів, має можливість вакцинуватися залишковими дозами.
Своєю чергою, UNICEF проводить освітню роботу шляхом інформаційних і поведінкових кампаній, онлайн-навчання медичного персоналу і закупівлі обладнання (завдяки зусиллям UNICEF українські лікарні отримали понад 300 кисневих концентраторів.). UNICEF також взяла участь у Національній кампанії солідарності, спрямованій на підтримку медичного персоналу, який, ризикуючи власним життям, продовжує працювати в умовах пандемії. Результатом кампанії стало офлайн-охоплення майже 26,5 млн населення, онлайн-охоплення приблизно 18,8 млн осіб, а також більш як 400 тис онлайн-реакцій.
Щодо онлайн-навчання медичного персоналу, експерт зазначила, що на сайті UNICEF Ukraine та Youtube-каналі «Doctor Bulavinova» практично щотижнево з’являються нові відео з найважливіших тем, пов’язаних із COVID‑19. Зокрема, на цих ресурсах можна знайти актуальні дані щодо вакцинації проти COVID‑19 в Україні, ведення хворих на COVID‑19, ознайомитися з досвідом провідних іноземних фахівців та ін.
Наприкінці доповіді К. Булавінова відповіла на питання слухачів.
? Чи може негативний результат експрес-тесту на COVID‑19 бути представлений як результат тестування в разі госпіталізації?
– Негативний результат експрес-тесту у хворого на COVID‑19 не дає підстав для заперечення наявності інфекції. Якщо в пацієнта спостерігають відповідну клінічну картину захворювання, він має пройти обстеження на COVID‑19 за допомогою ПЛР-тесту.
Проблемою є також отримання негативних результатів навіть ПЛР-тестування в пацієнтів із вираженою тяжкою клінічною картиною COVID‑19, що значуще ускладнює процес госпіталізації.
Через це в деяких регіонах доводиться розгортати окремі відділення для пацієнтів із клінічною картиною COVID‑19 і негативним результатом тесту ПЛР.
? Чи доцільно дублювати позитивний результат експрес-тесту на COVID‑19?
– Ні, позитивний результат експрес-тесту на COVID‑19 є достатньо специфічним, і його дублювання недоцільне з клінічної точки зору.
? Чи є відсутність однієї нирки протипоказанням до вакцинації проти COVID‑19?
– Відсутність однієї нирки є не протипоказанням, а прямим показанням до вакцинації проти COVID‑19! Пацієнт з однією ниркою має набагато вищі ризики, пов’язані з ускладненнями інфекційних захворювань, зокрема COVID‑19, тож потребує специфічної профілактики.
? Чи дає щеплення вакциною AstraZeneca можливість подорожувати країнами Європи?
– На сьогодні немає достовірних даних щодо того, чи будуть впроваджені паспорти вакцинації або інші умови для перетину міжнародного кордону. Також ніде ніким не обговорювалося значення вакцин тих чи інших брендів щодо можливостей подорожування. Часто питають також про те, які документи є свідченням того, що особа була вакцинована проти COVID‑19. Після другої дози вакцини проти COVID‑19 кожна особа матиме можливість отримати довідку про факт вакцинації. Проте поки що немає інформації щодо запровадження паспортів вакцинації в Україні.
? Чи є наявність декларації із сімейним лікарем обов’язковою умовою для проведення вакцинації проти COVID‑19?
– Ні, наявність декларації із сімейним лікарем не є необхідною для проведення вакцинації проти COVID‑19, оскільки доступна можливість внесення даних в електронну систему особи без декларації.
? Які ускладнення можуть розвинутися внаслідок вакцинації проти COVID‑19?
– По-перше, саме формулювання «ускладнення» є не зовсім коректним – правильно застосовувати термін «вакцинальні реакції». До можливих вакцинальних реакцій після щеплення проти COVID‑19 належать біль і почервоніння в місці ін’єкції, загальне нездужання і підвищення температури.
? Назвіть головні цілі масової вакцинації проти COVID‑19.
– Загалом можна виділити три головні цілі. Це зменшення:
- тяжкості перебігу і летальності в разі захворювання на COVID‑19;
- потреби в госпіталізації та, як наслідок, навантаження на медичну систему;
- ризику передачі COVID‑19 від людини до людини.
Лікар-педіатр, старший ординатор дитячого відділення лікарні м. Треллеборг, член Європейської асоціації з дитячих інфекційних хвороб (ESPID), кандидат медичних наук Інна Германенко (Швеція) поділилася зі слухачами досвідом лікування COVID‑19 у Швеції.
 Свій виступ спікер почала з еволюції уявлень щодо COVID‑19 у Швеції. Перші повідомлення про COVID‑19 з’явилися ще 16 січня 2020 року, і хоча на той момент вважалося, що ризик поширення інфекції є доволі низьким, уже тоді медична спільнота почала обговорювати питання своєчасної діагностики випадків COVID‑19. 31 січня 2020 року у Швеції був діагностований перший випадок COVID‑19, у зв’язку із чим розпочалося активне обговорення та оцінка ризику інфекції для суспільства, а також наявних засобів захисту. Через місяць був діагностований другий випадок захворювання на COVID‑19, тож був визначений високий ризик завезення інфекції з інших країн і відбулася переоцінка ризику як середнього. 11 березня 2020 року трапився перший летальний наслідок від COVID‑19 у пацієнта похилого віку, який перебував у будинку літніх людей. Наприкінці лютого 2020 року відбулася прес-конференція щодо зростання кількості випадків COVID‑19, пов’язаних із поверненням з Італії, Німеччини та Ірану подорожуючих. 2 березня 2020 року збирається нарада за участю прем’єр-міністра стосовно забезпечення роботи в умовах кризи; вирішується обмежити польоти в Іран, 6 березня – в Італію. 10 березня оприлюднюють рекомендації щодо зменшення відвідування будинків літніх людей. 11 березня ВООЗ оголошує пандемію COVID‑19. 13 березня урядом Швеції оголошено принцип «Якщо хворий – залишайся вдома», введено обмеження – до 500 осіб у місцях скупчення людей, наголошено на важливості дотримання дистанції і можливості переходу на дистанційну форму роботи. Уже в квітні МОЗ Швеції оголошує про важливість утримання від аерозольгенерувальних процедур і визначення терміну «суперпоширювач інфекції», а на початку червня виходить наказ щодо організації роботи в закладах охорони здоров’я в умовах ризику утворення аерозолів.
Свій виступ спікер почала з еволюції уявлень щодо COVID‑19 у Швеції. Перші повідомлення про COVID‑19 з’явилися ще 16 січня 2020 року, і хоча на той момент вважалося, що ризик поширення інфекції є доволі низьким, уже тоді медична спільнота почала обговорювати питання своєчасної діагностики випадків COVID‑19. 31 січня 2020 року у Швеції був діагностований перший випадок COVID‑19, у зв’язку із чим розпочалося активне обговорення та оцінка ризику інфекції для суспільства, а також наявних засобів захисту. Через місяць був діагностований другий випадок захворювання на COVID‑19, тож був визначений високий ризик завезення інфекції з інших країн і відбулася переоцінка ризику як середнього. 11 березня 2020 року трапився перший летальний наслідок від COVID‑19 у пацієнта похилого віку, який перебував у будинку літніх людей. Наприкінці лютого 2020 року відбулася прес-конференція щодо зростання кількості випадків COVID‑19, пов’язаних із поверненням з Італії, Німеччини та Ірану подорожуючих. 2 березня 2020 року збирається нарада за участю прем’єр-міністра стосовно забезпечення роботи в умовах кризи; вирішується обмежити польоти в Іран, 6 березня – в Італію. 10 березня оприлюднюють рекомендації щодо зменшення відвідування будинків літніх людей. 11 березня ВООЗ оголошує пандемію COVID‑19. 13 березня урядом Швеції оголошено принцип «Якщо хворий – залишайся вдома», введено обмеження – до 500 осіб у місцях скупчення людей, наголошено на важливості дотримання дистанції і можливості переходу на дистанційну форму роботи. Уже в квітні МОЗ Швеції оголошує про важливість утримання від аерозольгенерувальних процедур і визначення терміну «суперпоширювач інфекції», а на початку червня виходить наказ щодо організації роботи в закладах охорони здоров’я в умовах ризику утворення аерозолів.
Стосовно дітей і молоді були прийняті такі рішення:
1 березня – обговорюється необхідність карантину для дітей, проте через відсутність науково доведених даних щодо користі карантину рішення не було схвалено. При цьому директори шкіл можуть, з огляду на епідситуацію, приймати відповідне рішення самостійно.
13 березня – вводять тимчасові правила про закриття шкіл.
17 березня – школи й гімназії, коледжі й університети, де навчаються підлітки віком від 17 років, переводять на дистанційне навчання.
19 березня – парламент дозволяє уряду закривати школи.
Початок пандемії COVID‑19 у Швеції насамперед позначився на старшому поколінні жителів (передусім тих, хто проживав у будинках літніх людей або зі своїми дітьми або внуками). Масками і захисними екранами у Швеції активно почали користуватися лише у квітні-травні 2020 року.
З 11 березня по 17 квітня 2020 року кількість смертей від COVID‑19 зросла з 1 випадку до 112 випадків на добу.
Уже в березні цього ж року смертність осіб старше 65 років у групі іммігрантів була на 220% вище, ніж смертність упродовж 2016-2019 рр., і лише на 19% – у групі скандинавів.
На початку травня 2020 року розпочалася сумісна робота Товариства лікарів-інфекціоністів, гігієністів і клінічних мікробіологів щодо створення Національної програми проти COVID‑19, яку було опубліковано у червні 2020 року.
Далі Інна Германенко проінформувала слухачів, як проходить сьогодні процес вакцинації у Швеції. Тут застосовують 3 вакцини проти COVID‑19: дві м-РНК вакцини та одну векторну. Станом на 10 березня 2021 року 1 дозу вакцини отримали 690 тис (8,4%) населення, 2 дози – 320 тис (3,9%). Першими вакцинували осіб літнього віку, потім – медичних працівників. Основна проблема, пов’язана з щепленням, – обмежена кількість вакцин.
Вакцинація у Швеції сприяла суттєвому зниженню захворюваності на COVID‑19.
Як наголосила спікер, переважна більшість населення позитивно налаштована щодо вакцинації проти COVID‑19.
Досвідом лікування і вакцинопрофілактики COVID-19 в Ізраїлі поділився лікар-анестезіолог, реаніматолог медичного центру Рамат-Авів і Ланіадо Борис Бриль (Ізраїль).
 Протоколи лікуваня в Ізраїлі, зазначив Борис Бриль, змінювалися лише декілька разів: першою зміною стало виключення гідроксихлорохіну і хлорохіну з менеджменту лікування COVID‑19, наступні зміни були пов’язані із застосуванням кортикостероїдних препаратів і антикоагулянтної терапії (АКТ) в госпіталізованих пацієнтів. Водночас хворих із легкими формами COVID‑19 в Ізраїлі не лікують, застосовують тільки симптоматичну терапію. Варто зазначити, що ізраїльські лікарі практично не використовують комп’ютерну томографію органів грудної клітки (КТ ОГК) для діагностики COVID‑19.
Протоколи лікуваня в Ізраїлі, зазначив Борис Бриль, змінювалися лише декілька разів: першою зміною стало виключення гідроксихлорохіну і хлорохіну з менеджменту лікування COVID‑19, наступні зміни були пов’язані із застосуванням кортикостероїдних препаратів і антикоагулянтної терапії (АКТ) в госпіталізованих пацієнтів. Водночас хворих із легкими формами COVID‑19 в Ізраїлі не лікують, застосовують тільки симптоматичну терапію. Варто зазначити, що ізраїльські лікарі практично не використовують комп’ютерну томографію органів грудної клітки (КТ ОГК) для діагностики COVID‑19.
Завдяки вакцинації (на момент доповіді в країні було вакциновано 85% населення старше 65 років) в Ізраїлі спостерігається різкий спад захворюваності на COVID‑19. Більшість населення щеплюють вакциною Pfizer, 5% – Moderna. Щодо ускладнень, то зафіксовано 260 скарг від вакцинованих на почервоніння і помірну болючість у місці ін’єкції, 227 – на підвищення температури і легкий озноб, 234 скарги – на біль у м’язах, 203 – на головний біль, 144 – на загальну слабкість, 82 – на біль у суглобах, 37 скарг – на відчуття мурашок по тілу, 32 скарги – на нудоту, 23 – на висип, 22 – на запаморочення, 19 скарг – на незначний набряк обличчя, 9 – на біль у грудях, 8 – на болі в животі, 7 – на синкопе, 6 – на діарею, 4 скарги – на тимчасовий параліч лицевого нерва, 3 – на підвищення артеріального тиску. 17 вакцинованих відразу після процедури потребували госпіталізації, упродовж 48 год після того були виписані. Спікер наголосив, що згадані скарги є типовими для будь-якої вакцини і спостерігаються в приблизно такій самій кількості, що й при інших щепленнях.
На сьогодні в Ізраїлі впроваджені так звані зелені паспорти вакцинації, де вказані особисті дані і кількість доз вакцини з позначенням номерів партії препаратів.
Завдяки успішній вакцинації Ізраїль повністю вийшов із карантину – відкриті всі заклади громадського харчування, музеї, проводяться розважальні заходи тощо. Здійснюється також вакцинація дітей віком від 16 років і вагітних в усіх трьох триместрах вагітності.
Лікування пацієнтів із COVID‑19 в Ізраїлі здійснюють за протоколами, подібними до рекомендацій CDC – Центрів із контролю і профілактики захворювань (Centers for Disease Control and Prevention – CDC), і залежить воно від ступеня тяжкості захворювання. До госпіталізованих пацієнтів застосовують АКТ, у разі тяжкого перебігу захворювання – глюкокортикоїди. Антибактеріальну терапію призначають лише за умови підтвердженої бактеріальної інфекції.
В Ізраїлі дуже суворе ставлення до пропаганди антивакцинального руху. Спікер навів такий приклад: лікаря, який публічно висловлював антивакцинальні ідеї, було покликано на засідання етичної комісії. Лікарю було дано 2 міс на збір наукових даних, за допомогою яких він зміг би довести свою позицію. Оскільки лікареві не вдалося знайти будь-яких клінічних досліджень, на чиї результати він зміг би спиратися в обстоюванні своїх суджень, його ліцензію на медичну практику було скасовано назавжди.
«Вакцинація від COVID‑19: коло проблем, нагальні рішення» – такою була тема виступу доцента кафедри дитячих інфекційних хвороб і дитячої імунології Національного університету охорони здоров’я ім. П.Л. Шупика (м. Київ), кандидата медичних наук Федіра Лапія (Україна).
 Спочатку Ф. Лапій нагадав слухачам будову SARS-CoV‑2, оскільки знання структурних елементів вірусу є важливим для розуміння принципу дії вакцин проти COVID‑19. Як відомо, SARS-CoV‑2 – це РНК-вмісний вірус, оточений оболонкою. Оболонка, своєю чергою, містить шипи глікопротеїну S (шипоподібний антиген), М-протеїн, димери гемаглютинін-естерази, білок N та Е-протеїн.
Спочатку Ф. Лапій нагадав слухачам будову SARS-CoV‑2, оскільки знання структурних елементів вірусу є важливим для розуміння принципу дії вакцин проти COVID‑19. Як відомо, SARS-CoV‑2 – це РНК-вмісний вірус, оточений оболонкою. Оболонка, своєю чергою, містить шипи глікопротеїну S (шипоподібний антиген), М-протеїн, димери гемаглютинін-естерази, білок N та Е-протеїн.
Саме завдяки шипам S-протеїну, що роблять форму вірусу схожою на корону, він і отримав свою назву. Значення S-протеїну в реплікації вірусу полягає в забезпеченні його прикріплення до клітини з подальшим до неї проникненням. Основна імунна відповідь на вакцинацію спрямована на розпізнавання S-протеїну SARS-CoV‑2.
Станом на 1 березня 2021 року у світі на різних стадіях клінічних досліджень перебувала 81 вакцина проти COVID‑19, а якщо враховувати також доклінічні дослідження, то загальна кількість вакцин налічує 308 варіантів. Усі вакцини проти COVID‑19 можна розділити на 4 основні типи:
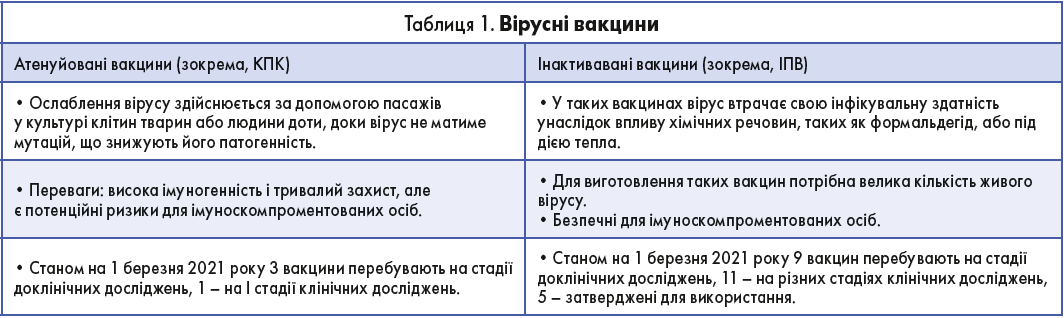
- Вірусні вакцини (інактивовані, атенуйовані).
- Векторні вакцини (на основі вірусного вектора, що реплікується, і вірусного вектора, що не реплікується).
- Білкові вакцини (білкові субодиниці та вірусоподібні частинки.
- Вакцини на основі нуклеїнових кислот (НК) – ДНК і РНК.
Усі вакцини можна об’єднати за деякими спільними характеристиками. Зокрема, вірусні і білкові виготовлені за класичною технологією (на відміну від новітніх вакцин на основі НК і векторних вакцин).
На початок березня 2021 року до використання затверджено 12 вакцин проти COVID‑19, зокрема 2 РНК-вакцини, 4 векторні (вірусний вектор, що не реплікується) вакцини, 5 інактивованих і 1 субодинична протеїнова вакцин. Спікер навів порівняльну характеристику кожного типу вакцин.
Прикладом векторної вакцини є University of Oxford / AstraZeneca (комерційні назви – Covishield, ChAdOx1 nCoV‑19; далі – AstraZeneca) – вакцина на основі не здатного до реплікації (делеція генів Е 1 і Е 3) аденовірусу шимпанзе, що експресує спайк-білок (шипоподібний антиген) SARS-CoV‑2. Мавпячий аденовірус дає можливість уникнути проблем, пов’язаних із наявним у людей імунітетом до аденовірусу, та не є вірулентним для організму людини. В основі технології вироблення вакцини лежить вмонтування гена, що кодує шипоподібний антиген SARS-CoV‑2, у геном непатогенного для людини аденовірусу шимпанзе. Модифікований аденовірус проникає всередину клітини, після чого антиген COVID‑19 починає експресуватися на її поверхні, індукуючи імунну відповідь. Між іншим місцеві запальні реакції на вакцинацію AstraZeneca пов’язані саме зі знищенням клітин, що представляють імунній системі антиген SARS-CoV‑2. Вакцина AstraZeneca здатна індукувати потужну імунну відповідь з боку Т- і В-клітин після введення однієї дози.
Представником векторної вакцини також є Sputnik V. Її відмінність полягає в застосуванні не зміненого аденовірусу шимпанзе, як в AstraZeneca, а аденовірусу людини 26 серотипу (перша доза) та аденовірусу людини 5 серотипу (друга доза).
Найбільш перспективним при вакцинації проти COVID-19, із погляду імуногенності та індукування вироблення вірус-нейтралізувальних антитіл, є спайк-білок SARS-CoV‑2 – шипоподібний антиген, проти цього білка працюють Т-лімфоцити: СД4 і СД8.
Вакцина на основі НК: принцип дії вакцини полягає у вбудовуванні НК в клітини людини, які потім виробляють копії вірусного білка. Більшість із таких вакцин використовують гени, що кодують шипоподібні білки SARS-CoV‑2.
РНК- і ДНК-вакцини безпечні й прості у виробництві: для їх виготовлення потрібен лише генетичний матеріал, а не сам вірус.
Доповідач наголосив, що і мРНК-вакцини (Moderna, Pfizer), і векторні вакцини (AstraZeneca) індукують вироблення одного антигена – спайк-протеїну SARS-CoV‑2, – тож в обох випадках імунна відповідь направлена на білок, що відповідає за приєднання вірусу до клітини людини.
За звичайних умов вироблення і дослідження вакцин – процес тривалий. Найдовшою є ІІІ фаза клінічних досліджень – зазвичай це приблизно 3-5 років. В умовах пандемії COVID‑19, з огляду на високу летальність захворювання, таке довге очікування неприпустиме. Саме тому було вирішено схвалити застосування вакцин у разі отримання задовільних проміжних результатів випробувань безпеки та ефективності препаратів. Загалом клінічні дослідження спрямовані на перевірку таких показників вакцини:
- Імуногенність (визначається в ІІ фазі клінічних досліджень) – здатність утворювати гуморальний і/або клітинно-опосередкований імунітет. Цей показник, за даними клінічних досліджень, має перевищувати 90% (крім вакцин для профілактики грипу). Для комбінованих вакцин кожен із компонентів має відповідати цьому показнику. Термін «імуногенність» не еквівалентний терміну «ефективність». Імуногенність – це відсоток осіб, в яких була зареєстрована відповідь на антиген. Для дослідження цієї характеристики у випробування вакцини Moderna було залучено 600 осіб, AstraZeneca – 1346, Pfizer – 576, Sputnik V – 76.
- Ефективність (визначається в ІІІ фазі клінічних досліджень) – варто відрізняти поняття Efficacy та Effectiveness:
– Efficacy визначається як відсоткове зменшення частоти випадків хвороби в групі вакцинованих проти групи невакцинованих осіб за оптимальних (ідеальних) умов;
– Effectiveness визначається як зниження кількості випадків захворювання на інфекційну хворобу після вакцинації проти кількості випадків захворювання до вакцинації; демонструє ефективність в умовах, наближених до реальних.
Ефективність вакцини визначає прямий і непрямий захист (тобто захист невакцинованих осіб завдяки вакцинованим) і залежить від рівня охоплення щепленнями, кореляції вакцинального штаму і штаму, що циркулює, дотримання умов «холодового ланцюга» та ін.
Спікер зазначив, що жодна із застосовуваних 12 вакцин станом на 1 березня 2021 року не закінчила ІІІ фази клінічних досліджень – усі вакцини продовжують вивчати. Ранні результати клінічних досліджень продемонстрували Efficacy для AstraZeneca на рівні 70,4%.
Також дослідження демонструють, що дотримання тривалішого інтервалу між дозами пов’язане з підвищенням імуногенності вакцини і зростанням рівня нейтралізувальних антитіл.
6 березня 2021 року в журналі The Lancet були опубліковані нові наукові дані щодо вакцинації проти COVID‑19. На сьогодні Велика Британія застосовує політику максимального охоплення першою дозою та відтермінування другої дози вакцини AstraZeneca до 12 тиж після введення першої дози. Згідно з опублікованими у The Lancet даними, ефективність після першої дози становить приблизно 76%, при цьому антитіла зберігаються з 22-го до 90-го дня з мінімальним зниженням. Ефективність є значно вищою після двох доз – вона становить 81,3%, якщо другу дозу введено через 12 тиж після першої дози або пізніше. Для порівняння: ефективність вакцини в разі введення доз з інтервалом менше 6 тиж становить лише 55,1%.
Рекомендації щодо вакцинації НТГЕІ у Німеччині від 4 березня 2021 року також стверджують, що інтервал між двома щепленнями має становити за можливості 12 тижнів. При цьому для завершення вакцинації необхідно введення двох доз вакцини AstraZeneca.
Маємо також сказати, що в населення є певні сумніви щодо ефективності вакцини AstraZeneca в осіб із супутніми захворюваннями. Федір Лапій представив увазі слухачів дані, згідно з якими частка таких осіб серед учасників клінічних дослідженнь безпеки й ефективності AstraZeneca, становила 36%. Зокрема, у дослідженні брали участь пацієнти з такими супутніми патологіями, як ожиріння (19,6% учасників), серцево-судинні захворювання (13,5%) – здебільшого артеріальна гіпертензія (9,9%), захворювання органів дихання (10,2%) – здебільшого астма (6,2%) і цукровий діабет (3,3%). Отже, ефективність і безпечність застосування AstraZeneca добре вивчені в осіб із коморбідними захворюваннями.
Окремі питання щодо вакцинації AstraZeneca – рекомендації стратегічної консультативної групи SAGE (Scientific Advisory Group for Emergencies):
- Особи віком ≥65 років – вакцинацію рекомендовано. Дані про безпеку й імуногенність у цій віковій популяції дають підстави припустити, що вакцина є ефективною, хоча до клінічних випробувань було залучено відносно невелику кількість учасників зазначеного віку. У дуже немічних осіб похилого віку, чия прогнозована тривалість життя становить менше 3 міс, потрібна індивідуальна оцінка ризику і користі від вакцинації (дата рекомендацій – 10 лютого 2021 року);
- Особи віком <18 років – вакцинацію не рекомендовано.
- Пацієнти з гострим COVID‑19 – вакцинація рекомендована тільки після повного одужання від гострої інфекції та за умови дотримання критеріїв припинення ізоляції. Хворим з інфекцією, підтвердженою за допомогою ПЛР-тесту, пропонується відкласти вакцинацію на 6 місяців.
Нещодавно опубліковані дані J. Bernal та співавт. про використання вакцини AstraZeneca в осіб віком від 65 років продемонстрували ранню «Effectiveness» вакцини щодо запобігання госпіталізації і зменшення ризику смерті від COVID‑19. Вибірка учасників дослідження становила понад 7,5 млн осіб. Через 4 тиж після першої дози захист від симптоматичного COVID‑19 становив 60-73%. Ефективність вакцини спостерігали вже через 14-20 днів після щеплення, вона досягала 60% на 28-34-й день і 73% – із 35-го дня. Також зазначалася 37% ефективність щодо зниження ризику екстреної госпіталізації.
Рекомендації Національної технічної групи експертів із питань імунопрофілактики для тих, хто перехворів на COVID‑19:
- Рекомендувати вакцинацію особам із задокументованим COVID‑19 в анамнезі з відтермінуванням вакцинації на 6 міс від часу інфекції.
- За бажанням особи, яка підлягає вакцинації відповідно до групи пріоритетності, вакцинація може бути проведена раніше 6-місячного терміну при достатній кількості доз.
Необхідно наголосити, що вакцинація тих, хто перехворів на COVID‑19, є безпечною. Згідно з даними клінічних досліджень, не було виявлено жодних додаткових побічних ефектів у 345 осіб, яким було зроблено щеплення AstraZeneca після того, як вони перехворіли на COVID‑19. Також вакцинація в інкубаційний період або вакцинація вже інфікованої COVID‑19 особи не підвищує ризик виникнення побічних реакцій і не впливає на тяжкість перебігу COVID‑19.
Стосовно необхідності проведення серологічного тестування при вакцинації, доповідач зазначив, що воно не рекомендоване як перед, так і після щеплення вакциною проти COVID‑19. На сьогодні не визначений рівень антитіл, що гарантує захист проти COVID‑19.
Ще одним важливим моментом є те, що наявність сезонної і побутової алергії не є протипоказанням до вакцинації проти COVID‑19. Такі пацієнти можуть бути вакциновані в період загострення захворювання. Протипоказанням до вакцинації є тяжка алергія до одного з компонентів вакцини або у відповідь на попередню дозу.
Як показують результати опублікованого в авторитетному журналі The Lancet препринту, ефективність ChAdOx1 nCoV‑19 проти британського варіанту SARS-CoV‑2 подібна до такої вакцин проти інших штамів. Крім того, вакцинація ChAdOx1 nCoV‑19 сприяє скороченню тривалості і зменшенню вірусного навантаження, що може мати значний вплив на зменшення поширення інфекції.
Дуже актуальній темі застосування антикоагулянтів у менеджменті COVID‑19 присвятив свій виступ ректор НМУ ім. О.О. Богомольця, професор кафедри хірургії, анестезіології та інтенсивної терапії ІПО НМУ ім. О.О. Богомольця, доктор медичних наук, професор Юрій Кучин (Україна).  Застосування АКТ у 2009 р. – під час пандемії грипу – було суворо заборонене. Такі самі рекомендації стосувалися менеджменту COVID‑19 у перші місяці пандемії COVID‑19. Одне з перших досліджень впливу антикоагулянтів на летальність у разі COVID‑19 було проведено в Іспанії (Ayerbe L. et al., 2020). У дослідженні взяли участь 2075 пацієнтів. Згідно з його результатами застосування гепарину асоціювалося зі зниженням летальності при COVID‑19 із поправкою на вік і стать.
Застосування АКТ у 2009 р. – під час пандемії грипу – було суворо заборонене. Такі самі рекомендації стосувалися менеджменту COVID‑19 у перші місяці пандемії COVID‑19. Одне з перших досліджень впливу антикоагулянтів на летальність у разі COVID‑19 було проведено в Іспанії (Ayerbe L. et al., 2020). У дослідженні взяли участь 2075 пацієнтів. Згідно з його результатами застосування гепарину асоціювалося зі зниженням летальності при COVID‑19 із поправкою на вік і стать.
З погляду патофізіології, препарати гепарину не лише впливають на коагуляцію, але й мають протизапальний (особливо на ендотелій судин) і, імовірно, навіть певний противірусний ефект (блокування проникнення вірусів у клітини). 2020 року були опубліковані результати метааналізу досліджень впливу гепарину на перебіг COVID‑19 (Joseph A. et al.), згідно з якими:
- є обмежена кількість фармакологічних методів лікування COVID‑19;
- гепарин може бути корисним для лікування коагулопатії в разі COVID‑19;
- використання терапевтичної антикоагуляції при COVID‑19 систематично не оцінювалось;
- треба враховувати баланс між перевагами і ризиками АКТ;
- необхідні рандомізовані клінічні випробування ефективності гепарину в лікуванні COVID‑19.
Далі професор Ю. Кучин дав порівняльні характеристики двох інструкцій до застосування нефракціонованого і низькомолекулярного гепарину(НФГ і НМГ). Показаннями до застосування НФГ є профілактика й лікування тромбоемболічних захворювань і їх ускладнень, запобігання післяопераційним тромбозам і емболіям, а також зсіданню крові під час лабораторних досліджень, діалізу та ін. Водночас, згідно з інструкцією до застосування, показаннями до використання НМГ є:
- профілактика венозних тромбоемболічних ускладнень у хірургічних пацієнтів із помірним і високим ризиком;
- профілактика венозних тромбоемболічних ускладнень у терапевтичних пацієнтів із гострими захворюваннями;
- лікування тромбозу глибоких вен;
- запобігання утворенню тромбів під час гемодіалізу;
- гострий коронарний синдром;
- лікування нестабільної стенокардії та інфаркту міокарда (ІМ).
Спікер зазначив, що в жодній з інструкцій як показання не вказана пневмонія або вірусна інфекція. Тому призначення АКТ пацієнтам із COVID‑19 має здійснюватися за конкретними показаннями (наприклад, високий ризик тромбоемболічних ускладнень).
Відповідно до останніх рекомендацій ESC (2019) щодо діагностики і менеджменту легеневої емболії, НМГ мають переваги перед НФГ, крім наявності в пацієнтів тромболізису або ниркової дисфункції. Украй небезпечними ускладненнями системного тромболізису є великі (майже 10%) та інтракраніальні (майже 2%) кровотечі.
Рекомендації останнього затвердженого протоколу «Надання медичної допомоги для лікування коронавірусної хвороби (COVID‑19)» стосовно проведення АКТ:
- НМГ є препаратами вибору для тромбопрофілактики в пацієнтів із факторами високого ризику розвитку венозних тромботичних ускладнень;
- у пацієнтів із вираженою дисфункцією нирок НФГ можна розглядати на основі ретельної оцінки співвідношення ризику/користі;
- у пацієнтів із гепарин-індукованою тромбоцитопенією в анамнезі фондапаринукс має розглядатися як альтернативне лікування.
Спікер наголосив, що ані позитивний результат ПЛР на COVID‑19, ані наявність пневмонії самі по собі не є показаннями до АКТ. Її призначають лише пацієнтам із високим ризиком розвитку венозної тромбоемболії (ВТЕ).
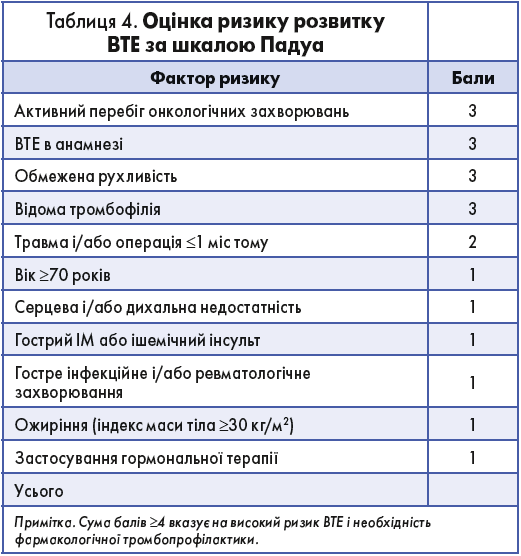
Оцінка такого ризику має проводитися за шкалою Падуа (табл. 4).
Пацієнти з COVID‑19, які до захворювання отримували АКТ, мають її продовжувати. При цьому необхідно розглянути доцільність переходу на НМГ. За підозри на ВТЕ в умовах стаціонару необхідне введення антикоагулянтного препарату в дозі 4000 МО одноразово. Якщо стан пацієнта критичний і потребує лікування в умовах відділення інтенсивної терапії, доза антикоагулянту визначається з урахуванням кліренсу креатиніну (КК): якщо КК<30 мл/хв/1,7 м2 – 4000 МО 1 р./добу, якщо КК >30 мл/хв/1,7 м2 – 4000 МО 2 р./добу. У разі підтвердженої ВТЕ треба розпочати АКТ в лікувальних дозах. Після виписки зі стаціонару необхідно розглянути питання щодо проведення тривалої або стандартної тромбопрофілактики за допомогою НМГ (4000 МО/добу впродовж 4-6 тиж і 4000 МО/добу впродовж 2 тиж відповідно).
Згідно з нещодавно опублікованими результатами дослідження D. Barnes та співавт.:
- Багато хворих на COVID‑19 мають підвищені ризики ВТЕ, тому госпіталізованим пацієнтам показана фармакологічна тромбопрофілактика.
- Рекомендується дотримуватися доказових принципів тромбопрофілактики максимально можливим чином.
- Рекомендується продовжувати тромбопрофілактику після виписки в пацієнтів із високим ризиком тромбозів.
- Рекомендується призначити повний 3-місячний курс тромбопрофілактики терапевтичними дозами антикоагулянтів пацієнтам із COVID‑19, які перенесли епізод ВТЕ під час госпіталізації.
Щодо моніторингу рівня D-димеру в менеджменті COVID‑19:
- НЕ рекомендується щоденне рутинне визначення рівня D-димеру для оцінки або корекції АКТ. D-димер має застосовуватися лише як маркер тяжкості стану й прогнозу.
- НЕ рекомендується збільшувати дозу антикоагулянтів на основі оцінки одного лише D-димеру. Однак у разі одночасного клінічного погіршення це може бути причиною інтенсифікації терапії, наприклад при переході з одноразового введення 4000 МО/добу на дворазове введення препарату.
- Рекомендується постійний моніторинг нових даних стосовно біомаркерів для лікарів і лабораторій.
- НЕ рекомендується застосовувати тромболітичні препарати в пацієнтів із COVID‑19, окрім як у рамках клінічних досліджень, якщо немає інших клінічних показань до цього: ІМ з елевацією ST, гострого порушення мозкового кровообігу за ішемічним типом або масивної тромбоемболії легеневої артерії з гемодинамічними порушеннями.
На ключових помилках у менеджменті COVID‑19 і правильному алгоритмі лікування пацієнтів із коронавірусною інфекцією зосередив свою увагу професор кафедри анестезіології та інтенсивної терапії НМУ ім. О.О. Богомольця, президент Асоціації анестезіологів України, доктор медичних наук, професор Сергій Дубров.
 Передусім професор С. Дубров зазначив, що в лікуванні хворих на COVID‑19 вітчизняні лікарі мають послуговуватися двома основними джерелами – Стандартом медичної допомоги «Коронавірусна хвороба (COVID‑19)», затвердженим наказом МОЗ України від 07.01.2021 № 10 і Протоколом «Надання медичної допомоги для лікування коронавірусної інфекції (COVID‑19)», затвердженим наказом МОЗ України від 31.12.2020 № 3094. Згадані нормативно-правові акти є обов’язковими до використання всіма лікувальними закладами.
Передусім професор С. Дубров зазначив, що в лікуванні хворих на COVID‑19 вітчизняні лікарі мають послуговуватися двома основними джерелами – Стандартом медичної допомоги «Коронавірусна хвороба (COVID‑19)», затвердженим наказом МОЗ України від 07.01.2021 № 10 і Протоколом «Надання медичної допомоги для лікування коронавірусної інфекції (COVID‑19)», затвердженим наказом МОЗ України від 31.12.2020 № 3094. Згадані нормативно-правові акти є обов’язковими до використання всіма лікувальними закладами.
Далі спікер розповів про найпоширеніші помилки в терапії COVID‑19, які трапляються на амбулаторному етапі надання медичної допомоги.
Більшість із таких помилок пов’язана з госпіталізацією пацієнтів із COVID‑19.
Показаннями до госпіталізації є:
- приналежність хворого до групи ризику: тяжкий перебіг артеріальної гіпертензії, декомпенсований цукровий діабет, імуносупресивні стани, тяжка хронічна патологія дихальної та серцево-судинної систем, ниркова недостатність, аутоімунні захворювання;
- наявність гострого респіраторного дистрес-синдрому (ГРДС), сепсиcу і/або септичного шоку, синдрому поліорганної недостатності;
- середньотяжкий або тяжкий стан пацієнта при збільшенні частоти дихальних рухів вище фізіологічної норми, кровохарканні або сатурації ≤92%.
Рішення щодо необхідності госпіталізації пацієнта з COVID‑19 у більшості випадків приймає лікар первинної ланки. Інформативною і простою у використанні є шкала CURB‑65, яка охоплює оцінку 5 параметрів (кожен оцінюється в 1 бал):
- сплутаність свідомості;
- рівень сечовини >7 ммоль/л;
- частота дихання >30/хв;
- артеріальний тиск (систолічний АТ <90 мм рт. ст., діастолічний АТ ≤60 мм рт. ст.);
- вік >65 років.
Інтерпретація шкали CURB‑65:
- 0-1 бал (низький ризик смерті) – можна проводити лікування в домашніх умовах, проте завжди необхідно враховувати соціальні обставини і бажання пацієнта;
- 2 бали (помірний ризик смерті) – необхідно розглянути можливість короткочасної госпіталізації або амбулаторного лікування під ретельним спостереженням;
- ≥3 бали – високий ризик смерті;
- 4-5 балів – показана госпіталізація у відділення інтенсивної терапії.
Спікер зазначив, що картина КТ ОГП жодним чином не має впливати на тактику лікування пацієнтів із COVID‑19. Так само інформативним, проте безпечнішим методом оцінки стану легеневої тканини у хворих на COVID‑19 у динаміці є УЗД легень.
Частою помилкою є необґрунтоване призначення дексаметазону й антибактеріальних препаратів (АБП) сімейними лікарями. Згідно з протоколом надання медичної допомоги пацієнтам із COVID‑19 протимікробні засоби показані і мають бути призначені виключно за наявності лабораторно підтвердженої супутньої бактеріальної інфекції або обґрунтованої підозри на неї. Неаргументоване призначення АБП пацієнтам із COVID‑19 є грубим порушенням протоколу. Пацієнти з легким і середньотяжким перебігом COVID‑19, які перебувають на амбулаторному лікуванні, потребують повноцінного харчування, адекватної регідратації і симптоматичного лікування із застосуванням жарознижувальних засобів (парацетамолу, ібупрофену тощо) у разі фебрильної температури (≥38,5 °C). У протоколі також зазначено, що пацієнтам із легким і середньотяжким перебігом COVID‑19, які не потребують кисневої підтримки, не варто призначати кортикостероїди. Застосування системних глюкокортикостероїдів доцільне лише у хворих на COVID‑19, які потребують кисневої підтримки.
Щодо найчастіших помилок в умовах стаціонару, то й тут вони стосуються необґрунтованого призначення АБП. Згідно з даними дослідження Мічиганського університету (м. Енн-Арбор, США), яке було присвячено аналізу якості надання медичної допомоги в 38 госпіталях, понад 50% пацієнтів із підозрою на COVID‑19 отримували АБП. При цьому в 96,5% із них виділили лише SARS-CoV‑2 (на який, як відомо, антибіотик не діє), тобто лише 3,5% пацієнтів мали бактеріальну інфекцію.
Показанням до застосування АБП у разі COVID‑19 є наявність чітких доказів приєднання бактеріальної інфекції.
Іще однією проблемою є помилки в призначенні і проведенні тромбопрофілактики в госпіталізованих пацієнтів із COVID‑19. Згідно з наказом МОЗ України № 2116 рекомендується призначати профілактичну АКТ за допомогою НМГ пацієнтам без попередніх показань до АКТ або з ризиком розвитку ВТЕ за шкалою Падуа. ≥4 бали вказують на високий ризик ВТЕ і необхідність призначення медикаментозної профілактики.
Протипоказаннями до її проведення є:
- кількість тромбоцитів <50×109/л;
- травма з високим ризиком кровотечі;
- активна кровотеча;
- гепарин-індукована тромбоцитопенія;
- геморагічний інсульт;
- гострий бактеріальний ендокардит;
- нестабільна артеріальна гіпертензія: систолічний АТ >180 мм рт. ст. або діастолічний АТ >110 мм рт. ст;
- печінкова недостатність.
За наявності протипоказань до медикаментозної профілактики ВТЕ треба застосовувати механічні заходи профілактики (переміжна пневматична компресія нижніх кінцівок).
Однією з основних проблем і помилок є також широке призначення нових пероральних антикоагулянтів пацієнтам із COVID‑19 як сімейними лікарями, так і лікарями стаціонару. Але препарати групи нових пероральних антикоагулянтів несумісні з глюкокортикостеро їдами. Сучасні рекомендації вказують на необхідність застосування НМГ у менеджменті COVID‑19, а не нових пероральних антикоагулянтів.
Помилкою є й призначення тоцилізумабу, зокрема застосування його в пацієнтів із бактеріальною інфекцією. Тоцилізумаб протипоказаний при підвищенні рівня прокальцитоніну вдвічі, оскільки може призводити до розвитку сепсису, септичного шоку й смерті.
Важливим моментом у комплексі лікування хворих на COVID‑19 є так звана проун-позиція. Згідно з рекомендаціями ВООЗ дотримання прон-позиції в дорослих пацієнтів із COVID‑19 рекомендовано впродовж 12-16 год/добу (зі зміною положення кожні 2-4 год), а також у дітей у разі тяжкого ГРДС. Вагітним рекомендовано декубітальне положення.
Наостанок доповіді Сергій Дубров наголосив, що наявність IgG не має прямої кореляції з імунітетом і не є протипоказанням до вакцинації проти COVID‑19, а ось рутинне серологічне тестування не рекомендоване ні до, ні після щеплення.
Підготувала Анастасія Козловська