7 червня, 2016
Технология моноклональных антител в Украине: история, достижения, перспективы
В ноябре 2015 г. за цикл научных работ «Моноклональные и рекомбинантные антитела для экспериментальной биологии, медицины и ветеринарии» коллектив авторов (Д.Ф. Глузман, С.П. Сидоренко, Л.М. Скляренко, Л.Н. Шлапацкая) удостоен Государственной премии Украины в области науки и техники. Все исследования, касающиеся применения моноклональных антител (МКАТ) в онкологии, проводились на базе Института экспериментальной патологии, онкологии и радиобиологии им. Р.Е. Кавецкого НАН Украины (ИЭПОР). О научных исследованиях и внедрении их результатов в клиническую практику нам рассказали ученые, имеющие к этой теме самое непосредственное отношение.
 Директор ИЭПОР, академик НАН Украины, доктор медицинских наук, профессор Василий Федорович Чехун:
Директор ИЭПОР, академик НАН Украины, доктор медицинских наук, профессор Василий Федорович Чехун:
– Представленная работа – результат многолетнего труда большой группы ученых. Зачастую Государственные премии присуждаются за отдельный фрагмент большого цикла исследований: например, за фундаментальное обоснование какого-либо процесса или разработку конкретной технологии. Работа наших специалистов представляет собой полный замкнутый цикл, начиная с идеи определения антигенных опухолевых структур, создания и развития гибридомных технологий и заканчивая получением и очисткой МКАТ, способных взаимодействовать с опухолевыми антигенами. Таким образом, эта работа показывает комплексный подход к решению глобальной проблемы: от глубоких фундаментальных исследований, разработки биотехнологии до использования полученных биотехнологических продуктов в диагностических целях.
Усилиями сотрудников ИЭПОР параллельно с Институтом биохимии им. А.В. Палладина НАН Украины удалось создать диагностические панели на основе МКАТ, которые используются для выявления многих патологических процессов и верификации диагноза. Речь идет и об онкологических заболеваниях, и о заболеваниях, связанных с тромбообразованием и нарушением функционирования сердечно-сосудистой системы. Благодаря этой работе на украинский рынок выведен ценный диагностический инструмент. Кроме того, в ходе этой научной работы получен целый ряд новых фундаментальных знаний.
Сегодня ИЭПОР располагает коллекцией гибридом, которые позволяют получать различные моноклональные антитела, всего 123 реагента. Благодаря такому многообразию МКАТ можно создавать разные диагностические панели для мониторинга и выявления широкого спектра патологических процессов. Прежде всего это дифференциальная диагностика онкологических заболеваний; также МКАТ, позволяющие осуществлять мониторинг ВИЧ-инфицированных больных и пациентов с некоторыми другими заболеваниями. Фактически благодаря этой научной работе в Украине сформировалась отдельная отрасль, позволяющая производить моноклональные антитела для применения в медицине.
Мне приятно поздравить с получением Государственной премии всех исследователей, причастных к этой разработке. Они показали всем нам пример того, как применять на практике результаты фундаментальных исследований, которые проводятся в украинских научно-исследовательских институтах. Светлана Павловна Сидоренко и ее научная группа специализировались на идентификации новых антигенных детерминант и гибридомных технологиях, совершенствовании технологии очистки МКАТ. Исследовательская группа под руководством Даниила Фишелевича Глузмана проверяла качество МКАТ, сравнивала их с теми, которые были получены от зарубежных производителей. Я хотел бы акцентировать внимание на том, что для разработок подобного уровня необходимо продолжительное время и серьезное финансирование. Несмотря на неизбежные сложности, нашим ученым удалось получить уникальные продукты, которые соответствуют международным требованиям, предъявляемым к современным диагностическим системам.
После проведения технических, преклинических и клинических испытаний ИЭПОР получено свидетельство о государственной регистрации № 11072/2011 на медицинское изделие «Антитела моноклональные», срок действия которого неограничен. Согласно приказу Государственной службы Украины по лекарственным средствам от 14.12.2012 № 1050 разработка внесена в Государственный регистр медицинской техники и изделий медицинского назначения и разрешена к применению на территории Украины.
Важно, что внедрение нашей разработки в клиническую практику отвечает реалиям сегодняшнего дня. В настоящее время диагностика различных патологических процессов, в первую очередь опухолей, невозможна без методов проточной цитофлуориметрии, иммуноцитохимии и иммуногистохимии, которые предполагают использование МКАТ. Ранее для осуществления этого вида исследований мы закупали МКАТ у импортных производителей. Сегодня мы с гордостью можем вывести на украинский рынок собственные диагностические продукты, которые соответствуют мировым стандартам и способны определять ценовую политику в области диагностики целого ряда патологических состояний. Также мы рассматриваем конкретные возможности расширения сферы применения наших диагностических панелей, ищем партнеров, которые помогут донести эту разработку до клинических лабораторий на всей территории Украины.
 Заведующий отделом иммуноцитохимии и онкогематологии ИЭПОР, доктор медицинских наук, профессор Даниил Фишелевич Глузман:
Заведующий отделом иммуноцитохимии и онкогематологии ИЭПОР, доктор медицинских наук, профессор Даниил Фишелевич Глузман:
– Исследования, отмеченные сегодня Государственной премией Украины, проводятся в нашем институте с 1982 г. В 1983 г. были получены первые МКАТ, предназначенные для выявления антигенов лейкоцитов и лимфоцитов. Они впоследствии сыграли значимую роль в развитии не только украинской, но и мировой онкологии, иммунологии, гематологии и патологической анатомии.
Как все начиналось? Наша лаборатория тогда входила в состав отдела молекулярных механизмов канцеро- и лейкозогенеза. В 1973 г. к нам в отдел пришла студентка Светлана Сидоренко: ее привела академик Зоя Андреевна Бутенко. Позднее Светлана Павловна поступила в аспирантуру в отдел иммунологии, к профессору Юлиану Александровичу Уманскому; после его смерти в 1981 г. часть его сотрудников перешла к нам в отдел.
Тогда мы очень активно занимались исследованиями отличий между Т‑ и B-лимфоцитами, используя розеточные методы, ведь морфологически эти две популяции клеток между собой не отличались. В 1975 г. Георг Келлер и Цезар Мильштейн предложили гибридомную технологию получения МКАТ. В 1993 году в г. Бостоне (США) я встретил Цезара Мильштейна на конгрессе, посвященном МКАТ. С появления гибридомной технологии началась активная работа по определению антигенов лимфоцитов, а также опухолевых антигенов, во всем мире произошел всплеск гибридомной технологии. Первые гибридомы и МКАТ в бывшем Советском Союзе были получены в г. Москве в Онкологическом научном центре АМН, эти исследования проводили научные группы под руководством Гарри Израилевича Абелева и Юлия Марковича Васильева. Обмен опытом с этими учеными позволил ИЭПОР начать исследования в области гибридомных технологий, которыми занялась С.П. Сидоренко с группой сотрудников.
Благодаря полученным с помощью гибридомной технологии МКАТ мы смогли различать популяции Т- и В- лимфоцитов, исследовать свойства различных клеточных линий, чтобы диагностировать лейкозы и другие заболевания крови. В этих исследованиях мы изучали линии взятых у больных лейкозом и лимфомами клеток с целью установить их специфичность, используя МКАТ, полученные путем гибридомной технологии. Можно сказать, научная группа под руководством Светланы Павловны конструировала самолеты, а мы учили их летать.
Исходно мы начинали не с иммуноцитохимических исследований с использованием МКАТ, а с обычной цитохимии ферментов. Это позволило нам быстро наладить и применить для определения связывания антитела с антигеном не только флуоресцентный, но и иммуноферментный цитохимический метод. Мы были пионерами в широком использовании иммуноцитохимических методов как в Украине, так и в бывшем Советском Союзе.
В целом с появлением технологии получения МКАТ связан выход на принципиально новый технологический уровень сначала в исследованиях, потом в диагностике, а потом и в терапии многих заболеваний, в первую очередь онкологических и онкогематологических.
Для уточненной современной диагностики конкретного заболевания нужен набор антител. Например, для диагностики тех или иных форм острых и хронических лейкозов необходим набор от 10 до 20 МКАТ. Существует возможность конструирования около 200 разновидностей диагностических панелей. Особенно широко иммуногистохимические методы применяются в онкологии для диагностики лимфом. Раньше лимфомы считались одним из наиболее сложных разделов в патогистологической диагностике, поскольку их гистология очень сложна. Благодаря МКАТ стали известны стадии развития Т‑ и В-лимфоцитов, и теперь можно с высокой точностью определить тип и цитологический вариант заболевания у отдельных пациентов.
Сегодня МКАТ, которые изготавливают в ИЭПОР, укомплектованы в наборы для дифференциальной диагностики опухолей разного гистогенеза, лейкозов и лимфом, исследования экссудатов из серозных полостей, а также оценки иммунологического статуса человека. Кроме того, использование набора МКАТ при диагностике лейкозов позволяет определить тканевое и органное происхождение опухолевых клеток в тех случаях, когда не удается выявить локализацию первичной опухоли.
Сегодня наш отдел выполняет функции референтной лаборатории, где диагностика опухолей кроветворной и лимфоидной тканей проводится в соответствии с современной классификацией ВОЗ 2008 г. Эта классификация основывается на клинико-генетических данных, использовании морфологических и цитохимических методов исследования клеток периферической крови, пунктатов костного мозга и лимфатических узлов, и, конечно, иммунофенотипировании с использованием МКАТ к линейно-специфическим и дифференцировочным антигенам.
В наш отдел с курьерской почтой доставляют образцы крови, мазки крови и костного мозга практически из всех областей Украины, а при некоторых заболеваниях сами пациенты могут пройти обследование. Много лет мы добивались создания отдельного диагностического центра, ведь ежегодно нами обследуются более трети всех онкогематологических больных страны. Было даже подписано соответствующее распоряжение в Министерстве здравоохранения – но пока дело не сдвинулось с мертвой точки.
 Заведующая отделом молекулярной и клеточной патобиологии ИЭПОР, доктор биологических наук, профессор, член-корреспондент НАН Украины Светлана Павловна Сидоренко:
Заведующая отделом молекулярной и клеточной патобиологии ИЭПОР, доктор биологических наук, профессор, член-корреспондент НАН Украины Светлана Павловна Сидоренко:
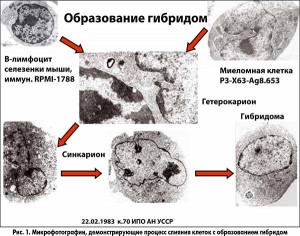
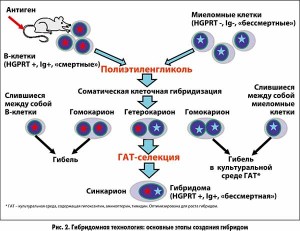
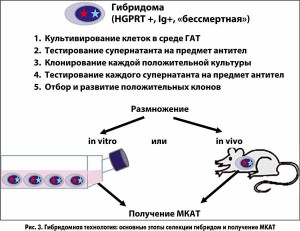
– Получение гибридом производится в несколько этапов. На первом этапе осуществляется иммунизация мыши, у которой впоследствии будут взяты лимфоциты, вырабатывающие антитела заданной специфичности. В самом начале наших исследований мы иммунизировали мышей живыми клетками, что позволило нам открыть новые антигены. В настоящее время в подавляющем большинстве случаев уже известна конкретная белковая молекула, которой, соответственно, иммунизируют мышь. В итоге получаются лимфоциты, синтезирующие антитела заданной специфичности. Далее производится их слияние с миеломными клетками. В отличие от В-лимфоцита, миеломная клетка бессмертна. Когда клетки сливаются, из их ядер образуется синкарион, а впоследствии эта химерная клетка превращается в гибридому – бессмертную клетку, которая в огромных количествах продуцирует антитела определенной специфичности (рис. 1-3). Для отбора и дальнейшего размножения этих клеток используется культивирование в специальной культуральной среде, предназначенной для выращивания гибридом (рис. 3). К сожалению, гибридомы со временем могут терять способность к продукции антител. Для получения больших количеств МКАТ они культивируются или в специальных реакторах, или с использованием лабораторных мышей.
Идея проведения исследований в области изучения МКАТ принадлежит профессору Юлиану Александровичу Уманскому, который заведовал отделом иммунологии в то время, когда я только начинала работать. Именно Ю.А. Уманский поручил мне заняться новым на то время и перспективным направлением: гибридомной технологией получения МКАТ. Он же отправил меня и Елену Петровну Ветрову в Москву на обучение к специалистам, которые уже занимались этими исследованиями. После смерти Ю.А. Уманского в 1981 г. Вадим Григорьевич Пинчук, бывший тогда директором ИЭПОР, поручил мне продолжить всю научную переписку, в том числе со шведскими учеными, профессорами Георгом и Евой Кляйн (George and Eva Klein), у которых Ю.А. Уманский проходил стажировку и с которыми впоследствии активно сотрудничал.
Что сказать о начале исследований? Мне кажется, залог успеха в науке – это идеи и огромное желание работать. Первую гибридизацию мы провели в 1983 г., первая публикация вышла в 1986 г. Все гибридомы, которые мы получали, мы относили к серии ИПО. Осознав, что полученные нами результаты уникальны, мы отправили запросы о сотрудничестве в несколько зарубежных лабораторий. Кто-то не ответил, кто-то отказал, кто-то посоветовал обратиться позднее, поменять тематику. Руководитель американской лаборатории Эдвард Кларк (Edward A. Clark) заявил: «Приезжайте завтра», но вначале устроил мне экзамен по телефону. На тот момент вместе с покойной Еленой Петровной Ветровой мы уже создали 59 гибридом.
В 1991 г., на третий день после провозглашения Украиной независимости, я прилетела в г. Сиэтл (США), чтобы работать по американскому гранту в отделах микробиологии и иммунологии Университета штата Вашингтон. Профессор Э. Кларк тогда всем рассказывал (и, кажется, рассказывает до сих пор), что мы делали гибридомы на проточной воде, используя подручные средства. Действительно, первые гибридомы, которые до сих пор считаются уникальными в мире, мы получили в ИЭПОР в комнате № 70, не имея автоматических пипеток и используя реактивы, которые нам передали коллеги из Швеции. Э. Кларк подключил меня к международным исследованиям, в ходе которых изучались и полученные нами антитела. В результате появилось несколько оригинальных публикаций, в том числе в журналах Naturе Immunology и Immunity. Потом было еще много грантов, совместных публикаций с зарубежными учеными.
В чем состоит наш научный приоритет? Разрабатывая гибридомную технологию, мы впервые в мире идентифицировали несколько антигенов. Целый ряд полученных нами МКАТ были включены в исследования международных рабочих совещаний по изучению антигенов дифференцирования лейкоцитов человека Human Leucocyte Differentiation Antigens (HLDA) Workshops и получили номенклатуру CD150 (МКАТ ИПО‑3), CD95 (МКАТ ИПО‑4), CD37 (МКАТ ИПО‑24). Они были референтными антителами на пятом, шестом, седьмом и девятом HLDA Workshops, которые проходили соответственно в 1993, 1996, 2000 и 2010 годах. Особую гордость у нас вызывает антиген, которому, согласно международной номенклатуре, было присвоено название CD150. Мы изучили структуру, экспрессию и функции CD150, а также CD150‑опосредованных сигнальных каскадов в нормальных и злокачественно трансформированных Т- и В-лимфоцитах. Оказалось, что CD150 – представитель и основатель нового семейства молекул. Молекулы, входящие в это семейство, содержат уникальные сигнальные мотивы ITSM, которые мы же исследовали и которым присвоили название. Эта работа частично проведена в ИЭПОР, частично – в г. Сиэтле по гранту Медицинского института Говарда Хьюза (HHMI). Этот сигнальный мотив уже вошел в учебники по иммунологии.
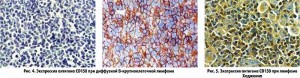
Сегодня CD150 продолжает вызывать пристальный научный интерес. Почему? Как известно, 95% лейкозов и лимфом у взрослых людей имеют B-клеточное происхождение, что связано со сложным процессом дифференцировки этих клеток: он осуществляется в 4 этапа с двунитевым разрывом молекул ДНК. CD150 экспрессирован почти на всех стадиях дифференцировки, включая зрелые В-лимфоциты. В нормальных клетках уровень экспрессии CD150 повышается при их созревании, а клетки лейкозов и лимфом практически не экспрессируют эту молекулу. Так, существуют два варианта хронического лимфолейкоза: с хорошим и плохим прогнозом, причем поверхностная экспрессия CD150 может служить в качестве прогностического маркера при хроническом лимфолейкозе (рис. 4-5).
Кроме того, CD150 является рецептором вируса кори. Около 20 лет назад было показано, что вирус кори использует рецептор CD46 для проникновения в клетку; однако это было показано для лабораторного штамма, который используется для вакцинации. Штамм дикого типа связывается только с CD150 – это открытие было сделано японскими учеными в 2000 г. с помощью полученных нами антител. В свою очередь вирус кори показал цитопатогенный эффект в отношении некоторых опухолевых клеток: существует ряд свидетельств об излечении больных лимфомой Ходжкина после заражения корью или вакцинации вирусом кори. Исследования показали, что это связано с воздействием на рецептор CD150. Таким образом, рецептор кори CD150, который представлен на поверхности клеток целого ряда опухолей, является потенциальной мишенью для онколитической терапии вирусом кори и терапии МКАТ.
В той же гибридизации мы получили гибридомы, продуцирующие антитела, которые распознают CD95. Эти антитела зарубежные коллеги до сих пор называют best killer in the world, потому что они обладают крайне высокой аффинностью и индуцируют апоптоз клеток наиболее эффективным образом.
В настоящее время приоритетными направлениями наших исследований являются анализ рецептор-опосредованных сигнальных каскадов клеток с целью поиска потенциальных мишеней для уточняющей диагностики и терапии злокачественных новообразований, а также выяснение роли в сигнальных каскадах протеинкиназ семейства PKD2, которые регулируют дифференцировку и жизнедеятельность нормальных и злокачественно трансформированных клеток.
В целом, если рассматривать науку как здание, по моему убеждению, существует две категории ученых: те, кто строят это здание по кирпичику, совершая какие-то открытия, и те, кто в лучшем случае делают внешний косметический ремонт. К сожалению, ученых из первой категории не так уж много, и замечательно, что нам удалось внести свой вклад в построение «здания науки».
Подготовила Катерина Котенко