1 квітня, 2016
Новый взгляд на статистический феномен Уилла Роджерса при раке желудка
Под феноменом Уилла Роджерса чаще всего понимают существование так называемых прыгающих или перепрыгивающих этапы регионарных метастазов при раке желудка (РЖ).
Существование феномена «перепрыгивания» при РЖ, доказанное многими исследователями [1, 2], делает биопсию сигнального лимфоузла малоэффективной. Поэтому на первое место при РЖ выходит не определение сигнального лимфоузла для данного этапа регионарного метастазирования, а выполнение профилактической биопсии максимального количества близлежащих лимфоузлов – профилактическая лимфатическая диссекция.
Закономерности прогрессирования рака грудной железы и некоторых других злокачественных опухолей подчиняются концепции Холстеда: распространение опухолевых клеток по лимфатическим этапам происходит постепенно, пошагово, последовательно. Прорыва этапа не происходит, опухолевые клетки должны полностью освоить предыдущую метастатическую нишу, чтобы подготовить следующую и двигаться дальше. Не может быть поражен следующий локорегионарный этап, если до этого не был освоен предыдущий. Поэтому при удалении какого-либо сигнального коллектора или сигнального лимфатического узла и негативном патоморфологическом ответе дальнейшее расширение объема диссекции считается нецелесообразным.
В литературе выделено четыре направления лимфогенного метастазирования при РЖ (А.В. Мельников, 1960), каждый из которых имеет четыре этапа, или шага.
I направление: отток лимфы происходит из большой кривизны пилорического отдела, а также из прилегающих передней и задней стенок. Этапы метастазирования: а) желудочно-ободочная связка; б) ретропилорические узлы; в) брыжейка начальной части тонкой кишки; г) забрюшинные лимфатические узлы (парааортальные).
II направление: лимфоотток из малой кривизны пилорического отдела и прилегающих передней и задней стенок. Этапы метастазирования по малой кривизне: а) по ходу правой желудочной артерии; б) печеночно-двенадцатиперстная связка; в) непосредственные ворота печени; г) лимфатические узлы внутри печени.
III направление: отток лимфы из тела желудка, кардиального отдела малой кривизны, медиальной части свода желудка. Этапы метастазирования: а) малый сальник; б) желудочно-поджелудочная связка; в) забрюшинные надпанкреатические и парааортальные лимфатические узлы; г) средостение-параэзофагеальные узлы выше диафрагмы.
IV направление: отток лимфы из вертикального отдела большой кривизны, прилегающих передней и задней стенок, значительной части свода желудка. Этапы метастазирования: а) желудочно-ободочная связка; б) желудочно-селезеночная связка; в) ворота селезенки; г) селезенка.
В связи с особенностями метастазирования считается, что определение стадии опухоли затруднено при удалении менее 16 лимфатических узлов при онкологических операциях на желудке. Адекватное стадирование может быть некорректным даже при радикальном объеме диссекции (D2) по причине математического закона Уилла Роджерса [1, 2], который в приложении к РЖ означает наличие метастазов, «прыгающих» или «перепрыгивающих» один из этапов лимфогенного метастазирования.
Интересно, что изначально феномен Уилла Роджерса не имел никакого отношения к миграции стадии при РЖ и к медицине вообще. Он касался кажущегося парадокса (фокуса), заключающегося в том, что перемещение численного элемента из одного множества в другое может увеличить среднее значение обоих множеств.
Для лучшей иллюстрации этого распространенного явления рассмотрим два множества X и Y:
X = {1, 2, 3, 4},
Y = {5, 6, 7, 8, 9}.
Среднее арифметическое элемен тов из множества X равно 2,5, из множества Y – 7.
Однако, если число 5 переместить из Y в X, получится:
X = {1, 2, 3, 4, 5},
Y = {6, 7, 8, 9}.
Соответственно, среднее значение элементов множества X повысится до 3, а среднее значение элементов Y – до 7,5.
Название данного феномена основывается на цитате, приписываемой американскому комику Уиллу Роджерсу [3]: «Когда оклахомцы покинули Оклахому и переехали в Калифорнию, то повысили средний интеллект обоих штатов». Реальный пример феномена Уилла Роджерса заключается в медицинском понятии «изменение состояния», суть которого состоит в следующем: улучшение методов диагностики какого-либо заболевания приводит к изменению состояния части населения со «здоровый» на «больной». Поскольку люди на самом деле нездоровы, удаление их из популяции «здоровых» повышает средний показатель здоровья этой группы. Добавление их в другое множество также повышает средний показатель здоровья в этой группе [1].
Соответственно, при проведении систематизации онкологических больных в одной и той же группе (например, с помощью VI и VII издания классификации TNM – в дальнейшем TNM VI и TNM VII) закономерно произойдет переход части больных из одной стадии в другую.
А это, в свою очередь, способно изменить показатели выживаемости, казалось бы, одной и той же группы больных. Интерес к данному явлению подогревается многогранностью его приложения к статистическим данным, касающимся РЖ и обсуждению этой тематики в общем.
Так, Sumin Chae и соавт. сравнили эффективность TNM VII с V\VI, как фактора прогноза при РЖ, и показали, что численность пораженных лимфатических узлов является главным прогностическим фактором. Исследование проводилось с целью оценить рациональность применения классификации TNM VII по сравнению с предшествующей [7]. Было проанализировано 295 больных, включенных в исследование в течение четырех лет. В соответствии с седьмой редакцией UICC пятилетняя кумулятивная выживаемость для N0, N1, N2, N3a и N3b составила 89,7; 73,6; 54,9; 23,1 и 5,4% соответственно (p=0,0001).
При использовании унивариантного анализа сделано заключение, что N-классификация TNM VI и TNM VII UICC/AJCC системы стадирования, T-классификация TNM VII UICC системы стадирования, размер и локализация опухоли, а также гистология, были достоверно ассоциированы с общей выживаемостью при РЖ. В то же время регрессионный многофакторный пропорциональный анализ по Коксу (multivariate Cox’s proportional analysis) показал, что N-классификация TNM VII UICC являлась независимым прогностическим фактором вместо N-классификации TNM VI UICC (p=0,0001).
N1 в TNM VI означает поражение метастазами 1-6 регионарных лимфатических узлов, в то время как N1 в TNM VII – поражение регионарными метастазами 1-2 регионарных лимфатических узлов. Это означает, что T1N1M0 в TNM VI и T1N1M0 в TNM VII – уже не одно и то же, и выживаемость этих двух групп будет разной. Таким образом, часть больных, ранее классифицируемых так, теперь окажется в другой стадии заболевания, соответственно, изменятся и показатели статистики. Это те самые «оклахомцы» Уилла Роджерса, переехавшие в Калифорнию:
Подводя итоги, можно сказать, что изучаемый феномен существует как бы в трех измерениях, трех смыслах.
Сэр Роберт Малдон, один из премьер-министров Новой Зеландии, знаменит фразой: «Новозеландцы, эмигрирующие в Австралию, повышают IQ обеих стран». Миграция пациентов в другую стадию при иной системе классификации является реально существующим событием. В частности, Daniele Marrelli назвал это явление «сдвигом» (shift) стадии [4].
Говоря о феномене миграции больных из стадии в стадию при разной классификации в одной и той же группе, необходимо привести пример из литературы.
Shiro Kikuchi и соавт. [6] исследовали 609 пациентов с распространенным РЖ, которые перенесли расширенные лимфодиссекции. При сравнении эффективности классификаций TNM VII и VI с точки зрения прогноза при РЖ не выявлено отличий в показателях 5-летней выживаемости. Исследователи делают вывод о том, что классифицирование больных по TNM VII и JCGC 14-й редакции не всегда превосходит TNM VI для определения прогноза после радикального хирургического лечения при распространенной стадии РЖ. Расширенные лимфодиссекции могут быть эффективны для N0-N3a, но никак не для N3b и M1 стадий TNM VII и JCGC 14-й редакции.
В нашем исследовании миграция подгрупп больных РЖ из одной стадии в другую, связанная с изменением системы стадирования, приводила к снижению риска смерти на 17% для II и на 55% – для III стадии. Сравнение продолжительности жизни больных РЖ в группах T4aN3aM0 (бывшая T3N2M0 по TNM VI) и T4bN3M0 (T4N2M0 по TNM VI) стадий выявило достоверность отличий в выживаемости, которая составила соответственно р=0,00146 и р=0,0137; соотношение рисков – 1,12 и 1,11.
Различные показатели выживаемости в одной и той же подгруппе (стадированной по разным TNM системам) объяснялись тем, что численность больных в одной и той же TNM-подгруппе была различной, то есть отмечали сдвиг или миграцию больных из одной подгруппы в другую. Ожидалось, что отличий между подгруппами не будет, поскольку это одни и те же больные. Однако при различных системах стадирования зафиксированы статистически достоверные отличия показателей выживаемости. Из 16 проведенных оценок только в 3 случаях отмечены сравнимые значения выживаемости больных: T3N1M0 (VI) и T4aN2M0 (VII), T4N1M0 (VI) и T4bN2M0 (VII), а также T4N2M0 (VI) и T4bN3M0 (VII) (р>0,05).
За последние 10 лет онкологические и хирургические стационары пережили переход от IV к V, а со временем к VI и VII изданию Международной классификации TNM. Мог ли данный факт повлиять на статистику РЖ и показатели качества лечения больных? Ведь процесс занял всего 10-12 лет. Многочисленные исследования, опубликованные в иностранной и отечественной литературе, велись в различных системах исчисления, с разными переменными, например, исследования больных РЖ IV стадии теперь корректно сравнивать не только с IV, но также с IIIa, IIIb, IIIc и даже IIb стадиями.
Приводим некоторые отличия между TNM VI и TNM VII.
1. Разделение индекса Т1 на Т1а и Т1b стадии прогрессирования первичной опухоли.
2. Разделение фенотипа опухоли Т4 на Т4а и Т4b стадии.
3. Т2а и Т2b индексы теперь отсутствуют, вместо них введены IIа и IIb стадии.
4. Цифровые значения индексов Т и N приобрели новые качественные значения, о чем будет сказано ниже.
5. Значения индекса N3 теперь разделены на N3а и N3b.
6. Пересмотру подверглись стадии РЖ, например, IV стадия теперь означает исключительно наличие отдаленных метастазов, III стадия разделена на три подстадии: a, b, c.
7. Те TNM-сочетания, которые ранее означали одну стадию, теперь означают другую:
T1N1M0 (VI) = T1а,bN2M0 (VII)
T2aN1M0 (VI) = T2N2M0 (VII)
T2bN1M0 (VI) = T3N2M0, T3N1M0 (VII)
T3N1M0 (VI) = T4aN1M0, T4aN2M0 (VII)
T4N1M0 (VI) = T4bN2M0 (VII)
T1N2M0 (VI) = T1a,bN3аM0 (VII)
T2aN2M0 (VI) = T2N3аM0 (VII)
T2bN2M0 (VI) = T3N3аM0 (VII)
T3N2M0 (VI) = T4aN3аM0 (VII)
T4N2M0 (VI) = T4bN3аM0 (VII)
T2bN3M0 = T3N3bM0 (VII)
T3N3M0 (VI) = T4aN3bM0 (VII)
Почти без изменений остались:
TisN0M0 (VI) = TisN0M0 (VII)
T1N0M0 (VI) = T1a,bN0M0 (VII)
T1N1M0 (VI) = T1a,bN1M0 (VII)
T1N3M0 (VI) = T1a,bN3bM0 (VII)
T2aN1M0 (VI) = T2N1M0 (VII)
T2aN3M0 (VI) = T2N3bM0 (VII)
T4N1M0 (VI) = T4bN1M0 (VII)
T4N3M0 (VI) = T4bN3bM0 (VII)
S.S. Kim и соавт. [8] из университетского колледжа в г. Сеуле (Южная Корея) при проведении ретроспективного анализа 266 больных РЖ, прооперированных в 2000-2009 гг., выявили отсутствие отличий в показателях выживаемости больных, классифицированных по TNM VII: между стадиями IIа и IIв, IIв и IIIа, и IIIа и IIIв (70 vs 71%, p=0,530; 71 vs 80%, p=0,703; 80 vs 75%, p=0,576, соответственно), хотя соответствующие статистические отличия в 5-летней кумулятивной выживаемости были выявлены среди групп, выделенных по TNM VI. Так, при анализе групп по TNM VII 5-летняя выживаемость не отличалась между T2 и T3 (86% vs 82%, p=0,655), а также между N1 и N2, N3a и N3b (79 vs 81%, p=0,506; 41 vs 17%, p=0,895, соответственно). Исследователи делают вывод, что TNM VII имеет худшие возможности для определения прогноза у больных РЖ в сравнении с TNM VI.
Daniele Marrelli и соавт. [9] проанализировали 2090 больных с некардиальным РЖ, которые были прооперированы в период 1991-2005 гг. Для сравнения симулирована оценка всех этих больных по TNM VII. Были прослежены изменения в распределении больных РЖ по стадиям в TNM VI и TNM VII. Во многом благодаря сдвигу большого количества случаев из Iв в стадию IIа, а также из IIIа и IV стадий в стадии IIIв и IIIс канцерзависимая 10-летняя выживаемость составила 53±1%. Прослежены достоверные различия по критерию T (T2 vs T3, p<0,001) и N (N1 vs N2, p<0,001). Уровень выживаемости подгруппы N3a (7-15 пораженных лимфатических узлов) был существенно выше по сравнению с N3b (>15 пораженных лимфоузлов; р<0,001). Стадии Iв и IIа по TNM VII продемонстрировали аналогичный прогноз, в то время как между другими подгруппами были выявлены достоверные отличия. Анализ категорий внутри стадий TNM VII показал неоднородность уровней выживаемости в стадиях IIв, IIIв и IV. Сделан вывод о том, что TNM VII для некардиального РЖ демонстрирует подгруппы больных с неодинаковым прогнозом, причем распределение по стадиям и выживаемость пациентов существенно изменились по сравнению с TNM VI.
Возможно ли, используя теорию вероятности, в том числе статистический анализ вероятности по методике Кокса, спрогнозировать частоту феномена «прыгающих» метастазов при РЖ? Отметим, что в процессе хирургического лечения РЖ этот феномен выявляется не всегда (наиболее удаленные коллекторы не могут быть иссечены во всех случаях). Попыткой ответить на этот вопрос стало исследование, проведенное на базе абдоминального онкохирургического отделения КУ «Одесский областной онкологический диспансер».
Материалы и методы. Всего в наше исследование было включено 188 пациентов, оперированных по поводу РЖ в период 2007-2011 гг. Это были только радикально или условно радикально прооперированные больные, (120 мужчин и 68 женщин). Средний возраст составил 60,6±10,5 лет.
В общей сложности больным выполнены 126 гастрэктомий и 62 дистальных субтотальных резекции. Гастрэктомии выполнялись по методике Бондаря с формированием терминолатерального петлевого муфтообразного позадиободочного эзофагоеюноанастомоза с межкишечным соустьем по Брауну. Дистальные субтотальные резекции заканчивались в большинстве случаев формированием позадиободочного гастроэнтероанастомоза по Бильрот-2 в модификации Гофмейстера-Финстерера.
Изучалась продолжительность жизни больных РЖ, вошедших в исследование. Информация о продолжительности жизни была получена из Областного канцер-регистра, обновление данных которого осуществлялось 1 раз в 3 мес. Далее составлялись таблицы продолжительности жизни для каждой группы, стадии и использованного метода лечения. Выживаемость изучалась при помощи построения модели регрессии пропорциональных интенсивностей рисков Д.Р. Кокса (1972) по формуле:
hi(t) = h0(t) × еb1X1+ b2X2+ b3X3+… + bnXр, где
h0(t) – исходная опасность;
b1...bn – коэффициенты регрессии;
X1...Xр – прогностические факторы.
Когда b=0, отношение опасности равно 1.
Наблюдения были цензурированы: для тех больных РЖ, с кем удавалось поддерживать контакт, цензор =0, если же больной умирал, цензор =1. При анализе выживаемости изучалась частота события во времени – медиана выживаемости больных. Точкой отсчета являлась дата операции, шкала времени (продолжительность жизни больных, мес), событие (смерть больного).
Областной канцер-регистр является примером цензурированной выборки, то есть выборки, которую необходимо математически проанализировать, но которая в силу объективных и субъективных причин не содержит полной информации. Метод Каплана-Майера, как и метод построения таблиц дожития и другие методы, имеет дело с цензурированными выборками. У него всего один недостаток: он не позволяет оценить достоверность различий между двумя кривыми выживаемости.
Стандартно учитывалось правое цензурирование – уход больного из-под наблюдения либо смерть от других причин и левое отсечение – неравномерность включения больных в исследование (больные включались в исследование в 2007, 2008, 2009 и т.д. годах). При построении графиков шкала Y включала процент выживших больных S, а шкала X – месяцы наблюдения. Преимущество модели по Коксу заключается в возможности добавления ковариант, отсутствии необходимости корректно стратифицировать группы, обосновывать правильность стратификации, как в логранговой (метод логистической регрессии) и каплан-майеровской математических моделях.
Итак, по численности критерию сравнения соответствовали: группа T3N1M0 TNM VI сравнивалась с двумя соответствующими TNM VII.
T4aN1M0 TNM VII (n=20)→ р=0,023 <0,05 р=0,00029 <0,05
T4aN2M0 TNM VII (n=25)→ р=0,00239 <0,05 р=0,072 >0,05.
Как видно, независимо от вида рандомизации при переходе из одной классификации в другую больные имели различную выживаемость. А это означает, что так называемое изменение состояния произошло везде, кроме одного случая: р=0,072 >0,05. Таким образом, феномен имел место там, где T4N1M0 TNM VI прошла сравнение с 2-мя группами TNM VII.
T4bN1M0 TNM VII (n=22)→ р=0,00468 <0,05 р=0,00326 <0,05
T4bN2M0 TNM VII (n=12)→ р=0,0164 <0,05 р=0,0526 >0,05
То же само е имело место и в другой группе (n=34), где в результате миграции из стадии в стадию продолжительность жизни больных, перенесших радикальное лечение, менялась. Лишь в одном вычислении из трех сравнение показало отсутствие перемен: р=0,0526 >0,05.
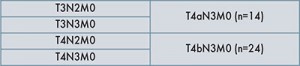
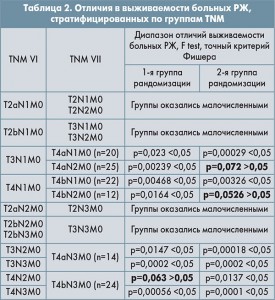
Другие группы были сравнительно малочисленны для подобного рода сравнений, кроме отраженных в таблице:
Группы T3N2M0 и T3N3M0, стадированные по TNM VI здесь, согласно всем нововведениям, теперь соответствуют группе T4aN3M0 по классификации TNM VII.
Напомним, что точный критерий Фишера F и критерий согласия Пирсона χ2 могут быть использованы для сравнения групп всего с 2-мя членами. При этом цифровые значения в такой таблице при использовании χ2 не могут быть менее 5. В нашей таблице числовые значения выглядели так:
Сравнение производилось с группой TNM VI, имевшей подобные цифровые значения численности групп.
Феномен Уилла Роджерса прослеживался вне зависимости от группы рандомизации: р=0,0147; р=0,00018; р=0,0002; р=0,0002. Две группы рандомизации позволяют верифицировать различия с наибольшей вероятностью.
В одной рандомизированной группе TNM VI в случае перехода части больных из T4N2M0 в T4bN3a,bM0 TNM VII (р=0,063) «изменения состояния» не произошло. Только в этой ситуации введение TNM VII не повлияло на выживаемость больных РЖ. В остальных случаях искомый феномен наблюдался и был верифицирован. Численность групп больных была достаточной для оценки.
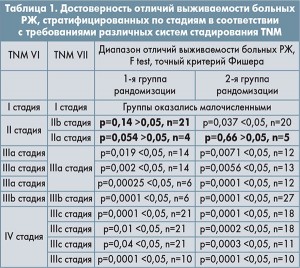
Следующим способом проверки подлинности нашей гипотезы о переходе больных из одной классификации в другую явилась попытка сравнения их выживаемости в зависимости от стадии. Для этого произведено математическое сравнение аналогичных по описанию стадий, как это зафиксировано в классификациях.
В таблице приводится обобщенное сравнение графиков выживаемости больных РЖ, классифицированных по TNM VI и TNM VII, которые также еще были рандомизированы. Сами графики не приведены для упрощения восприятия всего массива информации.
В данном случае численность больных в подгруппах оказалась более подходящей для анализа. Только в группе с первой стадией не представилось возможности проверить теоретические выводы.
II стадия→ IIb стадия→ р=0,14 >0,05, n=21→ р=0,037 <0,05, n=20→
IIa стадия→ р=0,054 >0,05, n=4→ р=0,66 >0,05, n=5
Сравнивались II и IIb стадии с точки зрения изменения выживаемости для математической верификации реальности трансфера больных из одной группы в другую.
II стадия→ IIb стадия→ 21-20=1→
IIa стадия→ 4-5=-1
Только в одном случае такая верификация была достигнута: р=0,037 <0,05, n=20, при сравнении первой рандомизированной группы, классифицированной по TNM VII. В трех остальных случаях феномен перехода отсутствовал, однако количество больных там было неудовлетворительно низким. Напомним, что статистически достоверным считалось р<0,05, что достаточно для медико-биологических исследований.
Итак, феномен Уилла Роджерса подтвердился. Статистические показатели, в том числе самый важный с точки зрения онколога – изменение выживаемости, радикально поменялись.
В некоторых случаях р<0,001, в одном случае даже <0,0001 (n=71, что при условии использования точного критерия Фишера достаточно для подтверждения статистических различий). Миграция 2+1+(-6)=-3 означает обратную миграцию пациентов между группами.
То же самое наблюдалось при сравнении IIIb стадии. Получены следующие математические показатели: р=0,0001 <0,05, n=6 и р=0,0001 <0,05, n=27.
IV стадия→ IIIc стадия→ р=0,0001 <0,05, n=21→ р=0,0001 <0,05, n=18→
IIIc стадия→ р=0,01 <0,05, n=21→ р=0,0002 <0,05, n=18→
IIIc стадия→ р=0,04 <0,05, n=21→ р=0,0003 <0,05, n=11→
IIIc стадия→ р=0,0001 <0,05, n=10→ р=0,0001 <0,05, n=10
Аналогичные показатели получены для перехода IV стадии в IIIc стадию (n=130). Переформатирование группы согласно TNM VII привело к радикальному изменению статистики (р=0,0001; р=0,0001; р=0,01; р=0,0002; р=0,04; р=0,0003; р=0,0001; р=0,0001). При использовании новой классификации 16 больных автоматически перешли в другую группу.
IV стадия→ IIIc стадия→ 21-18=3
IIIc стадия→ 21-18=3
IIIc стадия→ 21-11=10
IIIc стадия→ 10-10=0.
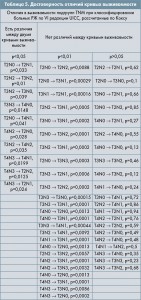
Интересно также сравнить группы в рамках одной и той же классификации (то, чем медицинские исследователи обычно и занимаются), определяя возможность стратифицировать больных так, чтобы имелись достоверные отличия в выживаемости между группами. Насколько TNM VI способна разделить больных РЖ на группы, достоверно отличающиеся по выживаемости? Забегая вперед, следует отметить, что на нашей выборке больных TNM VI проявила себя на качественно лучшем уровне по сравнению с TNM VII.
Таким образом, с высокой математической точностью удалось показать, что большинство групп пациентов, образованных в соответствии с TNM VI, статистически отличались. С нашей точки зрения, в этом и заключается цель создания какой-либо классификационной системы: с ее помощью должны создаваться группы, отличающиеся друг от друга по тем или иным объективным признакам. В данном случае анализировались различия в выживаемости больных РЖ: у 21 пары кривых выживаемости различия отсутствовали; у 25 пар были различия сверхвысокой мощности (р<0,01, в ряде случаев: р<0,001 и р<0,0001); у 10 пар кривых – статистически значимые различия (р<0,05).
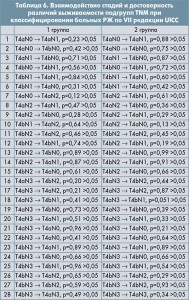
Следующим шагом стало проведение подобного анализа для TNM VII. Что будет, если тех же самых больных РЖ, оцениваемых ранее по TNM VI, классифицировать в соответствии с TNM VII? Насколько будут различаться полученные TN-группы? (Поскольку в данном случае речь шла только о радикально прооперированных больных, критерий М=0). Для достижения максимальной чистоты эксперимента больные РЖ были рандомизированы на две группы, между которыми и проводилось дальнейшее сравнение.
Напомним, что при сравнении выживаемости больных РЖ, оцениваемых по TNM VI, удалось получить три группы, которые различались по силе достоверности отличий показателей выживаемости. Группы были разделены на 21, 25 и 10 подгрупп, в которых сравнивались кривые выживаемости по степени достоверности отличий.
Качество классификации определяется способностью математически показать отличия между группами, очень близкими по описанию «степень распространения по критерию T» и «степень распространения по критерию N».
К сожалению, в этой же самой группе больных, классифицированных теперь уже по TNM VII, отличий в выживаемости между подобными группами выявить не удалось (табл. 6).
Вероятность выявления отличий между группами, классифицированными по TNM VII, всегда составляла менее 95%, а этого недостаточно для проведения медико-биологических исследований.
Отметим, что выполненная работа вызвана исключительно исследовательским интересом и ни в коем случае не направлена на критику различных изданий TNМ-классификации. Мы надеемся, что в процессе получения большего количества материала будут прослежены новые, не менее интересные тенденции. В то же время численность группы, включенной в наше исследование (n=188), была сравнима с двумя из четырех известных подобных исследований: 295 Sumin Chae и соавт., 266 – Kim S.S. и соавт., 609 – Shiro Kikuchi и соавт. и 2090 больных Daniele Marrelli и соавт.
Таким образом, в онкологии феномен Уилла Роджерса проявляет себя в трех измерениях, в трех смыслах. В привычном узком смысле он связан с наличием «перепрыгивающих», биологически агрессивных «проникающих» метастазов. Перед нами замечательный пример того, какой несовершенной может быть система стадирования при раке вообще и при РЖ в частности. «Прыгающие» (или «минующие» – skipping) лимфотропные метастазы приводят к разнородному описанию критерия N, и, соответственно, невыполнению большего объема лимфодиссекции и дальнейшей терапии. Хотя, что первично в данном случае – яйцо или курица? – неадекватное стадирование или выбранный объем лимфатической диссекции?
В более широком смысле феномен Уилла Роджерса приводит к перемещению больных из одной стадии/группы исследования в другую при изменении способа классификации. Он противоречит опыту наблюдателя, поскольку перемещение хотя бы одного числа из большого множества в другое приводит к изменению показателей в группах. Феномен увеличивает числовое значение среднего показателя в каждом из множеств, а это означает изменение среднеквадратичного отклонения или медианы выживаемости. «Оклахомцы» Уилла Роджерса мигрируют.
Кроме того, этот феномен свидетельствует о значимости правильного распределения значений в группах. В каждом последующем издании TNM-классификации стратификация больных РЖ осуществляется по-новому. В связи с этим в проводимых метаанализах сравнение групп больных, стадированных в соответствии с различными редакциями TNM-классификации, может быть некорректным. Все это свидетельствует о том, что феномен Уилла Роджерса в онкологической науке и практике не должен оставаться незамеченным.
Литература
1. Feinstein A.R., Sosin D.M., Wells C.K. (June, 1985). «The Will Rogers phenomenon. Stage migration and new diagnostic techniques as a source of misleading statistics for survival in cancer». The New England Journal of Medicine, 312 (25): 1604-8. doi: 10.1056/NEJM198506203122504. PMID 4000199.
2. Sormani M.P., Tintorе M., Rovaris M., Rovira A., Vidal X., Bruzzi P., Filippi M., Montalban X. (2008). «Will Rogers phenomenon in multiple sclerosis». Annals of Neurology 64 (4): 428-433. doi: 10.1002/ana.21464. PMID 18688811. Edit
3. The grapes of wrath. John Steinbeck. Herman Finkelstein Collection (Library of Congress). Publisher: New York: The Viking Press, [1939] ©1939.
4. Marrelli D., Morgagni P., de Manzoni G. et al. (2012). Prognostic value of the 7th AJCC/UICC TNM classification of noncardia gastric cancer: analysis of a large series from specialized Western centers. Ann Surg. 255 (3): 486-491.
5. Лемешко Б.Ю. Рекомендации по стандартизации. Прикладная статистика. Правила проверки согласия опытного распределения с теоретическим. Часть I. Критерии типа хи-квадрат. – М.: Изд-во стандартов. 2002. – 87 с.
6. Kikuchi S., Futawatari N., Sakuramoto S. et al. (2011) Comparison of staging between the old (6th edition) and new (7th edition) TNM classifications in advanced gastric cancer. Anticancer Res.; 31 (6): 2361-2365.
7. Kim S.S., Choi B.Y., Seo S.I. et al. (2011) The Comparison between 6th and 7th International Union Against Cancer/American Joint Committee on Cancer Classification for Survival Prognosis of Gastric Cancer. Korean J Gastroenterol.; 58 (5): 258-263.
8. Chae S., Lee A., Lee J.H. (2011) The effectiveness of the new (7th) UICC N classification in the prognosis evaluation of gastric cancer patients: a comparative study between the 5th/6th and 7th UICC N classification. Gastric Cancer; 14 (2): 166-171.
9. Marrelli D., Morgagni P., de Manzoni G. et al. (2012) Prognostic value of the 7th AJCC/UICC TNM classification of noncardia gastric cancer: analysis of a large series from specialized Western centers. Ann Surg.; 255 (3): 486-491.