31 березня, 2016
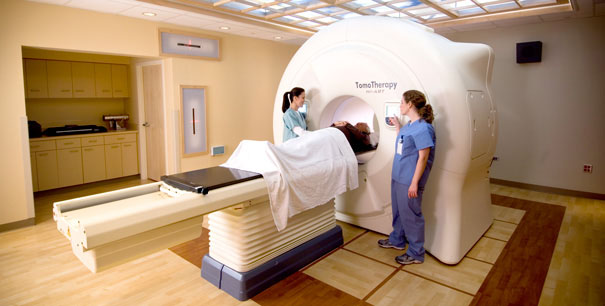
TomoTherapy – технология, изменившая стандарты лучевой терапии рака
 Последнее десятилетие связано с быстрым развитием современных методов противоопухолевой терапии.
Последнее десятилетие связано с быстрым развитием современных методов противоопухолевой терапии.
Вслед за изменениями стандартов хирургического и системного лечения резко возросли требования к лучевой терапии. Наряду с максимальной эффективностью обязательным условием современного радиационного лечения является его безопасность, а именно прецизионное облучение только опухолевой ткани, снижение дозовой нагрузки на расположенные рядом критические органы и уменьшение степени проявлений ранней и поздней токсичности.
Наиболее совершенным технологическим воплощением современной лучевой терапии, отвечающей требованиям сегодняшней онкологической практики, является томотерапия (TomoTherapy).
История развития лучевой терапии рака
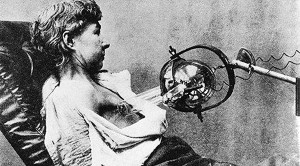
Первые попытки воздействовать на рост злокачественных опухолей с помощью Х-лучей были совершены всего через несколько месяцев после их открытия Конрадом Рентгеном в декабре 1895 г. (рис. 1).
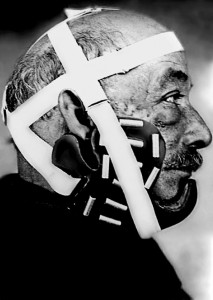
Эмиль Груббе уже в 1896 г. провел облучение молочной железы при неоперабельной карциноме (имя первой пациентки Rose Lee), а Виктор Деспень, врач из Лиона, через 5 месяцев после открытия Х-лучей использовал катодную трубку Крукса (рис. 2) для облучения больной с огромной опухолью в желудке.
Как писали в то время в медицинских журналах, у онкологических больных «впервые появилась надежда там, где ее не было…».
Следует отметить, что Иван Павлович Пулюй (1845-1918) – украинский и австро-венгерский физик и электротехник, который известен также как организатор науки, общественный деятель и автор первого перевода Библии на украинский язык, – начал использовать катодные лучи за 15 лет до К. Рентгена. Первая его статья о происхождении катодных лучей и их фотографическом действии была подана в «Доклады Венской академии наук» еще 13 февраля 1896 г. Сегодня имя И.П. Пулюя носит Тернопольский технический университет, улицы в г. Киеве и г. Львове.
В том же 1896 г. Анри Беккерель открыл эффект самопроизвольной радиоактивности солей урана, за что в 1903 г. он, а также Пьер и Мария Кюри были удостоены Нобелевской премии по физике «в знак признания их совместных исследований явлений радиации».
Это открытие имело огромный резонанс в обществе, а радиоактивный радий тут же начал использоваться в медицинских клиниках для борьбы с раком (рис. 3). Так, врач из Парижа Анри-Александр Данло в 1901 г. положил начало одному из направлений терапевтической радиологии, которое было названо брахитерапией (прежнее название – контактная лучевая терапия, или кюри-терапия).
Этот метод лечения заключался во введении зерен с источниками излучения внутрь пораженного органа. Брахитерапию применяли для лечения рака кожи, предстательной железы, молочной железы, пищевода, влагалища, тела и шейки матки, бронхов, желчных протоков, языка.
К сожалению, повальное увлечение солями радиоактивного радия и вера в его исцеляющие силы привели к тому, что в больницах начали предлагать новые анекдотичные методы терапии, которые имели самые серьезные негативные последствия для больных: ингаляции радием, применение радиевых мазей и внутривенных инъекций растворами, содержащими соли радиоактивного радия, употребление радиевой воды и даже шоколада с радием (рис. 4).
О том, что помимо лечебного эффекта радий чаще всего приводит к образованию многочисленных злокачественных опухолей, стало известно только в начале 1930-х гг. Шоком для общества стала смерть Эбена Макберни Байерса (1880-1932), богатого американского промышленника и спортсмена, скончавшегося от многочисленных метастазов радиационно-индуцированного рака вследствие употребления популярного патентованного лекарства, приготовленного из радия и растворенного в воде.
В память о жертвах применения Х-лучей в госпитале St. Georg в Гамбурге (Германия) был открыт мемориал, на котором в 1936 г. было выгравировано 169, а в 1959 г. – уже 359 имен людей, смерть которых напрямую была связана с «лечебным» использованием радия.
Тем не менее параллельно с непроверенными и опасными методами лечения активно развивалось другое направление лучевой терапии, происходило совершенствование новых технологий. Первую половину ХХ века можно назвать «эпохой киловольтов», поскольку для наружного облучения опухолей использовали катодные трубки Х-лучей – технологию, которую разработал Уильям Кулидж.
С 1946 г. началась «эпоха мегавольтов». Ей предшествовало открытие Ирэн и Фредериком Жолио-Кюри в 1934 г. явления искусственной радиоактивности. Первая радиологическая революция связана с именами Гарольда E. Джонсона и Джона Куннингама, которые в 1951 г. создали «бомбу для рака» на основе нового источника гамма-лучей – радиоактивного кобальта-60. Технология позволяла достигать энергии пучка фотонов в 1,2 МэВ и доставлять дозу облучения 45-60 Гр к глубоко расположенным опухолям. Впервые кобальт-60 для терапии рака был использован в г. Саскатун (Саскачеван, Канада). В западных клиниках в виде коммерческой технологии этот метод использовали на протяжении 20-30 лет.
Вторая радиологическая революция ХХ века связана с разработкой линейного ускорителя. Идея его создания принадлежит Эрнесту Томасу Уолтону (1929 г.). В Западном полушарии «отцом» линейного ускорителя принято считать Эдварда Леонарда Гинзтона, который был cоучредителем компании Varian (1948) и сооснователем Силиконовой долины.
В линейном ускорителе благодаря микроволновой технологии питания мощность рентгеновских лучей возрастает от 6 до 20 МэВ, а энергия в тканях опухоли может быть повышена до 70 Гр.
В новой технологии изменились планирующие системы (2D) и появилась дозиметрия. Это изменило позиции лучевой терапии в те годы. Радиационные онкологи стали полноправными членами мультидисциплинарной онкологической команды.
Радиочувствительность и радиорезистентность опухолевых клеток
Параллельно с совершенствованием технологий лучевой терапии активно развивались фундаментальные направления радиобиологии. Были получены уникальные данные, позволившие понять молекулярные механизмы радиорезистентности раковых клеток, а также изучить пути индукции канцерогенеза в биологических тканях после воздействия ионизирующей радиации.
Еще в 1906 г. Клаудиус Рего, работавший в институте Кюри, обнаружил, что Х-лучи вызывают бесплодие. На основании этого наблюдения был сделан вывод, что Х-лучи можно использовать для воздействия на быстрорастущие клетки, каковыми являются клетки рака.
В дальнейшем Дж. Бергонье и Л. Трибондо показали, что клетки биологического организма действительно обладают разной радиочувствительностью. В организме человека радиочувствительными являются гаметы, эритробласты, эпидермальные стволовые клетки и стволовые клетки желудочно-кишечного тракта, ооциты, лимфоциты. Минимальной чувствительностью обладают нейроны и мышечные клетки.
Закон Бергонье – Трибондо гласит, что клетки тем чувствительнее к облучению, чем они быстрее размножаются, чем продолжительнее фаза митоза и чем они менее дифференцированы. По мере накопления данных по радиобиологии были внесены дополнения в закон: наиболее чувствительными являются недифференцированные клетки, которые хорошо кровоснабжаются и имеют активный метаболизм. В последнее время доказано, что на радиочувствительность влияют также молекулярно-биологические особенности клетки (в частности, мутации KRAS и EGFR).
Несколько позже австралийский радиобиолог Хуберт Родни Уитерс обобщил теоретические данные и сформулировал закон радиобиологии, получивший название 4R (рис. 5).
Известно, что смерть клетки после воздействия ионизирующего излучения обусловлена прямым и непрямым повреждением – двухцепочечным разрывом ДНК (последствия действия свободных радикалов). Большинство излучений, как правило, сублетальные. При высоких дозах происходит накопление сублетальных повреждений, что ведет к отсроченной смерти клетки. Нормальные ткани и ткани опухоли часто различаются по своей способности к репарации этих повреждений.
В первые пять часов после облучения в опухолевых клетках запускаются механизмы репарации ДНК – Repair of DNA damage (1-я R). Затем в течение пяти часов происходит перераспределение клеток в клеточном цикле – Redistribution of cells in the cell cycle (2-я R). После этого на протяжении от одного часа до пяти дней осуществляется реоксигенация тканей – Reoxygenation (3-я R) и, наконец, в течение 5-7 недель – процесс репопуляции, то есть восстановление численности поврежденных клеток – Repopulation (4-я R).
На состояние радиорезистентности влияют такие факторы, как положение клетки в клеточном цикле. Наиболее резистентными к ионизирующей радиации являются клетки в фазе S и G2, наиболее чувствительными – клетки в фазе G1 и M.
Уровень гипоксии опухоли также влияет на состояние радиорезистентности. Большинство солидных опухолей имеют зоны, где содержание кислорода колеблется между бескислородным (0%), гипоксическим (1% – 7,5 мм рт. ст.) и нормоксическим (8% – 60 мм рт. ст.). Радиорезистентность раковых клеток проявляется при содержании кислорода <10 мм рт. ст. и становится максимальной при 0,5 мм рт. ст.
Клетки различных регионов опухоли гетерогенны и отличаются по уровню кровоснабжения и активности метаболизма. Существуют зоны с хорошей или низкой перфузией тканей, гипоксические зоны, клетки в состоянии пролиферации, клетки в состоянии повышенного метаболизма. Эти регионы опухоли по-разному будут реагировать на лучевую терапию.
Однако солидная опухоль состоит не только из однородных или гетерогенных опухолевых клеток. Опухоль представлена стволовыми клетками рака, гетерогенными злокачественными клетками и нормальными клетками, контаминирующими опухоль. Кроме того, солидная опухоль представлена клетками сосудистой и иммунной систем, а также соединительнотканной стромой.
Это обстоятельство следует учитывать при понимании механизмов радиорезистентности, ранней и поздней токсичности, а также реиндукции канцерогенеза.
Влияние радиотерапии на опухолевое микроокружение – сосудистую систему и строму
Ионизирующая радиация приводит к повреждению не только раковых клеток, но также клеток опухолевого микроокружения.
Биологический эффект ионизирующего излучения длится не минуты и часы, а месяцы и годы. При этом ранний биологический эффект, состоящий из воспалительной и пролиферативной фазы, сменяется поздним биологическим эффектом, во время которого происходит ремоделирование облученных тканей.
В реализацию как раннего, так и позднего радиобиологического эффекта вовлечены сосуды и строма опухоли.
Ранними последствиями влияния ионизирующей радиации на сосудистую систему являются дисфункция эндотелиальных клеток (повышенная проницаемость, отделение от базальной мембраны, апоптоз), агрегация тромбоцитов, претромботические состояния, микротромбы, диапедез, адгезия клеток воспаления, разрушение кровеносных сосудов, снижение их плотности, нарушение перфузии тканей, гипоксия, увеличение производства цитокинов, хемокинов, гипоксического фактора HIF-1α.
Поздними последствиями являются повреждение ангиоархитектоники – утолщение интимы сосудов, тромбозы, медионекроз, облитерирующий эндартериит, атеросклероз, ухудшение доставки кислорода к тканям и гипоксия.
Постлучевые повреждения соединительной ткани ведут к развитию радиационного фиброза. Этому состоянию предшествуют хроническое воспаление, иммунные реакции и ремоделирование тканей. В механизмах развития радиационного фиброза принимают участие опухоль-ассоциированные фибробласты, провоспалительные цитокины, интерлейкины IL-1, IL-6, IL-8, гранулоциты-макрофаги, колониестимулирующие факторы (GM-CSF), циклооксигеназа 2 (СОХ-2), трансформирующие факторы роста (TGF-β), протеолитические ферменты, компоненты внеклеточного матрикса.
Важным механизмом является повышение активности гепараназы, что создает условия для инвазии раковых клеток в ткани микроокружения во время проведения лучевой терапии.
В целом механизмы формирования фиброза при заживлении ран (операция, травма) и фиброза при облучении (лучевая терапия) резко отличаются: активность формирования радиационно-индуцированного фиброза сохраняется в течение многих лет и никогда не прекращается.
Ранние и поздние осложнения радиотерапии
К многочисленным ранним осложнениям радиотерапии относят мукозиты, радиодерматиты, диарею, алопецию, цистит, проктит, пневмонит, супрессию костного мозга.
Эти осложнения, ввиду наличия манифестных клинических проявлений, легко распознаются и подвергаются активной терапии.
Не меньшую, а возможно, и большую проблему представляют поздние осложнения лучевой терапии, которые редко регистрируются в практике онколога из-за длительного субклинического асимптомного течения. К таковым относятся, например, уплотнение и уменьшение в объеме тканей молочной железы (плохой эстетический эффект терапии), фиброз и ригидность легких, мальабсорбция и стриктуры тонкой кишки, поздняя ишемия и перфорации кишечника, гематурия, телеангиоэктазии кожи, эндокринная недостаточность, бесплодие, а также развитие радиационно-индуцированного вторичного рака.
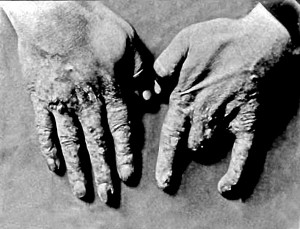
Жертвами многочисленных осложнений, вызванных облучением, в начале эры радиотерапии становились и сами врачи-радиологи (рис. 6).
Рецидив рака и метастазирование как осложнения радиотерапии
Еще в 1927 г. Герман Джозеф Мюллер изучал генетические эффекты облучения, в том числе влияние Х-лучей на риск развития рака. В 1946 г. за свои работы в области радиогенетики он был удостоен Нобелевской премии по физиологии и медицине.
К настоящему времени накоплены убедительные доказательства того, что облучение здоровых тканей микроокружения опухоли способствует инвазии и метастазированию раковых клеток, а облученная строма здоровых тканей способствует инициации канцерогенеза.
Известны результаты экспериментов, когда после облучения здоровых тканей молочных желез у крыс с последующей трансплантацией в зоны развившегося радиационного фиброза нормальных миоэпителиоцитов последние трансформировались в раковые клетки.
Радиационно-индуцированные опухоли щитовидной железы, шейки матки, прямой кишки, молочной железы, развившиеся через несколько лет после облучения здоровых тканей соответствующей анатомической области, – известные факты в практике онкологов.
Биологические эффекты влияния радиотерапии на микроокружение опухоли, как причины онкологических рецидивов и метастазирования, реализуются через воспаление, модуляцию канцер-ассоциированных макрофагов, иммунную модуляцию, ремоделирование микроокружения и формирование фиброза в зоне облученных тканей.
При облучении нормальных тканей, расположенных рядом с опухолью, происходит активация фибробластов, дисфункция эндотелия сосудов, воспаление, ремоделирование тканей, развивается необратимое повреждение стромы и радиационный фиброз, который со временем способствует возникновению рака de novo.
Третья революция в области радиационных технологий – TomoTherapy
Сегодня происходит изменение лечебной парадигмы во всех направлениях терапии рака, в том числе и в области радиационного лечения.
Изменению парадигмы лучевой терапии способствовали два обстоятельства: совершенствование технологий и главенствующий в онкологии тезис о необходимости проведения персонифицированного лечения рака.
Современная парадигма персонифицированной лучевой терапии сводится к эскалации и гипофракционированию дозы, улучшению точности доставки энергии излучения c одновременной (online) визуализацией облучаемого очага, изменению режимов терапии в процессе лечения (адаптация) и вокселизации – преобразованию изображения тканей опухоли в воксели с помощью компьютерной графики.
Реализация этих требований стала возможна в системе томотерапии (TomoTherapy) – едином радиотерапевтическом комплексе, включающем сверхсовременный линейный ускоритель и сверхсовременный компьютерный томограф.
Первый линейный ускоритель был создан в 1948 г. (Эдвард Гинзтон), а первый компьютерный томограф – в 1971 г. (лауреат Нобелевской премии по физиологии и медицине Годфри Хаунсфилд). В 1980 г. возникла идея скомбинировать обе технологии для достижения максимально эффективного и точного воздействия на опухоль, но не на близко расположенные здоровые ткани микро- и макроокружения.
В апреле 1994 г. первый пациент получил облучение с помощью томотерапии на оборудовании, разработанном корпорацией Nomos. Первоначально система предназначалась исключительно для облучения опухолей головного мозга и включала жесткую фиксацию черепа для предупреждения движения пациента.
 Рис. 7. Новая система Helical Tomotherapy разработана в университете Wisconsin-Madison (авторы Thomas Rockwell Mackie и Paul Reckwerdt)
Рис. 7. Новая система Helical Tomotherapy разработана в университете Wisconsin-Madison (авторы Thomas Rockwell Mackie и Paul Reckwerdt)Новая система Helical Tomotherapy была разработана в университете Wisconsin–Madison профессором Томасом Роквэллом Макки и Полом Реквердтом (рис. 7). Усовершенствованная технология предназначалась для лечения опухолей различных локализаций. Лечение первого пациента было проведено в 2002 г.
В системе томотерапии используются рентгеновские лучи мощностью от 6 до 20 МВ, что позволяет доставлять к опухоли энергию в дозе 60-70 Гр. Такая эскалация дозы требует предельной точности облучения, тем более что в процессе терапии опухоль изменяет контур, форму и объем. К тому же, большинство опухолей и окружающих тканей подвижны. Это может приводить к облучению критичных органов и резкому повышению радиационно-индуцированной токсичности. Избежать этих осложнений позволяет КТ 3-4D планирование, осуществляемое в режиме online.
Принципиально новое технологическое решение радиационной терапии – томотерапия (TomoTherapy®) – позволяет проводить конформное облучение опухоли с использованием технологий IMRT (Intensity-modulated radiation therapy), IGRT (Image guided radiotherapy) и MVCT (Megavoltage computer tomographie). Использование современных систем доставки излучения (линейный ускоритель) с одновременным КТ-моделированием и 3D модуляцией облучения позволяет достигать большой однородности дозы и точности облучения. Планирование терапии сложных объемов опухоли и распределение дозы согласно DVH (графических показателей) позволяет уменьшить области облучения (PTV) критических органов, а также проводить реконструкцию фактической дозы в процессе терапии. Все это клинически проявляется повышением эффективности, снижением токсичности и повышением безопасности лечения.
Принципиальным отличием томотерапии от других видов лучевого лечения является значительно более широкий спектр клинического применения. Так, с помощью томотерапии можно облучать опухоли больших размеров (до 30 см), опухоли сложной конфигурации и геометрии, опухоли, расположенные рядом с критичными органами (сердце, слизистая полости рта, пищевод, спинной мозг и т.д.) (рис. 8).
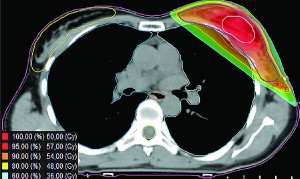 Рис. 8. Изодозное распределение в тканях опухоли и в критичных органах при томотерапии рака молочной железы
Рис. 8. Изодозное распределение в тканях опухоли и в критичных органах при томотерапии рака молочной железыС помощью томотерапии за счет спиральной доставки облучения можно проводить одновременную терапию сразу нескольких мишеней (облучать опухоль и синхронные метастазы, или же несколько синхронных метастазов в различных анатомических областях). Прецизионная томотерапия позволяет осуществлять повторное облучение опухолей.
Эта технология является незаменимой при терапии больших по протяженности опухолей (например, рак пищевода), мезотелиомы плевры (не облучая при этом легкое), распространенных лимфомах кожи, тотальном облучении костного мозга (перед трансплантацией), при раке единственной почки, раке предстательной железы, опухолях «головы и шеи», тотальном облучении лимфатических узлов и особенно при краниоспинальном облучении.
Преимущества краниоспинального облучения с помощью томотерапии заключаются в проведении сеанса терапии с одним изоцентром, в однородности дозы облучения (нет «холодных», «горячих» точек в местах стыковок полей), в высоком градиенте дозы между планируемым объемом облучения и органами риска и, конечно же, в ежедневном визуальном контроле.
Технологию томотерапии можно использовать по протоколам стереотаксической радиохирургии.
О том, что томотерапия способна изменить терапевтическую парадигму и расширить возможности лечения онкологических больных, свидетельствует следующий клинический случай.
У больной 56 лет на фоне крупноузлового цирроза печени вирусной этиологии стадии «В-С» по классификации Чайлд-Пью (Child-Pugh) возникла гепатоцеллюлярная карцинома. Учитывая наличие печеночно-клеточной недостаточности выполнить резекцию было невозможно; в выполнении ортотопической трансплантации печени больной было отказано.
В 2012 г. в Запорожском онкологическом диспансере была выполнена радиочастотная термоабляция, которая привела к стойкой ремиссии, сохранявшейся в течение трех лет. В 2015 г. наступил биохимический и радиологический рецидив заболевания. Признаков внепеченочного распространения опухоли не было. Наличие крупноузлового цирроза печени исключало возможность проведения хирургического лечения, а размеры опухоли (7 см в диаметре) не позволяли выполнить процедуру радиочастотной термоабляции повторно.
В Украинском центре томотерапии (г. Кировоград) была проведена томотерапия в области опухоли. Достигнута регрессия 60% объема опухолевого очага. Токсичности во время лечения не было. Динамика уменьшения объема опухоли в процессе томотерапии зафиксирована на КТ-рентгенограммах. Появилась возможность выполнить повторную радиочастотную термоабляцию остаточной опухоли.
Данное наблюдение подтверждает, что томотерапия, в отличие от обычных методов лучевой терапии, позволяет проводить лечение опухолей тех локализаций, которые ранее никогда не подлежали такому виду лечения (например, первичный рак печени).
Таким образом, томотерапия, изменившая парадигму лечения рака, является максимально эффективной технологией лучевой терапии, поскольку позволяет обеспечивать эскалацию и высокую конформность дозы в режиме реального времени. Режимы IGRT и IMRT позволяют создавать высокий градиент дозы облучения между планируемым объемом (опухолью) и близлежащими органами риска (критичными органами).
В целом технология TomoTherapy характеризуется отсутствием острых и поздних осложнений терапии, не сопровождается формированием радиационного фиброза в окружающих тканях и не способствует индукции канцерогенеза с развитием вторичных опухолей de novo.
Уже сегодня можно сделать заключение, что возможность использования томотерапии способна изменить стандарты противоопухолевого лечения в Украине.