15 червня, 2021
Цукровий діабет і гострі коронарні синдроми
 Цукровий діабет (ЦД) – один з основних чинників ризику хронічного коронарного синдрому (ХКС), а в >40% пацієнтів із гострими коронарними синдромами (ГКС) спостерігається ЦД. ЦД зумовлює зростання відсотка смертності в пацієнтів із ГКС, включаючи гострий інфаркт міокарда (ІМ) без підйому сегмента ST (ІМбпST), гострий ІМ із підйомом сегмента ST (ІМпST), реваскуляризацію, зокрема тромболіз або черезшкірне коронарне втручання (ЧКВ) тощо.
Цукровий діабет (ЦД) – один з основних чинників ризику хронічного коронарного синдрому (ХКС), а в >40% пацієнтів із гострими коронарними синдромами (ГКС) спостерігається ЦД. ЦД зумовлює зростання відсотка смертності в пацієнтів із ГКС, включаючи гострий інфаркт міокарда (ІМ) без підйому сегмента ST (ІМбпST), гострий ІМ із підйомом сегмента ST (ІМпST), реваскуляризацію, зокрема тромболіз або черезшкірне коронарне втручання (ЧКВ) тощо.
ГКС можна розподілити на дві основні групи:
• гострий ІМбпST. У пацієнтів із ГКС за такого стану спостерігається нестабільна стенокардія або ІМ із патологічним зубцем Q. Хворі на ЦД і ГКСбпST зазвичай літнього та/або старечого віку, в яких частіше верифікуються серцево-судинні захворювання, ЦД, артеріальна гіпертензія (АГ) та хронічна ниркова недостатність, а також частіше спостерігаються атипові симптоми;
• гострий ІМпST характеризується значнішим ураженням міокарда, небезпекою реінфарктів, менш сприятливим прогнозом (>30% хворих помирають у гострий період).
Головні етіологічні чинники
ГКС є проявами ХКС, а також зазвичай результатом розриву атеросклеротичних бляшок у коронарних артеріях (КА). Загальні чинники ризику: куріння, АГ, ЦД, дисліпопротеїнемії, чоловіча стать, гіподинамія, сімейна спадкова схильність до розвитку ожиріння, сімейний анамнез раннього ІМ (вік <55 років) і порушення режиму дієтичного харчування.
Епідеміологія
Американська асоціація серця (AHA) повідомляє, що кожну 41 с реєструється новий епізод серцевого нападу серед пацієнтів із ХКС. Хвороби серцево-судинної системи є основною причиною смерті в США, а на ХКС страждають ≈15,5 млн.
Основні патофізіологічні особливості
Гіперглікемія може бути фізіологічною реакцією на гіперпродукцію контрінсулярних гормонів при активації системного стресу. У пацієнтів зі значними ділянками ішемії міокарда та вираженою дисфункцією лівого шлуночка (ЛШ) спостерігається активація симпатичної нервової системи, що зумовлює зростання рівня глюкози. Гіперглікемія може бути індикатором системної й органоспецифічної дисрегуляції метаболізму (особливо порушень сигнальних шляхів інсуліну). Інсулінорезистентність спричиняє не лише гіперглікемію, а й зменшення продукції енергії міокардом та іншими органами, що зумовлює нижчу толерантність до гіпоперфузії. Пригнічення сигнальних шляхів інсуліну підвищує уразливість до ішемії, оскільки цитопротекторні ефекти молекул сигнального каскаду інсуліну втрачаються. Гостра гіперглікемія пов’язана зі збільшенням продукції активних форм кисню, активацією оксидантного стресу, індукцією протромботичного стану, погіршенням функції ендотелію тощо.
Класифікація ГКС:
1) нестабільна стенокардія;
2) гострий ІМбпST;
3) гострий ІМпST.
Усі ці синдроми пов’язані з гострою ішемією КА; їх диференціюють за симптомами, результатами електрокардіографії (ЕКГ) і рівнями серцевих біомаркерів. Синдроми доцільно розрізняти, оскільки прогноз і лікування відрізняються.
Класифікація ГКС і гострого ІМ на етапі попереднього діагнозу
1. ГКС із підйомом сегмента ST (ГКСпST). Гострий ІМ із підйомом сегмента ST (до цієї групи належить також блокада лівої ніжки пучка Гіса (БЛНПГ), що гостро з’явилася.
2. ГКС без підйому сегмента ST (ГКСбпST). Клінічний діагноз (у т. ч. остаточний) після підтвердження/виключення ІМ:
» гострий ІМпST (до цієї групи належить також БЛНПГ, що гостро з’явилася);
» гострий ІМбпST;
» нестабільна стенокардія.
Нестабільною є стенокардія, що гостро з’явилася; обтяжена стенокардія спостерігається, коли тяжкість і тривалість ішемії недостатні для розвитку некрозу кардіоміоцитів. Включає пацієнтів із затяжним (>20 хв) ангінозним нападом у спокої, стенокардією, що вперше з’явилася, а також прогресивною й постінфарктною стенокардією. Стенокардія, що вперше з’явилася, спостерігається в попередні 28 діб; її тяжкість відповідає щонайменше II функціональному класу (ФК) за класифікацією Канадського кардіоваскулярного товариства (CCS). Прогресивна стенокардія – гостре ускладнення раніше стабільної стенокардії в попередні 28 діб із появою характеристик, притаманних щонайменше III ФК за класифікацією CCS (2020).
ГКС без стійкого підйому сегмента ST на ЕКГ
ГКСбпST – це клінічні ознаки, що гостро з’явилися, чи симптоми ішемії міокарда за відсутності на ЕКГ стійкого (тривалістю >20 хв) підйому ST щонайменше у двох суміжних відведеннях і відсутня БЛНПГ, що гостро з’явилася. Може закінчитися без розвитку вогнищ та/або з розвитком некрозу міокарда (ІМ із формуванням або без формування патологічних зубців Q на ЕКГ). Це хворі з ангінозним нападом і зі змінами на ЕКГ, що свідчать про гостру ішемію міокарда (але без підйому ST). Зміни на ЕКГ характеризуються стійкою чи швидкоминущою депресією ST, інверсією, згладженістю чи псевдонормалізацією зубця Т. Результати ЕКГ у перші години можуть бути нормальними, але ймовірні стійка чи тимчасова депресія ST, інверсія, згладженість або псевдонормалізація зубців Т. У багатьох випадках виявляється пристінковий тромбоз КА. Надалі в частки хворих з’являються ознаки некрозу міокарда, зумовлені (крім основної причини розвитку ГКС) емболіями дрібних судин міокарда фрагментами тромбу та матеріалом з атеросклеротичної бляшки. Проте зубець Q на ЕКГ з’являється рідко; такий стан позначають як «ІМ без підйому сегмента ST».
ГКС із підйомом сегмента ST або БЛНПГ, що гостро з’явилася
Спостерігаються стійкі підйоми ST, що свідчать про гостру повну оклюзію КА. ГКСпST діагностується у хворих з ангінозним нападом або іншими атиповими відчуттями (дискомфортом) у грудній клітці, а також стійким (зберігається не <20 хв) підйомом ST або «нової» (що вперше з’явилася) БЛНПГ на ЕКГ. Зазвичай у хворих із ГКСпST пізніше спостерігаються ознаки некрозу міокарда – підвищення рівнів біомаркерів і змін ЕКГ, включаючи утворення зубців Q. Гострий ІМпST – ІМ, за якого в ранні терміни захворювання відзначаються стійкі (тривалістю >20 хв) підйоми ST щонайменше у двох суміжних відведеннях ЕКГ. До цієї категорії також належать пацієнти з БЛНПГ.
Клінічні критерії ГКС:
• затяжний (>20 хв) ангінозний біль у спокої;
• стенокардія не менш як ІІІ ФК – за класифікацією CCS це стенокардія, що з’явилася вперше (протягом попередніх 28 днів);
• прогресивна стенокардія не менш як ІІІ ФК;
• за стенокардії, що з’явилася після ІМ.
Можуть спостерігатися атипові прояви: епігастральний біль, диспепсія, посилення задишки.
Атиповий біль
Це пацієнти з ГКС й атиповим болем у грудях старшого віку (здебільшого жінки), в яких спостерігається більше супутніх захворювань, діагностичних помилок, а отже, їх лікування було розпочато несвоєчасно. У хворих на ГКС з атиповим болем у грудях відзначаються вища внутрішньолікарняна смертність і постлікарняна смертність незалежно від наявності ЦД в анамнезі.
Критерії гострої ішемії міокарда для діагностики гострого ІМ (достатньо щонайменше одного):
→ симптоми ішемії міокарда;
→ ішемічні зміни ЕКГ, які гостро з’явилися (чи ймовірно гостро з’явилися);
→ поява патологічних зубців Q на ЕКГ;
→ підтвердження за допомогою методів візуалізації нових ділянок міокарда зі втратою життєздатності чи порушенням скоротливості у вигляді змін, характерних для ішемічного походження;
→ коронарна ангіографія або автопсія – внутрішньокоронарний тромбоз.
Неатеросклеротичні причини ГКС
• Неатеросклеротичні механізми спричиняють значну кількості подій ГКС і потребують специфічних діагностичних і терапевтичних стратегій.
• Спонтанне розшарування КА найчастіше трапляється в молодих жінок, а використання традиційної стратегії консервативного лікування – важливий ризик раннього клінічного погіршення стану.
• Емболії КА можуть спричинити ГКС через прямі, парадоксальні або ятрогенні механізми.
• Спазм КА може з’являтися на рівні епікарда чи мікросудинного русла, а інвазивне тестування КА може поліпшити діагностику.
• Ураження міокарда часто перебігає безсимптомно, але може зумовити ГКС; для діагностики, можливо, знадобиться інвазивне тестування.
• Стрес-індукована кардіоміопатія (синдром такоцубо) часто асоціюється з дисфункцією ендотелію та може призвести до появи гострої обструкції вивідних трактів.
Діагностика
Першим кроком оцінки є ЕКГ, яка допомагає розрізнити гострий ІМпST, гострий ІМбпST і нестабільну стенокардію. У настановах AHA (2020) зазначено, що будь-якому пацієнту з підозрою на ГКС необхідно провести ЕКГ протягом 10 хв після прибуття в лікарняний заклад.
Лабораторні діагностичні дослідження
Із метою підтвердження/виключення ІМ і оцінки ризику несприятливого результату в усіх пацієнтів із підозрою на ГКСбпST необхідно досліджувати динаміку рівня високочутливого тропоніну Т (hs-cTnT) або I (hs-cTnI). Пацієнтам із підозрою на ГКС тест на hs-cTnI проводять одразу під час надходження до відділення, а також через 3 год. Висока ймовірність наявності захворювання до проведення аналізу та підвищений рівень hs-cTnI є суттєвими свідченнями ГКС, тоді як низька ймовірність захворювання й нормальні показники hs-cTnI свідчать про ймовірну відсутність ГКС. Підвищення рівня hs-cTnI >99-го перцентиля верхніх референтних значень у хворих з ішемією міокарда свідчить про гострий ІМ. Однак визначення hs-cTn або hs-cTnI необхідне для остаточного підтвердження діагнозу, а первинна лікувальна стратегія будується на підставі клінічної картини й ЕКГ. Крім того, вирішення питання про тромболітичну терапію чи проведення первинного ЧКВ не слід відтерміновувати до отримання інформації щодо рівня тропоніну. У клінічній практиці як кількісний біомаркер ступеня дисфункції ЛШ використовують мозковий натрійуретичний пептид (BNP) або N‑кінцевий proBNP (NT‑proBNP). Рівні BNP і NT‑proBNP є потужними прогностичними маркерами у хворих на ГКС; зокрема, в пацієнтів з ІМпST корелюють із розміром зони ІМ і дисфункцією ЛШ. Зміни рівня NT‑proBNP можуть бути предиктором розвитку фібриляції передсердь у хворих на ГКС.
Інструментальні діагностичні дослідження
1. ЕКГ. На догоспітальному етапі в усіх пацієнтів із підозрою на ГКС рекомендується протягом 10 хв зареєструвати й інтерпретувати ЕКГ у спокої щонайменше у 12 стандартних відведеннях. Для ГКСбпST характерні:
■ ознаки ішемії міокарда, про яку свідчать минущі (тривалістю <20 хв) підйоми ST щонайменше у двох суміжних відведеннях ЕКГ;
■ минущі чи стійкі депресії ST (особливо горизонтальні чи кососпадні) щонайменше на 0,05 мВ;
■ виражені (≥0,2 мВ) симетричні негативні зубці Т у грудних (прекардіальних) відведеннях також допускають наявність гострої ішемії міокарда;
■ неспецифічні ознаки – зміщення ST <0,05 мВ та інверсія зубця Т <0,1 мВ.
У всіх пацієнтів із підозрою на ІМпST рекомендується:
■ зареєструвати ЕКГ у спокої щонайменше у 12 стандартних відведеннях;
■ на догоспітальному етапі варто зареєструвати ЕКГ протягом 10 хв і невідкладно її інтерпретувати;
■ у хворих на ІМпST для своєчасного виявлення й усунення порушень ритму серця необхідно якнайшвидше розпочати моніторування ЕКГ.
2. Ехокардіографія (ЕхоКГ). Усім хворим із підозрою на ГКСбпST рекомендується провести ЕхоКГ з обов’язковою оцінкою фракції викиду (ФВ) ЛШ. У пацієнтів з ІМпST для підтвердження діагнозу, оцінки тяжкості ураження та визначення прогнозу потрібно провести ЕхоКГ (оптимально в першу добу госпіталізації).
3. Коронарографія (КГ), сцинтиграфія й магнітно-резонансна томографія (МРТ) міокарда. Доцільність КГ і терміновість її виконання при ГКСбпST визначаються клінічною картиною захворювання та результатом стратифікації ризику несприятливого результату. У пацієнтів з ІМпST (у рамках стратегії первинного ЧКВ і стратегії з фармакоінвазивним підходом) проведення КГ є обов’язковим. Основне завдання – верифікація гострої оклюзії або ускладненого стенозу КА для подальшого його усунення за допомогою застосування методу ЧКВ / аортокоронарного шунтування (АКШ).
Комп’ютерно-томографічна КГ використовується з метою виключення ГКС у хворих із невисокою ймовірністю ішемічної хвороби серця за відсутності ішемічних змін на ЕКГ і підвищеного рівня hs-cTnI або hs-cTn у крові. У пацієнтів із підозрою на ГКСбпST рекомендується проведення сцинтиграфії міокарда з 99mTc-пірофосфатом у спокої. МРТ серця за ГКCпST рекомендується як кращий метод для уточнення локалізації й обсягу ураження міокарда (навіть за відносно невеликих розмірів вогнищ некрозу), а також для диференційної діагностики уражень міокарда.
Лікування (загальні підходи)
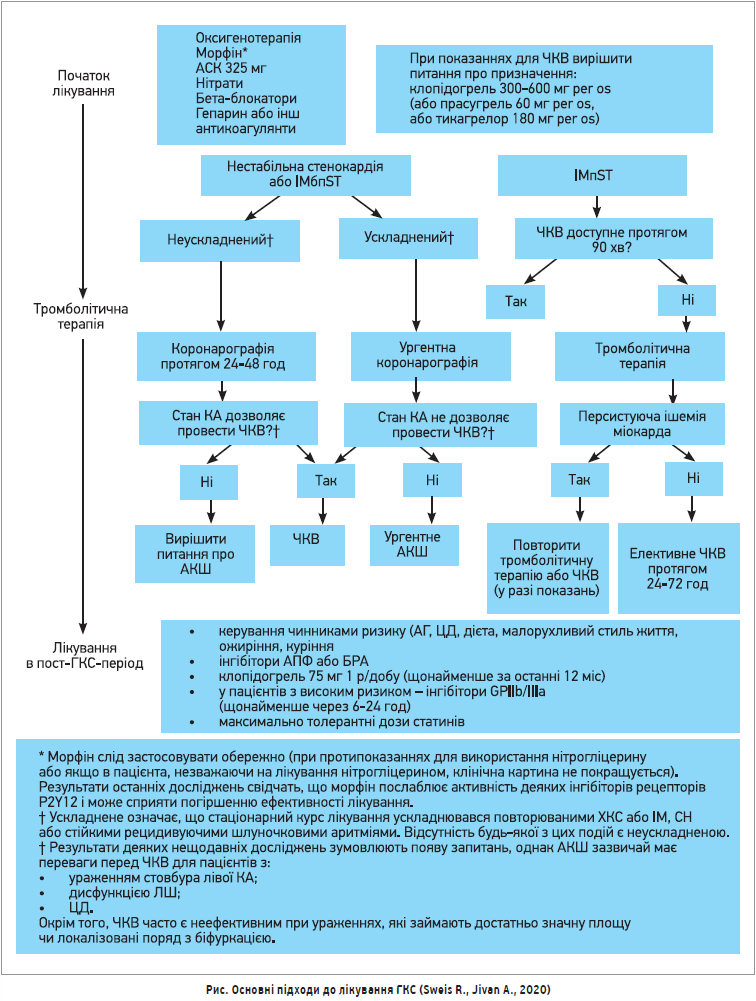
Основні підходи до лікування ГКС продемонстровано на рисунку (Sweis R., Jivan A., 2020).
Першопочаткове лікування всіх ГКС включає прийом ацетилсаліцилової кислоти (АСК) (300 мг), болюсне призначення гепарину та внутрішньовенну інфузію гепарину (за відсутності протипоказань); водночас рекомендується антиагрегантна терапія тикагрелором або клопідогрелем. Тикагрелор пацієнтам, які отримують тромболізис, не призначається. Забезпечують контроль болю за допомогою морфіну/фентанілу та кисню в разі гіпоксії. З метою зняття болю також можна використовувати нітрогліцерин сублінгвально або інфузійно. Проте в разі ішемії нижньої стінки ЛШ нітрогліцерин може спричинити виражену гіпотензію; його слід застосовувати з особливою обережністю (якщо взагалі доцільно). Подальше лікування ГКС залежить від того, чи це є ІМпST/ІМбпST або нестабільна стенокардія. У рекомендаціях AHA (2020) зазначається, що в разі ІМпST варто терміново провести катетеризацію та ЧКВ з початком часу процедури <90 хв. Рекомендується застосування тромболітика (тенектеплази тощо), якщо відсутня можливість провести ЧКВ менш ніж за 120 хв. У настановах AHA передбачено час «від дверей до голки» (тенектеплаза / інші тромболітики) <30 хв.
Обрання стратегії реперфузії у хворих на ЦД має базуватися на багатьох чинниках, зокрема оцінка клінічного статусу (гемодинамічна/електрична нестабільність, тривала ішемія), ускладнення ХКС, показання/протипоказання для проведення ЧКВ і дистальні анастомози за АКШ, ішемічне навантаження, ЕхоКГ оцінки функції ЛШ і будь-яких інших супутніх захворювань.
Знеболення
Для зменшення вираженості симптомів, пов’язаних з ішемією міокарда, пацієнтам із ГКСбпST рекомендується сублінгвальний прийом органічних нітратів швидкої дії. Внутрішньовенне введення наркотичного аналгетика (переважно морфіну) за ГКСбпST рекомендується для купірування больового синдрому, пов’язаного з ішемією міокарда, що зберігається на тлі застосування органічних нітратів нетривалої дії та блокаторів β-адренергічних рецепторів (ББ). Для хворих на ІМпST доцільним є внутрішньовенне введення морфіну. Відмінна риса ангінозного нападу при ІМ – слабка реакція чи взагалі відсутність реакції на нітрогліцерин. Однак, якщо ангінозний напад не слабшає через декілька хвилин після припинення дії провокувального чинника чи якщо напад розвинувся в спокої, пацієнту слід сублінгвально прийняти нітрогліцерин у дозі 0,4-0,5 мг або аерозольно (спрей).
Корекція гіпоксемії
Із метою усунення гіпоксемії (SaO2 <90% або PaO2 <60 мм рт. ст.) застосовується оксигенотерапія. У пацієнтів з ІМпST і тривалими ішемічними симптомами, АГ, серцевою недостатністю (СН) із метою симптоматичного лікування використовується внутрішньовенна інфузія нітратів (нітрогліцерину або ізосорбіду динітрату). Обмеження: відсутність протипоказань.
Бета-блокатори
Збереження ішемії міокарда в пацієнтів із ГКСбпST потребує якнайшвидшого призначення ББ (за відсутності протипоказань). Хворим з ІМпST і високим артеріальним тиском при збереженні симптомів ішемії міокарда, тахікардії рекомендується внутрішньовенне введення лікарського препарату з групи ББ. Умова: відсутність ознак гострої СН. Мета: контроль ішемії.
Блокатори кальцієвих каналів
Через відсутність доказів позитивного впливу на прогноз пацієнтам із ГКСбпST не рекомендується рутинне застосування блокаторів кальцієвих каналів.
Блокатори ренін-ангіотензин-альдостеронової системи
Інгібітори ангіотензинперетворювального ферменту (ІАПФ), блокатори рецепторів ангіотензину ІІ (БРА), антагоністи мінералокортикоїдних рецепторів (АМР):
▶ усім пацієнтам, які не мають протипоказань, рекомендується застосування ІАПФ;
▶ у хворих із ГКСбпST (за ФВ ЛШ ≤40%), АГ, ЦД, хронічною хворобою нирок доцільним є призначення ІАПФ;
▶ у пацієнтів із ГКСбпST (за непереносимості ІАПФ) варто використовувати БРА, переважно валсартан (якщо до препаратів цієї групи відсутні протипоказання);
▶ у пацієнтів із СН, зниженою ФВ ЛШ, ЦД або ІМ передньої стінки ЛШ доцільно використовувати раннє (в перші 24 год ІМпST) призначення ІАПФ;
▶ хворі на ГМбпST із СН або ЦД при ФВ ЛШ ≤40%, а також пацієнти з ГКСбпST та СН II-IV ФК за New York Heart Association при ФВ ЛШ ≤35%, які не мають істотного зниження функції нирок (рівень креатиніну в крові >221 мкмоль/л у чоловіків або >177 мкмоль/л у жінок) і гіперкаліємії (рівень K+ у крові >5,0 ммоль/л). Рекомендується до терапевтичних доз ІАПФ і ББ додати препарат із групи АМР (переважно еплеренон);
▶ у постінфарктний період (за верифікації хронічної СН і ФВ ЛШ <35%) використання максимально переносимих доз ІАПФ/БРА доцільно замінити на сакубітрил/валсартан.
Ліпідознижувальна терапія
• Під час госпіталізації всім пацієнтам із ГКСбпST, ІМпST (незалежно від вихідного рівня холестерину в крові) варто розпочати чи продовжити лікування високими дозами інгібіторів ГМГ-КоА‑редуктази (якщо відсутні протипоказання й високі дози статинів добре переносяться).
• Якщо в пацієнта в постінфарктний період (за використання максимально переносимої дози статину) концентрація холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у крові залишається підвищеною, рекомендується додати езетиміб.
• Якщо у хворого в постінфарктний період (за використання максимально переносимої дози статину в поєднанні з езетимібом) концентрація ХС ЛПНЩ у крові залишається підвищеною, варто додати препарат із групи блокаторів пропротеїнової конвертази субтилізин-кексинового типу 9 (PCSK9) (алірокумаб або еволокумаб).
Антитромботична терапія
На початку лікування для пацієнтів із ГКСбпST доцільним є використання потрійної антитромботичної терапії (поєднання АСК, інгібітора Р2Y12-рецепторів тромбоцитів і антикоагулянта) з подальшим переходом на вживання АСК з інгібітором Р2Y12-рецепторів тромбоцитів або поєднання апіксабану, дабігатрану етексилату, ривароксабану чи непрямих антикоагулянтів (антагоністів вітаміну K) з одним або двома антиагрегантами.
Антитромботична терапія в пацієнтів з ІМпST
Усім хворим за відсутності протипоказань (незалежно від вихідної стратегії реперфузії, інсульту) рекомендується тривалий (невизначено довгий) прийом АСК. У пацієнтів, які в попередній тиждень регулярно не вживали АСК, навантажувальна доза (LD) АСК становить 150-325 мг; постійна підтримувальна доза (MD) становить 75-100 мг 1 р/добу. АСК (після проведення первинного ЧКВ) за відсутності внутрішньочерепного крововиливу в анамнезі, тривалої кровотечі доцільно комбінувати з тикагрелором (LD – 180 мг, MD – 90 мг 2 р/добу протягом 12 міс). Мета: зниження сумарного ризику (смерті й ІМ), ризику тромбозу стента. У період подвійної антитромботичної терапії (DAPT) доцільним є використання інгібіторів протонної помпи. Щодо пацієнтів, які отримують антагоністи вітаміну K, то варто утриматися від парентерального використання антикоагулянтів (у т. ч. під час ЧКВ) за умови, що значення міжнародного нормалізованого відношення (МНВ) дорівнює чи перевищує 2,0 (для ЧКВ – 2,5). При меншому значенні МНВ рекомендується використання стандартного болюсу нефракціонованого гепарину (НФГ).
Парентеральне призначення антиагрегантів
У пацієнтів із ГКСбпST (в умовах широкого застосування DAPT) парентеральне введення інгібіторів глікопротеїнових рецепторів (GP) IIb/IIIa тромбоцитів рекомендується тільки як рятівний засіб у разі виникнення тромботичних ускладнень або феномена slow/no-reflow під час проведення ЧКВ.
Внутрішньовенна інфузія НФГ (у комплексі з тромболітичною терапією) рекомендується для підтримки реперфузії (зниження ризику тромботичних ускладнень) у випадках, коли фондапаринукс натрію й еноксапарин протипоказані (зокрема, через виражену ниркову недостатність).
Антитромботична терапія у хворих на ЦД і ГКС
Хворі на ЦД і пацієнти з фізіологічним глюкозотолерантним тестом (ГТТ) повинні отримувати однакові лікарські препарати в однакових дозуваннях. Результати TRITON-TIMI та PLATO досліджень продемонстрували, що інгібітори P2Y12 (прасугрель і тикагрелор) довели вищу ефективність порівняно з клопідогрелем. Використання інгібіторів GP IIb/IIIa сприяло зменшенню смертності у хворих на ЦД із ГКСбпST у період до застосування клопідогрелю, але їхнє значення слід докладніше вивчити. Тієнопіридини як антитромботичні лікарські засоби застосовуються рідше у хворих на ЦД, ніж у пацієнтів із фізіологічним ГТТ, що негативно впливає на показники летальності. DAPT з АСК і клопідогрелем вважається стандартом у лікуванні людей із ГКСбпST. Незважаючи на використання DAPT, рецидиви атеротромботичних подій продовжують спостерігатися (особливо у хворих на ЦД).
Інше медикаментозне лікування
ЦД 2 типу в пацієнта з ГКСбпST – необов’язкове показання до переведення на інсулінотерапію. Якщо у хворого з ЦД 2 типу з’явилася потреба у використанні інсуліну, після стабілізації стану рекомендується перехід на пероральні цукрознижувальні засоби.
Інвазивне лікування
У пацієнтів із ГКСбпST (у стаціонарних умовах) на підставі оцінки ризику несприятливого результату рекомендується обрати та реалізувати одну зі стратегій лікування – КГ із наміром виконати реваскуляризацію міокарда (транслюмінальну балонну ангіопластику та стентування КА чи АКШ у перші 2-72 год після госпіталізації чи спочатку неінвазивне лікування).
У більшості хворих з ураженням однієї КА відразу після проведення КГ варто провести ЧКВ у ділянці оклюзії. Обрання методу реваскуляризації (в пацієнтів з ураженням декількох КА) потребує спеціального обговорення з урахуванням клінічного стану хворого, переваг методу реваскуляризації, поширеності й особливостей коронарного атеросклерозу, наявності супутніх захворювань, можливості тривалий час використовувати DAPT, потреби в тривалому використанні антикоагулянтів.
Особливості інвазивного лікування ГКСбпST у пацієнтів із ЦД
Для лікування хворих із ГКСбпST і ЦД рекомендується:
• використання інвазивної стратегії лікування;
• у стабілізованих хворих на ЦД і ГКСбпST (з ураженням декількох КА) та прийнятним хірургічним ризиком краще проводити АКШ;
• при проведенні ЧКВ у пацієнтів із ГКСбпST і ЦД рекомендується використовувати сучасні стенти для КА (коронарні стенти), що виділяють лікарський препарат, або коронарні стенти зі спеціальним антипроліферативним лікарським покриттям).
Вторинна профілактика ГКС без підйому ST
◆ Зміна стилю життя, дотримання рекомендованої дієти та режиму фізичної активності.
◆ Якнайраніше розпочати терапію статинами та продовжувати її впродовж невизначеного часу.
◆ Якщо не вдається досягти цільового рівня ХС ЛПНЩ (<1,8 ммоль/л), варто додати езетиміб.
◆ ІАПФ за дисфункції ЛШ (ФВ <40%) або в разі клінічних ознак СН та/або супутньої АГ (цільовий рівень АТ ≤140/90 мм рт. ст., при ЦД ≤130/85 мм рт. ст.).
◆ Можлива альтернатива – БРА (зокрема, при незадовільній переносимості ІАПФ).
◆ ББ – за відсутності протипоказань.
◆ Антагоністи альдостерону (еплеренон) – у разі зниженої функції ЛШ (ФВ <40%) або клінічних ознак СН та/або ЦД.
Лікування хворих із ГКСбпST і ЦД
→ Визначення рівня глюкози/HbA1c у крові має бути проведено негайно під час надходження до стаціонару хворого з ГКСбпST (або в разі обґрунтованої підозри на нього).
→ Зниження рівня глюкози потрібно проводити за гіперглікемії >10 ммоль/л, ретельно контролюючи результати лікування, щоб не допустити стану гіпоглікемії.
→ Контролювати стан функції нирок, намагаючись мінімізувати кількість контрасту, що використовується за КА чи ЧКВ (особливо у хворих із початково порушеною функцією нирок або в тих пацієнтів, які отримують метформін). У цієї групи хворих рання інвазивна тактика є кращою за консервативне лікування.
→ Оптимальні результати досягаються при використанні сучасних стентів із лікарським антипроліферативним покриттям.
→ Медикаментозна терапія (в т. ч. антитромботична) за умови ретельного контролю стану функції нирок є такою самою, як і у хворих без ЦД.
→ Моніторинг хворих найкраще проводити міжпрофесійною групою, до складу котрої входять лікар відділення невідкладної допомоги, кардіолог, ендокринолог, фармацевт і первинні медичні працівники.