31 березня, 2016
Молекулярно-генетичні аспекти патогенезу раку яєчників

 Протягом останніх 50 років рак яєчника (РЯ) залишається основною причиною смерті онкогінекологічних хворих, особливо в індустріально розвинених країнах. Смертність від РЯ перевищує смертність від усіх онкогінекологічних захворювань разом узятих [1, 2] і посідає п’яте місце серед причин смерті від усіх злоякісних пухлин у жінок [2, 3]. Високі показники смертності при РЯ зумовлені тим, що початкові стадії (І-ІІ) захворювання діагностують лише у третини вперше виявлених хворих, а поширені форми становлять 70% спостережень [4]. П’ятирічна виживаність при РЯ становить 20-25% [2, 4]. Хоча Україна належить до країн, що розвиваються, за даними Національного канцер-реєстру, показники захворюваності досить високі – 15,5 на 100 тис. жіночого населення з тенденцією до зростання за стабільно високих показників смертності – 8,1 на 100 тис. Протягом одного року після встановлення діагнозу РЯ помирає 40,2% з уперше виявлених хворих [5, 6]. Колосальні зусилля з покращення ранньої діагностики, зокрема протеомікс білкових молекул, асоційованих з РЯ, високоінформативні променеві методи діагностики, зусилля, спрямовані на лікування поширених форм РЯ (агресивне хірургічне та інтенсивне медикаментозне), не вплинули на цю сумну статистику. Однією з фундаментальних причин відсутності позитивної динаміки в розв’язанні проблеми РЯ може бути хибність нашого розуміння природи цього захворювання.
Протягом останніх 50 років рак яєчника (РЯ) залишається основною причиною смерті онкогінекологічних хворих, особливо в індустріально розвинених країнах. Смертність від РЯ перевищує смертність від усіх онкогінекологічних захворювань разом узятих [1, 2] і посідає п’яте місце серед причин смерті від усіх злоякісних пухлин у жінок [2, 3]. Високі показники смертності при РЯ зумовлені тим, що початкові стадії (І-ІІ) захворювання діагностують лише у третини вперше виявлених хворих, а поширені форми становлять 70% спостережень [4]. П’ятирічна виживаність при РЯ становить 20-25% [2, 4]. Хоча Україна належить до країн, що розвиваються, за даними Національного канцер-реєстру, показники захворюваності досить високі – 15,5 на 100 тис. жіночого населення з тенденцією до зростання за стабільно високих показників смертності – 8,1 на 100 тис. Протягом одного року після встановлення діагнозу РЯ помирає 40,2% з уперше виявлених хворих [5, 6]. Колосальні зусилля з покращення ранньої діагностики, зокрема протеомікс білкових молекул, асоційованих з РЯ, високоінформативні променеві методи діагностики, зусилля, спрямовані на лікування поширених форм РЯ (агресивне хірургічне та інтенсивне медикаментозне), не вплинули на цю сумну статистику. Однією з фундаментальних причин відсутності позитивної динаміки в розв’язанні проблеми РЯ може бути хибність нашого розуміння природи цього захворювання.
Класична концепція патогенезу епітеліального РЯ ґрунтувалася на положенні про те, що всі нозологічні форми РЯ походять з поверхневого незрілого целомічного епітелію, що вкриває поверхню яєчника, або з кортикальних інклюзивних кіст, утворених цим епітелієм [4, 7]. У результаті метапластичних змін целомічний епітелій здатен диференціюватися в епітелій серозного, муцинозного, ендометріоїдного типів тощо. Через нагромадження мутацій виникають відповідні варіанти РЯ, серед яких більшість (70%) становлять високозлоякісні серозні карциноми. Усі епітеліальні злоякісні пухлини яєчника вважалися однією хворобою. Водночас залишалося нез’ясованим, які процеси передують виникненню РЯ (кісти? пограничні пухлини?) та який стан слід вважати передраком яєчника, що до деякої міри зумовлювало невисоку ефективність запропонованих скринінгових програм [3].
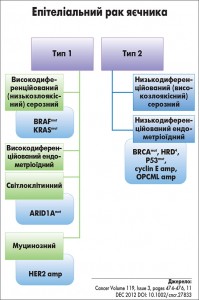
Клінічні спостереження та фундаментальні дослідження останнього десятиліття змусили переглянути традиційну концепцію патогенезу РЯ. Усе більш очевидною ставала гетерогенність цього захворювання. На підставі ґрунтовного молекулярно-генетичного та клініко-морфологічного аналізу I.-M. Shih та R. Kurman вперше сформулювали принципово нову дуалістичну модель патогенезу РЯ, яка розподіляє всі типи яєчникових карцином на дві категорії: І тип – низькозлоякісні, ІІ тип – високозлоякісні [8].
До пухлин І типу – низькозлоякісних – віднесли спочатку низькозлоякісний серозний, ендометріоїдний, муцинозний, світлоклітинний РЯ. Вони схильні до повільного росту, мають торпідний перебіг, у клінічній практиці зустрічаються у вигляді великих кістоподібних мас без перитонеальної дисемінації. Незважаючи на великі розміри пухлин, їх виявляють переважно в І стадії. Для пухлин І патогенетичного типу характерна невисока чутливість до цитостатиків. Низькозлоякісні (високодиференційовані) серозні карциноми (НЗСК) часто асоційовані з мутаціями KRAS, BRAF, PTEN, PIK3CA, CTNNB1, ARID1A, PPP2RIA, що призводять до пошкодження сигнальних шляхів [9-14]. Мутації генів KRAS, BRAF, ERBB2 було ідентифіковано також у серозних пограничних пухлинах, причому типи мутацій були однакові в проліферуючих кістах з атипією та в 2/3 НЗСК [9-14]. Тому пограничні пухлини яєчників обґрунтовано можна вважати передраковими станами НЗСК [11, 12]. Пухлини І патогенетичного типу є генетично нестабільними, проте виявлені генетичні зміні притаманні лише цьому типу. Shih та співавт. продемонстрували окремий тип метилювання ДНК, який зустрічається при серозних цистаденомах, пограничних та НЗСК, проте ніколи не виявляється при високозлоякісних серозних карциномах [15].
Пухлини ІІ патогенетичного типу добре відомі клініцистам як високозлоякісні, агресивні. Їх виявляють на поширених ІІІ-ІV стадіях з вираженим карциноматозом, навіть якщо ураження яєчників має зовсім невеликі розміри. Для пухлин ІІ патогенетичного типу характерна швидка прогресія та висока летальність, незважаючи на первинно високий рівень відповіді на хіміотерапію. До них віднесли серозні низькодиференційовані високозлоякісні та низькодиференційовані ендометріоїдні карциноми. Саме вони становлять майже 75% усіх випадків РЯ. У 95% пухлин ІІ патогенетичного типу виявляють мутації ТР53 [16], але не знаходять мутацій, притаманних низькозлоякісним формам РЯ. На момент діагностики вони демонструють значну кількість хромосомних аберацій, але в ході розвитку хвороби залишаються генетично стабільними. У 50% спорадичних високозлоякісних серозних карцином зустрічається інактивація гена BRCA, зумовлена мутаціями або гіперметилюванням промотора (рис.).
Тривалий час передракові стани високозлоякісних серозних карцином (ВЗСК) яєчників залишалися невідомими. Відкриття, що висвітлило їх походження і принципово вплинуло на сучасну концепцію РЯ, сталося на початку тисячоліття під час аналізу операційного матеріалу профілактичних сальпінгоофоректомій у жінок з BRCA-мутаціями [17-23]. Дослідники сподівалися знайти початкові передракові зміни яєчників у здорових жінок з підвищеним генетичним ризиком. Проте результати досліджень не виявили змін у тканині видалених яєчників, натомість в епітелії фімбрій фаллопієвих труб було виявлено серозні інтраепітеліальні карциноми in situ [24]. Більше того, у серозних трубних інтраепітеліальних карциномах (СТІК) виявилися гіперекспресованими продукти тих самих онкогенів – циклін Е1, Rsf-1, синтетаза жирних кислот, що і у ВЗСК. Гіперекспресованим був також мутантний білок ТР53. Причому типи мутацій СТІК та ВЗСК яєчників були однаковими [17, 20, 26]. Ці факти свідчили, що СТІК можуть бути передраком для ВЗСК. Отже на підставі молекулярних досліджень отримано докази трубного (фімбріального) походження принаймні BRCA-позитивних ВЗСК [17, 25]. Чому ж раніше СТІК не розглядали як передрак яєчника? Очевидною є причина – передракові патологічні зміни яєчника шукали в самому яєчнику. Дослідження труб здійснювалося в доволі обмеженому обсязі (переважно 1-2 зрізи в ампулярній частині з ділянкою фімбрій або без неї). Сьогодні Американська асоціація директорів відділів хірургічної патології рекомендує 2-етапний підхід до дослідження труб залежно від ризику наявності СТІК. Має бути зроблено мінімально по три зрізи в істмічній, ампулярній та фімбріальній частинах із кроком у 2-3 мм. Такий підхід аналогічний SEE-FIM протоколу, запропонованому Medeiros при дослідженні матеріалу від жінок з мутаціями BRCA1 та BRCA2 [21].
Наступні серії досліджень фаллопієвих труб у хворих зі спорадичними ВЗСК (без мутацій BRCA) згідно з SEE-FIM протоколом [16] виявили СТІК у 45-60% [26, 27]. Це дозволило зробити висновок про те, що спорадичні ВЗСК, подібно до тих, що виникли в жінок з вродженими BRCA-мутаціями, виникають зі СТІК [19]. Водночас СТІК були виявлені лише при ВЗСК, але не при ендометріоїдному, світлоклітинному, муцинозному РЯ. Молекулярно-генетичні дослідження показали, що СТІК мають коротші теломери, ніж ВЗСК [27]. Саме цей важливий факт більше, ніж будь-який інший, свідчить про те, що СТІК є джерелом ВЗСК, а не навпаки.
Проте СТІК знайдені в 66% досліджених ВЗСК. Звідки взялася решта?
Другий можливий механізм розвитку ВЗСК, на думку R. Kumar, – імплантація нормального фімбріального епітелію на оголеній після овуляції поверхні яєчника. Цей епітелій здатен формувати кортикальні інклюзивні кісти, які можуть зазнавати злоякісної трансформації [8]. Отже частина серозних пухлин може виникати з інклюзивних кіст, як припускалося раніше, але не з целомічного, а з імплантованого трубного (мюлерового типу) епітелію.
Таким чином, основний висновок дуалістичної моделі патогенезу РЯ про те, що більшість найагресивніших форм РЯ виникає за межами яєчників, може допомогти у створенні нових підходів до профілактики, скринінгу та лікування РЯ. Виявлення жінок – носіїв вроджених мутацій BRCA1, BRCA2 та інших генів, що кодують ДНК репарази, забезпечує ефективну профілактичну стратегію щодо ВЗСК. Саме для таких жінок двобічна сальпінгектомія зі збереженням яєчників може виявитися ефективним засобом зниження ризику розвитку цього найпоширенішого типу РЯ. Такий висновок представлений у матеріалах 61-ї щорічної конференції Американської колегії акушерів-гінекологів [28]. Він став обґрунтуванням для видалення фаллопієвих труб при проведенні гістеректомій, що можуть виконуватися за різними показаннями і за відсутності обтяженого генетичного анамнезу [29].
Дуалістична модель патогенезу РЯ, сконцентрована на серозних типах пухлин, не пояснювала походження високодиференційованого ендометріоїдного та світлоклітинного РЯ. Нещодавно отримані докази того, що можливим гістогенетичним джерелом ендометріоїдних та світлоклітинних карцином можуть бути вогнища ендометріозу, що формуються як наслідок ретроградної менструації [30]. Висока частота мутацій РІ3К (phosphatidylinositol 3-kinase), її каталітичної субодиниці PIK3CA та тумор-супресорного гена АRID1A (AT-rich interactive domain-containing protein 1A) у вогнищах ендометріозу та в ендометріоїдних та світлоклітинних карциномах поєднали патогенетично ці захворювання [31, 32]. Ген АRID1A кодує BAF250a, компонент хроматин-ремоделюючого комплексу. Пошкодження цього гена знайдені тільки в ендометріоїдних та світлоклітинних карциномах, але не виявлялися в серозних пухлинах. Перев’язування труб запобігало виникненню ендометріоїдного та світлоклітинного раку, але не серозних карцином [33]. Отже є підстави вважати, що обидва типи пухлин походять з ендометріального епітелію. Цікаво, що в жінок, хворих на ендометріоз, у клітинах ендометрію виявлені ті самі генетичні пошкодження, що і у вогнищах ендометріозу. У жінок без ендометріозу генетичні пошкодження ендометрію були інакші [36].
У муцинозних карциномах виявлено такі ж мутації KRAS, що і в пограничних муцинозних пухлинах [34-36]. Гістогенетичне походження цих пухлин залишається нез’ясованим. Більшість із них демонструє гастроінтестинальну диференціацію. Менша частина диференціюється подібно до ендоцервікального епітелію. Зроблено припущення, що останні також походять із вогнищ ендометріозу [37]. Для муцинозних пухлин гастроінтестинального типу не виключено метастатичне походження зі шлунково-кишкового тракту (шлунок, апендикс). Виявлення мутацій, характерних для кожного типу пухлин яєчників, відкриває нові можливості для застосування таргетної терапії.
Таким чином, сьогодні термін «рак яєчників» є дещо застарілим, оскільки об’єднує різні захворювання, що розрізняються за епідеміологічними та генетичними факторами ризику, різними передраковими станами, молекулярними змінами під час онкогенезу, типом метастазування, відповіддю на хіміотерапію та прогнозом [38, 39]. При цьому більшість пухлин походить не з яєчникової тканини, а з епітелію труб, ендометрію, можливо, зі шлунково-кишкового тракту. Проте всі захворювання цієї групи об’єднує розповсюдження ракових клітин на яєчник. На підставі оцінки клінічного перебігу, гістопатології, імуногістохімії, молекулярної генетики виділено щонайменше п’ять типів пухлин: 1) низькодиференційована високозлоякісна серозна карцинома (ВЗСК – 70% від усіх нозологічних форм РЯ); 2) ендометріоїдна карцинома (ЕК – 10%); 3) світлоклітинна карцинома (СКК – 10%); 4) муцинозна карцинома (МК – 3%); 5) високодиференційована низькозлоякісна серозна карцинома (НЗСК – 5%) [40]. Зазначені пухлинні типи охоплюють 98% випадків РЯ і можуть бути діагностовані на рівні світлової мікроскопії. Завершується процес створення нової FIGO класифікації РЯ, яка би ґрунтувалася на визначенні цих основних п’яти типів пухлин [41].

Хоча термін «рак яєчників» є патогенетично неточним, модифікація термінології навряд чи відбудеться найближчим часом. Непідготовлена заміна може стати джерелом непорозумінь у науковій літературі та клінічній практиці. Тому наразі термін «рак яєчників» залишається. Проте всі, хто стикається з цією проблемою, мають усвідомлювати клінічну та гістогенетичну гетерогенність станів, які він об’єднує (таблиця).
Література
1. Weiderpass E. Malignant tumors of the female reproductive system / E. Weiderpass, F. Labreche // Saf Health Work 2012. – Vol. 3, N 3. – Р. 166-180.
2. Cancer statistics, 2014 / R. Siegel, J. Ma, Z. Zou, A. Jemal // CA Cancer J Clin 2014. – N 64. – P. 9-29.
3. Crauford R. Ovarian cancer / R. Crauford, Yin-Ling Woo // Gynaecological Oncology: [Ed. M.I. Shafi, H. Earl, Li Tee Tan]. – Cambridge University Press, 2010. – P. 119-131.
4. Cannistra S.A. Ovarian cancer, fallopian tube carcinomaand peritoneal carcinoma / S.A. Cannistra, D.M. Gershenson, A. Recht // Principles and Practice of Oncology: [Ed. V.T. De Vita, T.S. Lawrence, S.A. Rosenberg]: [9th ed.]. – Philadelphia: Lippincott, Williams, Wilkins, 2011. – P. 1368-1391.
5. Рак в Україні: 2013-2014. Захворюваність, смертність, показники онкологічної служби // Бюлетень національного канцер-реєстру України. – Видання № 16. – К., 2015.
6. Воробьева Л.И. Гормональный канцерогенез и обоснование применения гормональной терапии в лечении больных раком яичника (обзор литературы) / Л.И. Воробьева, В.С. Свинцицкий, Ю.Г. Ткаля // Клин. онкология. – 2013. – Т. 1, № 9. – С. 56-64.
7. Copeland L.J. Epithelial Ovarian Cancer // DiSaia P., Creasman W. Clinical Gynecologic oncology. – 2007. – P. 313-367.
8. Kurman R.J., Shih le M. The origin and pathogenesis of epithelial ovarian cancer: a proposed unifying theory. Am J Surg Pathol 2010; 34. – P. 433-443.
9. Seidman J.D., Kurman R.J. Ovarian serous borderline tumors: a critical review of the literature with emphasis on prognostic indicators. Hum Pathol 2000; 31. – P. 539-557.
10. Longacre T.A., McKenney J.K., Tazelaar H.D., Kempson R.L., Hendrickson M.R. Ovarian serous tumors of low malignant potential (borderline tumors): outcome-based study of 276 patients with long-term (> or =5-year) follow-up. Am J Surg Pathol 2005; 29. – P. 707-723.
11. McKenney J.K., Balzer B.L., Longacre T.A. Lymph node involvement in ovarian serous tumors of low malignant potential (borderline tumors): pathology, prognosis, and proposed classification. Am J Surg Pathol 2006; 30. – P. 614-624.
12. Patterns of p53 mutations separate ovarian serous borderline tumors and low- and high-grade carcinomas and provide support for a new model of ovarian carcinogenesis: a mutational analysis with immunohistochemical correlation / G. Singer, R. Stоhr, L. Cope et al. // Am J Surg Pathol 2005. – Vol. 29, N 2. – P. 218-224.
13. Nakayama K., Nakayama N., Kurman R.J., Cope L., Pohl G., Samuels Y., Velculescu V.E., Wang T.L., Shih le M. Sequence mutations and amplification of PIK3CA and AKT2 genes in purified ovarian serous neoplasms. Cancer Biol Ther 2006; 5. – P. 779-785.
14. Mutations in BRAF and KRAS characterize the development of low-grade ovarian serous carcinoma / G. Singer, R. Oldt III, Y. Cohen et al. // J Natl Cancer Inst 2003. – Vol. 95, N 6. – P. 484-486.
15. Shih le M., Chen L., Wang C.C., Gu J., Davidson B., Cope L., Kurman R.J., Xuan J., Wang T.L. Distinct DNA methylation profiles in ovarian serous neoplasms and their implications in ovarian carcinogenesis. Am J Obstet Gynecol 2010; 203. – P. 584 e581-582.
16. Ahmed A.A., Etemadmoghadam D., Temple J., Lynch A.G., Riad M., Sharma R., Stewart C., Fereday S., Caldas C., Defazio A., Bowtell D., Brenton J.D. Driver mutations in TP53 are ubiquitous in high grade serous carcinoma of the ovary. J Pathol 2010; 221. – P. 49-56.
17. Callahan M.J., Crum C.P., Medeiros F., Kindelberger D.W., Elvin J.A., Garber J.E., Feltmate C.M., Berkowitz R.S., Muto M.G. Primary fallopian tube malignancies in BRCA-positive women undergoing surgery for ovarian cancer risk reduction. J Clin Oncol 2007; 25. – P. 3985-3990.
18. Carcangiu M.L., Radice P., Manoukian S., Spatti G., Gobbo M., Pensotti V., Crucianelli R., Pasini B. Atypical epithelial proliferation in fallopian tubes in prophylactic salpingo-oophorectomy specimens from BRCA1 and BRCA2 germline mutation carriers. Int J Gynecol Pathol 2004; 23. – P. 35-40.
19. Colgan T.J., Murphy J., Cole D.E., Narod S., Rosen B. Occult carcinoma in prophylactic oophorectomy specimens: prevalence and association with BRCA germline mutation status. Am J Surg Pathol 2001; 25. – P. 1283-1289.
20. Finch A., Shaw P., Rosen B., Murphy J., Narod S.A., Colgan T.J. Clinical and pathologic findings of prophylactic salpingo-oophorectomies in 159 BRCA1 and BRCA2 carriers. Gynecol Oncol 2006; 100. – P. 58-64.
21. Medeiros F., Muto M.G., Lee Y., Elvin J.A., Callahan M.J., Feltmate C., Garber J.E., Cramer D.W., Crum C.P. The tubal fimbria is a preferred site for early denocarcinoma in women with familial ovarian cancer syndrome. Am J Surg Pathol 2006; 3. – P. 230-236.
22. Paley P.J., Swisher E.M., Garcia R.L., Agoff S.N., Greer B.E., Peters K.L., Goff B.A. Occult cancer of the fallopian tube in BRCA-1 germline mutation carriers at prophylactic oophorectomy: a case for recommending hysterectomy at surgical prophylaxis. Gynecol Oncol 2001; 80. – P. 176-180.
23. Shaw P.A., Rouzbahman M., Pizer E.S., Pintilie M., Begley H. Candidate serous cancer precursors in fallopian tube epithelium of BRCA1/2 mutation carriers. Mod Pathol 2009; 22. – P. 1133-1138.
24. Dysplastic changes in prophylactically removed Fallopian tubes of women predisposed to developing ovarian cancer / J.M. Piek, P.J. van Diest, R.P. Zweemer // J Pathol 2001. – Vol. 195, N 4. – P. 451-456.
25. Intraepithelial carcinoma of the fimbria and pelvic serous carcinoma: Evidence for a causal relationship / D.W. Kindelberger, Lee Y., A. Miron et al. // Am J Surg Pathol 2007. – Vol. 31, N 2. – P. 161-169.
26. Sehdev A.S., Kurman R.J., Kuhn E., Shih le M. Serous tubal intraepithelial carcinoma upregulates markers associated with high-grade serous carcinomas including Rsf-1 (HBXAP), cyclin E and fatty acid synthase. Mod Pathol 2010; 23. – P. 844-855.
27. Kuhn E., Meeker A., Wang T.L., Sehdev A.S., Kurman R.J., Shih le M. Shortened telomeres in serous tubal intraepithelial carcinoma: an early event in ovarian high-grade serous carcinogenesis. Am J Surg Pathol 2010; 34. – P. 829-836.
28. ACOG News Releases May 8, 2013 New Orleans, LA. Wednesday Paper #1: Incorporating Routine Bilateral Salpingectomy at the Time of Hysterectomy with Ovarian Preservation.
29. J.N. McAlpine, G.E. Hanley, M.M. Woo, A.А. Tone et al. Opportunistic salpingectomy: uptake, risks, and complications of a regional initiative for ovarian cancer prevention. Amer J Obst and Gynecol 2014. – V. 210, N 5. – P. 471.e1–471.e11.
30. Bulun S.E. Endometriosis. N Engl J Med 2009; 360. – P. 268-279.
31. Kuo K.T., Mao T.L., Jones S., Veras E., Ayhan A., Wang T.L., Glas R., Slamon D., Velculescu V.E., Kuman R.J., Shih le M. Frequent activating mutations of PIK3CA in ovarian clear cell carcinoma. Am J Pathol 2009; 174. – P. 1597-1601.
32. Wiegand K.C., Shah S.P., Al-Agha O.M., Zhao Y., Tse K., Zeng T., Senz J., McConechy M.K. et al. ARID1A mutations in endometriosis-associated ovarian carcinomas. N Engl J Med 2010; 363. – P. 1532-1543.
33. Rosenblatt K.A., Thomas D.B. Reduced risk of ovarian cancer in women with a tubal ligation or hysterectomy. The World Health Organization Collaborative Study of Neoplasia and Steroid Contraceptives. Cancer Epidemiol Biomarkers Prev 1996; 5. – P. 933-935.
34. Gemignani M.L., Schlaerth A.C., Bogomolniy F., Barakat R.R., Lin O., Soslow R., Venkatraman E., Boyd J. Role of KRAS and BRAF gene mutations in mucinous ovarian carcinoma. Gynecol Oncol 2003; 90. – P. 378-381.
35. Mayr D., Hirschmann A., Lohrs U., Diebold J. KRAS and BRAF mutations in ovarian tumors: a comprehensive study of invasive carcinomas, borderline tumors and extraovarian implants. Gynecol Oncol 2006: 103. – P. 883-887.
36. Enomoto T., Weghorst C.M., Inoue M., Tanizawa O., Rice J.M. K-ras activation occurs frequently in mucinous adenocarcinomas and rarely in other common epithelial tumors of the human ovary. Am J Pathol 1991; 139. – P. 777-785.
37. Rutgers J.L., Scully R.E. Ovarian mullerian mucinous papillary cystadenomas of borderline malignancy. A clinicopathologic analysis. Cancer 1988; 61. – P. 340-348.
38. Gilks C.B. Ovarian carcinoma pathology and genetics: recent advances / C.B. Gilks, J. Prat // Hum Pathol 2009. – Vol. 40, N 9. – P. 1213–1223.
39. Prat J. Ovarian carcinomas: five distinct diseases with different origins, genetic alterations, and clinicopathological features / J. Prat // Virchows Arch 2012. – Vol. 460, N 3. – P. 237-249.
40. Surface epithelial stromal tumours: tumours of the ovary and peritoneum / K.R. Lee, F.A. Tavassoli, J. Prat et al. // World Health Organization Classification of Tumours: Pathology and Genetics of Tumours of the Breast and Female Genital Organs: [Ed. F.A. Tavassoli, P. Devilee]. – Lyon: IARC Press, 2003. – P. 117-145.
41. Prat J. Staging classification for cancer of the ovary, fallopian tube, and peritoneum / Int J Gyn Obst 2014; 124. – P. 1-5.