28 березня, 2016
Вемурафениб при высокодифференцированном серозном раке яичников c мутацией BRAF V600
В программе по изучению генома рака Cancer Genome Atlas и в других подобных проектах по исследованию наиболее распространенных типов опухолей мутация BRAF V600 была идентифицирована в различных немеланомных злокачественных новообразованиях, включая колоректальный рак, немелкоклеточный рак легких, папиллярный рак щитовидной железы, диффузные глиомы, холангиокарциному, волосатоклеточный лейкоз, множественную миелому, гистиоцитоз из клеток Лангерганса, болезнь Эрдгейма – Честера и др. Во многих опухолях мутация BRAF V600 ассоциируется с агрессивным фенотипом, сниженной безрецидивной и общей выживаемостью. Вемурафениб – таргетный препарат, ингибитор V600E-мутированного BRAF, продемонстрировавший высокую эффективность в лечении меланомы и одобренный FDA по этому показанию в 2011 г. Ниже представлено клиническое наблюдение пациентки с высокодифференцированным серозным раком яичников (ВДСРЯ), ранее получившей несколько линий терапии, у которой лечение вемурафенибом обеспечило стойкий симптоматический, радиологический и биохимический ответ.
Клинический случай
Пациентка 74 лет поступила на лечение в госпиталь им. Жоржа Помпиду (Франция). Двенадцать лет назад (в 2003 г.) у нее был диагностирован ВДСРЯ. В 1970 г. перенесла овариэктомию справа по поводу пограничной серозной опухоли яичника, в 1973 г. – гистерэктомию с овариэктомией слева по поводу контралатерального рецидива. Тридцать лет спустя (в 2003 г.) появилась боль в малом тазу, произошла компрессия правого мочеточника и была диагностирована нерезектабельная высокодифференцированная папиллярная серозная аденокарцинома IVB стадии по классификации FIGO с метастазами в наддиафрагмальных лимфатических узлах. Иммуногистохимическое исследование свидетельствовало в пользу гинекологического происхождения опухоли (AE1/AE3+, CK7+, CK20-).
С 2003 по 2011 г. заболевание удавалось контролировать несколькими линиями платиносодержащей химиотерапии (в комбинации с паклитакселом, пегилированным липосомальным доксорубицином или гемцитабином), гормонотерапии (тамоксифен, ингибитор ароматазы) и терапии бевацизумабом. Ни одна из этих схем не обеспечила объективного ответа по критериям RECIST, однако у пациентки наблюдалась стабилизация заболевания продолжительностью 3 года на фоне лечения бевацизумабом.
Биопсия шейного лимфоузла, проведенная в марте 2011 г., подтвердила ранее установленный диагноз высокодифференцированной серозной папиллярной аденокарциномы, положительной по рецепторам эстрогенов (ER) и отрицательной по рецепторам прогестерона (PR). Последующий молекулярный анализ показал отсутствие мутаций KRAS; в то же время была обнаружена мутация BRAF V600E. С июня 2011 по март 2013 г. пациентка получала паклитаксел 1 раз в неделю в монотерапии или в комбинации с экспериментальным препаратом моноклональных антител против HER3, что обеспечило стабилизацию заболевания.
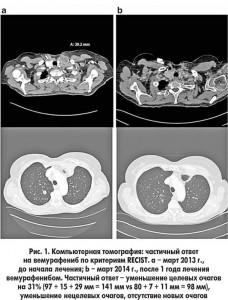
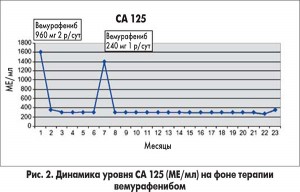
В апреле 2013 г. по данным компьютерной томографии (КТ) были выявлены метастазы в брюшине, лимфатических узлах и легких (рис. 1а), что сопровождалось повышением уровня ракового антигена (СА) 125 с 300 до 1600 МЕ/мл. 20 апреля 2013 г. начато лечение вемурафенибом в полной дозе (960 мг 2 р/сут). Однако через 10 дней терапию пришлось приостановить из-за кожной токсичности 3-й степени. Интересно, что за эти 10 дней практически полностью прошла боль в животе, а уровень СА 125 снизился до 360 МЕ/мл (рис. 2).
В сентябре 2013 г., после 4 мес без лечения, КТ выявила новые метастазы в брюшине, уровень СА 125 повысился до 1400 МЕ/мл. Было решено возобновить прием вемурафениба в значительно сниженной дозе – 240 мг/сут. Даже при использовании такой низкой дозы вемурафениб обеспечил частичный ответ (по критериям RECIST) в целевых и нецелевых очагах по данным КТ, при этом уровень СА 125 снизился до 300 МЕ/мл (рис. 1b; рис. 2), что сопровождалось полным купированием боли в животе, и на этот раз без токсических проявлений со стороны кожи. Заболевание оставалось контролированным с частичным ответом, продолжавшимся 1 год. Учитывая хорошую переносимость низкодозовой терапии вемурафенибом, в октябре 2014 г. было принято решение удвоить дозу до 2 таблеток в день (480 мг/сут). В декабре 2014 г., опасаясь потенциального клинического прогрессирования в лимфоузле (несмотря на хорошую переносимость терапии и стабилизацию заболевания с уровнем СА 125 265 МЕ/мл), пациентке увеличили дозу вемурафениба до 3 таблеток в день (720 мг/сут). В марте 2015 г. у пациентки отсутствовали симптомы, уровень СА 125 составлял 365 МЕ/мл, КТ-сканирование показало сохраняющийся частичный ответ. По состоянию на июнь 2015 г.: пациентка продолжает принимать вемурафениб; сохраняется частичный ответ по критериям RECIST и данным КТ; уровень СА 125 снизился до 300 МЕ/мл (ответ СА 125 по критериям GCIG); сохраняется симптоматический ответ; заболевание контролируется более 21 мес.
Обсуждение
Высокодифференцированный (low-grade) серозный рак яичников – относительно новое понятие, которое основано на двухуровневой системе классификации по степени дифференцировки, предложенной Anderson и впоследствии принятой Комитетом по редким опухолям Гинекологической онкологической группы (GOG). ВДРСЯ часто (в 60% случаев) ассоциируются с серозными опухолями с низким злокачественным потенциалом, также известными как серозные пограничные опухоли.
В отличие от низкодифференцированного (high-grade) серозного рака яичников, ВДСРЯ является медленнорастущей опухолью. У пациенток, которых можно прооперировать, полная резекция способна оказывать существенное положительное влияние на прогноз. Однако в нерезектабельных случаях объективный ответ на химиотерапию удается получить очень редко. Ретроспективный анализ 58 пациенток с рецидивным ВДРСЯ показал, что общая частота ответа в платиночувствительной и платинорезистентной когортах была 4,9 и 2,1% соответственно. Стабилизация заболевания наблюдалась у 60% больных. Медиана времени до прогрессирования составила 29,0 недель с существенной разницей между платиночувствительной и платинорезистентной когортами (34,7 vs 26,4 недель соответственно). Медиана общей выживаемости – 87,1 мес.
Несмотря на то что рак яичников является гетерогенным заболеванием, в последние годы при всех эпителиальных злокачественных новообразованиях яичника применяется единый подход к лечению, и специфическая терапия ВДРСЯ не разработана. В серии случаев и в ретроспективном анализе были получены данные об определенной эффективности бевацизумаба. При ВДРСЯ, положительном по рецепторам эстрогенов и/или прогестерона, может применяться гормонотерапия.
По своей биологии ВДРСЯ значительно отличается от высокодифференцированного серозного рака яичников. Двухуровневая система классификации позволила лучше понять патофизиологию ВДРСЯ. В частности, было установлено, что это заболевание характеризуется высокой частотой мутаций в сигнальном пути МАР-киназы (МАPK), низкой частотой мутации гена р53, более высокой экспрессией ER и PR, а также РАХ2 и IGF-1. Сигнальный путь MAPK играет важную роль в прогрессировании ВДРСЯ. Около 30% низкодифференцированных серозных пограничных карцином содержат мутацию KRAS, а мутации BRAF обнаруживаются примерно в 5% ВДРСЯ. В ретроспективном анализе 75 пациенток с высокодифференцированным серозным или серозным пограничным раком яичников мутации BRAF V600 присутствовали в 35% случаев. При этом наличие мутации BRAF V600 ассоциировалось с более ранней стадией заболевания и лучшим прогнозом. Интересно, что среди 22 пациенток, получавших химиотерапевтическое лечение в качестве адъювантной терапии или при прогрессировании заболевания, мутации BRAF V600 ни в одном случае обнаружены не были. В целом эти данные, а также приведенный клинический пример свидетельствуют о том, что вемурафениб имеет значительный терапевтический потенциал не только при меланоме, но и при других опухолях, содержащих мутацию BRAF V600.
Combe P., Chauvenet L., Lefrere-Belda M.A. et al. Sustained response to vemurafenib in a low grade serous ovarian cancer with a BRAF V600E mutation. Invest New Drugs. 2015 Dec; 33 (6): 1267-70.
Перевел с англ. Алексей Терещенко