22 січня, 2016
Трастузумаб для подкожного введения при HER2-положительном раке грудной железы: доказательная база и практический опыт в 7 клинических центрах Германии
Таргетная анти-HER2 терапия моноклональным антителом трастузумаб (Герцептин®) на сегодня является стандартным лечением пациентов с ранним и метастатическим раком грудной железы (РГЖ), положительным по рецепторам эпидермального фактора роста человека 2 типа (HER2). Пациенты с РГЖ ранних стадий получают трастузумаб в качестве адъювантной терапии длительностью 1 год. У больных с метастатическим РГЖ лечение трастузумабом обычно продолжается до прогрессирования заболевания или дольше.
Еще недавно трастузумаб назначался только внутривенно. Доза препарата определялась в зависимости от массы тела пациента. Чтобы достичь быстрого насыщения рецепторов HER2, лечение начинали с более высокой нагрузочной дозы, после чего препарат назначался в более низкой дозе для поддержания терапевтического уровня трастузумаба в крови.
В августе 2013 г. стала доступной подкожная (п/к) форма трастузумаба, предназначенная для лечения пациентов с HER2-положительным РГЖ. Трастузумаб для п/к введения назначается в фиксированной дозе 600 мг (независимо от массы тела пациента) в фиксированном объеме 5 мл, при этом нагрузочная доза не требуется. Введение препарата занимает не более 5 мин, тогда как на инфузию внутривенного (в/в) трастузумаба требуется 90 мин при назначении нагрузочной дозы и 30 мин при последующих инфузиях. Длительность наблюдения за пациентом после введения обеих форм трастузумаба одинаковая.
В данной статье рассмотрены результаты основных исследований с п/к трастузумабом и представлен опыт использования препарата в 7 клинических центрах Германии за период 18 мес.
Разработка п/к формы трастузумаба
Инъекционный объем п/к трастузумаба составляет 5 мл. Введение объемов >2 мл обычно является болезненным и ограничивается физиологией внеклеточного матрикса подкожной ткани. Объединение трастузумаба с рекомбинантной гиалуронидазой человека (rHuPH20) позволяет временно устранить этот барьер (который состоит из волокнистых белков, гиалуроновой кислоты, гликозаминогликанов и других сложных линейных полисахаридов), что обеспечивает легкость и безболезненность п/к введения трастузумаба.
Чтобы максимально упростить назначение и исключить ошибки, связанные с выбором дозировки, для п/к трастузумаба была разработана фиксированная доза, не зависящая от массы тела пациента. Назначение фиксированной дозы 600 мг позволяет поддерживать достаточную концентрацию в крови и насыщение рецепторов HER2 уже с первого цикла лечения.
В исследовании III фазы HannaH 596 пациентов с HER2-положительным неметастатическим местнораспространенным РГЖ в дополнение к неоадъювантной химиотерапии получали трастузумаб п/к в фиксированной дозе 600 мг (n=297) или трастузумаб в/в (8 мг/кг нагрузочная доза, затем 6 мг/кг) (n=299) 1 р/3 нед. Сывороточная концентрация препарата непосредственно перед хирургическим вмешательством составила 69,0 нг/мл в группе п/к введения и 51,8 нг/мл в группе в/в введения. Полная патологическая ремиссия была достигнута у 45,4 vs 40,7% пациентов соответственно. По частоте неблагоприятных событий і3 степени группы не различались.
Анализ результатов исследования, представленный на конгрессе Американского общества клинической онкологии (ASCO) в 2015 г., показал, что достижение полной патологической ремиссии, определяемой как отсутствие инвазивных опухолевых клеток в грудной железе и в подмышечных лимфоузлах, ассоциировалось с достоверно высшей выживаемостью без событий независимо от способа введения трастузумаба.
В настоящее время профиль безопасности трастузумаба для п/к введения оценивается в исследовании SafeHer, международном клиническом исследовании III фазы с участием 2500 пациентов с РГЖ ранних стадий, разделенных на две группы для применения трастузумаба п/к при помощи медперсонала (обычные шприц и игла) либо самостоятельно (одноразовый предварительно наполненный шприц).
Исследование PrefHer: опыт пациентов и медперсонала
В исследовании PrefHer оценивали предпочтение пациентами п/к или в/в формы трастузумаба, а также удовлетворенность медперсонала обоими вариантами терапии. Кроме того, изучали, какой способ п/к введения трастузумаба, по мнению пациентов, более предпочтителен: с использованием обычного шприца или одноразового предварительного наполненного шприца; а также затраты времени и ресурсов, соответствующих каждому методу применения.
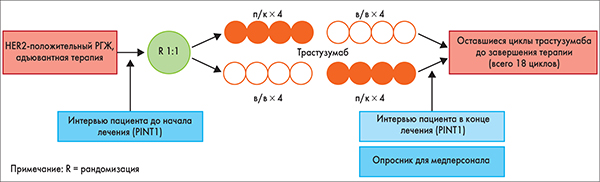
После завершения операции и химиотерапии (неоадъювантной или адъювантной) пациентов (n=488) рандомизировали на 2 группы. Пациенты группы А (n=245) получали адъювантную терапию, состоявшую из 4 циклов трастузумаба п/к (600 мг каждые 3 нед) и затем 4 циклов трастузумаба в/в (6 мг/кг каждые 3 нед). В группе Б (n=243) последовательность п/к и в/в назначения была обратной.
Пациенты также были разделены на две когорты. В 1 когорте трастузумаб вводился п/к с помощью одноразового инъекционного устройства, во 2 когорте применялся обычный шприц. После 8 циклов трастузумаб вводили в/в пациентам 1 когорты и в виде п/к инъекций больным 2 когорты. Всего пациенты обеих когорт получили 18 циклов терапии трастузумабом (рис. 1).
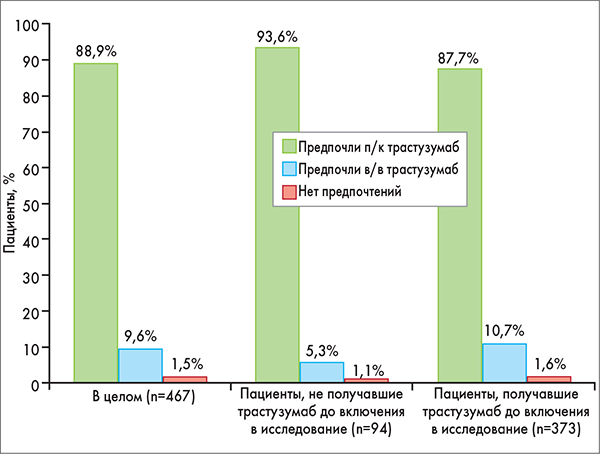
Результаты показали, что подавляющее большинство пациентов предпочли п/к способ введения трастузумаба – 88,9%, в то время как в/в способ – только 9,6% (р<0,0001); 1,5% не смогли отдать предпочтение тому или иному методу (рис. 2). Значительное преимущество п/к трастузумаба не зависело от последовательности назначения (п/к → в/в или в/в → п/к). В качестве наиболее важных причин выбора п/к формы пациенты назвали экономию времени (80,3%) и менее выраженные болевые ощущения (34,3%) (табл. 1).
При опросе медперсонала было установлено, что 77% предпочли п/к путь введения, 3,0% – в/в форму и 20% не имели предпочтений относительно способа введения препарата.
Исследование PreferHer-Time-and-Motion
В рамках клинического исследования PreferHer было проведено неинтервенционное субисследование PreferHer-Time-and-Motion, в котором собирали данные относительно времени, затрачиваемого пациентом и медперсоналом на назначение различных форм трастузумаба. В субисследовании приняли участие 17 клиник Канады, Дании, Франции, России, Испании и Швейцарии.
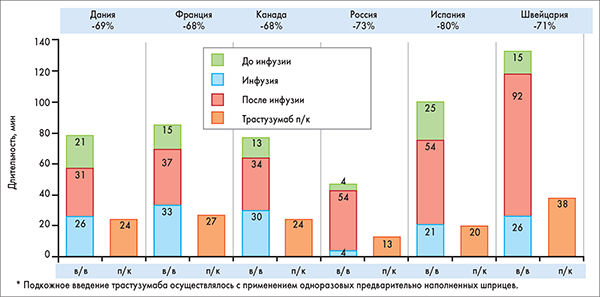
Полученные результаты существенно отличались в разных странах, однако во всех клиниках наблюдалась значительная экономия времени пациента при использовании п/к трастузумаба. В среднем каждая манипуляция длилась на 34-95 мин меньше по сравнению с в/в введением (рис. 3). При лечении 10 пациентов в год экономия времени составила от 103 ч (Россия) до 248 ч (Швейцария) для п/к vs в/в трастузумаба.
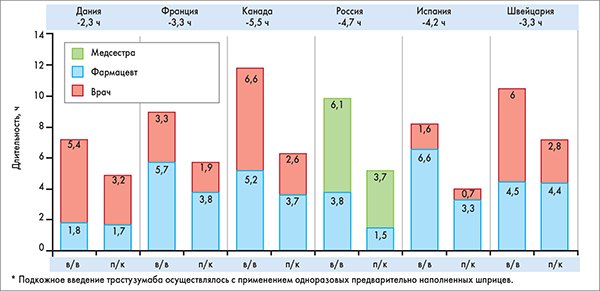
Активное время медперсонала включало сумму времени, затрачиваемого на все задачи, связанные с подготовкой и введением трастузумаба. По этому показателю п/к трастузумаб также продемонстрировал значительные преимущества: экономия времени при проведении 1 манипуляции составила 7,4-18,7 мин, при проведении 18 циклов для 1 пациента (1 год терапии) – 2,3-5,5 ч (рис. 4).
Временные затраты пациента и медперсонала при использовании п/к трастузумаба были ниже для обоих методов (с помощью обычного шприца или одноразового инъекционного устройства).
В субисследовании также было установлено, что переход с в/в на п/к форму препарата сопровождался значительными преимуществами для пациента, среднего медперсонала, врачей и клинического центра в целом, при этом наибольшую пользу получали пациенты.
Реальный клинический опыт применения п/к трастузумаба в Германии
Во всех 7 клинических центрах, принявших участие в проекте, основной причиной для перехода на п/к трастузумаб была потенциальная польза для пациентов. Существенным мотивационным фактором также стали результаты исследований HannaH и PrefHer.
В каждом центре лечение ежегодно проходили 100-600 больных с РГЖ ранних стадий и 20-180 пациентов с метастатическим РГЖ.
Выбор времени посещения клиники для введения трастузумаба был более гибким для п/к формы. В некоторых центрах визиты назначали строго в послеобеденное время.
Рекомендованная доза п/к трастузумаба составляла 600 мг независимо от массы тела пациента. Препарат назначали каждые 3 нед; на 1 введение тратилось 2-5 мин. В одних центрах введение препарата осуществляла медсестра, в других – врач или медсестра в зависимости от присутствия на рабочем месте.
Кроме пациентов – участников клинических исследований, за некоторыми исключениями всем больным предлагали выбрать один из способов введения трастузумаба. В трех центрах в/в назначение по схеме 1 р/нед осуществляли у пациентов высокого риска с кардиоваскулярными факторами риска; в одной клинике пациентам с дерматологическими заболеваниями, такими как псориаз, не рекомендовали п/к путь введения.
Во всех центрах предпочтение отдавали п/к трастузумабу в случаях, когда отсутствовала необходимость в одновременном назначении других препаратов.
Пациенты, получавшие химиотерапию или препараты моноклональных антител для в/в введения, обычно получали в/в трастузумаб, особенно при уже установленном центральном венозном катетере. В трех клиниках была поставлена задача перевести всех пациентов, получавших в/в трастузумаб, на трастузумаб для п/к введения, при этом в подавляющем большинстве случаев больные предоставили свое согласие.
Приверженность пациентов к п/к трастузумабу была высокой во всех 7 клинических центрах. Большинство пациентов (70-90%) отдали предпочтение п/к способу введения. Практически во всех случаях при переходе на п/к трастузумаб были получены положительные отзывы, и комплайенс был очень высок. Важным преимуществом п/к формы препарата, по мнению пациентов, был более гибкий выбор времени посещения клиники, что облегчало интеграцию терапии в повседневную жизнь (например, введение препарата можно было осуществить утром до работы). Клиники отметили рост количества пациентов, активно интересующихся п/к трастузумабом, вероятно, благодаря обмену информации в самих учреждениях и на интернет-форумах.
Опыт применения п/к трастузумаба по отзывам медперсонала также был позитивным. Большинство опрошенных отметили более легкое введение п/к трастузумаба и большую гибкость в назначении визитов пациента в клинику. Последнее преимущество позволяло минимизировать переработки и поддерживать стабильность фонда заработной платы.
Обсуждение
Опыт применения п/к трастузумаба в 7 клинических центрах во многих аспектах отражает результаты исследования PrefHer. Пациенты явно предпочитали п/к введение препарата. Большинство пациентов ранее получали в/в трастузумаб в комбинации с химиотерапией и, следовательно, имели возможность сравнить два пути введения. Как было продемонстрировано в субисследовании Time-and-Motion, п/к трастузумаб обеспечивает существенную экономию времени пациентов. Кроме того, пациенты отметили большую гибкость в выборе времени посещения клиники, что позволяло им жить более полноценной жизнью, пребывая на долгосрочной системной противоопухолевой терапии.
 Общая оценка клинических центров, использовавших п/к трастузумаб в течение 1 года и дольше, была положительной (табл. 2). Ожидания медперсонала относительно большей гибкости в проведении терапии полностью оправдались. Очевидно, наибольшими достижениями можно считать явные преимущества для пациентов и их более высокую удовлетворенность лечением. Трастузумаб для п/к введения предоставляет клиникам больше пространства для маневра, позволяя гибко выбирать время для визитов даже в случае нехватки персонала. Это имеет огромное значение, поскольку ряд факторов, таких как усложнение противоопухолевой терапии, недостаток квалицированных кадров и жесткое регулирование рабочего времени, затрудняют оказание амбулаторной онкологической помощи.
Общая оценка клинических центров, использовавших п/к трастузумаб в течение 1 года и дольше, была положительной (табл. 2). Ожидания медперсонала относительно большей гибкости в проведении терапии полностью оправдались. Очевидно, наибольшими достижениями можно считать явные преимущества для пациентов и их более высокую удовлетворенность лечением. Трастузумаб для п/к введения предоставляет клиникам больше пространства для маневра, позволяя гибко выбирать время для визитов даже в случае нехватки персонала. Это имеет огромное значение, поскольку ряд факторов, таких как усложнение противоопухолевой терапии, недостаток квалицированных кадров и жесткое регулирование рабочего времени, затрудняют оказание амбулаторной онкологической помощи.
Для клинических центров еще одной причиной перехода на п/к трастузумаб является безопасность. Фиксированная доза снижает риск ошибок в выборе дозировки. Кроме того, при терапии п/к трастузумабом используется оригинальное действующее вещество с доказанной эффективностью и хорошо изученным профилем безопасности.
В условиях реальной клинической практики п/к и в/в трастузумаб не различались по эффективности и переносимости; частота серьезных неблагоприятных событий при переходе на п/к путь введения не увеличилась.
Основной проблемой на сегодня является потребность в более честной системе реимбурсации. Все больше современных противоопухолевых препаратов назначаются перорально или подкожно, что, очевидно, занимает меньше времени по сравнению с в/в инфузией. Однако при использовании пероральных или п/к препаратов также необходимы значительные временные затраты среднего медперсонала и врачей, включающие консультирование пациентов и мониторинг побочных эффектов, которые в настоящее время не подлежат реимбурсации. Клинический центр, предлагающий своим пациентам более комфортный вид лечения, не должен испытывать из-за этого финансовых проблем только потому, что текущая политика реимбурсации не подразумевает адекватного возмещения затрат на этот сервис. По данным на декабрь 2014 г., назначение п/к трастузумаба едва достигло 14,0% всего количества препарата, назначаемого в Германии. За аналогичный период соответствующий показатель во Франции составил 23,7%, в Великобритании – 60,1%, а в Швеции – 76,4%. Онкологическая служба и система реимбурсации в этих странах отличаются от таковых в Германии. Очевидно, существует ряд причин неравного принятия новых методов терапии трастузумабом, несмотря на доказанную эффективность и предпочтения пациентов. Однако эти цифра также свидетельствуют о том, что доступ пациентов к современным противоопухолевым препаратам в значительной степени зависит от существующей системы реимбурсации.
Список литературы находится в редакции.
Статья печатается в сокращении.
Jackisch C., Muller V., Dall P. et al. Subcutaneous Trastuzumab for HER2-positive Breast Cancer – Evidence and Practical Experience in 7 German Centers. Geburtshilfe Frauenheilkd. 2015 Jun;75(6):566-573.
Перевел с англ. Алексей Терещенко