6 листопада, 2021
Закриті інфузійні системи – must-have відділення інтенсивної терапії
Пацієнти відділення інтенсивної терапії (ВІТ) мають підвищений ризик розвитку нозокоміальних інфекцій, у тому числі й інфекцій кровотоку, які значно збільшують тривалість перебування у стаціонарі, вартість лікування та смертність. Більшість інфекцій кровотоку пов’язані з використанням центральних венозних катетерів, без яких неможливо уявити медичну допомогу у ВІТ. У статті розглянуто особливості використання закритих інфузійних систем як способу зменшення захворюваності на інфекції кровотоку у пацієнтів ВІТ.
Ключові слова: закриті інфузійні системи, центральний венозний катетер, інфекції кровотоку.
Інфузійні системи для внутрішньовенного введення не є середньовічним винаходом, але ідея такого засобу лікування виникла у Середні віки. Того часу проводилися експерименти з метою переливання крові від людини тваринам, від людини людині, проте вони не мали успіху й невдовзі були заборонені офіційним наказом Ватикану. Перший вдалий інфузійний пристрій був створений англійським архітектором та математиком сером К. Реном (16321723): він складався зі свинячого міхура та пташиного пера для письма. Завдяки своєму винаходу Рену вдалося вводити сторонні речовини у кровоток собаки. Його інфузійний пристрій, хоча й був складним у застосуванні, проклав шлях до майбутніх інфузійних систем, які використовуються сьогодні.
На початку 30х років ХІХ ст. лікар Т. Латта у журналі The Lancet опублікував дані про ефективність введення у кров солоної води при лікуванні холери. Через декілька років лікарем Дж. Бланделлом було вперше виконано успішне переливання людської крові під час післяпологової кровотечі. Пізніше, у 1881 році, пацієнту було вперше успішно введено внутрішньовенно «фізіологічний розчин кухонної солі». Цікаво, що лише у 1940х роках медсестрам дозволили проводити внутрішньовенну терапію (до цього часу венопункція вважалася виключно лікарською маніпуляцією).
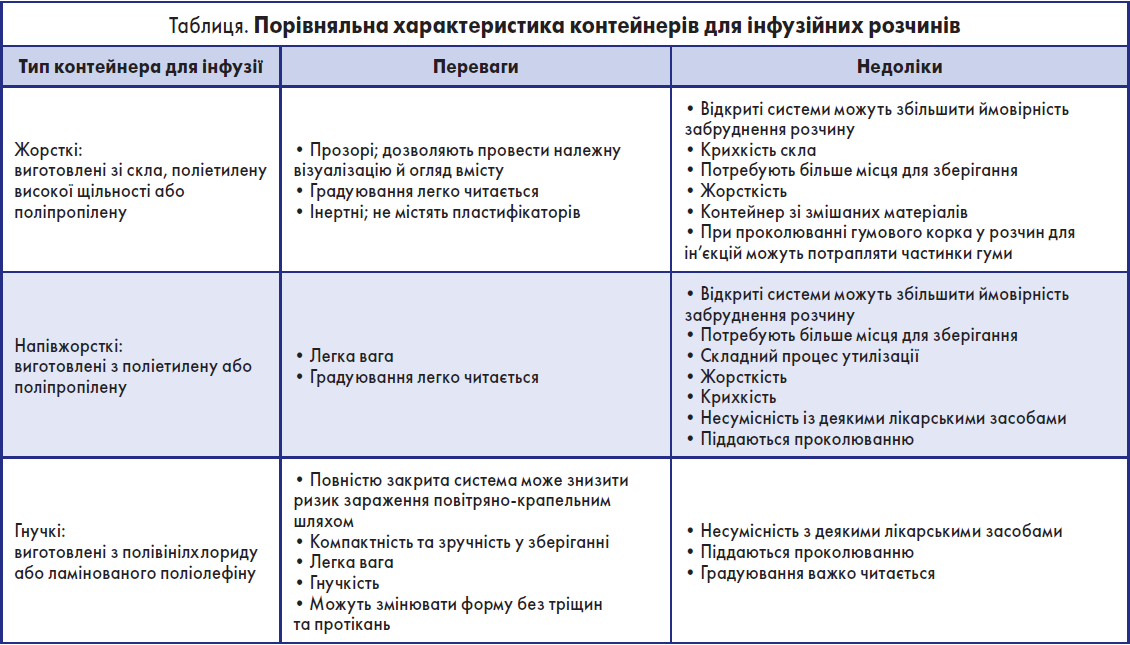
У першій половині ХХ ст. розчини для інфузії містилися у відкритих контейнерах, які накривали марлею, щоб запобігти забрудненню. У 1930х роках розчини почали зберігати у скляних вакуумних пляшках, а ще через кілька десятиліть – у поліетиленових пакетах. Сьогодні в усьому світі використовуються три типи контейнерів для інфузійних розчинів: жорсткі, напівжорсткі та гнучкі (таблиця), які є складовою двох типів інфузійних систем. Перший тип, відкриті інфузійні системи (використовуються жорсткі та напівжорсткі контейнери), потребує доступу повітря ззовні для спорожнення контейнера. Другий тип – закриті, що являють собою нерозбірну систему з гнучким контейнером, використання якої не потребує потрапляння повітря всередину [1].
Відкриті системи використовувалися у світовій практиці понад 75 років, доки у 1971 році у США не стався загальнонаціональний спалах інфекції Enterobacter cloacae, причиною якої було внутрішнє забруднення корків скляних пляшок із розчинами для внутрішньовенної інфузії одного американського виробника (CDC, 1971). До початку 1980х років Північна Америка та Західна Європа повсюдно перейшли на використання закритих систем [1].
Центральні венозні катетери (ЦВК) є найважливішими пристроями, які використовуються у пацієнтів ВІТ, адже вони дозволяють вводити лікарські засоби, розчини та продукти крові безпосередньо у центральну венозну систему, а також проводити гемодіалізну терапію та гемодинамічний моніторинг (Blot K. et al., 2014). Незважаючи на це ЦВК можуть піддавати тяжко хворих пацієнтів ризику розвитку ЦВКасоційованих інфекцій кровотоку (ЦВКАІК). ЦВКАІК визначаються як інфекції крові, що починаються щонайменше через 48 год після встановлення центрального катетера й не пов’язані з іншим джерелом інфекції. ЦВКАІК пов’язані зі збільшенням смертності та захворюваності, терміну перебування у стаціонарі та вартості лікування [2].
Міжнародний консорціум із контролю за нозокоміальними інфекціями (INICC) заявив, що загальна частота ЦВКАІК у ВІТ у країнах Африки, Азії, Східної Європи та Латинської Америки становить 4,9 інфекції на 1000 днів використання центрального катетера, що майже у п’ять разів вище, ніж у США (Rosenthal V.D. et al., 2014). Цікавим є факт, що саме у цих регіонах ще досі використовують відкриті системи для інфузії [1].
Використання відкритих інфузійних систем асоціюється з підвищеною захворюваністю на інфекції кровотоку серед пацієнтів ВІТ, що доведено численними дослідженнями. Так, дослідження, проведене у чотирьох країнах (Аргентина, Бразилія, Італія та Мексика), у яких переходили з відкритих систем для інфузії на закриті, виявило, що частота ЦВКАІК знизилася із 10,1 інфекції до 3,3 на 1000 днів використання центрального катетера, тобто частота ЦВКАІК зменшилась на 64%. Крім того, результати цього дослідження продемонстрували зниження смертності на 91% (Maki D.G. et al., 2011). За результатами іншого дослідження, проведеного в Латинській Америці того ж року, виявлено, що відношення ризику розвитку ЦВКАІК при використанні закритої та відкритої систем становило від 0,15 до 0,31 (p<0,001), що свідчить про клінічно значуще зниження ризику (Graves N. et al., 2011). Метааналіз 7 досліджень (n=4373) показав, що використання закритих систем поряд зі зниженням інфекцій кровотоку на 67% асоціюється зі зменшенням показників внутрішньолікарняного сепсису на 73% і госпітальної смертності у відділеннях реанімації та інтенсивної терапії на 23%. Тобто впровадження стратегії використання закритих інфузійних систем сприяє зменшенню захворюваності на інфекції кровотоку та смертності у пацієнтів ВІТ.
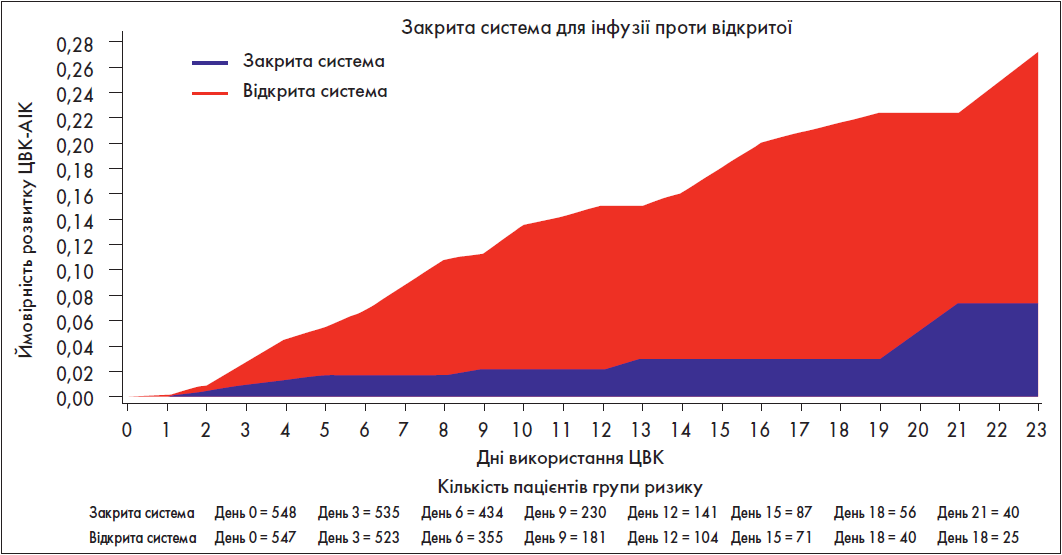
Крім того, M. Vilins та співавт. (2009) виявили, що захворюваність на ЦВКАІК залишається стало нижчою із часом при використанні закритих систем. Дослідники з Бразилії провели перспективне когортне дослідження (n=1125), за результатами якого виявили, що при використанні відкритих систем для інфузії швидкість виникнення ЦВКАІК була значно вищою, ніж при використанні закритих систем (6,5 проти 3,2 ЦВКАІК/1000 днів використання центрального катетера; відносний ризик [ВР] 0,49; 95% довірчий інтервал [ДІ] 0,260,95; p=0,031). Ймовірність розвитку ЦВКАІК залишалася відносно сталою протягом усього часу використання ЦВК та закритої системи (з 0,8% [24й день] до 0,7% [1113й день]), натомість невпинно зростала при використанні відкритої (з 1,5% [24й день] до 2,3% [1113й день]) (рис. 1).
Рис. 1. Ймовірність розвитку ЦВК-АІК залежно від часу (Vilins M. et al., 2009)
Пізніше подібні результати отримали й мексиканські дослідники (RangelFrausto M.S. et al., 2010): при використанні закритих систем ймовірність розвитку ЦВКАІК залишалась відносно сталою протягом усього періоду застосування (рис. 2).
Рис. 2. Ймовірність розвитку ЦВК-АІК залежно від часу (Rangel-Frausto M.S. et al., 2010)
Також дослідження показало, що шанс інфікування кровотоку був значно знижений (на 81%) у разі використання закритих систем (коефіцієнт пропорційних небезпек Кокса становив 0,19, р<0,0001), і при цьому показники смертності були статистично достовірно нижчими (23,4% проти 16,1%; ВР 0,69; 95% ДІ 0,540,88; р<0,01).
Ще однією, не менш важливою, перевагою використання закритих систем є те, що це стратегія економії коштів за рахунок зниження рівня інфекцій кровотоку без збільшення витрат на лікування. Адже вони сприяють зменшенню призначень антибіотиків, не потребують відповідного нагляду з боку персоналу й скорочують тривалість госпіталізації. Також їх застосування дозволяє знизити витрати, пов’язані з транспортуванням та утилізацією відходів.
N. Graves та співавт. (2011) проаналізували, що впровадження використання закритих систем у Латинській Америці зменшує фінансові витрати та смертність, тобто сприяє покращенню економіки країни. А у дворічному проспективному дослідженні типу «випадок – контроль», проведеному в одній італійській лікарні, нижчі показники ЦВКАІК (3,5 проти 8,2 на 1000 днів використання ЦВК) при порівнянні закритої та відкритої систем зумовили скорочення тривалості госпіталізації на 8,86 дня (8,55 проти 17,41). Загальні прямі медичні витрати на одного пацієнта без ЦВКАІК склали 9087 євро проти 18 241 євро у пацієнта із ЦВКАІК (Tarricone W.T. et al., 2010).
Іншими важливими перевагами використання закритих інфузійних систем є їхня більша зручність у використанні (вони легші на 40%, небиткі, займають менше складського простору на 5560%). Завдяки конструктивним особливостям підготовка закритої системи до початку інфузії потребує менше часу, усього 45 секунд, що вкрай важливо при наданні допомоги хворим у критичному стані.
Отже, перехід на закриті інфузійні системи є доцільним та економічно вигідним, адже їх використання знижує захворюваність, смертність, тривалість перебування пацієнтів у стаціонарі через нозокоміальні інфекції кровотоку, що підтверджено численними дослідженнями.
Література
- The Joint Commission. Preventing central lineassociated bloodstream infections: Useful Tools, An International Perspective. Nov. 20, 2013.
- Foka M. et al. Prevention of Central LineAssociated Bloodstream Infections Through Educational Interventions in Adult Intensive Care Units: A Systematic Review. Cureus 13(8): e17293. August 18, 2021.
Підготувала Марія Грицуля