24 січня, 2022
Порівняння бригатинібу та кризотинібу у лікуванні поширеного ALK-позитивного недрібноклітинного раку легені
Фінальні результати дослідження III фази ALTA-1L
Онкогенну мутацію гена кінази анапластичної лімфоми (ALK) виявляють у 3-5% хворих на недрібноклітинний рак легені (НДРЛ). Бригатиніб – пероральний інгібітор тирозинкінази (ТКІ), який проявляє високу активність проти злиття EML4-ALK. ALTA-1L – це дослідження III фази, у якому порівнювали ефективність бригатинібу та кризотинібу у лікуванні пацієнтів з поширеним ALK-позитивним (ALK+) НДРЛ, котрі раніше не отримували терапії. У попередніх номерах ми висвітлювали проміжні результати дослідження ALTA-1L, у яких бригатиніб забезпечував кращу ефективність, переносимість і якість життя пацієнтів з НДРЛ, ніж кризотиніб. У липні 2021 р. опубліковані фінальні результати дослідження III фази ALTA-1L, пропонуємо читачам їх огляд.
Матеріали та методи
Дизайн дослідження та пацієнти. ALTA-1L – відкрите рандомізоване дослідження III фази (NCT02737501). Пацієнти віком від 18 років із місцево-поширеним або метастатичним НДРЛ, які не отримували ALK-таргетну терапію, були рандомізовані (1:1) для перорального прийому бригатинібу у дозі 180 мг 1 раз на день (з 7-денною підготовчою фазою у дозі 90 мг 1 раз на день) або кризотинібу у дозі 250 мг 2 рази на день до прогресування захворювання, розвитку неприйнятної токсичності або іншого критерію припинення. Пацієнти були стратифіковані за наявністю/відсутністю метастазів у мозку та завершенням не менш ніж одного повного циклу хіміотерапії з приводу місцево-поширеного/метастатичного захворювання. Допускалися пацієнти з безсимптомними або стабільними метастазами в центральній нервовій системі. Пацієнти групи кризотинібу могли переходити на прийом бригатинібу після підтвердженого незалежним експертним комітетом у засліпленому режимі (BIRC) прогресування (після 10-денного вимивання кризотинібу).
Кінцеві точки. Первинною кінцевою точкою була виживаність без прогресування (ВБП), оцінена BIRC за Критеріями оцінки відповіді при солідних пухлинах (RECIST, версія 1.1). Вторинні кінцеві точки включали оцінені BIRC підтверджену частоту об’єктивної відповіді (ЧОВ), підтверджену внутрішньочерепну ЧОВ, внутрішньочерепну ВБП, загальну виживаність (ЗВ), тривалість відповіді (ТВ), безпеку та зміну загальної оцінки здоров’я (ЗОЗ)/якості життя (ЯЖ) порівняно з початковими (за Опитувальником якості життя – QLQ – Європейської організації з вивчення і лікування онкологічних захворювань, EORTC, C30, версія 3.0).
Результати
Пацієнти. Загалом 275 пацієнтів були рандомізовані для прийому бригатинібу (n=137) та кризотинібу (n=138). На початку дослідження у 96 (38%) з них були внутрішньочерепні метастази за оцінкою BIRC (n=47 у групі бригатинібу; n=49 у групі кризотинібу), а за оцінкою дослідника – у 81 (32%) пацієнта (n=40 у групі бригатинібу; n=41 у групі кризотинібу). На завершення дослідження (останній контакт з останнім пацієнтом – січень 2021 р.), приблизно через 3,5 року після включення останнього пацієнта (серпень 2017 р.), медіана (діапазон) спостереження становила 40,4 (0-52,4) міс у групі бригатинібу та 15,2 (0,1-51,7) міс у групі кризотинібу. Загалом 58 (42%) учасників групи бригатинібу та 16 (12%) групи кризотинібу продовжували приймати досліджуваний препарат до завершення дослідження. Медіана (діапазон) тривалості призначеного лікування становила 34,9 (0,1-52,4) міс у групі бригатинібу та 9,3 (0,1-51,5) міс у групі кризотинібу.
65 пацієнтів із групи кризотинібу перейшли на лікування бригатинібом після прогресування захворювання на тлі прийому кризотинібу; з них 23 (35%) пацієнти продовжували отримувати бригатиніб до кінця дослідження. Перехід відбувся у 46% (19 з 41) пацієнтів із метастазами у мозку на початку дослідження за оцінкою дослідників. Медіана тривалості лікування бригатинібом у 65 пацієнтів, які перейшли з кризотинібу, склала 17,3 (діапазон 0,1-37,5) міс.
Ефективність
Оновлені дані про ВБП. На час остаточного аналізу у 166 пацієнтів були події, пов’язані з ВБП (прогресування захворювання або смерть у групі бригатинібу – у 73 (53%) із 137; кризотинібу – у 93 (67%) із 138). Бригатиніб продовжував забезпечувати вищу ВБП за оцінкою BIRC порівняно з кризотинібом: оцінена за допомогою методу Каплана – Меєра 3-річна ВБП становила 43% (95% довірчий інтервал – ДІ – 34-51) у групі бригатинібу та 19% (95% ДІ 12-27) у групі кризотинібу; медіана ВБП 24,0 міс (95% ДІ 18,4-43,2) проти 11,1 міс (95% ДІ 9,1-13,0); співвідношення ризиків (СР) 0,48; 95% ДІ 0,35-0,66; р<0,0001 (рис. 1A). 4-річна ВБП за оцінкою BIRC становила 36% (95% ДІ 26-46) у групі бригатинібу та 18% (95% ДІ 11-26) у групі кризотинібу, хоча 4-річні дані були обмежені високою частотою цензурування та малим розміром вибірки (по 2 пацієнти у групі ризику в кожній групі; рис. 1A).
Оцінки дослідників узгоджувалися з оцінками BIRC. За оцінкою дослідників, частота 3-річної ВБП становила 45% (95% ДІ 36-54) для бригатинібу та 18% (95% ДІ 11-26) для кризотинібу; медіана ВБП 30,8 міс (95% ДІ 21,3-40,6) проти 9,2 міс (95% ДІ 7,4-12,7); СР 0,43; 95% ДІ 0,31-0,58; p<0,0001; рис. 1Б). Збільшення ВБП за оцінкою BIRC було послідовним в усіх підгрупах .
Частота й тривалість відповіді на лікування. Підтверджена ЧОВ за оцінкою BIRC відповідала такій у попередніх звітах. Середня ТВ у пацієнтів з підтвердженою відповіддю становила 33,2 міс (95% ДІ 22,1 – не досягнуто) для бригатинібу та 13,8 міс (95% ДІ 10,4-22,1) для кризотинібу (рис. 1В).
Внутрішньочерепна ефективність. Підтверджена внутрішньочерепна ЧОВ у пацієнтів із вимірюваними метастазами у мозку на початку дослідження відповідала такій у попередніх звітах. Медіана внутрішньочерепної ТВ у пацієнтів із вимірюваними метастазами у мозку на початку дослідження за оцінкою BIRC становила 27,9 міс (95% ДІ 5,7 – не оцінюється – НО) у групі бригатинібу та 9,2 міс (95% ДІ 3,9 – НО) у групі кризотинібу. У пацієнтів із будь-якими метастазами у мозку на початку дослідження за оцінкою BIRC 3-річна внутрішньочерепна ВБП дорівнювала 31% (95% ДІ 17-47) при застосуванні бригатинібу та 9% (95% ДІ 2-25) – кризотинібу (СР 0,29; 95% ДІ 0,17-0,51; p<0,0001), а 4-річна – 22% (95% ДІ 9-39; 2 пацієнти у групі ризику) при використанні бригатинібу та не оцінювалася (нуль пацієнтів у групі ризику) для кризотинібу (рис. 1Г). У всіх учасників (популяція призначеного лікування) 3-річна внутрішньочерепна ВБП становила 57% (95% ДІ 47-66) при застосуванні бригатинібу та 38% (95% ДІ 27-49) – кризотинібу (СР 0,44; 95% ДІ 0,30-0,65), а 4-річна – 46% (95% ДІ 34-57; 2 пацієнти у групі ризику) та 33% (95% ДІ 19-47%; 2 пацієнти у групі ризику) відповідно (рис. 1Ґ).
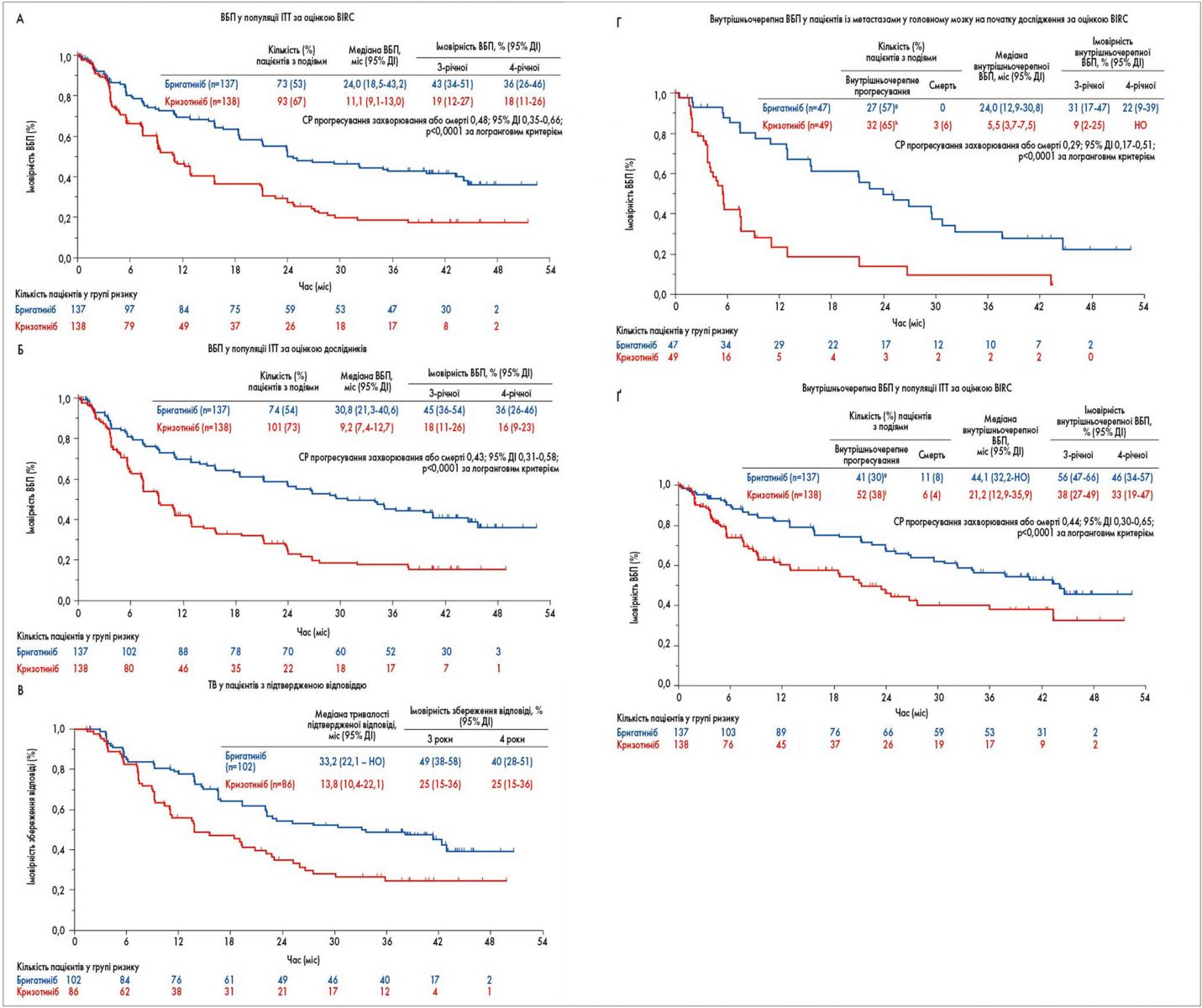 Рис. 1. Ефективність бригатинібу та кризотинібу при не лікованому ТКІ НДРЛ
Рис. 1. Ефективність бригатинібу та кризотинібу при не лікованому ТКІ НДРЛ
Графіки часу до події ілюструють оцінки Каплана – Меєра. Внутрішньочерепні та системні ефекти оцінювали різні незалежні експерти. Розглядалися лише ураження мозку. Пацієнти вважалися такими, що мали подію, якщо відбувалися радіологічне прогресування, променева терапія мозку або смерть. gВключає 1 пацієнта з променевою терапією головного мозку. hВключає 3 пацієнтів з променевою терапією головного мозку. jВключає 6 пацієнтів з променевою терапією головного мозку.
Ефективність переходу на лікування бригатинібом. У 65 пацієнтів, які перейшли на прийом бригатинібу (47% від усієї групи кризотинібу, 65% пацієнтів після прогресування захворювання на тлі застосування кризотинібу), медіана ВБП за оцінкою BIRC становила 16,8 міс (95% ДІ 10,1-23,9) при медіані спостереження 22,7 міс (діапазон 0,20-37,6 міс). Підтверджена ЧОВ за оцінкою BIRC дорівнювала 57% (95% ДІ 44-69) при медіані ТВ у пацієнтів з підтвердженою відповіддю 19,1 міс (95% ДІ 10,9-23,5).
Нова подальша лінія терапії раку. У групі кризотинібу більша частка пацієнтів отримувала подальшу протипухлинну терапію після припинення прийому досліджуваного препарату, ніж у групі бригатинібу. Із 121 пацієнта, які припинили прийом кризотинібу до закінчення дослідження, 103 (85%) отримували подальшу протипухлинну терапію; 99 (82%) – подальше лікування ALK ТКІ, найчастіше бригатинібом (80 (66%)) та алектинібом (28 (23%)). Із 78 пацієнтів, які припинили лікування бригатинібом, 46 (59%) отримували подальшу системну протипухлинну терапію, а 42 (54%) – подальше лікування ALK ТКІ, найчастіше лорлатинібом (22 (28%)) і алектинібом (16 (21%)). Із 27 пацієнтів, які припинили лікування бригатинібом і мали метастази у головному мозку на початку дослідження, 19 (70%) отримували подальше системне лікування, найчастіше лорлатиніб та алектиніб (по 10 (37%)). Серед 39 пацієнтів, які припинили лікування кризотинібом і мали метастази у головному мозку на початку дослідження, 32 (82%) отримували подальше системне лікування, найчастіше бригатиніб (24 (62%)), алектиніб і лорлатиніб (по 9 (23%)).
ЗВ. На час завершення дослідження померли 92 пацієнти (41 (30%) із групи бригатинібу; 51 (37%) із групи кризотинібу). Оцінена за методом Каплана – Меєра 3-річна ЗВ становила 71% (95% ДІ 62-78) у групі бригатинібу та 68% (95% ДІ 59-75) у групі кризотинібу без коригування для пацієнтів, які перейшли з прийому кризотинібу на лікування бригатинібом (СР 0,81; 95% ДІ 0,53-1,22; p=0,331; рис. 2A). Оцінена методом Каплана – Меєра 4-річна ЗВ становила 66% (95% ДІ 56-74; 7 пацієнтів у групі ризику) у групі бригатинібу та 60% (95% ДІ 51-68; 5 пацієнтів у групі ризику) у групі кризотинібу.
Серед пацієнтів з метастазами у головному мозку на початку дослідження за оцінкою дослідника померли 33 особи (11 (28%) із 40 у групі бригатинібу; 22 (54%) з 41 у групі кризотинібу). СР смерті становив 0,43 (95% ДІ 0,21-0,89; логранговий p=0,020; рис. 2Б). Оцінена методом Каплана – Меєра 3-річна ЗВ дорівнювала 74% (95% ДІ 57-85) у групі бригатинібу і 55% (95% ДІ 38-69) – кризотинібу, 4-річна ЗВ – 71% (95% ДІ 53-83; 4 пацієнти в групі ризику) і 44% (95% ДІ 28-59; нуль пацієнтів у групі ризику) відповідно. Перевага бригатинібу щодо виживаності порівняно з кризотинібом у цій підгрупі учасників дослідження була більшою у пацієнтів без попередньої променевої терапії головного мозку (СР 0,25; 95% ДІ 0,08-0,75; логранговий p=0,008), ніж в осіб, які раніше отримували променеву терапію головного мозку (СР 0,76; 95% ДІ 0,27-2,12; логранговий p=0,637).
Серед пацієнтів без метастазів у мозку на початку дослідження за оцінкою дослідників (n=97 у групі бригатинібу; n=97 у групі кризотинібу) 59 осіб померли (30 (31%) із групи бригатинібу; 29 (30%) – кризотинібу; СР 1,16; 95% ДІ 0,69-1,93; логранговий р=0,603; рис. 2В). При цьому 3-річна ЗВ оцінювалася в 70% (95% ДІ 59-78) у групі бригатинібу і 73% (95% ДІ 62-81) – кризотинібу, а 4-річна ЗВ – 64% (95% ДІ 52-74; 3 пацієнти в групі ризику) і 67% (95% ДІ 56-76; 4 пацієнти в групі ризику) відповідно.
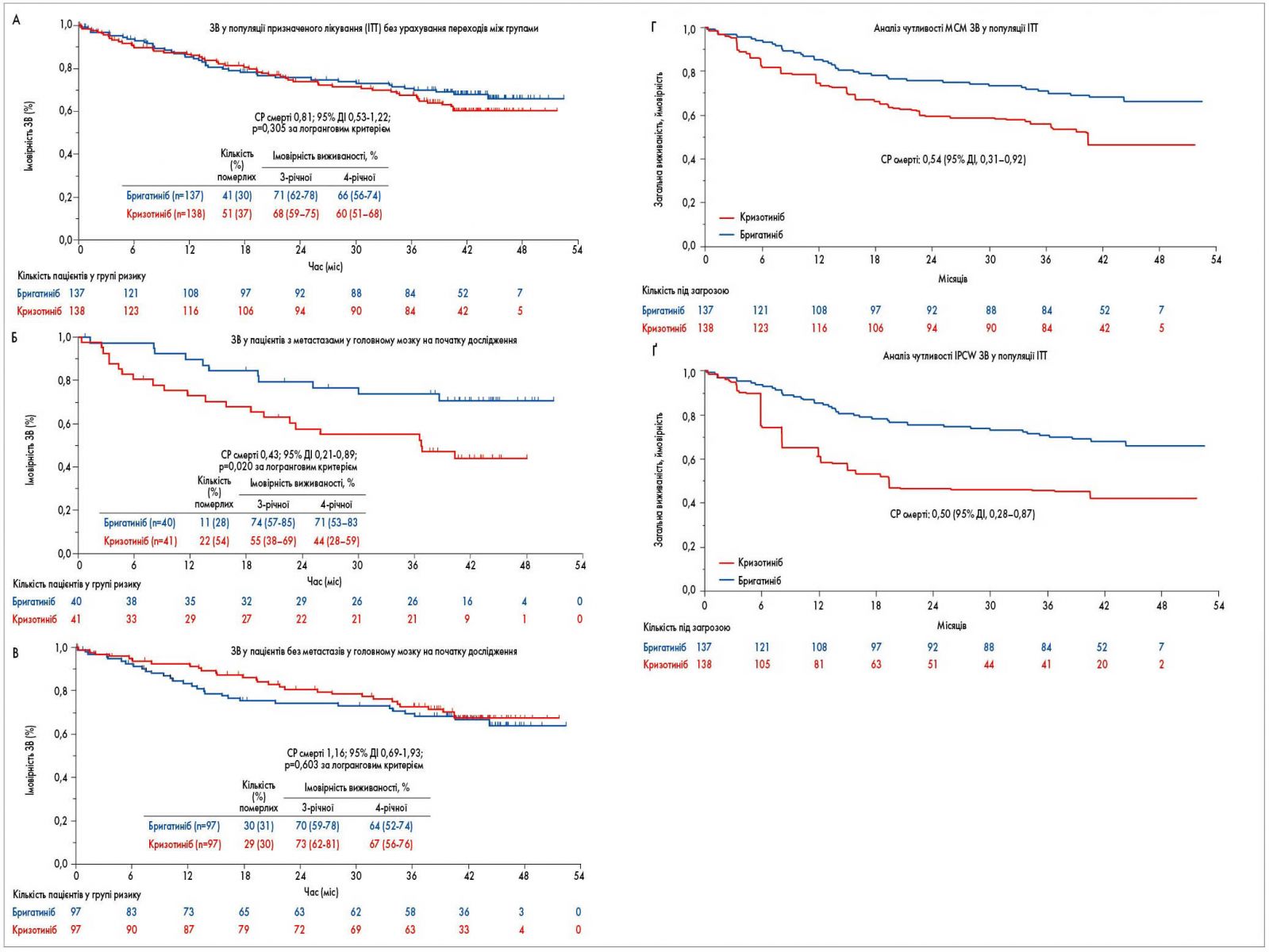 Рис. 2. ЗВ: A – у популяції призначеного лікування (ITT) без урахування переходів між групами; Б, В – в аналізах чутливості, які враховували перехід між групами за допомогою моделей (Б) МСМ та (В) IPCW Кокса, та у пацієнтів із метастазами (Г) й без метастазів (Ґ) у головному мозку на початку дослідження. IPCW – вага обернених імовірностей цензурування; МСМ – маргінальна структурна модель
Рис. 2. ЗВ: A – у популяції призначеного лікування (ITT) без урахування переходів між групами; Б, В – в аналізах чутливості, які враховували перехід між групами за допомогою моделей (Б) МСМ та (В) IPCW Кокса, та у пацієнтів із метастазами (Г) й без метастазів (Ґ) у головному мозку на початку дослідження. IPCW – вага обернених імовірностей цензурування; МСМ – маргінальна структурна модель
Для коригування потенційного часозалежного спотворюючого впливу зміни груп після припинення пацієнтами прийому кризотинібу було створено маргінальну структурну модель і модель Кокса з вагою обернених імовірностей цензурування.
Безпека
Найпоширенішими (>25% усіх пацієнтів) пов’язаними з лікуванням небажаними явищами (НЯ) будь-якого ступеня тяжкості були шлунково-кишкові розлади, підвищення рівня креатинінфосфокінази в крові, кашель і підвищення рівня амінотрансфераз. НЯ 3-5 ступеня спостерігалися у 78% пацієнтів у групі бригатинібу та у 64% – кризотинібу. Зниження дози внаслідок НЯ мало місце у 44 та 25% пацієнтів груп бригатинібу та кризотинібу відповідно. Лікування було перервано через НЯ у 72 проти 47% і припинено через НЯ у 13 проти 9% пацієнтів, які отримували бригатиніб і кризотиніб відповідно.
Оновлені дані про якість життя, пов’язану зі здоров’ям
Медіана часу до погіршення ЗОЗ/ЯЖ для бригатинібу становила 26,7 міс, а для кризотинібу – 8,3 міс (СР 0,69; 95% ДІ 0,49-0,98; логранговий p=0,047).
Порівняно з кризотинібом використання бригатинібу сприяло значному відтермінуванню погіршення емоційного та соціального функціонування, виникнення втоми, нудоти та блювання, втрати апетиту та запору (логранговий p<0,05). У жодному розділі істотної переваги кризотинібу не спостерігалося.
Обговорення
Фінальні результати дослідження ALTA-1L, присвяченого порівнянню ефективності застосування бригатинібу та кризотинібу у пацієнтів із поширеним ALK+ НДРЛ, які раніше не отримували ALK ТКІ, узгоджувалися з результатами перших двох проміжних аналізів. Бригатиніб забезпечував вищу порівняно з кризотинібом ВБП за оцінкою BIRC зі зниженням ризику прогресування або смерті на 52% (СР 0,48). Дані про ТВ були доповнені після попереднього аналізу: продемонстрована довша відповідь при застосуванні бригатинібу (медіана 33,2 міс), ніж кризотинібу (13,8 міс). Дані щодо ЗВ все ще доповнювалися під час заключного аналізу (частота подій 30%) і вказували на зіставну ЗВ в обох групах (СР 0,81). На ЗВ може вплинути дисбаланс протипухлинних методів подальшого лікування, включаючи високу частоту переходу на бригатиніб і вищу частоту подальшої протипухлинної терапії після припинення досліджуваного лікування в групі кризотинібу.
Бригатиніб продовжував демонструвати переконливу ефективність щодо впливу на внутрішньочерепні метастази. Ризик внутрішньочерепного прогресування був знижений на 56% у всіх пацієнтів (СР 0,44) і на 71% у хворих із будь-якими метастазами у головному мозку на початку дослідження (СР 0,29) при застосуванні бригатинібу порівняно з кризотинібом. Внутрішньочерепна відповідь була тривалою, з медіаною 27,9 міс в групі бригатинібу та 9,2 міс в групі кризотинібу у пацієнтів із вимірюваними метастазами у мозку на початку дослідження. СР для ЗВ при застосуванні бригатинібу порівняно з кризотинібом у пацієнтів із метастазами у головному мозку на початку дослідження становило 0,43 (логранговий p=0,020), незважаючи на високу частоту переходу з групи кризотинібу. Це свідчить про користь використання бригатинібу у пацієнтів із метастазами у мозку. Отримані дані щодо відповіді внутрішньочерепних метастазів на лікування дають підстави для подальшого вивчення оптимальної послідовності застосування препаратів при ALK+ НДРЛ у майбутніх дослідженнях.
Профіль безпеки бригатинібу у першій лінії терапії відповідав раніше відомому. Підвищення рівня креатинінфосфокінази в крові часто спостерігалося у пацієнтів, які отримували бригатиніб (50%), але не повідомлялося про випадки клінічно діагностованого рабдоміолізу. Відповідно до первинних клінічних результатів, бригатиніб також продовжував демонструвати переваги, пов’язані з ЯЖ (HRQoL), такі як відтермінування погіршення ЗОЗ/ЯЖ та багатьох інших показників HRQoL, порівняно з кризотинібом.
Таким чином, фінальні результати ALTA-1L свідчать про ефективність і безпеку, що узгоджуються з такими у двох проміжних аналізах. Бригатиніб продовжує демонструвати вищу ефективність і переносимість, а також кращу HRQoL, ніж кризотиніб. Вища ефективність бригатинібу порівняно з кризотинібом була послідовною для всіх варіантів злиття EML4-ALK, а також у пацієнтів з мутацією TP53 і без неї. Хоча дані про ЗВ залишилися неповними, припущення про перевагу щодо виживаності у пацієнтів із метастазами у головному мозку, які починають лікування з бригатинібу, дає змогу визначити вектор майбутнього вивчення оптимальної послідовності використання препаратів і обґрунтувати застосування бригатинібу як стандартного варіанта терапії раніше не лікованих пацієнтів з ALK+ НДРЛ.
За матеріалами Camidge D.R. et al. Brigatinib in ALK ІТК-naive ALKD NSCLC. Journal of Thoracic Oncology. https://doi.org/10.1016/j.jtho.2021.07.035.
Підготувала Ілона Цюпа
Стаття підготовлена за підтримки компанії «Такеда Україна».
C-APROM/UA/ALUN/0013
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 6 (73) 2021 р.



