16 вересня, 2022
Проблема хронічної кропив’янки. Частина 1: епідеміологія, імунопатогенез, супутні захворювання, якість життя та підходи до лікування
Хронічна спонтанна (ідіопатична) кропив’янка (ХСК) – це захворювання, яке характеризується появою пухирів, ангіоневротичного набряку (АНН) або обох симптомів впродовж понад 6 тиж; вражає 1-2% світової популяції. Частіше спостерігається в жінок і є значним тягарем, який ускладнює життя пацієнта, перешкоджає повсякденній рутинній діяльності, часто пов’язане із супутніми психічними розладами (депресією, тривогою) [1-2]. Середні щорічні прямі й непрямі витрати на ХСК у США оцінюють у 244 млн доларів, водночас витрати на ліки становлять 62,5%, на тимчасову непрацездатність – 15,7% загальних витрат [3]. Хоча патогенез ХСК досі не повністю вивчений, за останні роки було здійснено важливі досягнення щодо патофізіології захворювання [4].
Вважають, що ХСК є хронічним запальним захворюванням шкіри, у розвиток якого залучені різні клітини й медіатори запалення. Ці відкриття дали можливість віднайти точні й індивідуальні підходи до лікування цієї складної патології.
Учені досліджують імунологічні шляхи, які беруть участь у патогенезі ХСК; пропонують нові терапевтичні підходи, націлені на специфічні молекулярні мішені. У 2012 р. WAO (Всесвітня організація алергії) опублікувала погоджувальний документ щодо діагностики й лікування ХСК. З часу публікації цього документа відбувся прогрес у розумінні патогенезу хронічної кропив’янки (ХК), був накопичений достатній досвід для застосування біологічних препаратів, переважно омалізумабу, у пацієнтів із тяжким перебігом захворювання. З цих причин WAO вирішила розпочати оновлений огляд цієї статті, орієнтований на лікарів загальної практики в усьому світі, який містить найновішу інформацію про епідеміологію, імунопатогенез, супутні захворювання, якість життя, клінічні випадки, а також лікування ХСК та хронічної індукованої кропив’янки (ХІК), у тому числі кропив’янки в особливих груп населення, як-от діти й вагітні.
Епідеміологія, класифікація за тривалістю і пусковими механізмами. Значення реєстрів захворювання
Поширеність усіх типів кропив’янки становить менш ніж 10%, тоді як ХК розвивається лише приблизно у чверті з цих осіб [5, 6]. Точкова поширеність ХК на основі звітів про кодування в системах охорони здоров’я різних країн коливається від 0,1 до <1% в усьому світі. Наразі точкова поширеність є найкращим методом порівняння частоти ХК між різними групами населення, але розробка з цією метою стандартизованого і практичного інструменту залишається незадоволеною потребою. Із загальної кількості пацієнтів із ХК у третини спостерігають як висипання, так і АНН, у 30-40% – лише висипання, приблизно у 10% – ізольований АНН.
Захворювання має дуже широкий спектр клінічних проявів. У приблизно половини пацієнтів відбувається самостійне видужання від хвороби, у майже 80% вона зникає безслідно впродовж року. Однак у >10% тривалість реконвалесценції становить ≥5 років.
Хвороба вражає жінок удвічі частіше, ніж чоловіків, більшість пацієнтів мають вік старше 20 років [1, 7, 14]. Поширеність серед дітей варіює від <1% до майже 5%, що, своєю чергою, залежить від методології [15-17]. У частини пацієнтів відбувається загострення хвороби під час прийому нестероїдних протизапальних препаратів (НПЗП).
Спостереження, що ХІК виявляють набагато частіше серед родичів хворих, ніж у загальній популяції, припускає наявність генетичної схильності до захворювання і в такий спосіб клінічно підтверджує зв’язок між ХІК і людським лейкоцитарним антигеном DR4 [18].
Економічний тягар зазначеної патології є чималим. У США витрати, пов’язані з ХК, досягають 2050 доларів на рік на 1 пацієнта, що позначається як на самому хворому, так і на його родині [10, 19, 20].
Аналіз економічного навантаження з використанням паритету купівельної спроможності продемонстрував більш високі витрати на лікування та стаціонар пацієнтів у Франції – майже $3 тис проти <$1 тис в Італії; а втім втрата продуктивності праці була більшою в Німеччині, ніж у Франції, з >$1000 та >$500 відповідно.
Класифікація за тривалістю і тригерами
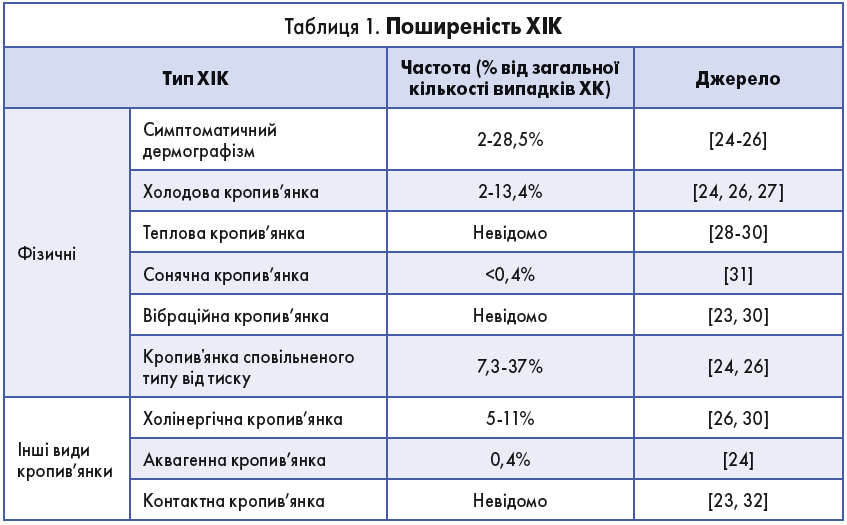
ХК зазвичай класифікують відповідно до тригерів і відомостей про ознаки й симптоми захворювання [6, 22, 23]. ХСК спостерігається набагато частіше (ХІК – лише у 15% хворих на ХК), однак у приблизно 75% хворих констатують наявність обох форм кропив’янки (табл. 1) [24-23].
Важливість створення реєстрів захворювання
У наданні медичної допомоги відбувся значний прорив, починаючи з прийняття рішень, які базуються переважно на набутому досвіді, до використання доведених і підтверджених процедур і втручань, які становлять основу доказової медицини [34]. Розробка рекомендацій також є частиною цього прориву, оскільки комісії з рекомендацій збирають і оцінюють опубліковані наукові дані та на основі їх загальної оцінки надають рекомендації [35].
Однак дані, отримані від реальних пацієнтів, є основою реєстрів, які, своєю чергою, є ключовими інструментами для визначення політики охорони здоров’я, вивчення природної історії та великої кількості змінних і для проведення клінічних досліджень. Використання панелей рекомендацій і реєстрів пацієнтів сприяє покращенню догляду за пацієнтами [36].
Реєстри в алергології дали дослідникам можливість отримувати дійсні дані, недоступні за допомогою інших методологій [36]. Тому використання таких реєстрів для ХК є неоціненним.
Онлайн-реєстр ХК, ініційований дослідниками і керований науковцями, доступний на www.urticaria-registry.com.
Реєстри надають корисну інформацію не лише для перегляду випадків із пацієнтами, а й щодо конкретних захворювань, якщо вони спричинені справжніми збудниками чи виникли внаслідок незначних супутніх чинників.
Імунопатогенез, ендотипи, біомаркери, прогностичні фактори
Ендотипи
Кропив’янку можна розділити на 3 клінічні фенотипи залежно від її тривалості (гостра або хронічна) та наявності чи відсутності тригерів (індукована чи спонтанна). ХСК, відома раніше як хронічна ідіопатична кропив’янка, належить до рецидивної, що триває більш ніж 6 тиж і виникає за відсутності тригера встановленої етіології (рис. 1). Кропив’янку завжди вважали хворобою, причиною якої є активовані мастоцити (проте сьогодні відомо, що в її розвитку має значення порушення регуляції не лише цих клітин, а й базофілів з їх подальшою активацією і дегрануляцією), а також інші клітини, наприклад еозинофіли, Т- і В-лімфоцити, епітеліальні та ендотеліальні клітини.
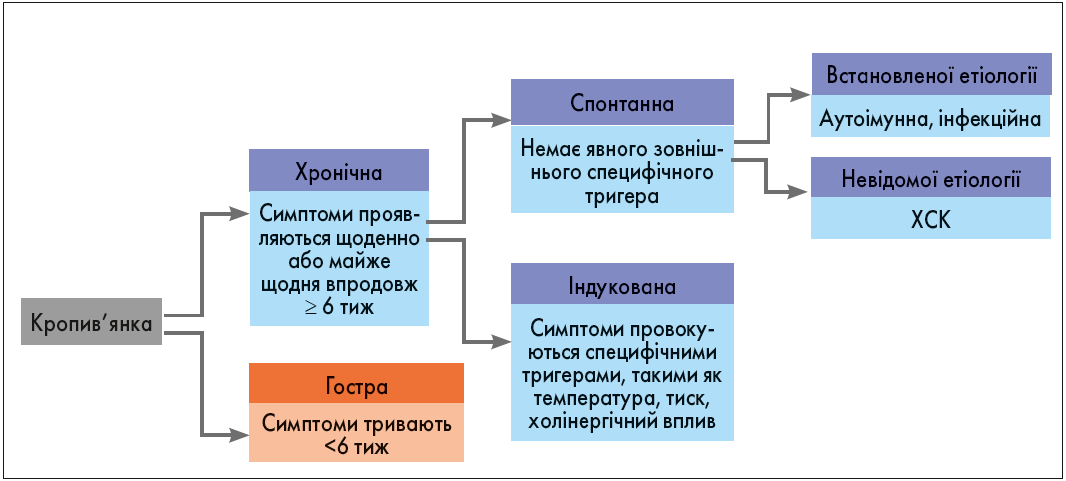 Рис. 1. Класифікація кропив’янки
Рис. 1. Класифікація кропив’янки
Мастоцити, розташовані в тканинах, можуть бути активовані декількома тригерами, зокрема імунологічними, що акцентує увагу на їх ролі у здійсненні природженої імунної відповіді на подразники шкіри і слизових оболонок.
Дегрануляція мастоцитів може бути зумовлена активацією кількох мембранних білків у результаті перехресного реагування на алергени, які розпізнаються молекулами IgE, фіксованими до високоафінних рецепторів на мембрані.
На мембрані мастоцитів розташована велика кількість інших рецепторів, які також можуть активувати ці клітини, наприклад C5aR – рецептор до анафілотоксинів системи комплементу (C5a), CRTh2 до PGD2, MRGPRX2 до нейропептидів (як-от речовина Р) або протеази й катіонних білків (таких як MBP і ECP), cKit до фактора стовбурових клітин (SCF), важливі рецептори цитокінів, наприклад IL‑4Ra і TSLP-R, різні типи TLR для розпізнавання PAMP і DAMP, а також деякі інгібувальні рецептори, такі як Siglec‑8, для пригнічення шляхів активації [22].
З дегрануляцією мастоцитів також пов’язаний процес коагуляції, який відбувається через активовані протеазою рецептори (PAR) з утворенням тромбіну і D-димеру. Нещодавно були доведені 2 основних механізми патогенезу ХК. Перший із них передбачає порушення регуляції внутрішньоклітинних сигнальних шляхів у мастоцитах і базофілах, що призводить до погіршення транспортної та інших функцій цих клітин. Другий механізм полягає у виробленні автоантитіл IgG до високоафінних рецепторів FcεRI або IgE як на мастоцитах, так і на базофілах (аутоімунітет II типу) або продукції аутоантитіл IgЕ, націлених на автоантигени, наприклад тиреопероксидазу (ТПО), ДНК, IL‑24 (автоімунітет I типу, або автоалергія) [42].
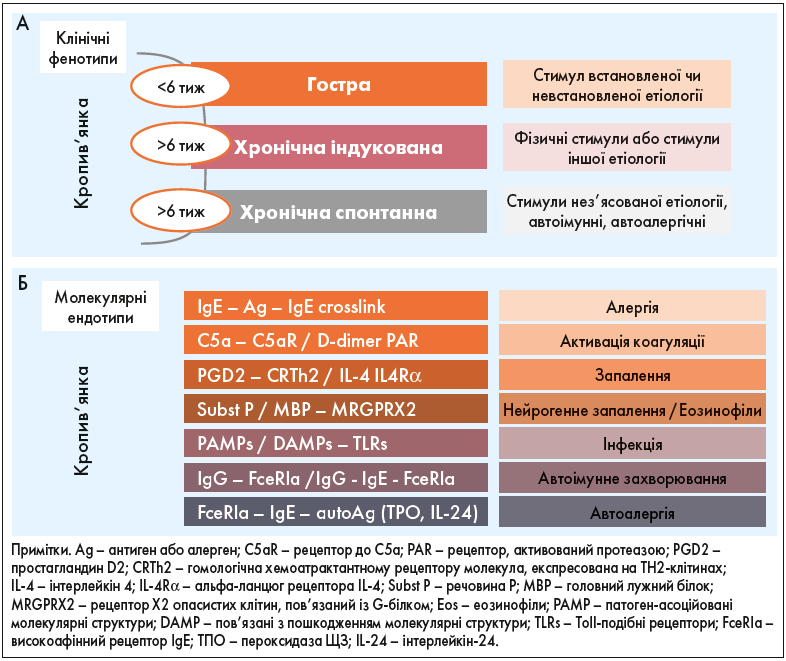
Унаслідок активації мастоцитів відбувається вивільнення великої кількості медіаторів запалення, як-от гістаміну, фактора активації тромбоцитів, триптази, лейкотрієнів і цитокінів, що призводить до подразнення чутливих нервів, вазодилатації та виходу плазми в позасудинний простір, а також залучення інших клітин у зону запального процесу [22]. Завдяки багатьом способам активації мастоцитів і участі в цьому процесі великої кількості клітин і біомолекул ми можемо зрозуміти різні ендотипи (молекулярні шляхи), які можна побачити серед клінічних фенотипів, обговорених вище (рис. 2).
Рис. 2. Клінічні фенотипи кропив’янки за її тривалістю (менше або більше 6 тиж) і за наявністю чи відсутністю факторів, що її провокують (індукована або спонтанна)
А. Подразниками можуть бути фізичні фактори, такі як температура, тиск, ультрафіолетове випромінювання та інші, наприклад вода, хімічні подразники або фізичні вправи. Подразники невідомої етіології можуть бути пов’язаніз автоімунними або автоалергічними механізмами. Б. Активація мастоцитів може бути зумовлена внутрішньою дисрегуляцією і/або зовнішнім подразником через мембранні рецептори.
Краще розуміння цих ендотипів допоможе знайти відповідні молекулярні мішені для біотерапевтичних засобів (рис. 3).
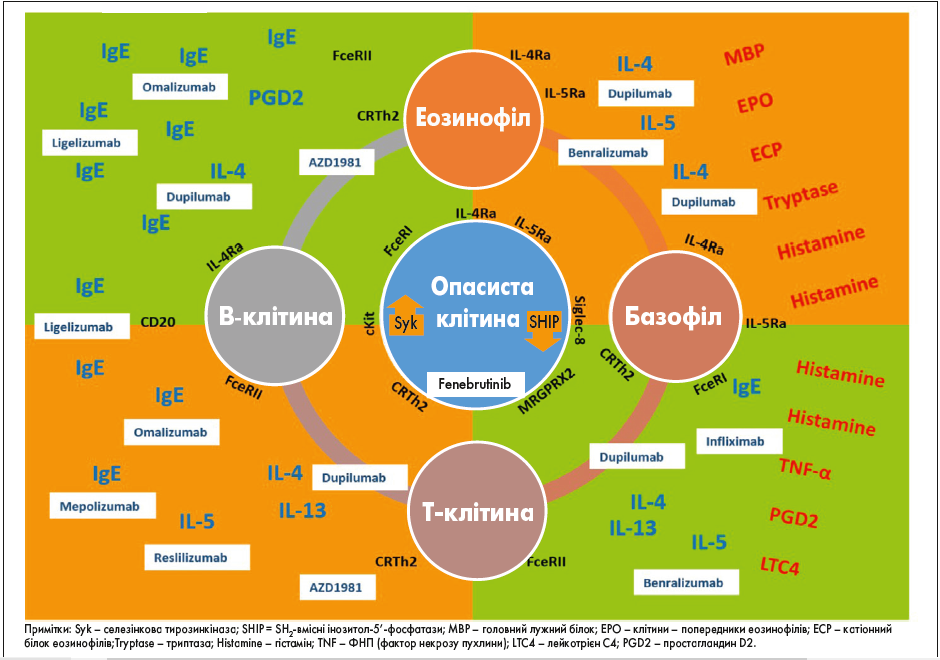 Рис. 3. Потенційні мішені для лікування ХК імунобіологічними препаратами
Рис. 3. Потенційні мішені для лікування ХК імунобіологічними препаратами
Біомаркери
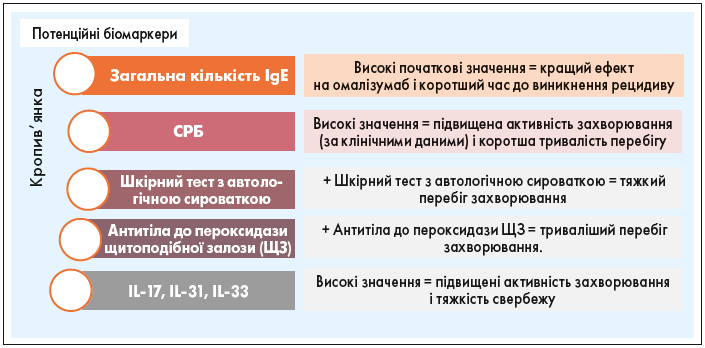
Біомаркер є об’єктивною ознакою, характеристикою, яку використовують як індикатор нормального або патологічного процесу, а також для оцінки фармакологічної відповіді на лікування. У разі кропив’янки, особливо ХСК, біомаркер був би корисним не лише для оцінки активності хвороби, її тяжкості та тривалості, а й для прогнозування відповіді організму на лікування. Було запропоновано декілька біомаркерів, але тільки 5 із них показали позитивні клінічні результати, тоді як решта не дала достатніх доказів (рис. 4) [42, 43]:
- Загальний рівень сироваткового IgE.
- СРБ.
- Шкірний тест з автологічною сироваткою (ASST).
- Автоантитіла до тиреоїдної пероксидази (анти-ТПО IgG).
Рис. 4. Потенційні біомаркери ХСК
Прогностичні фактори
В останніх дослідженнях на основі показника активності кропив’янки за 7 днів (UAS7) аналізували вихідні рівні загального IgE і відповідь на омалізумаб [44]. Не дивно, що вихідні рівні IgE мали тенденцію бути нижчими в пацієнтів, які не реагували на препарат, а вищі вихідні рівні IgE передбачали кращу відповідь на його застосування. Ремісія була значно коротшою в пацієнтів із рівнем IgE понад 100 МО/мл проти тих, у кого рівень IgE перебував у межах норми [45].
Було показано значущу кореляцію рівнів CРБ, чутливого маркера запалення, з активністю і тяжкістю захворювання. Високі рівні СРБ були пов’язані з підвищеною клінічною активністю захворювання, позитивними ASST і рівнями D-димеру, а також меншою тривалістю захворювання [46].
Позитивний ASST також корелював із тяжкістю захворювання (напади >4 разів на тиждень), але в період до початку захворювання жодних відмінностей зафіксовано не було. У пацієнтів з аутоантитілами IgG проти TПO спостерігали триваліший перебіг захворювання порівняно з пацієнтами без них. Проте відмінностей у тяжкості захворювання за наявності анти-ТПО не спостерігали [47].
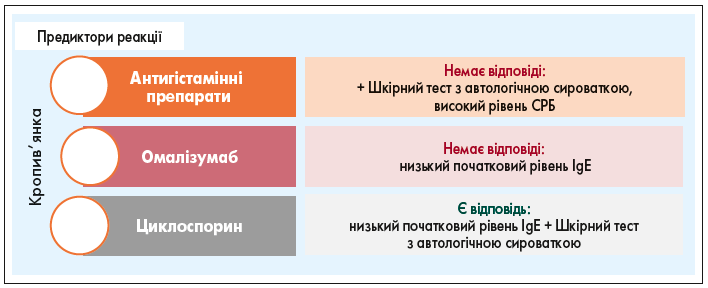
Зрештою запальні цитокіни можуть бути потенційними біомаркерами тяжкості захворювання при ХСК. Пацієнти з тяжким перебігом (на основі UAS7) мали вищі рівні IL‑17 і IL‑33 проти пацієнтів із легким перебігом захворювання. Тяжкість свербежу також асоціювалася з вищими рівнями IL‑31 (рис. 5) [48].
Рис. 5. Біомаркери як провісники імунної відповіді при ХСК
Краще розуміння ролі цих біомаркерів при кропив’янці може допомогти при розробці майбутніх стратегій лікування, а також для рекомендацій щодо поточного традиційного лікування.
Супутні захворювання при ХК
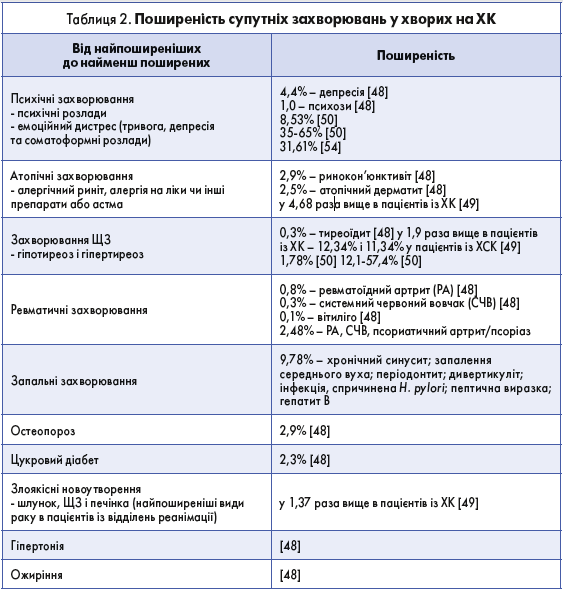
На якість життя пацієнтів значуще впливає не лише ХК, а й її зв’язок із широким спектром супутніх захворювань – аутоімунних, психічних і атопічних, які переважають саме в пацієнтів із ХК. Проте цей зв’язок є неоднозначним при поєднанні ХСК зі злоякісними новоутвореннями, серцево-судинними і шлунково-кишковими захворюваннями.
Поширеність різних супутніх захворювань, що спостерігають у хворих на ХК, наведена в таблиці 2.
Якість життя, пов’язана зі здоров’ям, при ХК
Глобальна оцінка захворювань і методів лікування має охоплювати, разом із клінічними й інструментальними дослідженнями, оцінку якості життя, пов’язану зі здоров’ям. Урахування стану пацієнта дає змогу отримати краще уявлення про вплив захворювання і методів його лікування на повсякденне життя [63]. Це особливо важливо для пацієнтів із хронічними захворюваннями – при цьому основною метою лікування є зменшення впливу захворювання на повсякденне життя і покращення суб’єктивного самопочуття.
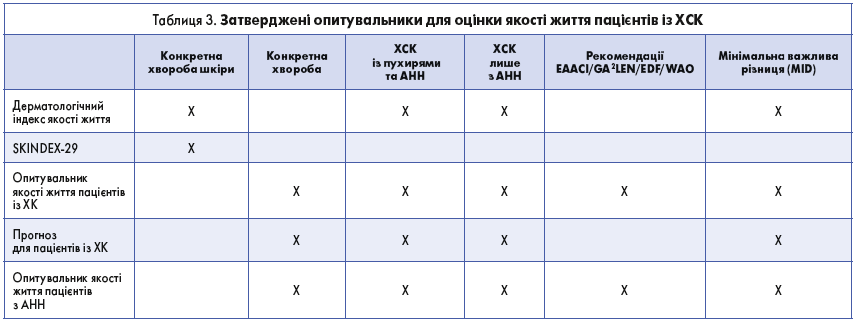
Дані про якість життя в пацієнтів із ХСК збирали протягом останніх 20 років. Наявність перевірених анкет, як загальних, так і специфічних, а також розробка нових спеціальних інструментів для ХСК дали можливість дослідити вплив хвороби на повсякденне життя пацієнта (табл. 3) [72-76].
Клінічні випадки: ХСК
ХСК проявляється у вигляді ізольованого висипу в приблизно 40% пацієнтів, висипу з АНН – у 40% та ізольованого АНН – у 20% випадків, на що потрібно звертати увагу при проведенні диференційної діагностики між гістамінергічним і негістамінергічним АНН.
Клінічний випадок 1: ХСК з АНН
Жінка, 33 роки, з 2013 р. має в анамнезі ХСК, у 2017 р. настала ремісія, але хвороба рецидивувала впродовж останніх 6 тижнів. Висип характеризувався непостійністю, великою площею ураження тіла пацієнтки – понад 90%, з оцінкою в 10 балів за ступенем тяжкості свербежу (за шкалою від 1 до 10). Оцінка активності кропив’янки за 7 днів (UAS7) охоплювала ступінь ураження висипом усього тіла (шкала 0-3) та інтенсивність свербежу (шкала 0-3), з максимальним тижневим балом 40 із 40.
Пацієнтка страждала на безсоння впродовж останніх декількох тижнів, не з’являлася на роботі, часто працювала понаднормово. Скаржилася на набряк губ та язика, що виникав щодня і був пов’язаний із кропив’янкою, на незначний дискомфорт у горлі, що супроводжувався кашлем, який визначався як вторинний унаслідок утрудненого ковтання слини через збільшення язика.
Окрім цього пацієнтка зазначила появу ґулі на ступнях. Висип супроводжувався значним свербежем, що завдавав болю і поєднувався з артралгіями й ознобом.
За 3 дні до запланованого прийому пацієнтка звернулася до центру невідкладної допомоги через дві різні скарги і щоразу отримувала короткий курс лікування глюкокортикоїдами (ГК) і дифенгідраміном, що допомогло зменшити тяжкість висипань й набряку, але щоразу, коли вона припиняла вживати ліки, симптоми загострювалися. Жінка заперечувала будь-який зв’язок із застосуванням рецептурних або безрецептурних препаратів чи продуктів харчування. В анамнезі пацієнтки не було захворювань ЩЗ, автоімунних хвороб або хронічних інфекцій. У сімейному анамнезі також не було ХСК або АНН. Пацієнтка зазначила загострення проявів хвороби в місцях компресії шкіри та в разі впливу низьких температур. Жінка працювала рентгенологом і на той час вигодовувала груддю 8-місячну дитину.
Під час фізикального обстеження виявлено правильну будову тіла і нормостенічний тип конституції особини жіночої статі, яка перебувала у важкому через тяжкість кропив’янки стані. Артеріальний тиск, пульс і частота дихання були в нормі. Оцінка за UAS під час візиту становила 40 балів, а контрольна оцінка тесту на кропив’янку (UCT) була 0 (шкала 0-16, при цьому 0 – абсолютно неконтрольована).
Вузлики виступали над поверхнею шкіри, еритематозні із синюшним відтінком і звивистими краями, що зливалися. Нижня губа набрякла.
Лімфаденопатії та органомегалії не було, дослідження серцево-судинної та дихальної систем патології не виявило. На шкірі пацієнтки при обстеженні за допомогою дермографометра висипу виявлено не було. Температурний тест на холодову кропив’янку показав негативний результат.
На момент візиту пацієнтка приймала 60 мг преднізолону впродовж 3 днів за призначенням лікаря невідкладної допомоги, однак її стан не покращувався.
Ураховуючи хронічний перебіг захворювання, візуальний стан висипу та загальну симптоматику, а також погану реакцію хворої на пероральні ГК, було вирішено провести лабораторні дослідження для визначення рівнів швидкості осідання еритроцитів (ШОЕ), СРБ, глюкозо‑6-фосфатдегідрогенази, тиреотропного гормону, автоантитіл до пероксидази ЩЗ, загального рівня IgE, індексу ХК, С3, С4, АНА, ревматоїдного фактора, загальний аналіз крові з підрахунком форменних елементів, а також біопсію шкіри для встановлення клінічного діагнозу васкуліту чи автоімунного стану, визначити біомаркери, щоб обрати оптимальні терапевтичні заходи в разі неефективності базової терапії H1-антигістамінними препаратами (АГП).
Пацієнтка отримала рекомендації повільно знижувати дозу преднізолону на 5 мг кожні 2 дні і починати приймати цетиризин у дозі 20 мг двічі на добу та монтелукаст по 10 мг на добу. Останні два препарати не є основними в міжнародних настановах, але рекомендовані Joint Task Force United States як препарати другого етапу лікування кропив’янки через їхню безпеку, низьку вартість і з огляду на тяжкість перебігу кропив’янки в пацієнтів.
Тиждень потому були переглянуті результати біопсії пацієнтки і проведена процедура зняття шва. Жінка все ще зменшувала дозу преднізолону, перебіг кропив’янки був інтермітуючим з UAS7 16 і UCT 10. Біопсія показала периваскулярну інфільтрацію лімфоцитами й еозинофілами, проте ознак васкуліту виявлено не було. Лабораторні дослідження показали, що рівень СРБ становив 17,87 мг/л (норма 6), функція ЩЗ була в нормі, а також – незначне збільшення кількості лейкоцитів до 11,7×109/л, незначне збільшення рівня периферичних нейтрофілів до 8,9×109/л (норма 1,6-6,1×109/л) і низький рівень IgE – 12 кОд./л (норма – ≤240 кОд./л). Незважаючи на низький рівень IgE, у пацієнтки спостерігалася позитивна відповідь на омалізумаб. Пацієнтці рекомендовано продовжити зниження дози преднізолону, приймати раніше призначену комбінацію АГП та антилейкотрієнового препарату і прийти на консультацію через 4 тиж для подальшого обстеження. Для оцінки наявності гіпертиреозу було призначене визначення рівнів вільних Т4 і Т3, аналіз на визначення рівня СРБ було проведено повторно. Пацієнтка підписала інформовану згоду на випадок необхідності прийому омалізумабу – третього етапу терапії.
Після проведення обстеження через 4 тиж пацієнтка припинила прийом преднізолону; її стан покращився, але тяжкість кропив’янки все ще оцінювалася за UCT у 7 і за UAS7 у 18 балів. Рівні вільних T3 і T4 та СРБ були в межах норми. Був схвалений омалізумаб у дозі 300 мг, і під час візиту була введена перша підшкірна ін’єкція. Через 4 тиж пацієнтка повернулася для подальшого обстеження та другої ін’єкції. Жінка повідомила, що тяжкість кропив’янки за UCT становить 16 балів, а за UAS7– 4 бали, загалом пацієнтка почувалася набагато краще без будь-яких побічних ефектів від ліків. Під час третьої ін’єкції через місяць пацієнтка повідомила, що тяжкість кропив’янки становила за UCT 16 балів і за UAS7– 0 балів.
Обговорення. Цей випадок кропив’янки з АНН є тяжким, асоційований з ознаками, що вказували на системний процес, з огляду на характер кропив’янки та пов’язані з нею системні симптоми.
Пацієнтка отримувала преднізолон у дозі, яку поступово знижували для забезпечення кращого самопочуття, перед початком другого етапу терапії. Тестування проводили для з’ясування клінічних підозр на васкуліт або автоімунний стан. Рівень СРБ виявився підвищеним, а скринінговий рівень ТТГ був низьким, однак подальше дослідження не виявило ознак гіпертиреозу.
Незважаючи на терапію преднізолоном і препаратами терапії другого етапу, стан пацієнтки не покращувався, тому вона була переведена на третій етап – лікування омалізумабом. Під час підготовки до початку цієї терапії в пацієнтки був визначений рівень загального IgE, оскільки низькі рівні асоціюються з повільнішою або гіршою відповіддю на лікування. Окрім того пацієнтка була обстежена на ТПО та CU-індекс, маркер високоафінних антитіл IgG до альфа-субодиниці Fc-R1, які в разі позитивного результату також свідчать про гіршу відповідь на омалізумаб.
У пацієнтки ці тести були негативними, і згодом хвора продемонструвала відмінну та швидку відповідь на омалізумаб. Необхідно зазначити, що жінка пов’язувала АНН з кропив’янкою, яка також контролювалася за допомогою омалізумабу, як було показано в post hoc аналізі даних клінічних досліджень. Додатковим нюансом цього випадку було те, що пацієнтка вигодовувала груддю під час лікування високими дозами АГП та омалізумабу.
Хоча контрольованих досліджень, які б демонстрували безпеку цих препаратів у вагітних і жінок, які годують груддю, немає, міжнародні рекомендації підтримують використання зазначених методів лікування в особливих групах населення на основі довготривалого клінічного досвіду та реєстрів безпеки [22]. Крім того, використання перевірених відомостей щодо результатів, повідомлених пацієнтом, є дуже корисним для визначення контролю і прийняття рішень щодо лікування.
Клінічний випадок 2: ХСК без АНН
Жінка, 26 років, хворіла на ХСК з 2017 року. Саме тоді вона стала помічати появу спонтанного висипу на різних частинах тіла, переважно на руках, ногах і стегнах. Її оцінка за UCT становила 8 балів, а за UAS7 – 20 балів, але інтенсивність свербежу була набагато нижчою, ніж площа ураження висипом. Тригерів, що спричиняли появу висипу, виявлено не було. Лікар первинної ланки нещодавно призначив їй курс преднізолону в поєднанні з димедролом, який вона застосовувала за потреби; однак висип і набряки з’являлися знову, коли вона не приймала ліки. Крім димедролу, який спричиняв у пацієнтки втому, їй також призначили монтелукаст. Але внаслідок прийому цього лікарського засобу пацієнтка страждала на нічні жахіття, тому препарат було відмінено. Пацієнтка працювала адміністративним помічником і стверджувала, що ліки заважали їй виконувати роботу.
Жінці кілька разів призначали зробити аналіз крові, у тому числі загальний аналіз крові і визначення рівня ТТГ, показники яких були в межах норми. Жодного зв’язку між ХСК і прийомом ліків чи вживанням продуктів харчування встановлено не було. Пацієнтка консультувалася в алерголога, який провів дослідження на аероалергени і харчові продукти, результати були негативними. Під час консультації був проведений фізикальний огляд, у ході якого було виявлено розсіяні еритематозні пухирі на руках. АНН не спостерігали. Інших важливих висновків під час фізикального огляду зроблено не було.
У зв’язку з хронічним перебігом ХСК і чутливістю до АГП пацієнтка розпочала прийом сучасного неседативного АГП ІІ покоління двічі на добу і запланувала повторний візит до лікаря через 4 тижні. Додаткові обстеження не проводили. Пацієнтка прийшла на консультацію через 4 тиж і мала результати за UCT 16 балів і за UAS7 – 0. Жінка переносила ліки без побічних ефектів, якість її життя значно покращилася. Пацієнтці було рекомендовано продовжити прийом препаратів і прийти на консультацію через 3-4 місяці. Під час її третього відвідування висипання все ще спостерігались, прийом неседативного АГП ІІ покоління зменшили до одного разу на добу.
Обговорення. Це відносно простий випадок ХСК, який спочатку належним чином не контролювався і не лікувався. Пацієнтка проходила курс лікування АГП І покоління, які спричинювали в жінки стомлюваність і впливали на виконання її робочих обов’язків. Крім того, алерголог провів шкірні тести з аероалергенами та харчовими продуктами, тоді як в анамнезі не було алергічного риніту, астми або харчової алергії [22].
Пацієнтка розпочала прийом неседативного АГП ІІ покоління в дозі, що вдвічі перевищує рекомендовану FDA (другий етап терапії), яка була дуже ефективною для запобігання рецидиву кропив’янки. Цю схему лікування продовжували доти, доки не стало зрозуміло, що в пацієнтки не було пухирів, що проривалися (UAS7 = 0), після чого дозу зменшили до одного разу на добу. Жінка зазначила, що після початку лікування якість її життя і роботи значно покращилася.
Зверніть увагу, що:
- Рекомендації корисні для орієнтування клініцистів у відповідній оцінці й веденні пацієнтів із ХСК.
- ХСК рідко спричинюється зовнішніми чинниками.
- Перевірені відомості щодо результатів, про які повідомляють пацієнти, є цінними для оцінки тяжкості захворювання і моніторингу реакції на лікування.
- Призначення численних досліджень, у тому числі шкірних тестів з аероалергенами або харчовими продуктами, не рекомендується, якщо дані історії хвороби не є підставою для їх проведення.
- У понад 40% пацієнтів із ХСК високі дози АГП забезпечували контроль хвороби.
- Пацієнти з кропив’янкою з/без АНН реагують на омалізумаб.
Терапевтичні та загальні підходи до лікування ХСК і ХІК
Загальні підходи
Збір анамнезу пацієнта і фізикальне обстеження можуть виявити симптоми – тригери довкілля, що провокують або підсилюють прояви ХК.
При виявленні захворювання необхідно уникати або зменшувати вплив фізичних чинників, харчових продуктів, контактних речовин, емоційного стресу, ліків (як-от НПЗП, інгібітори АПФ). Також доречним є лікування супутніх інфекцій, спричинених, наприклад, H. pylori, а також інфекцій сечовивідних шляхів, паразитарних інвазій, стоматологічних або гінекологічних інфекцій [22]. Необхідно лікувати інші коморбідні стани, такі як автоімунне захворювання ЩЗ, артеріальна гіпертензія та метаболічний синдром [11].
До 40% пацієнтів із ХСК зазначають загострення хвороби у разі прийому аспірину та інших НПЗП. У 10-15% пацієнтів із ХСК також спостерігається асоційована індукована кропив’янка. Унаслідок цього коморбідну індуковану кропив’янку потрібно лікувати [11].
Додатковими методами, що сприяють зменшенню свербежу як найбільш виснажливого симптому ХК та провідної причини дискомфорту в пацієнта, є застосування фізичних методів, наприклад холодних компресів (але не в пацієнтів із холодовою кропив’янкою).
Висновки
Поширеність ХК серед населення коливається в межах від 0,1% до 1,0%. Якість життя пацієнтів може бути серйозно порушена, а витрати на хворобу для системи охорони здоров’я можуть бути значними. Останніми роками розуміння патофізіології цього захворювання було доволі успішним, що спонукало науковців досліджувати нові препарати, особливо біологічні, у пацієнтів із тяжкою рефрактерною кропив’янкою. У прояві симптомів беруть участь кілька типів клітин, переважно мастоцити, базофіли, еозинофіли, Т- і В-лімфоцити, а також епітеліальні та ендотеліальні клітини. Припускається, що порушення регуляції внутрішньоклітинних сигнальних шляхів і автоімунні явища відіграють важливу роль в активації мастоцитів/базофілів, що спричиняє вивільнення медіаторів запалення в шкірі, що, своєю чергою, призводить до набряків і власне АНН.
Серед скарг пацієнтів спостерігають наявність висипань (приблизно 40%), АНН (40%) або обох симптомів (20%), які в більшості хворих на ХСК не спричинені певними тригерами, хоча в деяких пацієнтів у результаті впливу зовнішніх факторів, переважно фізичних, можна було запідозрити й підтвердити діагноз ХІК.
Також доречно зазначити, що в деяких пацієнтів може спостерігатися поєднання клінічної картини ХСК і ХІК.
Нині виявлено біомаркери, які є корисними для рутинної терапії й прогнозування перебігу ХК та її відповіді на різні види лікування. Але клініцисти мають дотримуватися рекомендацій, використовувати перевірені дані, про які повідомляють пацієнти, та призначати ліки з доведеною ефективністю і безпекою. Найближчим часом для лікування тяжкої і рефрактерної форм ХК використовуватимуть нові біологічні препарати та малі молекули, які зараз перебувають на стадії досліджень.
Список літератури – у редакції.
Реферативний огляд статті M. Sаnchez-Borgesa et al. The challenges of chronic urticaria part 1: Epidemiology, immunopathogenesis, comorbidities, quality of life, and management. World Allergy Organization Journal. 2021.
Переклад із англ. Дарини Павленко
Друкується в скороченому обсязі, повну версію дивіться:
https://www.worldallergyorganizationjournal.org/article/S1939-4551(21)00027-2/fulltext
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 1-2 (58-59) 2022 р.