16 січня, 2023
Пробіотики в профілактиці респіраторних вірусних інфекцій
 З моменту глобального спалаху тяжкого гострого респіраторного синдрому, спричиненого SARS‑CoV-2, дослідження були зосереджені на розумінні етіології коронавірусної хвороби (COVID‑19). Визначення та розробка профілактичних і терапевтичних стратегій для боротьби з пандемією все ще має вирішальне значення. Хоча вакцини знизили ризик смерті, госпіталізації та, до певної міри, інфікування, пошук додаткових профілактичних і терапевтичних засобів все ще триває. Тому існує нагальна потреба в додатковій терапії, яка запобігала б або покращувала симптоми в осіб, інфікованих SARS-CoV-2.
З моменту глобального спалаху тяжкого гострого респіраторного синдрому, спричиненого SARS‑CoV-2, дослідження були зосереджені на розумінні етіології коронавірусної хвороби (COVID‑19). Визначення та розробка профілактичних і терапевтичних стратегій для боротьби з пандемією все ще має вирішальне значення. Хоча вакцини знизили ризик смерті, госпіталізації та, до певної міри, інфікування, пошук додаткових профілактичних і терапевтичних засобів все ще триває. Тому існує нагальна потреба в додатковій терапії, яка запобігала б або покращувала симптоми в осіб, інфікованих SARS-CoV-2.
COVID‑19 має широкий спектр клінічних проявів, починаючи від безсимптомного, легкого перебігу (кашель і лихоманка, серед іншого) до тяжкого захворювання, що може спричинити смерть. Останніі дані свідчать про те, що в багатьох пацієнтів інфекція COVID‑19 має безсимптомний перебіг. Такі пацієнти можуть бути джерелом розповсюдження хвороби шляхом передачі вірусу іншим особам, що призводить до подальшого поширення COVID‑19. До загальних симптомів COVID‑19 належать лихоманка, втома, сухий кашель, ринорея, шлунково-кишкові симптоми (наприклад, діарея та нудота), задишка з гіпоксемією. У деяких пацієнтів спостерігалися тяжкі клінічні ознаки, такі як пневмонія, набряк легень, поліорганна недостатність і синдром гострого респіраторного дистрес-синдрому. Отже, COVID‑19 може вимагати багатовимірного терапевтичного втручання з переходом від вірусологічних підходів (рання стадія інфекції) до імуномодуляції (пізня стадія). Оскільки ефективного лікування поки що немає, триває пошук альтернативи, яка дасть змогу зміцнити власну імунну відповідь проти COVID‑19.
Найкращі способи зміцнити природний імунітет – це споживання:
- їжі, що підтримує кишкову мікрофлору, – пребіотиків, які вибірково стимулюють корисні кишкові бактерії;
- пробіотиків.
Всесвітня організація охорони здоров’я та Продовольча й сільськогосподарська організація ООН визначають пробіотики як живі мікроорганізми, які при введенні в адекватних кількостях є корисними для здоров’я господаря. Одним із найбільш багатонадійних ефектів пробіотиків для здоров’я людини є модуляція місцевої та системної імунної відповіді. Пробіотики з імуномодулювальною дією називають імунобіотиками.
Дослідження показали перехресний зв’язок між кишковою та легеневою системами, демонструючи взаємодії, які індукують імунологічні процеси при інфекції господаря. Оскільки наразі визнано тісний зв’язок між обома органами, використання пробіотиків може відіграти важливу роль у зниженні вірусної інфекції, як-от COVID‑19. Останні результати досліджень показують, що пробіотики можуть позитивно впливати на противірусний імунітет господаря. Цей огляд є спробою критично проаналізувати перспективи впровадження пробіотиків як імуномодуляторів для профілактики респіраторних вірусних інфекцій.
Пробіотики для модуляції імунної системи: імунобіотики
Нині імунобіотикам приділяється більше уваги, враховуючи їхній потенціал забезпечувати захист від вірусних інфекцій шляхом модуляції вродженого й адаптивного противірусного імунітету. Крім того, специфічні мікробні штами, що мешкають у кишковій екосистемі, які називаються пробіотиками наступного покоління, мають сприятливий вплив на здоров’я та розглядаються як харчові/нутрицевтичні добавки й біотерапевтичні продукти. Нові мікробні штами випробовуються щодо їх можливого використання в профілактиці та лікуванні багатьох захворювань. Zhang і співавт. припустили, що синбіотики, отримані з кишкової мікробіоти (штами біфідобактерій і пребіотики), стимулюють утворення антитіл, знижують назофарингеальне вірусне навантаження, знижують прозапальні маркери та відновлюють кишковий дисбактеріоз у пацієнтів із COVID‑19.
Імунобіотики позитивно впливають на імунну функцію та зменшують тяжкість інфекцій у шлунково-кишковому тракті (ШКТ), а також у дихальних шляхах. Було показано, що молочнокислі бактерії мають потенціал для покращення здоров’я шляхом модуляції імунної відповіді. Крім того, лікування пробіотичними штамами молочнокислих бактерій було пов’язане з покращенням мікробіому кишечнику й зменшенням алергії та шлунково-кишкових розладів.
У рандомізованому контрольованому клінічному дослідженні, що було проведено Jafari та співавт. за участю 37 пацієнтів із кістозним фіброзом для визначення впливу імунобіотиків на кишкову мікробіоту й імунітет, окрім покращення функції кишечнику, спостерігалося значне зменшення легеневих загострень у групі пацієнтів, які приймали імунобіотики, порівняно з групою плацебо. Пробіотики можуть мати протизапальну дію й у разі COVID‑19.
Імунобіотики та вірусні респіраторні інфекції
Імунобіотики мають помірний вплив на профілактику респіраторних вірусних інфекцій людини, але з’являється дедалі більше доказів того, що певні імунобіотики можуть бути ефективними в модуляції опосередкованого ШКТ противірусного вродженого імунітету. Повідомлялося, що лікування штамами Lactobacillus зменшило тяжкість інфекції дихальних шляхів вірусного походження.
Tang і співавт. продемонстрували: щоденне пероральне введення (протягом 28 днів) пробіотика L. rhamnosus GG порівняно з плацебо в 1132 пацієнтів із COVID‑19 зменшує тяжкість захворювання (лихоманка, озноб, головний біль, біль у м’язах, діарея тощо), пов’язане з корисними змінами мікробіому кишечнику. Li та співавт. зібрали в ретроспективному одноцентровому дослідженні дані 311 пацієнтів із COVID‑19 в Ухані (Китай), а також проаналізували й порівняли епідеміологічні, клінічні та медикаментозні характеристики пацієнтів, які приймали та не приймали пробіотики (L. rhamnosus GG). Виявили, що пробіотики покращують імунітет і знижують частоту вторинної інфекції в пацієнтів із COVID‑19.
Gutiérrez-Castrellón і співавт. вивчали вплив пробіотиків на симптоматику та вірусний кліренс у амбулаторних пацієнтів із COVID‑19 у рандомізованому чотириразово сліпому плацебо-контрольованому дослідженні. Їхні висновки показали, що пробіотичні добавки (Lactiplantibacillus plantarum і Pediococcus acidilactici) зменшили симптоми порівняно з плацебо. Вони зазначили, що пробіотики насамперед взаємодіють з імунною системою, а не змінюють склад мікробіоти товстої кишки в пацієнтів із COVID‑19.
Нещодавно проведене рандомізоване контрольоване дослідження ефективності та безпеки багатоштамового пробіотичного препарату (суміш штамів Lactobacillus, Bifidobacterium і Streptococcus thermophilus) у пацієнтів із синдромом подразненого кишечнику з переважанням діареї показало значне покращення симптомів, добру переносимість і безпечність пробіотичного препарату.
Рандомізоване подвійне сліпе паралельне плацебо-контрольоване дослідження, проведене Anaya-Loyola, оцінювало ефект Bacillus coagulans GBI‑30 проти інфекцій верхніх дихальних шляхів і ШКТ у дітей. Було показано, що щоденне застосування пробіотиків (1×109 КУО) протягом 3 міс значно зменшувало тривалість симптомів, пов’язаних з інфекцією.
Втручання імунобіотиків у кишково-легеневі шляхи
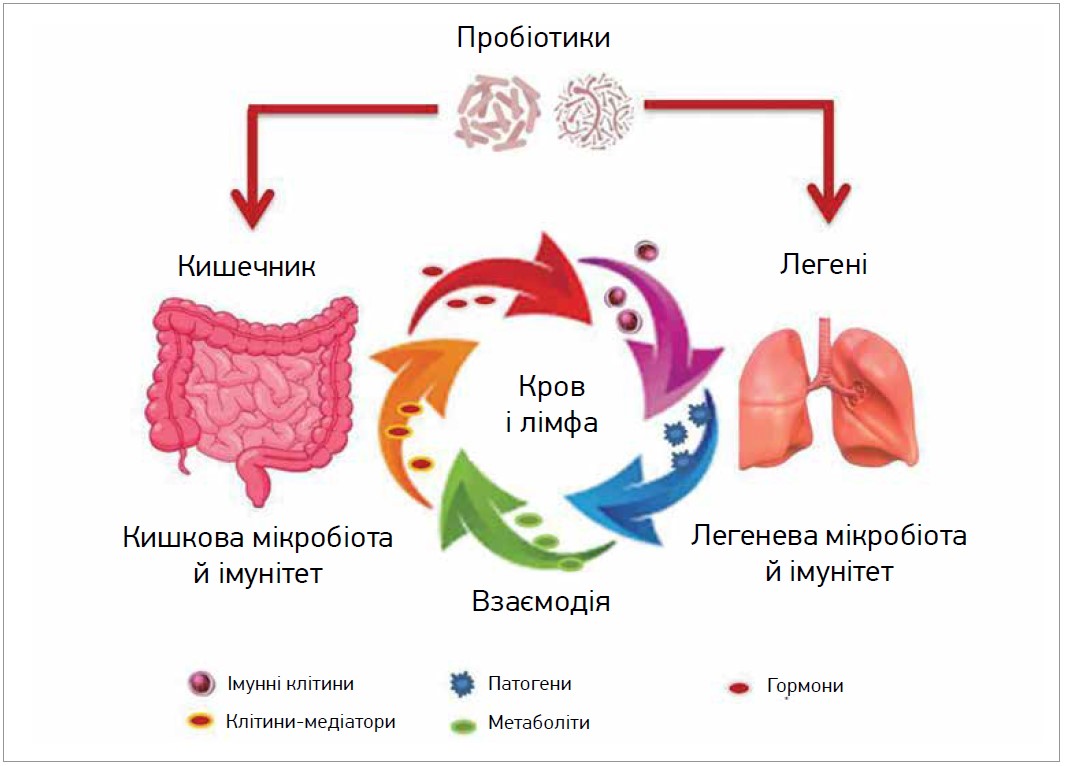
Деякі дослідження, присвячені взаємозв’язку між ШКТ і легеневою системою з погляду патогенезу та здоров’я, продемонстрували, що активність кишкової мікробіоти, а також втручання імунобіотиків впливають на легеневий імунітет через активний і складний двонаправлений перехресний зв’язок між кишечником і легенями, який називають кишково-легеневим. Спрощені взаємодії, що відбуваються в системі кишечник – легені людини, схематично представлено на рисунку.
Рис. Взаємодія між кишечником і легенями людини
Кишечник і легені пов’язані між собою за допомогою елементів кровообігу та лімфатичного потоку, як-от імунні клітини та медіатори, дружні чи шкідливі мікроби (віруси, бактерії), а також компоненти чи метаболіти, які підтримують взаємодію мікробіоти й імунної системи обох органів.
Anwar і співавт. виявили противірусну дію пробіотичних метаболітів на COVID‑19 за допомогою дослідження молекулярної динаміки з використанням метаболічного продукту L7 plantarum, який блокує проникнення шляхом зв’язування SARS-CoV‑2.
Зв’язок між кишечником і легенями відбувається через лімфатичну систему та кровообіг, що переносить посередники імунних клітин, як-от цитокіни, мікробні фрагменти, продукти та гормони. Відомо, що респіраторна вірусна інфекція спричиняє порушення кишкової мікробіоти, а мікроорганізми та/або їхні фрагменти можуть досягати легенів через транслокацію та циркуляцію крові з кишечнику в легені й навпаки.
Кишкова мікробіота відіграє важливу роль у модулюванні взаємодії господар – патоген. Мікробна популяція, що мешкає в кишечнику, налічує понад 2000 видів і перевищує 1014. Легенева бактеріальна біомаса менша за мікробіоту кишечнику. Згідно з даними Sze та співавт. у легеневих тканинах міститься близько 10-100 бактерій на 1000 клітин людини.
Зміни мікробіоти легенів та/або кишечнику спричиняють дисбіоз, який посилює запалення та гостре ураження легенів, що супроводжується загостренням симптомів. Зростання кількості досліджень доводить, що зміни мікробіоти кишечнику пов’язані зі змінами імунної відповіді та прогресуванням захворювання в легенях. Оскільки ACE2 присутній у кишкових клітинах, у пацієнтів із COVID‑19 виникає можливий перехресний зв’язок між легенями та кишечником. Діарея, пов’язана з виявленням вірусних нуклеїнових кислот у зразках фекалій пацієнтів із COVID‑19, може частково пояснити взаємодію між кишечником і легенями. Крім того, виявлено, що системний позитивний ефект індукується мікробіотою кишечнику через вироблення коротколанцюгових жирних кислот, які пригнічують запалення легенів.
Зв’язки в осі кишечник – легені зумовлені імунологічним процесом, індукованим мікробіотою, імунобіотиками та патогенами (вірусом). Точні механізми, що лежать в основі імунорегуляторної активності імунобіотиків у противірусному імунітеті, ще не повністю з’ясовані, але противірусний імунітет щодо звичайних респіраторних вірусів, включаючи грип, риновірус і респіраторно-синцитіальний вірус, був задокументований. Імунобіотики можуть відігравати важливу роль у підтримці належної імунної відповіді на респіраторну вірусну інфекцію. Вони можуть запобігти зміні розподілу дендритних клітин (ДК), а також зниженню активації Т‑клітин CD8(+) і CD4(+) при легеневій вірусній інфекції.
За даними Kitazawa та Villena, імунобіотичний штам Lactobacillus rhamnosus CRL1505 діє шляхом модуляції TLR3-опосередкованої імунної відповіді проти вірусного зараження в дихальних шляхах. Ho та співавт. встановлено, що Lactobacillus paracasei BRAP01 і Lactobacillus acidophilus AD300, асоційовані з вищим значенням IFN‑γ/IL‑10, посилюють цитотоксичність природних кілерів у крові людини. Імунобіотики, як-от L. rhamnosus і Bifidobacterium lactis HN019, які виявляють протизапальні властивості, можуть бути корисними для пацієнтів із COVID‑19.
Bonjardim заявив, що інтерферони сильно експресуються ДК, які розпізнають молекулярні структури вірусу через TLR. Отже, ці цитокіни індукують подальшу експресію прозапальних цитокінів, що призводить до активації адаптивного противірусного імунітету. Враховуючи потенційну імуномодулювальну дію імунобіотиків, можна припустити: введення імунобіотиків може запобігти неконтрольованому виробленню прозапальних медіаторів, що провокує цитокіновий шторм у разі COVID‑19.
Життєздатні імунобіотики або фрагменти, вивільнені вбитими бактеріями з кишечнику господаря, можуть досягати легенів кров’ю або лімфатичним потоком, щоби сприяти його імунній відповіді, подібно до того, як це відбувається в кишечнику. Крім того, імунобіотики суттєво змінюють композицію Lactobacillus spp. та Bifidobacterium spp., а також збільшують загальний уміст коротколанцюгових жирних кислот і пропіонової кислоти в кишечнику дітей.
З огляду на визнання їхніх імуномодулювальних властивостей можна вважати, що імунобіотики регулюють імунну відповідь у разі вірусної інфекції, як-от COVID‑19, за якої спостерігається втрата гомеостатичної рівноваги між клітинами Treg (IL‑10) і клітинами Th17 (IL‑17).
Висновки
Альтернативний підхід ґрунтується на потенційному застосуванні певних пробіотиків на тлі вірусної респіраторної інфекції. Враховуючи відсутність ефективної імунотерапії COVID‑19, бактеріотерапія на основі імунобіотиків є стратегією, яка може прямо чи опосередковано сприяти боротьбі з COVID‑19. Тому запропоновано, щоби пробіотики, добре задокументовані стосовно імуномодулюючої та респіраторної активності, розглядалися для інтенсивних клінічних випробувань в аспекті полегшення тривалості та тяжкості COVID‑19. Застосування Лактіалє® Мульті відновлює мікробний баланс, модулює противірусний імунітет у пацієнтів із легеневими ураженнями.
Довідка «ЗУ»
Зважаючи на наведену інформацію, особливо цікавим є мультиштамний пробіотичний комплекс компанії ADM Protexin Ltd., в Україні представлений під торговою назвою Лактіалє® Мульті (АТ «Фармак»). Кожна капсула сумарно містить 2×109 КУО пробіотичних мікроорганізмів, а саме 14 запатентованих компанією ADM Protexin Ltd. штамів пробіотичних бактерій (4 – біфідобактерій, 7 – лактобактерій і 3 – інших пробіотичних бактерій).
Науково доведено позитивний вплив пробіотичних мікроорганізмів, які входять до складу Лактіалє® Мульті, на нервову й імунну системи:
- Bifidobacterium longum нормалізує тривожну поведінку (зменшує збудливість кишкових нейронів, які можуть надсилати сигнали центральній нервовій системі, активуючи вагусний шлях);
- L. rhamnosus має вплив на рівень γ-аміномасляної кислоти в певних ділянках мозку та знижує рівень стрес-індукованого гормону кортикостерону, в результаті чого нормалізується поведінка, пов’язана з тривожністю й депресією;
- Bacillus subtilis має вплив на специфічний імунітет завдяки активації Т- та В-лімфоцитів і вивільненню IgG й IgA. Посилення неспецифічного імунітету пов’язано з активацією макрофагів і вивільненням із них прозапальних цитокінів, підвищенням бар’єрної функції слизової оболонки кишечнику;
- S. thermophilus, L. acidophilus, Lactococcus lactis ssp. lactis, Lactobacillus delbrueckii ssp. bulgaricus, Lactobacillus helveticus, Lactobacillus salivarius, Lactobacillus casei, Lactobacillus plantarum, Bifidobacterium bifidum, Bifidobacterium breve, Bifidobacterium infantis продукують молочну кислоту з вуглеводів;
- B. bifidum знижує утворення в кишечнику метаболітів, що мають канцерогенний потенціал.
Спосіб застосування – вживати під час прийому їжі:
- дітям 8-12 років – по 1 капсулі 1 раз на добу;
- дітям віком понад 12 років і дорослим – по 1 капсулі 2 рази на добу.
Під час прийому антибіотиків – по 4 капсули на добу. Для кращої засвоюваності інтервал між прийомом дієтичної добавки Лактіалє® Мульті й антибіотиків має становити 2 год. Після закінчення курсу антибіотиків прийом капсул Лактіалє® Мульті варто продовжувати ще щонайменше 2 тиж.
Усі штами в складі Лактіалє® Мульті мають розшифрований геном і код безпеки (PXN), а також тестовані на кислотостійкість, здатність до адгезії, інгібувальної дії щодо патогенів. Дія штамів Лактіалє® Мульті є доведеною, тому цю дієтичну добавку можна розглядати як варіант для корекції мікробіому та як імунобіотик у боротьбі з інфекційними захворюваннями.
Враховуючи імунологічні взаємодії в системі кишечник – легені та вирішальну роль пробіотиків у модуляції імунної відповіді, застосування Лактіалє® Мульті може бути успішним у профілактиці та лікуванні як кишкових розладів, так і захворювань дихальних шляхів, у тому числі COVID-19.
Медична газета «Здоров’я України 21 сторіччя» № 17 (534), 2022 р.