24 січня, 2023
Дитяче ожиріння: огляд поточних і прийдешніх варіантів лікування
Ожиріння все більш поширюється в педіатричній популяції по всьому світу. Водночас зі збільшенням поширеності також зростає і тяжкість ожиріння. У сукупності ці результати демонструють тривожну тенденцію і наголошують на значущості однієї з найбільших проблем громадського здоров’я. Дитяче ожиріння чинить вплив на багато органів в організмі та пов’язане як зі значною захворюваністю, так і з передчасною смертю. Поширеність ускладнень, спричинених ожирінням, як-от дисліпідемія, гіпертензія, жирове переродження печінки і психосоціальна стигматизація, у дітей також зростає дедалі більше.
Рекомендації щодо лікування наразі зосереджені на зміні способу життя та поведінки. Тоді як фармакотерапія і хірургічне лікування призначені для пацієнтів, в яких попередні заходи виявилися неефективними. Дослідження ожиріння в дорослих дало можливість розробити нові фармакологічні методи лікування, які були схвалені і запроваджені в клінічну практику; однак дослідження і впровадження цих методів лікування в педіатричну практику поки дещо відстає. Незважаючи на відносну нестачу широкомасштабних досліджень у порівнянні з дорослим населенням, проводяться випробування нових методів лікування, що допоможе в майбутньому розширити можливості лікування дитячого ожиріння. У цьому огляді підсумовано сучасні дані щодо лікування ожиріння у дітей, зокрема медикаментозні і хірургічні підходи, розглянуто як перспективні терапевтичні засоби, так і ті, що спричиняють втрату ваги, але мають інші показання. Для кожного з варіантів лікування наведено останні дослідження і продемонстровано потенційну ефективність і обмеження щодо застосування.
Вступ
Дитяче ожиріння стало проблемою охорони здоров’я в усьому світі. Щороку кількість дітей із надмірною вагою або ожирінням зростає. В Англії за Національною програмою вимірювання дітей проводять огляди серед дітей, що навчаються в нульовому (віком 4-5 років) і 6-му (віком 10-11 років) класах. Результати досліджень у 2019-2020 рр. показали, що поширеність ожиріння в нульових (підготовчих) класах становила 9,9% і зростала до 21,0% у 6-х класах [1]. За допомогою програми було з’ясовано, що хлопчики частіше страждають на ожиріння; також було встановлено, що діти, які мешкають у бідних районах, більш ніж удвічі схильніші до ожиріння порівняно з тими, хто живе в заможних районах [1]. Серед дорослого населення поширеність ожиріння зросла з 14,9% у 1993 р. до 28,7% у 2017 р. [3].
З ожирінням пов’язана низка ускладнень, це, зокрема, серцево-судинні захворювання, проблеми із суглобами, цукровий діабет (ЦД) 2 типу, неалкогольна жирова хвороба печінки, апное уві сні, проблеми статевого дозрівання та підвищений внутрішньочерепний тиск [4]. Ці стани чинять значний вплив не лише на фізичне, а й на психічне здоров’я та якість життя.
Важливим є вирішення проблеми дитячого ожиріння на ранніх стадіях, щоб запобігти появі ускладнень у майбутньому. Зі зменшенням кількості дітей з ожирінням зменшиться поширеність ожиріння серед дорослих.
Нині лікування дитячого ожиріння зосереджено на зміні способу життя і витрачанні більшої кількості калорій, аніж споживається [5].
У деяких пацієнтів зміни способу життя спрацьовували, але загальна тенденція зростання цієї проблеми показала, що цього не завжди достатньо [6]. Фармакотерапія набирає обертів серед дорослого населення, і попри те, що дані щодо ефективності цих ліків у дітей і молоді обмежені, імовірно, вони можуть бути цінним доповненням у лікуванні ожиріння в пацієнтів зазначеної категорії.
Метою цього огляду є оцінка як поточних методів лікування ожиріння в дітей, так і можливих терапевтичних варіантів для застосування в майбутньому, з основним акцентом на фармакологічних утручаннях.
Матеріали і методи
Головним джерелом для пошуку літератури, використаної в огляді, був PubMed. Ключовими словами були: дитяче ожиріння, підлітки, фармакотерапія, метморфін, орлістат, глюкагоноподібний пептид‑1, сибутрамін, топірамат, фентермін, лоркасерин, сетмеланотид, ліздексамфетамін, налтрексон, бупропіон, флуоксетин, зонісамід, метрелептин та баріатрична хірургія.Пошук даних зосереджувався на педіатричних дослідженнях осіб молодших 18 років, але, там, де дані були обмеженими, розглядали дослідження, проведені серед дорослого населення.
Визначення
Ожиріння характеризується надмірним накопиченням жиру в жировій тканині, діагностується за допомогою показника індексу маси тіла (ІМТ), що є відношенням ваги людини до її зросту.
У людей із сильно розвиненою мускулатурою ступінь ожиріння не корелює з ІМТ; однак для більшості людей ІМТ вважають точним показником для оцінки ожиріння. У дорослих ожиріння діагностують, якщо ІМТ ≥30 кг/м2, а надмірну вагу – якщо ІМТ ≥25 кг/м2. У педіатрії ожиріння виявляють, порівнюючи вагу з віком дитини, що відображає зміну складу тіла під час фізичного розвитку.
У багатьох країнах для визначення ваги і зросту використовують довідкові таблиці, що зумовлює різні визначення «ожиріння». Згідно з визначенням Всесвітньої організації охорони здоров’я (ВООЗ) надлишкова вага встановлюється, якщо ІМТ для певного віку більш ніж на 1 стандартне відхилення перевищує медіану нормативного показника росту й розвитку за ВООЗ, а ожиріння – якщо перевищує більш як 2 стандартні відхилення [7]. Міжнародна цільова група з питань ожиріння використовує для діагностування надмірної ваги в осіб віком 18 років граничні значення ІМТ 25, для ожиріння – 30, а також LMS-криві для кількох країн, створені для дитячої вікової групи [8].
У США Центри з контролю та профілактики захворювань (Centers for Disease Control and Prevention, CDC) визначають надлишкову вагу, якщо показник ІМТ перебуває в діапазоні від 85-го до 95-го перцентиля, а ожиріння –на рівні ≥95-го перцентиля, на основі центилів ІМТ за віком і статтю [9].
У Сполученому Королівстві Королівський коледж педіатрії та дитячого здоров’я (Royal College of Paediatrics and Child Health) визначає дитяче ожиріння як ІМТ, що становить ≥98-го перцентиля для дітей і підлітків того самого віку і статі. Надмірну вагу визначають як ІМТ, що становить ≥91-го перцентиля та <98-го перцентиля для дітей і підлітків того самого віку і статі.
Нефармакологічні методи лікування
Рекомендації Національного інституту охорони здоров’я та догляду (National Institute for Health and Care Excellence, NICE) наразі рекомендують зміну способу життя як основний підхід до лікування дитячого ожиріння, що передбачає необхідні зміни в дієті задля зменшення споживання калорій [5, 10].
У рекомендаціях NICE стверджується, що не доцільно заохочувати дотримуватися обмежувальних і незбалансованих дієт, оскільки вони неефективні в довгостроковій перспективі й можуть бути небезпечними. Усіх дітей з ожирінням потрібно заохочувати змінити свій раціон, але це не має бути єдиним підходом до лікування [11].Ojeda‐Rodriguez та співавт. довели, що інтенсивне втручання у спосіб життя (помірна гіпокалорійна дієта, фізичні вправи і навчання раціональному харчуванню) успішно знижує показник стандартного відхилення ІМТ (SDS) у дітей і молодих осіб з абдомінальним ожирінням [12].
На лікування ожиріння в дітей можуть впливати фактори довкілля. Важливо враховувати умови в школах: щоб фонтани з водою були у вільному доступі і щоб харчування зосереджувалося на забезпеченні дітей здоровими варіантами обіду [13]. Не дивно, що такі фактори, як відсутність сніданку, підвищений уміст жирів і вуглеводів у раціоні і низьке споживання здорової іжі (фруктів, овочів і молочних продуктів), пов’язані з розвитком ожиріння в дітей [14-16].
Було доведено, що підсолоджені напої підвищують ризик надмірної ваги або ожиріння в дітей, також було виявлено зв’язок між меншим умістом цукру і зниженням ІМТ [5, 17, 18-21]. У 2015 р. ВООЗ надала рекомендації щодо зменшення вмісту цукру в раціоні як дорослих, так і дітей [16, 22].
У 2018 р. Сполучене Королівство запровадило податок на солодкі напої, і, навіть незважаючи на те що загальний обсяг продажів безалкогольних напоїв не змінився, дані показують, що за останні декілька років люди купують менше солодких напоїв, а отже, споживають менше цукру [23]. Уряд Великої Британії продовжує підтримувати здоровий спосіб життя серед населення, обмежуючи з квітня 2022 року рекламу нездорової їжі [24]. Hamano та співавт. виявили, що доступність закладів швидкого харчування була значною мірою пов’язана з дитячим ожирінням [25]. Настанова, розроблена Ендокринним товариством, рекомендує зменшити споживання жиру й цукру, фаст-фуду та вживати свіжі фрукти замість соків [4, 26, 27]. У настанові також рекомендовано контролювати розмір порції та регулярність харчування, щоб уникнути перекусів впродовж дня [4, 6, 28-31]. Trier та співавт. довели, що мультидисциплінарна програма лікування значно знижує SDS ІМТ, але споживання солодких напоїв і закусок перед програмою не вплинуло на ступінь ожиріння на початку терапії або втрату ваги впродовж року лікування [32].
З огляду на обмежувальні дієти, Eneli та співавт. дослідили результат 12-місячної протеїно-зберігаючої модифікованої швидкої дієти (protein‐sparing modified fast, PSMF) за участю 21 дорослого з тяжким ступенем ожиріння. Дієта полягала в зменшенні вмісту калорій і вуглеводів і збільшенні кількості білків. Результати показали, що вага й ІМТ зменшилися на 3-му і 6-му міс, проте прихильність до цієї дієти впродовж дослідження знизилася [33]. Andela та співавт. опублікували огляд літератури для оцінки ефективності й безпеки в дітей і молодих людей дієти з дуже низьким умістом енергії (very‐low‐energy diet, VLED). В основі VLED лежить споживання менш ніж 800 кілокалорій на добу або менш ніж 50% загальних витрат енергії людиною [34]. З цього огляду можна зробити висновок, що зниження маси тіла в дітей і молоді є суттєвим, за умови дотримання VLED впродовж щонайменше 6 міс [34].Безпосереднє порівняння VLED і звичайної дієти становить труднощі через обмеження даних, але з огляду зрозуміло, що зниження ваги є значнішим за дієти VLED [34]. Були помітними покращення показників артеріального тиску (АТ), а також рівнів інсуліну і загального холестерину [34].
За умов дотримання VLED в молоді покращувався рівень глікованого гемоглобіну (HbA1c) і зменшувалася потреба в медикаментозній терапії ЦД 2 типу [34-36]. Схожі результати були задокументовані серед дорослого населення [37]. Науковці зазначили, що дані про побічні ефекти в переглянутих дослідженнях описані не дуже детально. Загалом, задокументованими побічними ефектами були втома і постуральна гіпотензія [34]. Незмінними залишаються занепокоєння щодо дефіциту електролітів, тому їх рекомендують приймати у вигляді добавок. Таким чином, дієта VLED є безпечною в разі короткострокового її дотримання, проте в разі довготривалих досліджень спостерігатимуться несприятливі ефекти [34].
Відповідно до Національних рекомендацій дітям варто вдаватися до вправ із помірним фізичним навантаженням по 60 хв щодня [11, 15, 16]. З’ясувалося, що поєднання аеробних і силових тренувань є кориснішим для втрати ваги і зменшення окружності талії [38]. Було доведено, що школа є важливим фактором у заохоченні дітей і молоді до фізичної активності та значно знижує ризик розвитку ожиріння [39, 40]. У ході розгляду підходів до боротьби з ожирінням виявилося, що фізична активність у школах сама по собі здатна зменшувати ІМТ, окружність талії в жінок, товщину шкірної складки та жирові відкладення [39]. Підмічено, що більш доступна фізична активність, як у школі, так і вдома, є кориснішою для дітей з ожирінням [39]. Сьогодні зміна способу життя є першим методом лікування дитячого ожиріння. Для отримання ефекту зміна способу життя має передбачати поєднання покращення дієти та фізичну активність.
Фізіологічні наслідки дитячого ожиріння широко описані в літературі, не лишаються непоміченими також емоційні і психологічні наслідки життя з ожирінням.
Дослідження показують, що діти й підлітки з надмірною вагою схильніші до розладів психічного здоров’я, таких як депресія, тривога, низька самооцінка, а також до психосоціальних проблем [41-44]. Park та співавт. довели, що діти, які живуть з ожирінням, відчувають стрес у 4,5 раза частіше, ніж їхні однолітки зі здоровою масою тіла [45]. Вважають, що психосоціальні проблеми і стигматизація життя з ожирінням разом із фізичними обмеженнями і зниженням якості життя замикають хибне коло. Це, своєю чергою, ще більше закарбовує проблеми з психічним здоров’ям і такий спосіб життя, що сприяє розвитку ожиріння. Таким чином, ожиріння відіграє роль провокаційного і підтримувального фактора, що призводить до серйозних наслідків для здоров’я молодої людини.
Враховуючи, що сім’я є основною складовою розвитку дитини, вважається, що вибір способу життя батьків формуватиме поведінку дитини через такі процеси, як рольова модель, стиль виховання, підкріплення, обмеження і контроль [46, 47].
Рекомендації NICE підкреслюють, що найуспішнішими підходами для зниження ваги є втручання, спрямовані на сім’ю [47, 48]. Доведено, що сімейноорієнтовані підходи, поведінкова терапія і когнітивно-поведінкова терапія (КПT) є ефективними методами лікування в разі їх поєднання з підтримуваними модифікаціями способу життя [47-51, 48, 52].
Програми, що передбачають підходи, спрямовані на зміну поведінки, виявилися ефективними щодо контролю ваги при зосередженні на контролі стимулів, самоконтролі й постановці цілей [48]. КПT досліджує взаємозв’язки між думками, почуттями й поведінкою. Вона являє собою директивний і структурований підхід для лікування багатьох станів і спрямована на полегшення дистресу й покращення якості життя, тим самим допомагаючи пацієнтам навчитися ставити під сумнів свої припущення і розвивати більш адаптивні когнітивні функції та моделі поведінки [53]. Існує обмежена кількість високоякісних досліджень, які вивчають ефективність КПT та інших терапевтичних моделей, що дещо утруднює формування висновків з цього приводу [48]. Проте важливим є врахування психологічних і системних компонентів, що провокують і підтримують ожиріння, супроводжуючися водночас із медичними і фізіологічними ускладненнями. Для забезпечення найкращого догляду необхідно боротися з ожирінням за допомогою комплексного підходу.
Фармакотерапія
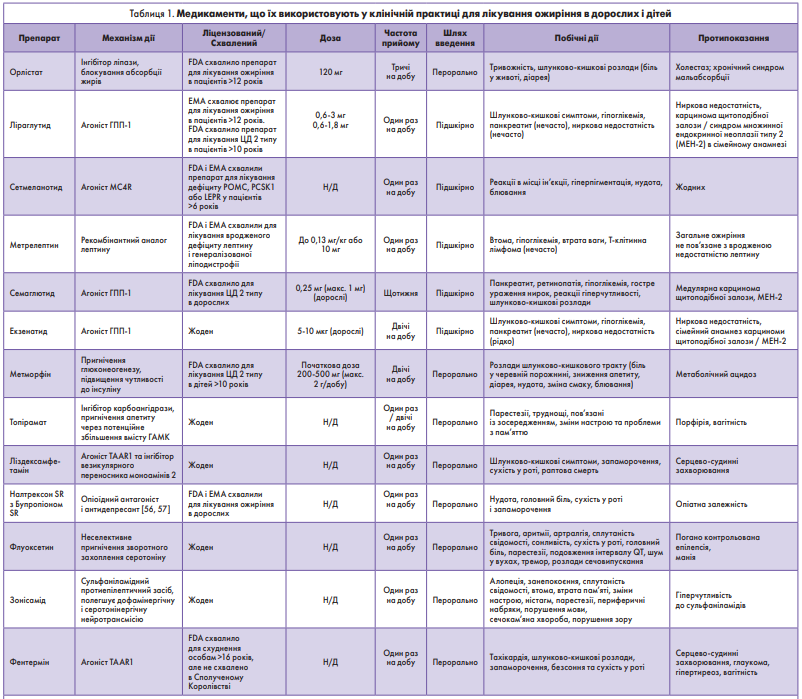
У разі неефективності зміни способу життя для лікування ожиріння в дітей варто розглянути медикаментозну терапію як доповнення до модифікації способу життя (табл. 1) [54, 55].
Препарати, схвалені для лікування ожиріння
Орлістат
Орлістат ліцензований FDA для лікування ожиріння в осіб старше 12 років [58]. Рекомендації NICE наразі радять починати прийом орлістату в цій віковій групі за наявності коморбідних фізичних чи психологічних станів [10, 59]. Орлістат є інгібітором кишечної ліпази, що зменшує гідроліз тригліцеридів і знижує абсорбцію жирів у кишечнику [60].
Нещодавньо проведений метааналіз щодо ефективності орлістату показав, що препарат знижує ІМТ на 0,5-4,2 кг/м2 порівняно з плацебо [60]. Це також було підтверджено кількома рандомізованими дослідженнями [61]. Було також доведено, що ті, хто приймає орлістат, у 2,44 раза частіше втрачають понад 5% маси тіла після 12 тиж лікування порівняно з плацебо [62]. Maahs та співавт. провели дослідження за участю 40 підлітків і з’ясували, що різниця в зниженні ІМТ між групами орлістату і плацебо була незначною [63]. Зниження ІМТ у кожній групі виявилося значним [46]. Найтриваліші з цих досліджень із подальшим спостереженням упродовж понад 12 міс свідчать про стійке зниження ІМТ у разі продовження прийому орлістату (ІМТ: -4,2 кг/м2 при 15-місячному спостереженні) [64]. Побічними ефектами орлістату є діарея, нетримання калу, метеоризм і біль у животі [61]. Через значні побічні ефекти препарату дослідження, проведене у Великій Британії, показало, що частота припинення лікування становила 45% до кінця першого місяця і 75% до кінця 3 місяців [65]. Крім шлунково-кишкових побічних ефектів орлістат також знижує адсорбцію жиророзчинних вітамінів, що надходять з їжею, тому при прийомі препарату рекомендується додатково вживати вітаміни A, D, E і K [4].
Аналоги глюкагоноподібного пептиду‑1
Глюкагоноподібний пептид‑1 (ГПП‑1) – це пептид, який секретується L-клітинами кишечнику [66]. Відомо, що ГПП‑1 виділяється нейронами центральної нервової системи, які відповідають за регуляцію апетиту [66, 67]. Цей пептид секретується впродовж дня, але під час прийому їжі його секреція збільшується [67]. Пептид запускає вивільнення інсуліну і пригнічує виділення глюкагону [67]. ГПП‑1 також уповільнює моторику шлунка, а отже, пригнічує апетит [67-69].
Період напіврозпаду ГПП‑1 становить 2 хв внаслідок швидкого його розщеплення ферментом дипептидилпептидазою 4 (ДПП‑4) [68]. Для запобігання швидкому розпаду ГПП‑1 застосовувалися два механізми: пряме інгібування ДПП‑4 і розробка аналогів ГПП‑1, стійких до розщеплення ферментом ДПП‑4 [68]. Інгібітори ДПП‑4 – ситагліптин і вілдагліптин – використовували для лікування діабету в дорослих [66, 68]. Аналогами, стійкими до ДПП‑4, є ліраглутид, семаглутид і ексенатид [66, 68]. Щодо дитячого ожиріння, то надаються все більше доказів того, що аналоги ГПП‑1, стійкі до ДПП‑4, можуть бути ефективними для лікування ожиріння, кожен з яких обговорюється нижче.
Ліраглутид
Підшкірне введення ліраглутиду схвалене FDA для лікування дітей із ЦД 2 типу (максимальна доза 1,8 мг) віком від 10 років [70, 71]. Нещодавно Європейське агентство з лікарських засобів (European Medicines Agency, EMA) ліцензувало ліраглутид (максимальна доза 3 мг) як доповнення до здорового харчування і підвищеної фізичної активності для контролю ваги в пацієнтів-підлітків віком від 12 років з ожирінням і масою тіла понад 60 кг [71]. Що стосується лікування ЦД 2 типу, надається все більше доказів, які свідчать про важливу роль ліраглутиду. Klein та співавт. провели подвійне сліпе рандомізоване контрольоване дослідження (РКД) впродовж 5 тиж за участю 19 дітей віком 10-17 років із ЦД 2 типу [72]. Цікавим є той факт, що при порівнянні з плацебо застосування вищих доз препарату сприяло значному покращенню рівня HbA1c, але не вплинуло на масу тіла [72].
Tamborlane та співівт. нещодавно провели дослідження, де вивчали роль ліраглутиду в лікуванні пацієнтів-підлітків із ЦД 2 типу, які вже отримували метформін [73]. Через рік спостереження пацієнти, які приймали ліраглутид, мали значно нижчий рівень HbA1c порівняно з плацебо. Також спостерігали зниження ІМТ; однак воно не виявилося статистично значущим [73]. Найпоширенішими побічними ефектами були шлунково-кишкові розлади, серед яких пацієнти найчастіше скаржилися на нудоту, особливо в перші 8 тиж лікування [73].
Дані випробувань ЦД 2 типу свідчать про те, що втрата ваги досягається при застосуванні вищих доз ліраглутиду, як показано в дослідженні, проведеному Kochar та співавт. [74]. Безпека таких доз була встановлена Danne та співавт. у подвійному сліпому РКД за участю 21 підлітка [75]. Ліраглутид приймали один раз на добу впродовж 5 тиж у максимальній дозі 3 мг. При цьому в групі ліраглутиду виникали легкі епізоди гіпоглікемії, але тяжкі епізоди не спостерігали [75].
У 2020 р. Kelly та співавт. опублікували дані РКД за участю підлітків з ожирінням, яким не вдалося успішно схуднути лише за допомогою змін способу життя [76]. У цілому, 125 учасників отримували ліраглутид (до 3 мг), тоді як 126 учасників – плацебо. Згідно з отриманими результатами через 56 тиж маса тіла та ІМТ значно зменшилися в групі ліраглутиду проти групи, що отримувала плацебо [76]. Зниження ІМТ більш як на 5% спостерігали в 51 зі 113 учасників, які отримували ліраглутид, порівняно з 20 зі 105 у групі плацебо [76]. Після припинення прийому в пацієнтів обох груп спостерігали збільшення ваги. У групі ліраглутиду повідомляли про шлунково-кишкові побічні ефекти. Також підкреслено, що препарат може підходити не всім особам [76]. Mastrandrea та співавт. нещодавно досліджували ліраглутид як препарат для зниження ваги в осіб віком 7-11 років [77]. Двадцять чотири дитини було рандомізовано на групу ліраглутиду (n=16) і групу плацебо (n=8) [77]. Результати дослідження показали зниження Z-показника ІМТ на -0,28 (p=0,0062) у групі ліраглутиду [77].
Нещодавно проведене дослідження у Великій Британії показало, що в поєднанні з інтенсивною програмою контролю ваги в пацієнтів, які отримували ліраглутид, спостерігали зниження ІМТ на 2,1 кг/м2 впродовж 3 місяців. Підкреслено, що ліраглутид добре переноситься всіма пацієнтами, які його приймали [78]. Kochar та співавт. довели, що ліраглутид є потенційним терапевтичним варіантом для лікування стійкого до терапії ожиріння. Підлітки з ожирінням, що спочатку контролювалося шляхом зміни способу життя, а потім прийомом пероральних препаратів, при цьому не досягнувши поставленої мети, взяли участь у 12-тижневому дослідженні ліраглутиду [74]. Воно показало, що 51% пацієнтів втратили 5-10% маси тіла, а 23% – понад 10% [74]. Результати також продемонстрували значне покращення систолічного АТ, рівня інсуліну, глюкози, HbA1c, ліпідного профілю і показників функції печінки [74].
Синдром Прадера-Віллі (Prader–Willi syndrome, PWS) – це генетичне захворювання, пов’язане з прогресуючим ожирінням, що може призвести до ранньої захворюваності і смертності. Доведено, що прийом ліраглутиду незначно покращує ІМТ і глікемічний контроль [79, 80]. Препарат застосовували у стандартній дозі для лікування ЦД 3 жінки віком від 19 до 22 років упродовж 3 місяців. За цей час не спостерігали зниження ІМТ, глікемії чи показників апетиту [81]. Наразі проводиться сліпе рандомізоване дослідження для вивчення впливу ліраглутиду на ІМТ у дітей із синдромом Прадера-Віллі [82].
Сетмеланотид
Сетмеланотид, агоніст рецептора меланокортину 4 (MC4R), продемонстрував потенціал для пацієнтів із мутацією проопіомеланокортину (POMC) і, імовірно, іншими генетичними захворюваннями [83, 56]. Продемонстровано, що він сприяє зниженню ваги в пацієнтів із дефіцитом MC4R. Попередні агоністи MCR4 спричиняли тахікардію і/або гіпертензію, але Collet та співавт. не зафіксували свідчень про жоден із цих ефектів впродовж 4-тижневого курсу [84]. Clément та співавт. нещодавно повідомили про результати відкритого багатоцентрового дослідження фази 3 у 7 країнах за участю пацієнтів із дефіцитом POMC або рецептора лептину (LEPR), які отримували сетмеланотид або плацебо впродовж року. Було зазначено, що 80% учасників у групі POMC і 45% учасників у групі LEPR досягли принаймні 10% втрати ваги [85]. Показники голоду також значно знизилися в обох групах – із дефіцитом POMC і дефіцитом LEPR [85].
З огляду на ці висновки, у листопаді 2020 року сетмеланотид був схвалений FDA та в липні 2021 року – EMA [86, 87]. Сетмеланотид показаний для постійного контролю ваги в пацієнтів віком від 6 років із підтвердженим дефіцитом POMC, пропротеїнконвертази субтилізину/кексину типу 1 і LEPR [86].
Метрелептин
Є синтетичним рекомбінантним аналогом лептину, що успішно використовується для зниження ваги в пацієнтів із дефіцитом лептину [88].
Препарат ліцензований як у Великій Британії, так і в США для лікування вродженого дефіциту лептину і генералізованої ліподистрофії [89, 90]. Ефективність застосування метролептину в пацієнтів педіатричного профілю з дефіцитом лептину була доведена в багатьох дослідженнях [91, 92]. Подібні сприятливі результати спостерігали і в пацієнтів із ліподистрофією, які лікувалися метролептином [93].
Сьогодні метрелептин не рекомендований для лікування пацієнтів з ожирінням, пов’язаним із дефіцитом лептину. Дослідження, за участю дорослих, продемонструвало, що антитіла до антиметрелептину синтезуються у більшості пацієнтів з ожирінням і пов’язані зі зниженням ефективності лікування [94].
Ускладненнями терапії метролептином є Т-клітинна лімфома (спостерігається у пацієнтів із ліподистрофією), втома, гіпоглікемія і втрата ваги [95, 96].
Препарати, які вивчаються в дослідженнях, але не ліцензовані для лікування ожиріння
Семаглютид (аналог ГПП‑1)
Понад рік тривало подвійне сліпе РКД O’Neil та співавт. за участю дорослих пацієнтів. Порівнювався семаглютид із ліраглутидом і плацебо за різного дозування, із підшкірним шляхом введення препаратів [97]. У пацієнтів, що лікувалися семаглютидом, спостерігали суттєві покращення маси тіла в порівнянні з плацебо. Найчастішими побічними ефектами були шлунково-кишкові симптоми.
Подальше дослідження показало, що в разі щоденного перорального прийому семаглютиду дорослими з ЦД 2 типу ефект щодо ваги був значним у порівнянні з підшкірним введенням ліраглутиду або плацебо [101]. Тривають клінічні випробування з оцінки впливу семаглютиду на лікування ожиріння в підлітків [102].
Екзенатид (аналог ГПП‑1)
Екзенатид застосовують для лікування ЦД 2 типу в дорослих [56]. Kelly та співавт. оприлюднили дані 22 пацієнтів-підлітків упродовж 3-місячного курсу прийому екзенатиду. У клінічній групі, яка отримувала препарат, спостерігали значне зниження ІМТ і ваги в порівнянні з плацебо [103]. Також зазначали незначне поліпшення показників систолічного АТ [103].
У 2017 р. Salehi та співавт. завершили 6-місячне дослідження, яке вивчало вплив екзенатиду на пацієнтів із синдромом Прадера-Вілля. Вік учасників становив від 13 до 25 років. Результати показали, що екзенатид значно знижував апетит і рівень HbA1c, але не впливав на вагу.
Використання препаратів не за призначенням
Метформін
Наразі метформін ліцензовано FDA для лікування дітей із ЦД 2 типу віком від 10 років [106, 107]. Доведено, що в педіатричних пацієнтів з ожирінням метформін знижує резистентність до інсуліну і серцево-судинний ризик [108]. Незважаючи на те що вплив метморфіну на інсулінорезистентність повсюдно визнаний, відомості про його ефективність щодо зниження ваги в пацієнтів з ожирінням обмежені. Нещодавно проведений метааналіз продемонстрував покращення ІМТ на -1,38 кг/м2 (95% ДІ від -1,93 до -0,82) від вихідного рівня порівняно з контролем через 6 міс; однак цей ефект не був статистично значущим через 12 міс [109]. Більш ніж три рандомізовані дослідження показали невелику, проте незначущу дію метформіну на втрату ваги в підлітків із гіперінсулінемією, недіабетичним ожирінням через 6 міс [61]. Найпоширенішими побічними ефектами метформіну є шлунково-кишкові порушення (нудота, здуття живота і діарея), однак поступове збільшення дози і титрування можуть допомогти зменшити прояви цих симптомів [110, 111]. Варто взяти до відома, що додавання метформіну до режимів схуднення не пов’язано з розвитком лактоацидозу в дітей [112].
Топірамат
Препарат ліцензований для лікування судом і профілактики мігрені [69]. Показано, що топірамат значно зменшує вагу в дорослого населення [113, 114]. Вважається, що механізм його дії здійснюється через низку нейромедіаторів і впливає на пригнічення апетиту і зменшення щоденного споживання калорій [56, 67, 115]. Fox та співавт. не виявили суттєвих змін ваги при лікуванні топіраматом у порівнянні з використанням замінників їжі. Учені встановили прямий зв’язок між прийомом топірамату і зменшенням кількості вісцерального жиру, умісту холестерину і ліпопротеїдів дуже низької щільності проти групи, що отримувала плацебо. Побічними ефектами топірамату є парестезії, погана концентрація, зміни настрою і проблеми з пам’яттю [57, 113, 118]. Топірамат є тератогенним препаратом, тому це потрібно враховувати під час його призначення жінкам дітородного віку [120].
Лісдексамфетамін
Лісдексамфетамін схвалений FDA для лікування синдрому дефіциту уваги і гіперактивності (СДУГ) у дітей старше 6 років, а також розладу харчової поведінки в дорослих. Вчені досліджували розмір вибірки із 43 осіб і зазначили, що 23,3% пацієнтів припинили прийом ліків через побічні ефекти. Найпоширенішими з них були зниження апетиту, безсоння, біль у животі та втрата ваги [123]. Зафіксовано випадки раптової смерті як у дорослих, так і в дітей після застосування ліздексамфетаміну, тому препарат протипоказаний пацієнтам із захворюваннями серцево-судинної системи, а тим, хто його приймає, необхідно регулярно проходити обстеження [122].
Налтрексон SR з бупропіоном SR
Налтрексон SR і бупропіон SR – комбінований препараті (Contrave), схвалений FDA для схуднення в дорослих, тоді як інший препарат, Mysimba, має схвалення EMA [124, 125]. Відповідно до рекомендацій NICE, наразі препарат не пропонується для лікування через відсутність довгострокових доказів і можливих загальних високих витрат [126].Серед побічних ефектів основним була нудота [127-129]. Препарат зазвичай добре переноситься, але необхідні додаткові докази для дослідження тривалої ефективності і безпеки [56].
Флуоксетин
Є селективним інгібітором зворотного захоплення серотоніну і схвалений для лікування депресії в дітей віком від 8 років [131]. У 1987 р. Levine та співавт. порівняли ефективність лікування схуднення флуоксетином і плацебо в дорослих з ожириннім без депресії. Пацієнти з групи, що отримувала флуоксетин, значно сильніше втратили вагу (-4,5±4,0 кг) за більш як 8-тижневий період у порівнянні з групою, що отримувала плацебо (-1,4±0,1 кг) [131].
Ця група насправді страждала від нестачі енергії, але в іншому вчені дійшли висновку, що сьогодні це безпечний і ефективний препарат [131]. Флуоксетин також порівнювали з плацебо впродовж 52 тижнів Darga та співавт. [132]. До 45-го тиж флуоксетин спричиняв значну втрату ваги порівняно з плацебо, але з часом пацієнти з групи флуоксетину набрали втрачену вагу, і наприкінці дослідження різниця в групах не була значущою [132]. У групі плацебо і групі, що отримувала флуоксетин, спостерігали значну втрату ваги через рік спостереження (-4,5 проти -8,2 кг відповідно) [132]. Goldstein та співавт. з’ясували, що застосування вищих доз флуоксетину є ефективнішим щодо зниження ваги в дорослих порівняно з плацебо або меншими дозами. Науковці зазначили як побічний ефект відсутність енергії, в іншому препарати переносилися добре [133]. Вплив флуоксетину на розлад харчової поведінки в дорослих був гіршим, на відміну від КПТ і плацебо впродовж 12-місячного курсу [134].
Зонісамід
Показаний при фокальних нападах у дітей. У дорослих під час застосування зонісаміду спостерігали втрату ваги [57]. Невелика низка пілотних даних показала, що зонісамід може бути ефективним для схуднення в педіатрії [116, 135]. Проте необхідні додаткові дослідження, щоб перевірити ефективність і безпеку цього препарату для схуднення в дітей і молоді.
Хірургічне втручання
Баріатрична хірургія
В основному призначають пацієнтам із тяжкою формою ожиріння з декількома супутніми захворюваннями, які не відповідають на застосування описаних вище засобів. Є міжнародна тенденція зростання частоти проходження баріатричної хірургії для лікування ожиріння [149]. Поточні міжнародні рекомендації припускають, що доцільність баріатричної хірургії варто розглядати в осіб, які досягли статевого дозрівання і мають ІМТ >40 кг/м2 або ІМТ >35 кг/м2 і серйозні супутні захворювання і в яких виявилося неефективним дотримання офіційної програми корекції способу життя [4, 150-152].Тенденція до збільшення кількості хірургічних втручань, імовірно, пояснюється очевидною ефективністю, описаною в численних систематичних оглядах; зменшення ІМТ через рік спостереження після баріатричної хірургії (кілька методів) становило -13,5 кг/м2 (95% ДІ від -14,1 до -11,9), а після бандажування шлунка -12,7 кг/м2 (95% ДІ 11,3-14.2) [153, 154]. Незважаючи на очевидну ефективність баріатричної хірургії і збільшення кількості пацієнтів, які проходять такі процедури, докази, що повністю підтверджують цей підхід, лишаються обмеженими. Дійсно, огляд Кокранівської бази даних підкреслює обмежену кількість доступних РКД, з одним дослідженням, включеним до огляду, з обмеженим довгостроковим спостереженням [154].
Дослідження, які підтверджують роль баріатричної хірургії, тривають, однак одним із найважливіших з них є підліткове дослідження LABS, яке показало, що після 3-річного спостереження середня вага знизилася на 27% (95% Дl 25-29) у групі, пацієнти якої проходили втручання. Результати такого типу процедури показали зниження ваги на 28% (95% ДІ 25-30) серед учасників, які перенесли шлункове шунтування, і на 26% (95% ДІ 22-30) у тих, кому була проведена рукавна гастректомія [155]. Втрата ваги зберігалася впродовж 5 років спостереження [156]. Щодо вибору втручання, вертикальна рукавна гастректомія в підлітків зараз застосовується набагато частіше, ніж шлункове шунтування Roux-en-Y, яке раніше було найпоширенішою процедурою [157]. До вибору рестриктивних операцій на шлунку (шлунковий рукав, бандаж) або нейрокогнітивних процедур (шунтування шлунка) необхідно підходити індивідуально, ураховуючи фактори з боку пацієнта як ключову частину прийняття рішення [153].
Окрім впливу на вагу важливим після операції є також зменшення проявів супутніх захворювань. Нещодавно проведений огляд, в якому порівнювали результати пацієнтів у програмі Teen-LABS із пацієнтами в програмі «Варіанти лікування діабету 2 типу в підлітків і молоді» (TODAY) (які отримували ліки і модифікували спосіб життя), показав, що рівень HbA1c знизився з 6,8% до 5,5% у Teen-LABS, але збільшився з 6,2% до 7,8% у групі TODAY [158]. Прояви інших супутніх захворювань, пов’язаних з ожирінням, таких як гіпертензія, дисліпідемія і протеїнурія, значно зменшилися в групі Teen-LABS [158]. Кілька інших досліджень підтвердили роль хірургічного втручання в зниженні проявів супутніх захворювань, пов’язаних з ожирінням [159-162].
Однією з найбільших проблем баріатричної хірургії є відомі негайні негативні прояви і невідомі довгострокові ефекти. Сьогодні є одне повідомлення про смерть після шлункового шунтування в педіатричного пацієнта [163]. Значними побічними ефектами після хірургічного втручання є демпінг-синдром, тяжкий гастроезофагеальний рефлюкс, жовчнокам’яна хвороба та хірургічні ускладнення (грижі, ранові інфекції, непрохідність тонкої кишки) [163-166]. Інші проблеми, пов’язані з довгостроковими результатами, зумовлені відносною нестачею скоординованих національних даних подальшого спостереження [153]. Єдиним винятком є дослідження AMOS шведської хірургії хворобливого ожиріння у підлітків (патологічне ожиріння в підлітків у Швеції), яке триває і фіксує дані 2-річного спостереження за великою когортою пацієнтів. Дослідження має на меті надати детальні дані щодо подальшого спостереження [167]. Ураховуючи нестачу даних довгострокового спостереження, дані щодо ефективності і безпеки баріатричної хірургії в довгостроковій перспективі є обмеженими.
Висновки
Для боротьби з поглибленням кризи охорони здоров’я, спричиненої зростанням рівня дитячого ожиріння в усьому світі, необхідні ефективні і добре досліджені варіанти лікування. Стосовно педіатричної популяції, кількість потенційних методів лікування і досліджень, які підтверджують їх використання, недостатня порівняно з терапевтичними опціями, доступними для дорослих з ожирінням. Поки є лише скромні докази, що підтверджують модифікацію способу життя і поведінки як підхід першої лінії в лікуванні ожиріння в дітей і молоді.
У пацієнтів, які не реагують на зміни способу життя або мають тяжку форму ожиріння, кількість варіантів лікування поступово збільшується. Незважаючи на те що ці методи лікування можуть мати побічні ефекти, що обмежують прихильність до лікування, збільшується доступність ліків із різними механізмами дії і хорошою переносимістю, що є ключовим у досягненні втрати ваги на додачу до змін способу життя.
У дітей і молодих людей, яким не вдалося зменшити вагу за допомогою медикаментозного лікування, баріатрична хірургія залишається альтернативним варіантом, хоча тверді докази її використання в педіатричній групі лишаються обмеженими, тому є потреба в даних довгострокового спостереження.
Реферативний огляд статті Louise J. Apperley et al. Childhood obesity: A review of current and future management options,
Clinical Endocrinology, 2022
Підготувала Дарина Павленко
Повну версію дивіться: https://onlinelibrary.wiley.com/doi/10.1111/cen.14625
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 4 (60) 2022 р.