26 січня, 2023
Спадковий ангіоневротичний набряк і вагітність: міжнародні рекомендації та реалії надання допомоги в Україні
Спадковий ангіоневротичний набряк (САН) – рідкісне генетичне автосомно-домінантне захворювання, що виникає внаслідок кількісного або якісного дефіциту інгібітора білка С1 плазми (C1-INH) і проявляється рецидивним локалізованим набряком шкіри чи слизових оболонок, який може бути надзвичайно болісним, виснажливим і навіть смертельним, якщо уражає гортань (ризик становить 30%). Набряк може уражати будь-яку частину тіла: кінцівки, обличчя, шлунково-кишковий тракт (сильні болі в животі, що імітують гострий живіт), верхні дихальні шляхи. Антигістамінні препарати, кортикостероїди або епінефрин не мають лікувального ефекту при нападах САН. Хвороба має два основні підтипи: 1 тип виявляється у 85% пацієнтів і характеризується низьким рівнем C1-INH, тоді як 2 тип – нормальним (навіть високим), але функціонально неефективним C1-INH. Поширеність САН оцінюється в діапазоні від 1:10 000 до 1:100 000 у загальній популяції. Це захворювання є важливою глобальною проблемою, оскільки значно впливає на якість життя самих пацієнтів та може викликати життєво небезпечні стани. Планування зачаття, вагітність і народження дитини – це ті питання, що мають важливе медичне та соціальне значення при спостереженні лікарем жінок із САН, адже зміни в організмі жінки під час вагітності потенційно можуть провокувати частіші напади САН і потребувати додаткової диференційної діагностики ускладнень вагітності. А надання допомоги при родорозрішенні таким жінкам має свої особливості.
САН – це рідкісне потенційно загрозливе для життя хронічне захворювання, що характеризується спорадичними, болісними та виснажливими нападами шкірного і підслизового набряку. Патофізіологічним підґрунтям САН є абсолютний або відносний дефіцит білка C1-INH, зумовлений мутацією гена SERPING1.
Недостатність білка C1-INH призводить до вивільнення надмірної кількості прозапального медіатора брадикініну і, як наслідок, суттєвого збільшення проникності судин. Клінічна картина САН часто нагадує таку при алергічних реакціях, утім, застосування антигістамінних препаратів, глюкокортикоїдів та адреналіну при цьому не дає жодного клінічного ефекту, оскільки лікування потребує призначення специфічних препаратів.
Ще одним характерним симптомом САН є гострий біль у животі, який може імітувати гостру хірургічну патологію (апендицит, аднексит, кишкову непрохідність, холецистит, панкреатит, тромбоз мезентеріальних судин та ін.) і призводити до непотрібних оперативних втручань. Оскільки за класифікацією САН відноситься до первинних імунодефіцитів, лікуванням таких пацієнтів має займатися імунолог.
Сучасні можливості діагностики та лікування САН в Україні
Діагностика САН в Україні впродовж останніх років стала доступнішою: визначати концентрацію й активність С1-INH, а також концентрацію C4 компонента комплементу в сироватці/плазмі крові, що потрібно для встановлення діагнозу САН, сьогодні можна в низці приватних лабораторій. Окрім того, ГО «Всеукраїнська асоціація дитячої імунології» було розпочато проєкт «Поширеність САН в Україні», в рамках якого за направленням лікаря-імунолога (та/або алерголога) проводяться обстеження осіб із підозрою на САН, лабораторний скринінг батьків, дітей і родичів пацієнтів із САН, а також виявлення нових хворих із зазначеною патологією. Як наслідок, кількість діагностованих випадків САН в Україні за останні 2 роки зросла майже вдвічі. Проте частота виявлення нових випадків САН в Україні все ще залишається вкрай низькою: станом на 2022 рік лише 80 людей в Україні мають підтверджений діагноз.
Що стосується можливостей лікування пацієнтів із САН в Україні, то починаючи з 2020 року пацієнти із САН мають змогу отримати сучасну терапію препаратом С1-INH людини, котрий використовують як для лікування гострих станів, так і з профілактичною метою. Слід зазначити, що згідно з наказом Міністерства охорони здоров’я України № 2711 від 28.12.2019 року, забезпечення препаратом пацієнтів, які мають підтверджений діагноз САН, відбувається коштом держави. Для того щоб пацієнт із САН зміг отримати лікування, він має перебувати на обліку в імунолога.
Про планування зачаття та народження дитини в сім’ях із САН, а також особливості перебігу САН у вагітних ми попросили розповісти завідувачку кафедри педіатрії, імунології, інфекційних та рідкісних захворювань Міжнародного європейського університету (м. Київ), доктора медичних наук, професора Анастасію Валеріївну Бондаренко.
? Яким є ваше ставлення до планування вагітності в сім’ях із САН?
– Безперечно, кожна людина, зокрема хвора на САН, має право на материнство/батьківство, тому вагітність, звісно, потрібно планувати. Водночас кожна особа також має право самостійно вирішувати, чи готова вона йти на ризик і народжувати дитину, яка може успадкувати САН від одного з батьків, або ж вона хоче народити дитину, котра не матиме цього захворювання, що стало можливим завдяки сучасним репродуктивним технологіям. Завдання лікаря в цьому випадку – надати пацієнту весь обсяг потрібної інформації, що допоможе здійснити цей вибір.
? Який перебіг має САН у вагітних?
– Зважаючи на особливість захворювання та вплив на його перебіг гормонального стану жінки, теоретично можна очікувати почастішання нападів САН у першій половині вагітності та зменшення їхньої кількості надалі. Проте, як показує клінічна практика, перебіг САН у кожної окремої вагітної може бути різним: тоді як у деяких напади САН під час вагітності справді є частішими, в інших вони не виникають узагалі. У цьому аспекті важливо забезпечити вагітній, хворій на САН, доступ до препарату C1-INH, що допоможе контролювати перебіг захворювання.
? Чи можливо знизити ризик успадкування САН?
– Ні зміна способу життя, ні дотримання різноманітних дієт і т. ін. не можуть зменшити ризику успадкування дитиною САН. Проте наразі доступною є рання пренатальна ДНК‑діагностика, що проводиться на 11-12-му тижні вагітності й надає змогу встановити наявність у плода мутації гена SERPING1, який кодує C1-INH і спричиняє розвиток САН. Питання доцільності пренатальної діагностики має вирішуватися індивідуально, адже якщо батьки планують зберігати вагітність навіть у разі виявлення мутації, то проведення такого дослідження не має сенсу. Крім того, сама процедура є інвазивною та супроводжується відносно високим ризиком ускладнень (1-5%), серед яких і переривання вагітності. Ще одним варіантом, який може бути запропонований парі, де один із партнерів має мутацію гена SERPING1, є екстракорпоральне запліднення (ЕКЗ), що надає змогу провести генетичну діагностику САН іще на етапі доімплантаційного розвитку ембріонів. У такому разі до порожнини матки переносяться лише ті ембріони, в яких ця мутація відсутня. Проте якщо хворою на САН є жінка, то гормональна стимуляція, що передує процедурі ЕКЗ, а також подальша гормональна підтримка вагітності може бути чинником ризику почастішання нападів. У такому випадку рекомендується профілактичне призначення плазмового концентрату C1-INH (pdC1-INH), яке має бути розпочате ще на етапі планування ЕКЗ і тривати протягом усієї вагітності.
? Якими є етичні аспекти проведення пренатальної та передімплантаційної діагностики САН?
– Важливо розуміти, що САН не належить до несумісних із життям захворювань, а сучасні методи лікування надають змогу досягнути майже нормальної якості життя в таких хворих. Водночас пацієнти із САН, які планують вагітність, мають бути поінформовані про доступність, переваги й ризики проведення ранньої пренатальної та передімплантаційної діагностики САН. Рішення щодо етичності їхнього проведення та подальшої тактики після отримання результатів генетичних досліджень залишається виключно за батьками.
? Коли та як можна діагностувати САН у дітей після народження?
– У дітей віком до 1 року антигенний уміст і функціональна активність C1-INH, а також рівень C4 компонента комплементу є низькими, тому результати біохімічних аналізів, проведених до досягнення дитиною 12-місячного віку, є неінформативними. Для ранньої діагностики САН у новонароджених може застосовуватися генетичне тестування, проте висока вартість є бар’єром для його широкого впровадження в клінічну практику. Загалом новонароджені з позитивним сімейним анамнезом вважаються потенційно хворими, допоки не встановлено протилежне, тому мають ретельно спостерігатися й обстежуватися якомога раніше; в ідеалі – до появи клінічних проявів, що надасть змогу забезпечити оптимальне лікування.
Тригери розвитку нападу САН
Найчастіше тригерами розвитку ангіоедеми при САН є стрес, травми та медичні втручання. Ще одним вагомим чинником, який може посилювати прояви САН, є підвищений рівень естрогенів, що спостерігається під час вагітності, на тлі застосування комбінованих пероральних контрацептивів (КОК) та замісної естрогенної гормонотерапії. Вагітність та пологи – ті фактори, які підвищують ймовірність розвитку фатальних ускладнень САН, як-от набряк гортані, мозкових оболонок та органів черевної порожнини. У цьому аспекті важливу роль відіграє проведення належної профілактики нападів САН на етапі вагітності та безпосередньо перед пологами.
Особливості ведення вагітних із САН в Україні. Сучасний стан проблеми
Життя триває, і ми в Україні вже маємо власний досвід зачаття та народження дітей у жінок із діагностованим САН. Зріс рівень обізнаності спеціалістів щодо цього захворювання. Однак особливості ведення вагітних із САН усе ще викликають багато запитань, що продемонстровано, зокрема, в клінічних випадках 1 та 2, які ми попросили прокоментувати завідувачку відділення акушерських проблем екстрагенітальної патології ДУ «Інститут педіатрії, акушерства і гінекології ім. О. М. Лук’янової НАМН України» (м. Київ), доктора медичних наук, професора Юлію Володимирівну Давидову.
Клінічний випадок 1
(надано алергологом-імунологом, доцентом Тетяною Юріївною Хіміч, м. Харків)
Пацієнтка Т., 38 років. Звернулася за консультацією до обласного алерголога м. Харкова у 2020 році зі скаргами на рецидивні набряки кінцівок і зовнішніх статевих органів, виражений дискомфорт, відчуття розпирання, періодичний абдомінальний біль, нудоту та блювання. Зі слів пацієнтки, появі набряків передували еритематозні висипання на шкірі. Зазначені симптоми провокувалися різноманітними чинниками (стрес, травма, інфекція (застуда), зміна якості їжі, перевтома, фізичне навантаження), тривали 3-5 діб і зазвичай зникали самостійно. Прийом сорбентів, значної кількості рідини та голод зменшували тяжкість прояву симптомів і їхню тривалість.
Анамнез. Хвороба дебютувала в 7-річному віці та проявлялася набряками зовнішніх статевих органів, верхніх і нижніх кінцівок. Вищезазначені симптоми виникали в середньому 1 р/міс і провокувалися переважно травмами, перевтомою та переїданням. Одного разу після травми відзначався набряк обличчя. Лікування антигістамінними та глюкокортикоїдними препаратами позитивного результату не надало. До алерголога хвора не зверталася. Крім того, 1-2 р/міс виникали напади інтенсивного абдомінального болю різної локалізації та характеру (за типом кишкової кольки й гострих болів у шлунку), нудоти, блювання, інколи – діареї, які тривали 3-5 діб. Пацієнтка не раз обстежувалася в гастроентеролога, було встановлено діагноз «Дискінезія жовчного міхура. Хронічний гастрит». Проте лікування з приводу гастропатології позитивного результату не надавало. Зважаючи на тривалий абдомінальний біль, хвору обстежили в онкоцентрі, де виключили онкологічні захворювання органів черевної порожнини. У період статевого дозрівання пацієнтка відзначила посилення болів у ділянці малого таза, з приводу чого неодноразово зверталася до гінекологів. Патології статевих органів виявлено не було. У віці 27 років під час обстеження в ендокринолога та гінеколога з приводу підвищеного рівня пролактину вперше було запідозрено наявність САН. Пацієнтку була скеровано на дообстеження до Центру алергічних захворювань верхніх дихальних шляхів ДУ «Інститут отоларингології ім. О. С. Коломійченка НАМН України» (м. Київ), де було виявлено зниження рівня C1-INH і встановлено діагноз САН. Упродовж 10 років проходить обстеження з приводу безпліддя. Згідно з висновками гінекологів, репродуктивні функції пацієнтки та її чоловіка не порушені. Через це хвора відзначає погіршення психоемоційного стану та підвищення частоти больового синдрому в ділянці малого таза.
Сімейний анамнез. Батько та дідусь пацієнтки також мали в анамнезі епізодичні напади ангіоедеми кінцівок середньої тяжкості, які провокувалися фізичними перенавантаженнями.
Огляд. Загальний стан задовільний, нормостенічна будова тіла, шкірні покриви блідо-рожевого кольору, набряки й ознаки кропив’янки відсутні.
Лабораторні методи дослідження. Під час проведення лабораторного обстеження виявлено зниження концентрації й активності C1-INH, а також рівня фактора комплементу С4. Батько пацієнтки від обстеження відмовився. На основі клініки, анамнезу та проведених досліджень установлено діагноз САН 1 типу.
Призначене лікування. Враховуючи високу частоту й активність нападів, рекомендовано довготривалу профілактичну терапію pdC1-INH у дозі 1000 МО 2 р/тиж. Проте через острах пацієнтки щодо прийому нового препарату за домовленістю з лікарем перші введення проводили 1 р/тиж. На тлі лікування стан значно покращився: напади ангіоедеми, в тому числі з абдомінальними проявами, були невираженими та турбували рідко (1 раз на 2-3 міс). Пацієнтка відзначила істотне поліпшення психоемоційного стану, що проявлялося, зокрема, зникненням постійного відчуття страху щодо розвитку симптомів САН. Хвора завагітніла, проте вагітність була позаматковою, що потребувало її переривання оперативним втручанням. Як наслідок стресового впливу напади САН почастішали, у зв’язку із чим пацієнтку перевели на стандартну профілактичну дозу та частоту введення препарату 1000 МО 2 р/тиж. Через 3 тиж лікування стан стабілізувався, напади САН не розвивалися. Згідно з висновком гінекологів, репродуктивна функція збережена.
Обговорення клінічного випадку
Цей клінічний випадок відображає складість диференційної діагностики САН та важкий тривалий шлях пацієнтки до встановлення діагнозу. І навіть перша підозра у лікарів щодо САН виникла під час дослідження репродуктивної функції пацієнтки тільки на 20-й рік наявних симптомів захворювання. Хоча пацієнтка мала часті абдомінальні прояви САН, позаматкова вагітність, ймовірно, не була спровокована наявністю цього захворювання. Однак симптоми абдомінального болю під час вагітності варто було диференціювати як із нападами САН, так і з небезпечними ускладненнями вагітності, зокрема її позаматковою локалізацією.
Клінічний випадок 2
(надано імунологом, професором Галиною Данилівною Коваль, м. Чернівці)
Пацієнтка А., 26 років. У 2020 році була скерована алергологом на кафедру клінічної імунології, алергології й ендокринології Буковинського державного медичного університету (м. Чернівці) з діагнозом «Набряк Квінке нез’ясованого генезу». При першому зверненні хвора скаржилася на рецидивні набряки кінцівок і зовнішніх статевих органів, виражений дискомфорт, відчуття розпирання, періодичний абдомінальний біль, нудоту та блювання. Зазначені симптоми провокувалися різноманітними чинниками (стрес, травма, інфекція (застуда), зміна якості їжі, перевтома, фізичне навантаження), тривали 3-5 діб і зазвичай зникали самостійно.
Анамнез. Хвороба дебютувала в 10-річному віці та проявлялася розвитком ангіоедеми різної локалізації: обличчя (особливо ділянки губ), шиї (кілька разів із локалізацією в ділянці гортані), грудної клітки, спини, абдомінальної ділянки, статевих органів, верхніх і нижніх кінцівок. Найчастішою локалізацією набряків були кисті рук, сідниці та стегна. Напади ангіоедеми виникали в середньому 1-2 р/міс і провокувалися різноманітними чинниками. Крім того, не рідше 1 р/міс виникали напади інтенсивного абдомінального болю, відчуття розпирання в животі, нудота, блювання, інколи – діарея, що тривали 3-5 діб. До моменту встановлення діагнозу САН пацієнтка неодноразово була госпіталізована до алергологічного відділення, де отримувала лікування адреналіном, препаратами глюкокортикоїдів, антигістамінними та сечогінними засобами. Також призначалися дієтотерапія з виключенням великої кількості продуктів харчування, що розцінювалися як імовірні алергени, неодноразово – антигельмінтна терапія, кількаразові курси плазмаферезу, процедури дуоденального зондування. У віці 12 років із приводу вираженого, резистентного до лікування, рецидивного абдомінального синдрому, що був розцінений як напад холециститу, було проведено холецистектомію. Усі вищеназвані методи лікування не надавали клінічного результату.
Сімейний анамнез. Рідний брат пацієнтки має в анамнезі епізодичні напади ангіоедеми.
Огляд. Загальний стан задовільний, будова тіла нормостенічна, шкірні покриви блідо-рожевого кольору, на задній поверхні лівого стегна відзначався щільний ізольований набряк без ознак кропив’янки та гіперемії.
Лабораторні методи дослідження. Під час проведення лабораторного обстеження виявлено зниження концентрації й активності C1-INH на тлі незміненого рівня фактора комплементу С4. З огляду на спадковий характер захворювання та сімейний анамнез лабораторна діагностика САН проведена брату та матері пацієнтки (батько проживає в іншій країні), в результаті чого було виявлено зниження активності C1-INH у брата хворої. На основі клініки, анамнезу та проведених досліджень установлено діагноз САН 1 типу.
Призначене лікування. Через часті напади хворій призначено терапію людським C1-INH у режимі довготривалої профілактики: 1000 МО кожні 3-4 дні. Особливості введення препарату та його дози обговорювалися з пацієнткою та її мамою. На тлі лікування стан значно покращився, протягом року було лише 2 напади ангіоедеми з локалізацією на кистях рук і сідницях. Через рік після встановлення діагнозу пацієнтка завагітніла. У 1-й місяць вагітності було 2 епізоди ангіоедеми з локалізацією на верхніх кінцівках. У період 2-3-го місяців вагітності такі напади були щотижневими. При цьому набряки постійно виникали в ділянці нижніх відділів живота, часто – на окремих ділянках верхніх кінцівок, сідницях і зовнішніх статевих органах. Також у цей час з’явився еритематозний висип на більшій частині тіла, який мав вигляд розпису та не супроводжувався свербінням. Найтяжчим перебіг САН виявився в другому триместрі, коли напади відзначалися кожні 3 дні та проявлялися набряками кистей, передплічь, абдомінальної та поперекової ділянок, сідниць, стегон і стоп, що завдавало вираженого фізичного дискомфорту. Залучення нових ділянок відбувалося ще до моменту розрішення попередньо виниклих набряків. Окрім того, зберігалися виражений абдомінальний біль (суб’єктивна оцінка болю – 10 із 10) й еритематозний висип. У третьому триместрі спостерігалося полегшення симптомів: набряк обмежився ділянкою низу живота та нижніх кінцівок, абдомінальний синдром турбував рідко. Під час опитування було встановлено, що пацієнтка не дотримувалася призначеної схеми лікування, що, ймовірно, і стало причиною погіршення перебігу захворювання протягом вагітності. Рекомендовано дотримання попередньо призначеної схеми введення препарату – 1000 МО кожні 3 дні.
Слід зауважити, що впродовж усієї вагітності ларингеальна локалізація набряку відзначалася всього 1 раз, тоді як до вагітності та до початку терапії C1-INH набряк обличчя та гортані виникав кожні 2 міс. У зв’язку з ризиком розвитку нападу САН під час пологів, який може ускладнити їхній перебіг і загрожувати життю дитини та породіллі, консиліумом фахівців було ухвалено рішення про плановий кесарів розтин. За кілька тижнів до цього з метою забезпечення додаткової короткострокової профілактики частоту введення C1-INH було збільшено до 3 р/тиж, а також рекомендовано введення препарату в цій самій дозі безпосередньо перед кесаревим розтином. В інтраопераційному та післяпологовому періодах нападів САН не спостерігалося. Наразі пацієнтка продовжує профілактичне лікування C1-INH у дозі 1000 МО кожні 3-4 дні.
Обговорення клінічного випадку
У цьому випадку, як і в попередньому, окрім тривалого шляху до встановлення діагнозу, маємо проблему дотримання пацієнтами частоти профілактичного введення препарату для лікування САН. На жаль, наші пацієнти досить часто не дотримуються призначеного лікування, особливо новими для них лікарськими засобами. І увагу на цій проблемі важливо загострювати під час кожної розмови з пацієнтом, адже лише введення адекватної кількості препарату може дати очікуваний терапевтичний ефект. Також цей випадок показав велике занепокоєння лікарів щодо вибору способу родорозрішення вагітної із САН, враховуючи ризик провокування нападу пологами, супутнім стресом і гіпотетичною можливістю проведення інтубації трахеї в разі ускладнень. Варто звернути увагу на те, що, згідно з міжнародними рекомендаціями, при виборі способу розродження вагітної із САН перевагу віддають вагінальним пологам у разі відсутності протипоказань. Також слід зазначити, що безпечним та ефективним варіантом профілактичного лікування САН під час вагітності, яка супроводжується почастішанням нападів САН, вважається довгострокова профілактика із застосуванням pdC1-INH, безпека призначення якого у цій когорті пацієнток із САН була доведена в дослідженні I. Martinez-Saguer та співавт. (2010).
Також ми поспілкувалися з Ю. В. Давидовою щодо особливостей профілактики та лікування САН у комплексному захисті соматичного і жіночого здоров’я.
? Що потрібно знати акушеру-гінекологу про етіологію та механізм розвитку САН?
– Важливо розрізняти САН і гістамін-опосередкований алергічний АН. На відміну від алергічного АН, який супроводжується кропив’янкою і свербежем шкіри, САН може самостійно розрішуватися впродовж 24-48 год, а для його лікування ефективними є призначення антигістамінних та глюкокортикостероїдних препаратів; напади САН опосередковуються брадикініном, для нього не є характерними свербіж, кропив’янка й утворення ямки при натисканні. Напад САН триває до 5 днів і не реагує на терапію антигістамінними та глюкокортикостероїдними препаратами.
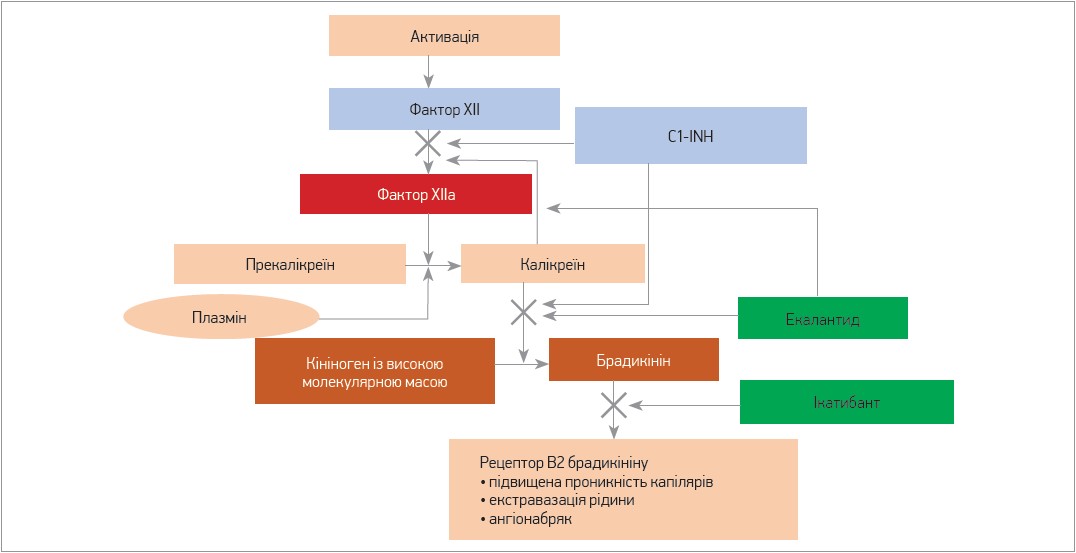
Патофізіологія САН представлена на рисунку. Активований фактор XII перетворює прекалікреїн на калікреїн, який відщеплює брадикінін (маленький пептид із 9 амінокислот) від кініногену з високою молекулярною масою. Брадикінін, діючи через B2-рецептор, спричиняє дисфункцію ендотеліальних клітин, екстравазацію рідини й ангіоневротичний набряк. Відсутність нормального рівня функціонального C1-INH є основним дефектом у переважальних формах САН (1 і 2 типи).
Рис. Патофізіологія САН
? Який перебіг має САН у жінок репродуктивного віку та в менопаузі?
– Насамперед відомо, що концентрація жіночих статевих гормонів відіграє важливу роль у виникненні та частоті нападів САН. Окрім того, на відміну від чоловіків у жінок напади є набагато частішими, а прояви САН – серйознішими, тому жінки із САН частіше потребують госпіталізації. Періоди менструації й овуляції можуть зумовлювати напади САН: у 62% пацієнток із САН загострення перебігу хвороби відбулося під час статевого дозрівання, у 80% – під час прийому КОК, а у 29% хворих симптоми виникають лише в періоди підвищеного впливу естрогену. Повідомляється про підвищений ризик синдрому полікістозних яєчників у жінок із САН із дефіцитом/дисфункцією C1-INH. Доведено, що використання контрацептивів, які містять виключно прогестин, сприяє зниженню частоти нападів САН. Кількість епізодів САН під час вагітності може збільшуватися, зменшуватися або залишатися незмінною. При цьому клінічні симптоми зазвичай є вираженішими протягом першого триместру, що зумовлено високою концентрацією естрогенів і нейроендокринними змінами, пов’язаними з ранньою вагітністю, як-от нудота. Що стосується тактики ведення пацієнток із САН під час вагітності, то доведену ефективність має призначення pdC1-INH із профілактичною метою або за потреби. Необхідно зауважити, що pdC1-INH – єдиний засіб, який міжнародні протоколи рекомендують застосовувати у вагітних (International consensus and practical guidelines on the gynecologic and obstetric management of female patients with hereditary angioedema caused by C1 inhibitor deficiency, 2012). Ослаблені андрогени протипоказані під час вагітності, оскільки вони проникають крізь плаценту та можуть впливати на розвиток плода. Про шкідливий вплив антифібринолітиків на плід не повідомлялося, але за відсутності спеціальних досліджень за участю людей їх можна розглядати для профілактики нападів САН під час вагітності, тільки якщо pdC1-INH недоступний і після ретельного розгляду їхньої потенційної користі та шкоди. Опублікованих даних щодо безпеки ікатибанту або екалантиду під час вагітності наразі немає.
? Які особливості мають ведення пологів і післяпологова реабілітація у пацієнток із САН?
– Враховуючи високу ймовірність ускладнень, пов’язаних із САН, які можуть виникати при вагітності, пологах, проведенні гінекологічних операцій, підборі методів контрацепції, лікування безпліддя, гінекологічна та перинатальна допомога жінкам із САН має надаватися мультидисциплінарною командою, обов’язково із клінічним імунологом у складі. Пацієнтки із САН із дефіцитом/дисфункцією C1-INH мають народжувати в установах, де є швидкий доступ до консультантів з акушерства, анестезіології, перинатології та pdC1-INH. Питання довгострокової профілактики нападів САН у вагітних слід розглядати індивідуально з урахуванням частоти та тяжкості набряків. Враховуючи той факт, що навіть при неускладненому перебігу вагітності існує ризик проведення додаткових втручань та маніпуляцій під час пологів, препарати pdC1-INH мають бути легкодоступними.
Метод вибору для вагітних із САН – вагінальні пологи. Проте навіть під час вагінальних пологів ризик нападів САН є досить високим і складає 6-8%. Тому, якщо в анамнезі пацієнтки наявні серйозні напади чи напади на статевих органах, що є вторинними внаслідок травми, або напади були частими протягом третього триместру, рекомендується короткочасна профілактика за допомогою pdC1-INH перед вагінальними пологами. У разі виникнення нападу потрібно забезпечити невідкладне лікування pdC1-INH і проконсультуватися з лікарем, який знайомий із САН. Якщо pdC1-INH недоступний, перевагу слід надавати плазмі, обробленій методом «розчинник-детергент», порівняно зі свіжозамороженою плазмою, застосування якої супроводжується ризиком передачі гемоконтактних захворювань і алосенсибілізації. Проте обидва препарати вважаються терапією другої лінії.
Кесарів розтин може спровокувати напад САН, тому перед його проведенням варто ввести pdC1-INH. Уведення pdC1-INH також рекомендується перед накладанням щипців або вакуум-екстракцією, проте екстрені процедури не слід відкладати, якщо pdC1- INH недоступний негайно.
При виборі знеболення перевага віддається епідуральній анестезії, оскільки інтубація для загальної анестезії може спровокувати ларингеальний напад. Під час післяпологового періоду ймовірною є підвищена частота нападів САН, тому рекомендується ретельне спостереження за породіллями протягом 72 год. Особливо це стосується породілей із набряком промежини, які перебувають у групі квазівисокого ризику. Лактація також може провокувати почастішання нападів САН, що пов’язано з підвищенням рівня пролактину в сироватці крові. Під час грудного вигодовування рекомендується призначення pdC1- INH, які можуть застосовуватися як для лікування за потреби, так і з профілактичною метою. Враховуючи можливий побічний вплив на стан здоров’я дітей, під час лактації слід уникати призначення транексамової кислоти й анаболічних андрогенів.
? Який вплив на стан плода та новонародженого чинить наявність у матері САН?
– Відомо, що наявність у плода C1-INH-САН може вплинути на кількість нападів у матері. Природа транспорту C1-INH крізь плацентарний бар’єр невідома, але, ймовірно, потрібен активний транспорт. Симптоми при САН із дефіцитом/дисфункцією C1-INH можуть виникати в будь-якому віці після народження, але про внутрішньоутробні симптоми ангіоневротичного набряку не повідомляється. Хоча дефіцит C1-INH присутній під час народження, клінічні симптоми рідко виникають у дитинстві. В новонароджених може спостерігатися крайова еритема як продромальний симптом, але рідко – набряк.
? На що варто звернути увагу за потреби переривання вагітності в пацієнтки із САН?
– Рекомендується короткочасна профілактика перед хірургічним абортом, але процедуру можна проводити без профілактики за умови, що невідкладне лікування нападу САН (pdC1-INH) доступно в цій установі.
? Яким методам контрацепції слід віддати перевагу пацієнткам із САН?
– Таблетовані КОК провокують виникнення нападів САН у раніше здорових пацієнток і загострюють раніше діагностований САН. Припинення прийому КОК сприяє полегшенню або зменшенню симптомів. Парентеральні естроген-прогестинові контрацептиви (пластир або вагінальне кільце) мають ефекти, подібні до естрогеновмісних таблетованих КОК. За даними ретроспективного аналізу, використання пероральних контрацептивів, що містять тільки прогестин, зменшує частоту нападів у 81,8% пацієнток із САН. У частини хворих під час прийому пероральних контрацептивів, що містять лише прогестин, припинено тривалу профілактичну терапію. Препарати з антигонадотропною дією (лінестренол, номегестрол і хлормадинон) є ефективнішими, ніж таблетки з низькими дозами прогестину (левоноргестрел, норгестрієнон і дезогестрел). Перед уведенням внутрішньоматкових спіралей короткострокова профілактика САН не є необхідною, але лікування нападу має бути доступним. Для екстреної контрацепції слід використовувати препарати, що містять тільки прогестин, і уникати засобів, які містять естроген. Бар’єрні методи контрацепції не впливають на появу симптомів САН.
? Чи впливає САН на репродуктивну функцію?
– Вплив САН на фертильність не є доведеним, а дані про вплив препаратів для профілактики цього захворювання на фертильність відсутні.
? Як підготувати пацієнтку із САН до застосування допоміжних репродуктивних технологій?
– Короткочасна профілактика нападу САН рекомендується перед проведенням сальпінгографії. При виборі внутрішньоматкової інсемінації або ЕКЗ високі рівні естрогенів, індукованих ін’єкційними гонадотропінами, можуть спричиняти напад САН. Тому рекомендовано проведення ЕКЗ під час натуральних циклів, коли рівень естрадіолу нижчий і ймовірність гіперстимуляції набагато менша. Короткострокова профілактика pdC1-INH має проводитися перед процедурами, які можуть спровокувати напад, і повинна використовуватися в разі нападу.
? На що потрібно звернути увагу перед проведенням гінекологічних хірургічних втручань у пацієнток із САН?
– Перед інтубацією або великими процедурами будь-якого типу слід розглянути короткострокову профілактику, що може включати наявний в Україні pdC1-INH, який уводиться якомога ближче до процедури, бажано протягом 1 год і обов’язково протягом 6 год. За експертними рекомендаціями, вводиться 10-20 Од/кг (або відповідно до інструкції для медичного призначення лікарського засобу відповідного виробника) із другою дозою в рівній кількості, доступною під час процедури.
? Чи впливає наявність у пацієнтки САН на тактику ведення онкогінекологічних захворювань?
– У пацієнток із раком молочної залози та САН слід уникати призначення андрогенів через їхні потенційні побічні ефекти. Препарати з антиестрогенною дією мають деякі агоністичні ефекти на рецептори естрогенів. Для тамоксифену доведено загострення симптомів САН, тому його слід застосовувати з обережністю, препаратами вибору можуть стати інгібітори ароматази. Під час лікування раку ендометрія можуть використовуватися андрогени.
? На що потрібно звернути увагу при виборі менопаузальної гормонотерапії у пацієнток із САН?
– Старт менопаузальної гормональної терапії призводить до загострення САН, що можна пояснити зниженням активності ангіотензинперетворювального ферменту, який бере участь у катаболізмі брадикініну, а також ефектами естрогенів і збільшенням рівнів фактора XII, прекалікреїну та брадикініну. Використання фітоестрогенів як альтернативного лікування припливів під час менопаузи в жінок із САН з дефіцитом/дисфункцією C1-INH не оцінювали. Проте з огляду на їхню естрогенну потужність призначення цих засобів у цьому випадку не рекомендується. Прогестерон і прогестини здатні полегшити припливи й можуть пропонуватися жінкам із САН. Тиболон, похідне норметилтестостерону, що використовується при ускладненому перебігу менопаузи, можна призначати, але не в комбінації з даназолом. У разі стійких припливів і безсоння можна застосовувати альтернативні негормональні препарати, як-от селективні інгібітори зворотного захоплення серотоніну, інгібітори зворотного захоплення серотоніну й норадреналіну та клонідин.
Стисла пам’ятка для акушерів-гінекологів стосовно пацієнток із САН
САН – рідкісний хронічний розлад, який характеризується спорадичними, болісними та виснажливими нападами набряку, що зазвичай є спонтанними, але можуть бути спровоковані фізичною травмою, емоційним стресом або гормональними коливаннями. Стратегії лікування включають негайне лікування окремих нападів, довгострокову профілактику, короткострокову профілактику перед потенційною подією, яка може мати тригерну дію, або комбінації цього. Вагітність потенційно може змінити частоту нападів САН. Застосування pdC1-INH під час вагітності рекомендовано останніми настановами. Ослаблені андрогени протипоказані під час вагітності.
Пологи / після пологів. Вагінальні пологи є методом вибору, який має пріоритет перед кесаревим розтином у жінок із САН. Профілактика САН під час вагінальних пологів не рекомендована як рутинна практика, але може бути розглянута в певних випадках залежно від особистих чинників ризику. Епідуральна анестезія пріоритетна перед інтубацією за потреби зменшення ризику потенційно смертельного нападу набряку гортані. Лактація може збільшити частоту нападів САН; pdC1-INH рекомендується жінкам, які бажають годувати грудьми.
Контрацепція. КОК призводять до загострення перебігу САН, тому протипоказані. Контрацептиви, що містять тільки прогестин, можуть зменшити частоту нападів.
Підготувала Ольга Гуйванюк
За підтримки ТОВ «Такеда Україна».
VV-MEDMAT-80022